溴氰虫酰胺在土壤中的吸附特性
2022-09-02郭南吕珍珍周雨杭曹战文梁爽侯志广逯忠斌
郭南,吕珍珍,周雨杭,曹战文,梁爽,侯志广,逯忠斌
(吉林农业大学植物保护学院,长春 130118)
农药是一类重要的农业生产资料,在保障农业生产安全中发挥了重大作用,但农药滥用带来的生态环境问题也非常严重,包括土壤和水环境污染、抗药性及农药残留与农产品质量问题等,开发低毒、高效、绿色农药势在必行。溴氰虫酰胺(cyantraniliprole,CNAP)是一种新型杀虫剂,属于第二代鱼尼丁受体类杀虫剂,2007年由杜邦公司开发。CNAP的作用机制新颖,其进入昆虫体内后,与神经及肌肉细胞中的鱼尼丁受体结合干扰钙离子通道活动,致使昆虫进食障碍、肌肉麻痹、活动力下降直至死亡。在国内CNAP已在水稻以及多种蔬菜上登记,可以有效防治鳞翅目、半翅目、鞘翅目害虫,与有机磷类、氨基甲酸酯类、拟除虫菊酯类、第一代鱼尼丁受体类农药无交互抗性。
据相关研究报道,CNAP 对家蚕(LC为0.3 mg·L)、蜜蜂(LC为2.9 mg·L)的急性经口毒性为高毒,对蚯蚓有慢性影响,对斑马鱼的急性毒性为低毒,但会显著影响斑马鱼胚胎发育,对斑马鱼胚胎的急性毒性为中毒。也有研究报道CNAP 对雌性大鼠具有生殖毒性(150 mg·kg·d)并会干扰大鼠的内分泌系统。而CNAP的制剂在水稻和蔬菜上广泛应用,而且能作为种子处理剂防治地下害虫,其有可能随着灌溉、降雨、地表径流等途径扩散到农田以外的自然生态环境中造成环境风险。开展CNAP 在农田土壤中的迁移规律研究十分重要,可为合理使用、安全生产、环境治理及剂型研发提供理论基础。吸附是评价农药在土壤中移动性的重要指标。因此,本研究较为系统地分析了CNAP在5种常见的不同类型农田土壤的吸附特性,探讨了吸附机理及pH对吸附行为的影响,为CNAP的科学使用和环境评价提供了数据支持。
1 材料与方法
1.1 仪器与试剂
5种土壤样品均取自农田耕层(20 cm)土壤,去除植株残体、石块等杂物后充分混合,风干后研磨,过80 目筛,置于干燥避光处保存。供试土壤的基本理化性质见表1。

表1 土壤的基本理化性质Table 1 Physical and chemical properties of the soils
仪器与试剂:安捷伦1200 型高效液相色谱仪;溴氰虫酰胺标准品(Dr.Ehrenstorfer GmbH 公司,纯度98.7%);甲醇、乙腈(色谱级,MREDA 公司提供);氯化钙(分析纯);超纯水;BS-2E 恒温振荡培养箱;TDL-5-A 离心机;IKA Vortex3 涡旋混匀器;LE204E分析天平;ST300 ZH酸度计。
1.2 试验方法
1.2.1 标准溶液配制
准确称取0.010 1 g 的CNAP 标准品粉末,用10 mL 甲醇溶解配制成1 000 mg·LCNAP 标准溶液,置于4 ℃冰箱中保存。
配制0.01 mol·L的CaCl溶液作为背景溶液,用于保持离子强度。使用背景溶液将1 000 mg·LCNAP标准溶液稀释至其他浓度用于后续试验。
1.2.2 吸附动力学试验
参考OECD 对化学品吸附性测试的批平衡方法。首先以1∶1、1∶3、1∶5、1∶10、1∶50 的固液比进行预试验,确定适宜固液比为1∶3,此时CNAP 在5 种供试土壤吸附率在20%~70%之间。称取5 种供试土壤2.00 g 于50 mL 三角瓶中,加入浓度为1 mg·L的CNAP 溶液6 mL,以120 r·min的频率,25 ℃恒温振荡。在0.1、0.3、0.5、1、2、4、6、12、24、48、72 h时分别取样,5 000 r·min离心5 min,取上清液过0.22 μm滤膜,使用HPLC测定CNAP浓度。每组样品3个重复,设置不含CNAP 的空白处理,不含土壤的对照处理。当上清液中CNAP浓度不再变化时即认为到达平衡时间。
1.2.3 等温吸附试验
参照前述试验方法,在3 个温度条件下进行等温吸附试验。溶液中的CNAP 浓度设置为0.5、1、5、10、50 mg·L,温度分别为15、25、35 ℃,振荡时间为动力学试验得到的平衡时间。样品经振荡、离心后,取上清液用HPLC测定CNAP浓度。
1.2.4 初始pH对吸附的影响
参照前述试验方法,配制浓度为1 mg·L的CNAP 溶液,并用HCl 溶液和NaOH 溶液调节初始pH为3、4、5、6。25 ℃恒温振荡至平衡,测定上清液中CNAP 浓度。在对CNAP 的其他研究中发现,其在碱性水溶液中会快速降解,所以不设置碱性条件。
1.3 分析方法
采用高效液相色谱法。色谱柱:BDS HYPERSIL C18 Dim.(mm)250×4.6;检测器:紫外检测器,检测波长265 nm;流动相:乙腈-水(60∶40,∶);流速:1 mL·min;进样量:10 μL;保留时间:4.2 min。
1.4 数据分析
吸附量采用如下公式计算:
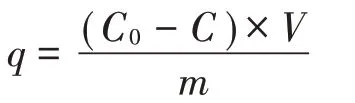
式中:为单位质量土壤对CNAP 的吸附量,mg·kg;为未加土壤水溶液中CNAP 的浓度,mg·L;为土-水体系水相中CNAP 的浓度,mg·L;为水溶液体积,L;为土壤质量,kg。
使用准一级动力学方程、准二级动力学方程和Elovich 方程研究CNAP 的吸附行为。使用Origin 软件对数据进行非线性拟合。
准一级动力学方程:
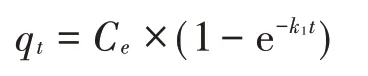
准二级动力学方程:
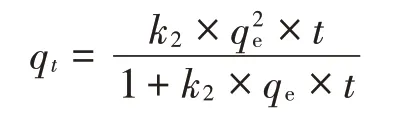
Elovich方程:

式中:q为时刻单位质量土壤对CNAP 的吸附量,mg·kg;为平衡时溶液中CNAP的浓度,mg·L;为准一级动力学吸附速率常数,kg·mg·h;为吸附时间,h;为平衡时单位质量土壤对CNAP 的吸附量,mg·kg;为准二级动力学吸附速率常数,kg·mg·h;为初始吸附速率常数,mg·kg·h;为Elovich方程常数,kg·mg。
采用Freundlich 等温吸附方程和Langmuir 等温吸附方程对等温吸附试验数据进行分析。Freundlich方程:

Langmuir方程:
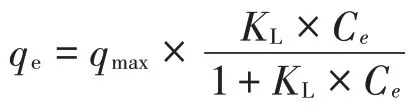
根据可计算经有机质标化的吸附常数,公式为:
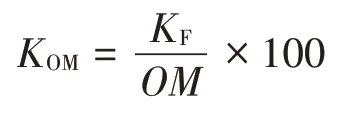
式中:为单位质量土壤对CNAP 的吸附量,mg·kg;为Freundlich吸附常数,L·kg;1/反映吸附的非线性程度;为最大吸附量,mg·kg;为Langmuir 常数,L·mg;为有机质吸附常数,mL·g;为土壤有机质含量,%。
吸附热力学数据使用Van’t Hoff方程计算。
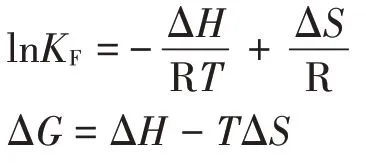
式中:为Freundlich 常数,吸附物质在固液两相中的分布常数;为吸附焓变,kJ·mol;为吸附熵变,kJ·mol·K;R 为理想气体常数,取值8.314 J·mol·K。拟合ln对1/的线性方程可得到和。
1.5 计算模拟
为了探究吸附机制,进一步对吸附体系进行了模拟计算,使用的程序有:量子化学计算程序ORCA和PSI4、第一性原理计算程序CP2K、波函数分析程序Multiwfn、分子建模可视化软件VMD。黄腐酸(Fulvic acid,FA)是一种小分子腐植酸,含有羧基、羟基、芳环和短碳链,能较好地代表土壤中有机质的结构。首先输入CNAP 和FA 的分子结构,在CP2K 中进行分子动力学模拟,在350 K 条件下可获得一批能量不同的构象。将能量最低构象作为初猜结构,使用ORCA 程序的密度泛函方法在B3LYP-D3/def2-SVP级别优化FA 和CNAP 的二聚体结构,最后在B3LYPD3/def2-TZVP 级别计算单点能并获得准确的波函数。使用PSI4 程序对上述体系做对称匹配微扰理论(SAPT)能量分解计算,计算级别为sSAPT0/jun-ccpVDZ。
2 结果与讨论
2.1 CNAP在不同土壤中的吸附动力学
图1 是1 mg·LCNAP 在5 种土壤中的吸附动力学曲线。从图中可以看出,在5 种不同土壤中的吸附动力学趋势是相似的,吸附过程可分为两个阶段:0~12 h吸附较快,水相中CNAP的浓度快速下降,12 h时的吸附量均达到平衡吸附量的80%以上,属于快吸附阶段。土壤矿物表面的有机质有丰富的极性官能团,包括羟基、羰基、氨基等,这些官能团能与CNAP形成大量的分子间氢键,降低吸附体系的能量,这可能是快速吸附的主要机理,也是大部分有机污染物在土壤中的吸附机制。12 h 后进入慢吸附阶段,水相中CNAP 浓度的变化平缓。一般而言,吸附的过程可分为4 个阶段:分子扩散、膜扩散、颗粒内扩散和表面吸附,通常分子扩散和表面吸附是迅速的,在土壤颗粒表层水膜中的扩散也是短程的,所以颗粒内扩散往往决定吸附速率。土壤矿物表面吸附位点达到饱和,CNAP 向矿物内部或者孔隙扩散,这个过程往往需要跨越能垒,扩散后表面吸附位点重新暴露继续吸附,造成吸附速率降低。CNAP 还可能与矿物表面的氧原子形成氢键,这类氢键与CNAP-有机质氢键相比较弱且数量较少,吸附能力较差,造成吸附速率降低。48 h 后吸附量不再增加,达到吸附平衡。先快速吸附后慢速吸附是一种典型的固-液吸附模式。褐土和潮土48 h 时吸附量无显著性差异。其他任意2 种土壤之间的平衡吸附量存在显著差异。在CNAP 的实际使用中应当考虑降水、灌溉可能造成的污染扩散,尽量避免在降水和灌溉前48 h内施用农药。
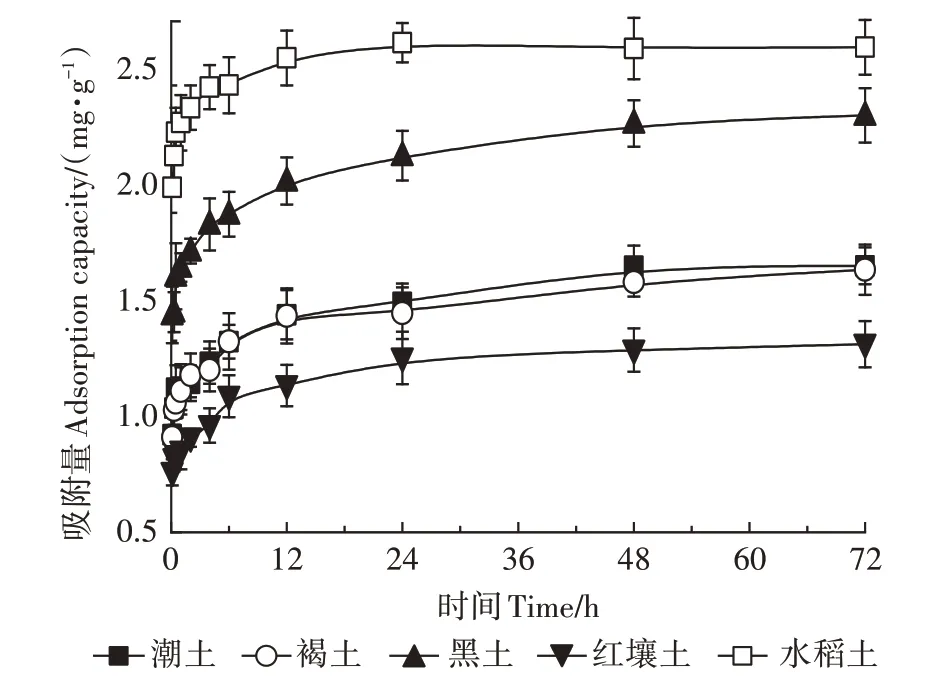
图1 吸附量随时间变化的曲线Figure 1 Curve of adsorption capacity over time
使用Elovich 方程、准一级动力学方程、准二级动力学方程分别对吸附动力学过程进行了分析。结果(见表2)表明,Elovich 方程能很好地描述CNAP 在土壤中的吸附行为。Elovich 方程主要用于描述固体表面的吸附行为,其假定吸附过程中活化能会随着吸附剂表面覆盖率的变化而变化,不考虑解吸的影响,而实际中吸附过程是吸附、解吸、扩散的综合过程,Elovich 方程在吸附平衡前能够更好地描述吸附过程。参数为Elovich 吸附模型的初始吸附速率,为吸附活化能的变化率。5 种土壤的初始吸附速率由小到大的顺序为红壤土<潮土<褐土<黑土<水稻土,与土壤有机质含量顺序一致。
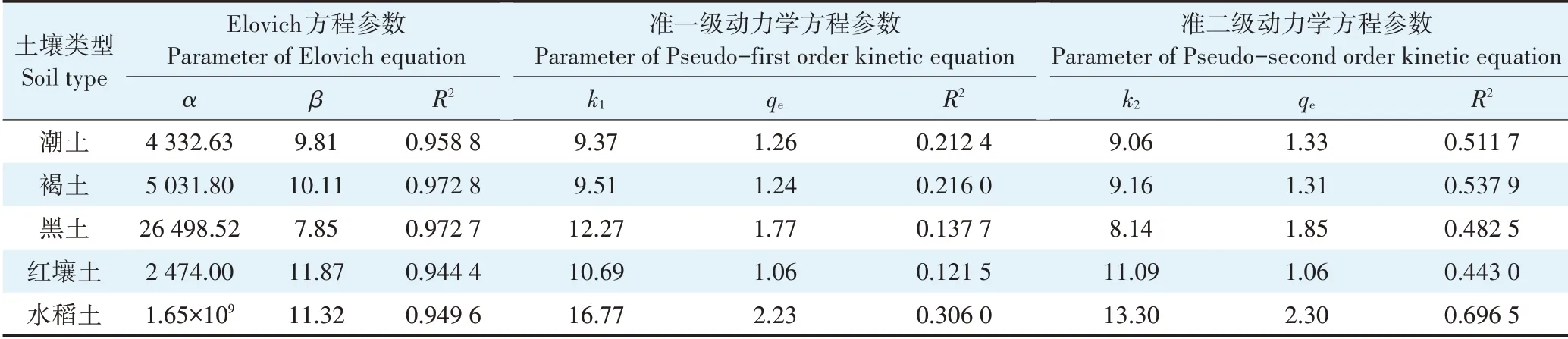
表2 CNAP的动力学吸附方程参数Table 2 Parameters of the adsorption kinetic equations for CNAP
2.2 CNAP在不同土壤中的等温吸附特性
等温吸附结果表明,CNAP 在不同土壤中的吸附量与水相中CNAP 的初始浓度密切相关,初始浓度越高,吸附量越高。由表3 可知,Freundlich 方程和线性方程的决定系数()平均值为0.998 2 和0.993 3,都能较好地描述不同温度下CNAP 的吸附行为。但是Langmuir方程在某些情况下存在参数发散的问题,无法达到收敛标准,高达10mg·kg,与实际情况不符。通过Freundlich 方程的拟合结果可知,相同温度条件下,潮土和褐土的吸附量差异较小,吸附量从小到大的顺序为红壤土<潮土<褐土<黑土<水稻土,与有机质含量的顺序基本一致。计算25 ℃时CNAP 在潮土、褐土、黑土、红壤土、水稻土中的有机质吸附系数,对结果取10 为底的对数,分别为4.184、4.330、3.997、3.134、4.118。根据EPA 对农药移动性的分级,CNAP 在红壤土中为弱移动性,在其他4 种土壤中几乎没有移动性。

表3 CNAP的等温吸附方程参数Table 3 Parameters of the adsorption isotherm equations for CNAP
对25 ℃时的Freundlich 方程吸附常数和土壤理化性质进行Pearson 相关性分析,结果见表4。表4显示,与土壤有机质含量呈显著正相关(<0.05),与沙粒含量有一定的负相关性但并不显著,与其他性质基本无相关性。这说明CNAP 在土壤中的吸附行为主要受土壤有机质的影响,同时吸附量也一定程度受到土壤机械组成的影响,黏粉粒含量的增加提高了吸附量,这是因为黏粉粒具有更高的比表面积,土壤有机质分布在矿物的表面,更高的比表面积可在矿物表面提供更多的吸附位点,提高吸附量。根据CNAP 的吸附特性可知,对于被CNAP 污染的土壤可以通过使用有机肥、高比表面积的吸附剂等方法控制污染。
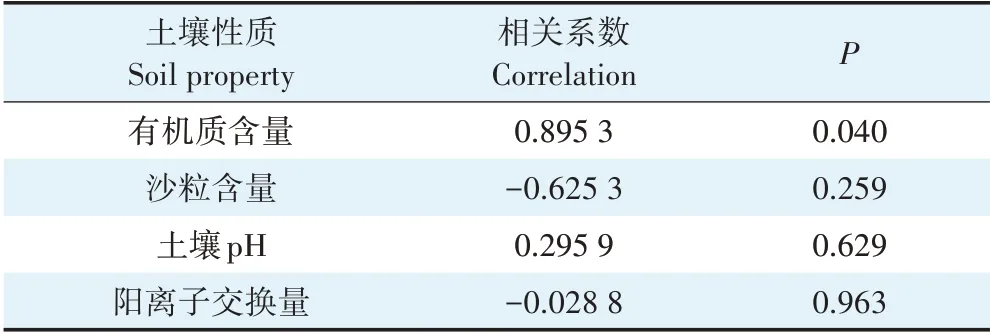
表4 KF与土壤性质的Pearson相关性分析Table 4 Pearson correlation analysis between KF and soil properties
2.3 CNAP在不同土壤中的吸附热力学
使用Van’t Hoff方程对3个温度下的等温吸附数据进行拟合分析,结果见表5。吸附焓变均为正值,说明CNAP 在土壤中的吸附属于吸热过程,符合温度越高吸附量越大的规律,且||<40 kJ·mol,属于物理吸附。以范德华力和氢键为主导的吸附作用的焓变分别为0~10 kJ·mol和2~40 kJ·mol,所以CNAP 的吸附机制可能包括范德华力和氢键。为正值表明CNAP 的吸附过程是熵增的过程,当焓变为正值时,熵增成为吸附作用的驱动力。当土壤处于吸附溶液中,吸附质分子进入吸附位点的过程会让其自由度减小,体系的熵减小。土壤也会吸附水分子,由于CNAP 分子的范德华体积远大于水分子,一个CNAP 分子的吸附致使多个水分子脱附,脱附行为产生的熵增大于水分子被吸附的熵减,所以熵增为吸附提供驱动力,这种机制也被称作疏水吸附机制。大部分条件下为负值,此时吸附是自发的过程。只有红壤土在15 ℃时>0,此时吸附不能自发进行,需要环境为其提供能量。随着温度的升高而降低,高温有利于吸附的发生,提高吸附量。

表5 CNAP在不同土壤上吸附行为的热力学参数Table 5 Thermodynamic parameters for adsorption of CNAP on different soils
2.4 初始pH对吸附量的影响
pH 对吸附量影响的结果见图2,CNAP 在潮土、褐土、红壤土中的吸附量随着pH的变化有显著变化,吸附量随着pH 的升高先增大后减小,最大吸附量在pH 为4~5 之间。红壤土最大吸附pH 比潮土、褐土低的原因可能是红壤土自身pH 较低。CNAP 在水中的预测pk为6.49,分子中含有2 个酰胺结构,在pH 较低时酰胺基可与溶液中的氢离子结合形成CNAP 正离子,借助阳离子交换作用能够增加吸附量。通常认为当溶质pk减去溶液pH 的值大于2 时,溶质在溶液中主要存在形态为正离子形态(>98%)。土壤矿物由于类质置换作用带负电荷,容易吸引带有正电荷的粒子。当氢离子浓度过高时,水合氢离子竞争吸附,降低吸附量。黑土和水稻土可能由于有机质含量较高,土壤质地黏重,对pH缓冲效果明显,能够有效缓冲吸附溶液中的氢离子,所以pH对吸附量的影响较小。
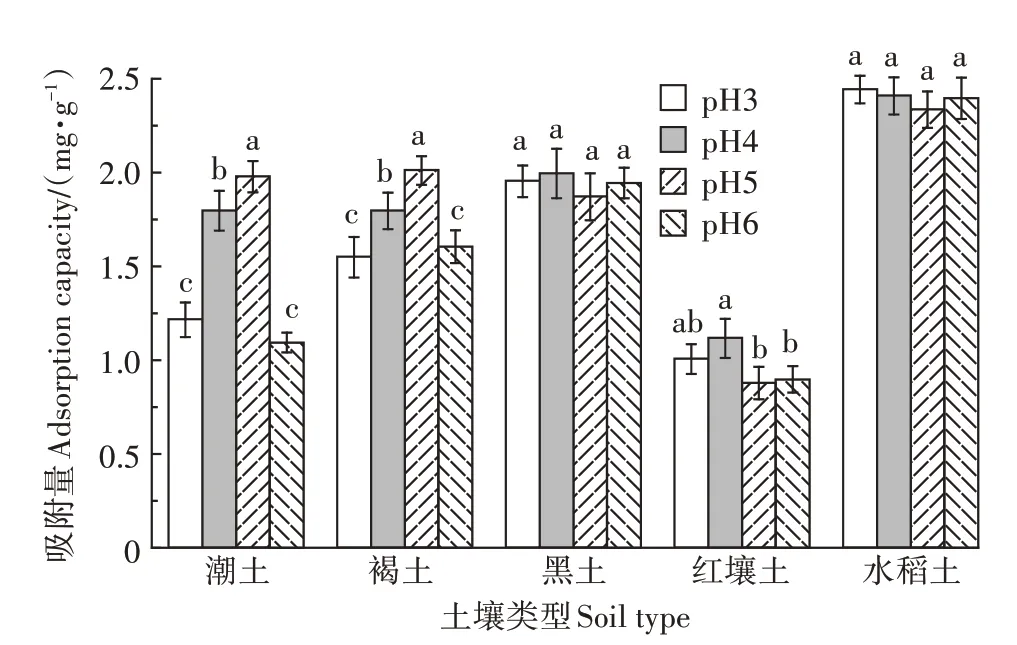
图2 不同pH条件下CNAP的吸附量Figure 2 Adsorption capacity of CNAP at different pH
2.5 吸附机制的计算模拟
能量计算显示,FA 和CNAP 结合之后能量降低,其相互作用能为-105.765 kJ·mol。本研究使用相互作用区域指示函数(IRI)法考察分子间的相互作用。结果如图3 所示,用不同的颜色绘制IRI 等值面。可见FA 和CNAP 之间有大片的绿色区域,此处为芳环之间的π-π 堆积作用,属于范德华力。自然界中的腐植酸也含有大量的芳环结构,可与CNAP 形成π-π 堆积,但是考虑到自然复杂环境中的腐植酸有较长的碳链并且能与黏土矿物结合在芳环附近形成空间位阻,且π-π堆积作用作用距离短,4.0 Å以上就可以认为π-π 堆积作用不存在,所以π-π 堆积作用仅在吸附构象较为理想时才能出现。π-π 堆积作用是疏水作用的机理之一,芳环靠近后会排出附近水分子,通过熵效应促进吸附,与前文热力学试验中得到的结论一致。图中用黄色虚线标记出了分子间氢键,可以看出FA 与CNAP 均含有大量易于形成氢键的基团,FA 的羰基氧和CNAP 的氨基氢能形成键能较强的NH···OC 氢键,此外CNAP 的氰基具有较强的吸电子效应,所以芳环上的氢原子也能与FA 中的羟基形成较弱的CH···OH氢键。

图3 FA和CNAP的IRI分析Figure 3 IRI analysis between FA and CNAP
能量分解计算结果显示FA 和CNAP 的相互作用能为-115.667 kJ·mol,静电作用、交换作用、色散作用、诱导作用的贡献分别为-98.766、156.317、-35.259、-137.959 kJ·mol。对吸引力贡献最大的是色散作用,其次是静电作用,FA 和CNAP 体系之间的色散作用主要表现形式为π-π 堆积,较弱的分子间氢键也存在色散作用;静电作用-98.766 kJ·mol,主要由FA和CNAP的分子间氢键贡献。
综上所述,推测在实际环境中,CNAP 与腐植酸之间能形成多个氢键,并且可能与腐植酸之间存在π-π堆积作用。
3 结论
(1)溴氰虫酰胺(CNAP)的吸附动力学过程符合Elovich 方程,1~12 h 为快吸附阶段,吸附平衡时间为48 h,平衡时吸附量由小到大的顺序为红壤土<潮土<褐土<黑土<水稻土。
(2)25 ℃时Freundlich 吸附常数在1.11~4.97 之间,在红土中具有弱移动性,在其他4 种土中不具有移动性。Freundlich吸附常数和有机质含量显著正相关,和黏粉粒含量正相关。在造成红壤污染后,CNAP有向地表水、地下水迁移的可能。
(3)CNAP 的吸附过程为吸热过程,吸附自由能变为负值,在常温下可以发生自发的吸附行为,升高温度有利于吸附。||<40 kJ·mol,属于物理吸附。
(4)初始pH 显著影响CNAP 在潮土、褐土、红壤土的吸附量,最大吸附量时的pH 为4~5。黑土和水稻土的吸附量不受初始pH的影响。
(5)CNAP 可与腐植酸形成氢键,推测氢键是吸附的主要机制。CNAP 和腐植酸中的芳环存在π-π堆积作用,但对吸附构象有较高要求,推测可能是次要机制。