血管内成形术治疗症状性非急性期颅内动脉狭窄或闭塞的临床疗效
2022-08-29文立利王森唐晓宇吴琪周龙江周晓明张鑫
文立利,王森,唐晓宇,吴琪,周龙江,周晓明,张鑫
颅内动脉粥样硬化性狭窄或闭塞是导致缺血性卒中的重要原因之一。急性期颅内动脉粥样硬化性狭窄闭塞的血管内治疗目前已经取得广泛共识[1],但是对于症状性非急性期颅内动脉粥样硬化性狭窄或闭塞的治疗,仍没有统一的标准。症状性非急性期的颅内动脉狭窄或闭塞的患者,即使经过强化药物治疗后仍有较高的年卒中率[2-4]。随着神经介入技术和器械的发展,血管内成形术治疗症状性非急性期颅内动脉狭窄或闭塞成为临床研究的热点之一,但其临床疗效尚不明确。本研究回顾性分析2016年7月—2020年6月在东部战区总医院神经外科采用血管内成形术治疗的44例症状性非急性期颅内动脉狭窄或闭塞患者,探讨血管内成形术的有效性及安全性。现报告如下。
1 资料与方法
1.1 一般资料 共纳入44例患者,其中男30例(68.2%),女14例(31.8%);年龄43~74岁,平均年龄(57±9.8)岁;既往病史高血压33例(75%),糖尿病9例(20.5%),高血脂2例(4.5%),脑梗死23例(52.2%);30例(68.2%)患者表现为一侧肢体无力麻木、口角歪斜或言语不清,8例(18.2%)表现为头晕,5例(11.4%)表现为眩晕、视物旋转或行走不稳,1例(2.3%)表现为一过性晕厥。DSA检查提示,44例患者共45处颅内动脉狭窄或闭塞,包括颈内动脉颅内段狭窄3例,闭塞3例,大脑中动脉M1段狭窄18例,闭塞 7例,基底动脉狭窄7例,椎动脉颅内段狭窄7例。35处狭窄中33处(94.3%)狭窄≥70%。41例患者入院采用改良Rankin评分(modified Rankin Scale,mRS)≤2分(93.2%)。见表1。纳入标准:(1)急性脑梗死≥2周;(2)狭窄和闭塞责任血管导致的缺血症状如短暂性脑缺血发作、头晕和走路不稳等,经药物保守治疗无效或症状反复发作;(3)CT灌注检查证实存在灌注异常(rCBF下降或基本正常、MTT相差3 s[5]及TTP相差4 s[6]);(4)DSA证实颅内动脉狭窄大于50%以上。排除标准:(1)颅内出血;(2)大面积脑梗死(大于同侧中动脉供血区1/3);(3)MR高分辨成像提示血管炎、烟雾病和夹层等性质病变。
1.2 治疗方法 所有患者术前3~5 d均接受双联抗血小板(阿司匹林100 mg/Qd+氯吡格雷75 mg/Qd)及他汀类药物治疗,并行血栓弹力图检查。若存在阿司匹林抵抗,则更换为西洛他唑(200 mg/Bid);若存在氯吡格雷抵抗,则更换为替格瑞洛(90 mg/bid)。所有患者均于气管插管全麻下进行血管内治疗。采用改良Seldinger技术经股动脉穿刺置入6F动脉鞘后,全身肝素化(肝素首次剂量为体质量的2/3 mg,1 h后追加首剂的半量,2 h后追加第2次的半量,3 h后追加 10 mg并维持此剂量至术毕),选择病变血管合适的工作角度造影并测量狭窄或闭塞段前后正常血管的直径。

表1 患者的基本人口学和临床特征
微导丝(Synchro 0.014或Traxcess 0.014)在微导管(Headway 17、Echelon-10或Prowler Selectplus)支撑下小心通过狭窄段,或在闭塞段近端小心探寻血管真腔后微导丝穿越闭塞段到达远端,微导管沿微导丝跟进并越过狭窄或闭塞段,手推造影确定微导管位于血管真腔内。通过交换技术置入Synchro 0.014 inch×300 cm微导丝后使用Gateway球囊缓慢扩张(球囊直径选择正常血管直径的80%)。对于完全闭塞的血管,一般使用1.5 mm×9 mm的Gateway球囊进行缓慢预扩,然后再更换为正常血管直径80%的球囊再次扩张。扩张后造影评估狭窄或闭塞段血管开通情况。若局部残留狭窄较重,可以行再次扩张或者更换直径较大的Gateway球囊再次扩张。扩张完成后行造影检查以及DynaCT检查,若造影未见静脉早显及CT无出血,则同期植入支架。否则只行单纯球囊扩张术。植入的支架根据血管直径大小和术者习惯选用Enterprise或Solitaire支架。支架植入后造影,并根据改良脑梗死溶栓分级(modified Thrombolysis in Cerebral Infarction Score,mTICI)分级判断开通后脑血流情况,mTICI 2b-3级定义为有效再通。
1.3 术后处理 术中血管再通后将患者血压降至术前基础血压的80%,并在术后3 d内逐渐将血压恢复至基础血压水平。手术结束后再次行DynaCT检查观察颅内有无出血或造影剂增强点征。无出血患者术后继续行双联抗血小板治疗,维持3个月后改为阿司匹林长期口服。对于术中或术后出血患者,停用抗血小板治疗,根据影像学复查血肿增加情况决定是否行脑室引流或颅内血肿清除术。术后存在缺血症状的患者,CT检查排除出血后给予替罗非班(静脉推注6 μg/kg,静脉泵维持0.1 μg·kg-1·min-1)治疗。
1.4 随访 术后6个月随访所有患者并记录有无卒中复发症状。采用mRS评分评估患者功能状态,mRS评分0~2定义为预后良好。采用DSA、CTA或MRA评估患者血管通畅情况以及有无再狭窄。
2 结 果
2.1 手术成功率 44例患者共进行45次血管内成形术,技术上均成功,无一例失败。44次手术同期行球囊扩张+支架植入术(图1、图2),1例单纯球囊扩张后造影发现静脉早显明显,给予二期支架植入。45次手术中,44次达到mTICI 3级血流,1次达到mTICI 2b级血流。见表2。
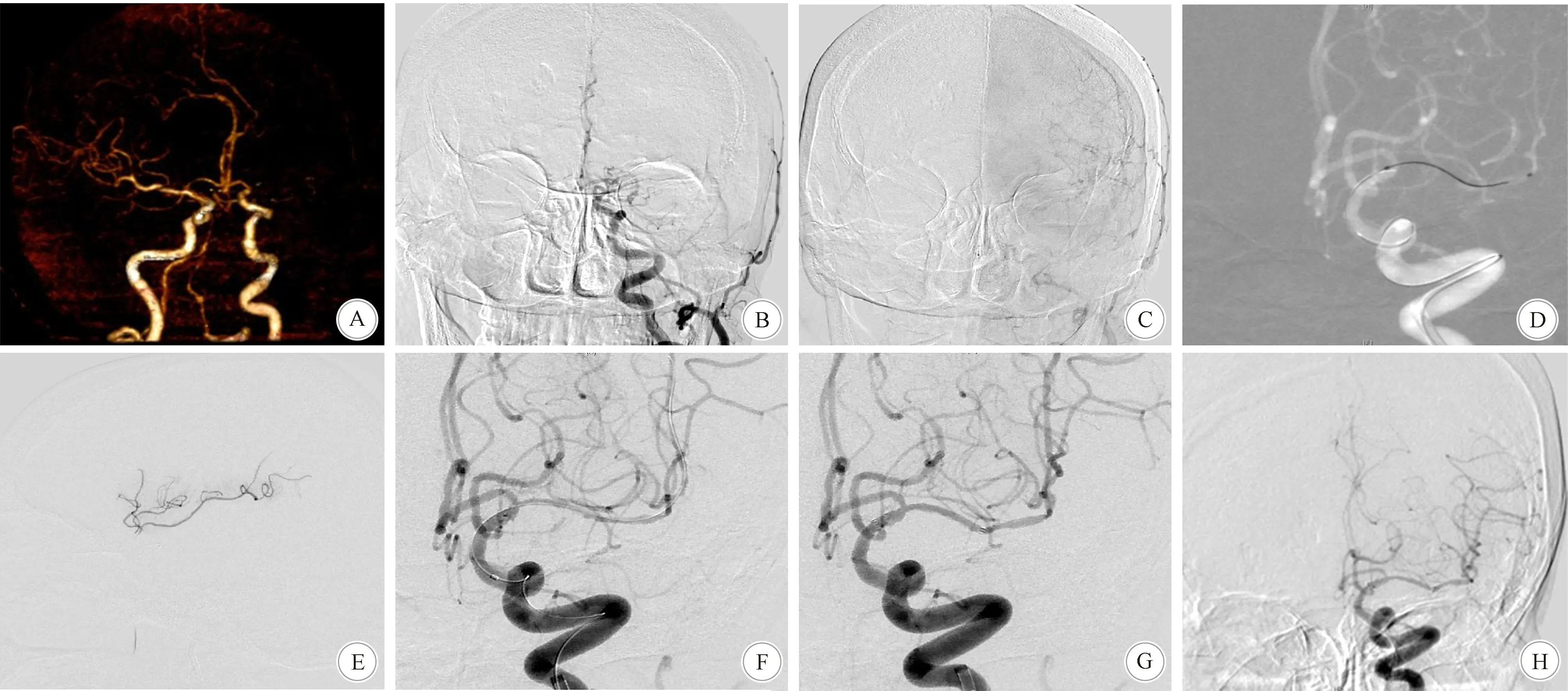
主诉“反复右下肢乏力20 d”; A:CTA示左侧大脑中动脉起始部闭塞; B、C:DSA是大脑中动脉起始部闭塞,造影晚期可见M2分支显影; D:微导丝引导微导管小心通过闭塞段到达M2分支; E:微导管造影提示微导管位于血管真腔内,远端血管通畅; F:1.5 mm×9 mm球囊扩张缓慢扩张闭塞段,造影提示血管通畅,mTICI 3级; G:同期植入一枚4.5 mm×22 mm Enterprise支架; H:半年后造影复查提示大脑中动脉血流通畅,未见狭窄图1 74岁女性患者CTA及DSA检查结果

主诉“头晕半年伴加重1个月”; A、B:DSA正侧位造影提示椎基底动脉近全闭塞; C、D:微导丝引导微导管小心通过近全闭塞段到达基底动脉中段,微导管手推造影提示基底动脉中上段血管未见严重狭窄,中段局部扩张; E、F:交换3米微导丝,从1.5 mm×9 mm球囊开始扩张狭窄段后继续更换2 mm×9 mm球囊继续扩张狭窄段; G、H:造影提示椎基底动脉狭窄缓解,血流mTICI 3级,同期植入一枚Enterprise支架; I-J:半年后DSA复查提示椎基底动脉未见狭窄,血流mTICI 3级图2 66岁男性患者DSA检查结果
2.2 临床结果及并发症 围手术期发生出血4例(1例术中交换导丝在M3段可能穿破血管,术后CT提示少量蛛网膜下腔出血,患者无任何症状;1例发生原额叶梗死区出血,保守治疗;1例发生基底节区高灌注出血保守治疗;1例术中发现静脉早显,术后出现基底节区大量出血导致脑疝)。3例患者出现围手术期缺血性事件(1例表现为言语不清,给予替罗非班治疗好转;2例MRI检查发现新梗死灶但患者无症状)。4例(9.1%)患者出院时mRS较入院时变差,其中1例脑疝死亡。见表2。

表2 手术结果
2.3 随访结果 术后6个月共37例(84.1%)进行了临床随访,35例(94.6%)表现为预后良好,1例患者因再狭窄出现卒中复发事件。31例(70.1%)患者在6个月内行影像学复查,28例(90.3%)患者血管通畅,未见明显狭窄或闭塞。1例(3.2%)出现轻度狭窄未手术干预,2例(6.4%)出现重度狭窄均给予再次血管内成形术。见表3。

表3 出院及随访结果
3 讨 论
本研究的血管内成形术治疗症状性非急性期颅内动脉狭窄或闭塞的围手术期出血和缺血并发症总发生率为15.6%,致死致残率为6.7%,手术技术相关并发症为2.2%,低于SAMMPRIS试验结果[2]。术后6个月的卒中复发率为2.7%,低于WASID研究结果[7],而mRS≤2分的患者占比达94.6%。国内的一些研究也显示,血管内成形术治疗症状性非急性期颅内动脉狭窄或闭塞具有较高的手术成功率和较低的并发症[8-11]。本研究认为这种结果可以归结于以下几个因素:(1)手术技术:术者的手术技巧和经验是决定手术成功与否以及并发症最重要的因素。SAMMPRIS研究中,手术者操作导致的并发症发生率明显高于国内的一些研究。其研究中心的入选仅需要手术者具备过去一年10例颅内支架手术操作。而研究表明,手术经验丰富的医生手术并发症发生率更低[12]。本研究中手术者均具备150台/年支架植入经验,手术操作并发症更低;(2)患者的评估与筛选:①患者原则上mRS≤2分,预期寿命>2年;②有责任血管相关的缺血症状或脑梗死证据,且脑梗死时间大于2周以上;③CTP有脑灌注不足的证据;④责任病变考虑动脉粥样硬化性质,且排除血管炎、夹层和烟雾病等;(3)合理的手术策略:所有患者在球囊扩张后支架植入前均常规行DynaCT检查。术中球囊扩张后造影发现静脉早显征象或CT检查提示可能出血,应避免同期支架植入而仅行单纯球囊扩张治疗;(4)严格的围手术期的血压管理和镇静治疗,防止术后再灌注出血。
随着人口老龄化的进展,脑卒中特别是缺血性脑卒中的发病率逐渐增加[13]。动脉粥样硬化引起的颅内动脉狭窄或闭塞是亚裔人群缺血性卒中的主要原因。2014年中国症状性颅内大动脉狭窄与闭塞研究结果显示,中国缺血性卒中或短暂性脑缺血发作患者中颅内动脉粥样硬化发生率为46.6%[4]。而对于颅内动脉完全闭塞的患者,1年后卒中再发风险高达7.27%,若合并多个危险因素,年卒中复发率甚至高达19.05%[4]。颅内动脉粥样硬化性狭窄或闭塞增加卒中风险的主要机制包括:(1)狭窄或闭塞处的血栓或动脉粥样硬化斑块脱落导致的栓塞;(2)脑低灌注导致短暂性脑缺血发作或分水岭梗死[14-15]。此外,长期脑低灌注引起的慢性脑缺血也可导致认知功能障碍和血管性痴呆[16- 17]。
对于症状性非急性期颅内大动脉狭窄或闭塞,选择药物治疗还是手术治疗一直存在争议[18]。抗血小板药物联合危险因素控制是颅内动脉粥样硬化性狭窄或闭塞所致缺血性卒中患者的主要药物治疗方案[19]。然而WASID研究显示患者缺血性卒中的两年发生率仍高达19.7%[3]。SAMMPRIS研究也显示,即使经过积极的双联抗血小板药物以及危险因素控制后,其30 d内的卒中或死亡率为5.8%,1年的主要重点事件为12.2%[2]。另一项研究显示药物保守治疗的两年内任何卒中的发生率高达26.9%,严重卒中发生率为4.8%[20]。因此,对于症状性非急性期颅内动脉狭窄或闭塞的患者,药物治疗效果不理想,积极的手术干预可能使患者获益,包括颅内外动脉搭桥术和血管内成形术。然而最佳的手术方式也存在争议。2011年Powers等[20]报道的颈内动脉闭塞患者颅内外动脉搭桥手术研究,结果并未证明颅内外动脉搭桥手术并没有使患者获益;同样的结果也被其他作者的研究证实[21]。
尽管SAMMPRIS和VISSIT实验结果并不支持血管内成形术应用于这部分患者[2,22],但随着神经介入器械及手术技术的发展,许多临床研究发现血管内成形术对于特定的患者仍具有潜在的获益[18,23]。一项关于症状性颅内动脉狭窄的支架成形术治疗效果的回顾性多中心研究显示,血管内成形术30 d内围术期并发症发生率为6.1%,远低于SAMMPRIS研究[8]。国内外多项临床研究显示血管内治疗对于狭窄率≥70%的症状性颅内动脉狭窄的技术成功率在99%以上,而30 d终点事件的发生率约6.7%~9.09%[9-11,24]。而对于症状性非急性期颅内动脉闭塞的患者,多个临床研究显示血管内成形术有效开通率在85.7%~100%,而30 d预后良好率约80%~94%[25-27]。本研究结果显示,对于症状性非急性期颅内动脉狭窄或闭塞的患者,手术技术成功率为100%,手术技术相关并发症为2.2%。术后6个月的卒中复发率为2.7%,预后良好的患者比例为94.6%。这些结果均提示,对于症状性非急性期的颅内动脉狭窄或闭塞患者,血管内治疗是可行有效的。
血管内成形术的围手术期并发症主要包括术中导丝刺破血管出血,球囊扩张过程中穿支撕裂出血,术后高灌注出血,支架内血栓、穿支闭塞或斑块脱落梗死等[25-29]。本研究中发生出血事件4例,一例为术中交换导丝在大脑中动脉M3段刺破血管,放置支架后即刻CT显示少量出血但患者无任何症状;一例为原梗死区出血,保守治疗后恢复良好;其余两例为术后高灌注出血,预后均不良。因此,如何降低围手术期并发症,进一步提高血管内治疗的安全性和有效性是未来研究的重点。
综上所述,对于症状性非急性期颅内动脉狭窄和闭塞,血管内成形术是安全、有效的方法,但必须严格评估与筛选合适患者且由经验丰富的手术医生进行手术。本研究为回顾性研究,病例为单中心、小样本,且随访时间较短,后期仍需要多中心的临床随机对照实验来进一步验证血管内成形术的安全与有效性。
利益冲突:所有作者均声明不存在利益冲突。
