二氧化钛光催化剂改性及制氢的研究进展
2022-08-26罗海南张宝营李凤丽
张 伟,罗海南,张宝营,李凤丽
(1.山东大学化学与化工学院,山东 济南 250100;2.枣庄学院化学化工与材料科学学院,山东 枣庄 277160)
能源问题是当今世界备受关注的热点问题之一。煤炭、石油、天然气等都是不可再生资源且对环境均有危害,因此寻找清洁可再生的能源迫在眉睫。氢能具有无污染、可再生、易运输等特点,是理想的可再生能源之一。传统的制氢方法主要有电解水制氢、热化学法制氢、人工光合作用制氢、生物制氢等,这些制氢方法需要的能量较高,不容易获得,因此限制了广泛制氢。
TiO2是一种N 型半导体材料,表面积大,带宽充足,所以具有极好的光催化活性。与CdS、SiC 等可用于光催化分解水产生氢气的半导体材料相比,TiO2光催化剂具有能耗低、反应无二次污染、性能稳定、反应条件平稳等优点,因此TiO2光催化成为一项新的绿色技术,引起了人们的普遍关注。氢主要存在于水中,用光催化分解水制氢,在制氢领域广泛应用。自1972 年,Fujishima 和Honda[1]发现TiO2光分解H2O 可以产生H2和O2以来,用半导体光催化制氢的研究,被认为是一项长期、高性能的战略性研究课题。光化学性能稳定的半导体TiO2,可以吸收更多的紫外线,但能量空间太大,对太阳光的利用率低,只有4%左右的紫外线能被利用。可见光占了太阳光总能量的45%,为了充分利用太阳能,人们对TiO2进行修饰,以提高TiO2吸收可见光的效率。目前对TiO2改性的方法主要有贵金属沉积、金属离子掺杂、非金属离子掺杂、离子共掺杂、染料光敏化、半导体复合等。本文综述了改进TiO2光催化活性的机理、TiO2在光催化制氢领域的研究进展,以及光催化制氢的影响因素。
1 光催化机理
TiO2是一种N 型半导体材料,有2 个能带(价带和导带),这样的结构使得TiO2可以吸收一定波长的太阳光。当TiO2表面受到太阳光的照射,价带中的电子吸收太阳光能后被激发到导带,价带上产生了空穴,导带上留下了电子。电子具有很强的还原性,因此价带的氧化性很强。电子和空穴可能会发生复合而释放能量,但有机物的降解并不需要这个过程,所以要抑制其复合。光生载流子催化的主要过程,是其跃迁到TiO2的表面,与有机污染物发生了氧化还原反应。在空穴处,H2O 和OH-被氧化成高活性的·OH,·OH 具有很强的氧化性,可以继续将表面的有机污染物氧化成H2O 和CO2。O2将导带中的电子捕获,将其还原成O2-。O2-的氧化性特别强,可以利用它的强氧化性,与H+发生作用,生成HOO·。HOO·也是很活泼的氧化自由基,可以继续发生反应,生成H2O2。最后O2-、·OH、HOO·这些活泼的氧化自由基对吸附在TiO2表面的有机污染物进行降解。TiO2光催化是基于电子和空穴可以有效分离,产生更多的活泼自由基,从而提高了光催化效率。光催化机理共有9 个步骤,具体见图1。
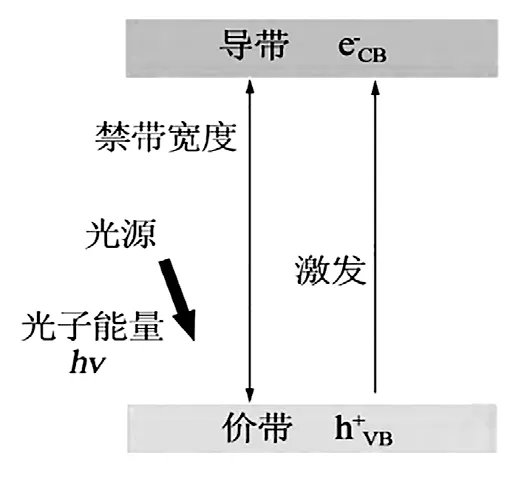
图1 光催化机理Fig.1 Photocatalytic mechanism
2 催化剂改性
2.1 贵金属沉积
贵金属沉积对TiO2光催化活性的提高有较大帮助。在研究中经常采用的贵金属掺杂元素有Pt、Pd、Ru、Ag 等。金属内部存在着自由移动的电子,不需要受到刺激就能在金属内部自由移动,这是金属与半导体最大的区别。当这些惰性金属沉积在TiO2上,或TiO2受到光激发后,TiO2导带的电子会自然地流向Pt 等惰性金属表面,这些惰性金属表面就会存在有电子,TiO2的价带上则会形成相应的空穴,因此有效分离空穴和电子,可以使TiO2表面的电极电势更负,从而使还原能力变得更强,TiO2光催化材料的活性变得更高。
刘守新等人[2]采用光化学沉积法,制备了在TiO2表面沉积金属Ag 的光催化剂,依据其对亚甲基蓝的降解速率,来测试光催化剂的活性。当使用0.1mol·L-1的AgNO3溶 液、1g 的TiO2、7 mL 的AgNO3溶液,AgNO3与Na2NO3的溶液体积比为2∶1时,亚甲基蓝的降解速率最高,光催化剂活性的提高最大。
2.2 金属离子掺杂
用金属离子掺杂的方法对TiO2进行改性的机理,是在TiO2的晶格中增加新的电荷,晶型类型由此发生了变化,晶格会产生缺陷,对电子的运动状况、跃迁速度产生影响,从而改变光催化速率。金属离子掺杂可以在TiO2表面产生缺陷或改变其结晶度,成为一个浅的光载流子捕获阱,TiO2会产生p-n型光响应共存的现象,从而延长时间并减少空穴与电子复合的可能性。
邓芳等人[3]以钛酸四正丁酯为原料,采用溶胶-凝胶法制备了掺杂Fe3+的TiO2光催化剂,测定了改性后的光催化剂对甲基橙的降解,探究了Fe3+的掺杂量对其降解效率的影响。实验结果表明,相同的煅烧温度下,掺杂Fe3+的TiO2粒子的直径比纯TiO2小。在自然光下,当Fe3+的最佳掺杂量为10.00%时,相应的脱色效率为28.37%,掺入Fe3+的TiO2,其光催化降解活性得到显著提高。
赵晨旭[4]采用正交实验方法,研究Cr3+、La3+掺杂的TiO2的光催化性能。结果表明,掺杂Cr3+后,TiO2由锐钛矿晶型向金红石晶型过渡的能力增强,晶粒变小,比表面积增大,对可见光的吸收能力增强,光催化活性得到提高,但随温度升高,光催化效率降低。掺杂La3+没有扩展对可见光的吸收范围,但是对晶型的相变有抑制作用,增大了比表面积,提高了光反应效率。掺杂量和反应温度都会影响光催化性能,温度过高或过低,La3+掺杂的TiO2光催化剂的活性都会降低。
刘国聪等人[5]采用研磨-溶胶法制备了掺杂Al 的TiO2材料。用甲基橙的降解率来评价Al/TiO2光催化材料的性能,结果表明,掺杂Al3+后,TiO2的颗粒变小,与纯TiO2相比,比表面积有较大增加,吸收波长变长。甲基橙浓度为20mg·L-1,降解率达到90%以上。
陆杰军等人[6]采用溶胶-凝胶法制得了掺杂Zn2+、V5+的TiO2光催化剂,用罗丹明B 的降解来研究其光催化活性。结果发现,二氧化钛由锐钛矿向金红石的转变,因掺入了Zn2+、V5+而改变得更快,光谱吸收范围更宽,紫外光吸收能力显著增强,光谱吸收谱得以扩大。
2.3 非金属离子掺杂
非金属离子是通过降低电子和空穴的复合,使电子增多,还原性增强,来提高光催化活性。用于非金属离子掺杂TiO2的主要有C、N、S 等元素,这些元素都有p 轨道电子,可以和O 轨道电子结合,也能够改变TiO2的能带宽度,其晶格内部也会产生一定的缺陷,这样就可以降低电子和空穴复合的几率,TiO2光催化材料的活性得以提高。
彭绍琴[7]采用简单的加热方法制得了S 掺杂的TiO2光催化剂。S 掺杂后,TiO2由锐钛矿相向金红石相的转变被阻止,晶粒的生长受到抑制,TiO2的吸收波长范围得到扩大,并向可见光方向移动,禁带宽度变得更窄。实验结果表明,TiO2掺杂S 后,甲基橙可在可见光下降解。在体系中加入H2O2可使降解速率加快,原因在于H2O2可以提供电子,使电极电势更负,还原能力更强。溶液呈酸性时,甲基橙有最快的脱色率。
由于掺杂元素不稳定,见光易分解,因此在实际中难以应用。科研人员探寻了一些辅助措施,以改善掺杂的非金属元素易分解而导致浓度降低的缺点,并对此进行了研究。
杨在志等人[8]借助超声辅助,采用溶胶-凝胶法制备了掺杂N 的介孔TiO2光催化剂。实验结果显示,高能超声的空化作用可以细化TiO2的晶粒结构,使晶粒均匀有序地排列,也可以增大N 掺杂的浓度,降低轨道能级,使TiO2光催化材料的能带宽度变窄,提高对光的吸收率和对有机物的催化降解速率。
从杨在志等人的研究可以发现,超声空化作用可以更显著地提高非金属掺杂的TiO2的光催化活性,今后可以借助此方法,寻找对降解有机污染物最有利的非金属离子。
2.4 离子共掺杂
单一的离子掺杂可以提高光催化活性,但效果不明显,因此,科研人员对离子共掺杂的TiO2进行研究。目前主要的共掺杂方法有N-B/TiO2、N-S/TiO2、N-W/TiO2、N-F/TiO2、N-V/TiO2等。
李琪等人[9]采用溶胶-凝胶法制得了V-N/TiO2,用苯酚模拟废水考察了V-N/TiO2的光催化活性。实验结果表明,在TiO2中共掺杂钒和氮后,表面积会增大,光吸收范围扩宽到了可见光区。在光催化下,苯酚的降解速度得到极大的提高,且V-N/TiO2重复使用多次后,催化活性仍能达到99%以上。
李晓辉等人[10]制备了F-N/TiO2光催化剂,用苯酚模拟废水考察光催化剂的催化活性。单一掺杂N,可将光的吸收范围拓宽到可见光区,掺杂F 则使TiO2的能带宽度变窄,有利于电子激发到TiO2表面。结果显示,适量的N-F 共掺杂,能够提高TiO2的光催化活性,增大比表面积,抑制锐钛矿晶相向金红石晶相的转变。
杨超等人[11]采用水热法合成了N-S 共掺杂的TiO2光催化材料,结果显示,TiO2晶型为锐钛矿,晶粒大小均匀,其降解甲基橙的效率特别高,达到98%以上。
共掺杂可以将吸收波长拓宽到可见光区,提高对光的吸收率,使TiO2的能带变窄,晶粒大小均匀,比表面积增大,降低电子和空穴的复合,所以共掺杂TiO2备受关注。但因用量及模拟物不太一致,因此难以得到最好的共掺杂TiO2体系光催化剂。
2.5 染料光敏化半导体
当能量大于导带和价带的宽度,才能有效利用太阳光能,但一些半导体的能量宽度只相当于紫外光的能量,所以科研人员开始研究一些与能量宽度大的半导体相近的染料,让其吸附在半导体表面,利用染料对可见光的吸收能力强的特点,扩宽吸收光谱的范围,提高对太阳光的利用。尤会敏等人[12]采用固体熔融法,制备了2,3,9,10,16,17,23,24-八羧基酞菁铁敏化二氧化钛的光催化材料,研究了其对亚甲基蓝、罗丹明B、酸性红、中性红等有机染料的降解效果。结果表明,降解100min 时,光催化材料对以上有机染料均有明显的降解效果。房永玲[13]采用水热法,分别制得了花状和球形的ZnO 颗粒,然后通过水热敏化和超声浸渍敏化法,合成了吲哚方酸菁染料与ZnO 复合的光催化材料,采用聚合诱导胶体凝聚法合成了TiO2纳米颗粒,通过浸渍敏化法合成了配比分别为1∶2、1∶3、1∶4、1∶5 的吲哚方酸菁染料敏化的TiO2复合光催化材料。实验结果表明,当配比为1∶3 时,光催化材料的活性最高,原因在于染料的敏化有利于电荷的跃迁转移。多次使用后光催化剂的稳定性仍保持良好,降解效率仍可以达到70%。同时还研究了其他染料结构敏化TiO2的性能,通过高斯几何分布,发现当染料敏化的TiO2通过氢键方式相连时,光催化活性最高。
2.6 半导体复合
半导体复合也是TiO2光催化剂改性的一种方法。半导体耦合体系是将2 种不同能隙的半导体结合在一起,2 种半导体之间的能量差要大,以使电子能从一个导体传输到另一个导体中,从而解决催化剂的可见光吸收能力小以及电子-空穴易复合的问题。半导体催化的机理见图2。

图2 半导体复合催化的机理Fig.2 Mechanism of semiconductor composite catalysis
杜欢等人[14]采用浸渍法合成了MnO2和ZnO半导体复合TiO2光催化材料,研究了复合的半导体材料对甲苯模拟废水的降解性能,以评价光催化材料的活性。实验结果显示,当MnO2与ZnO 的质量和与TiO2的质量比为1∶2 时,改性的光催化材料对光的吸收率和甲苯的降解效率最好。
曹春华等人[15]采用溶胶-凝胶法合成了氧化石墨烯复合TiO2光催化剂,通过太阳光对艳红X-3B溶液的降解效率,探究该材料的光催化降解活性。实验结果表明,氧化石墨烯的表面均匀沉积了TiO2小晶粒,增大了比表面积。当有机染料的浓度为100mg·L-1,催化剂的用量为0.8g·L-1时,艳红X-3B溶液的降解速率最大,催化剂用量增大时降解速率降低。氧化石墨烯复合TiO2光催化材料可以提高光催化制氢的活性,但会受到浓度和用量的限制,难以进行实际的应用。
李银辉等人[16]采用溶胶-水热法合成了掺杂WO3的SiO2/TiO2的复合光催化材料,并研究了其对甲基橙的降解效率。结果表明,半导体复合的TiO2抑制了其晶粒的聚集,提高了TiO2的稳定性,因此,该光催化剂的活性较大。虽然半导体复合体系的窄能量隙系统满足了能量水平的要求,但该复合体系见光易腐蚀,限制了该体系的应用。
3 光催化制氢的研究进展
3.1 贵金属沉积制氢
高丹等人[17]采用光沉积法制备了TiO2沉积Pt的光催化剂。在水中加入乙二醇,实验结果表明,乙二醇被用作光催化分解水制氢的电子供体,有利于电子在二氧化钛表面与氢离子结合,所以乙二醇可以明显提高光催化分解水制氢的效率,光催化效率得到提高,也有利于自身的降解。在TiO2表面,乙二醇污染物的吸附符合 Langmuir 吸附模型。溶液呈一定的弱碱性时(pH 约为8),光催化活性最高。当不同的物质与乙二醇共存时,对光催化制氢的效率也会产生不同的影响,如甘油会起到促进的作用,葡萄糖则会抑制光催化效率(表1)。

表1 不同物质对乙二醇制氢的影响Table 1 Effects of different substances on hydrogen production by ethylene glycol
徐俊英等人[18]采用水热合成法制得了001 晶面的高性能TiO2,通过光还原沉积法,在其表面沉积Pt,合成了Pt/TiO2,最后用浸渍法得到了伊红Y 敏化Pt 沉积的TiO2光催化材料。通过光催化制氢的效率来测定改性后材料的活性,实验结果表明,加入HF 后001 晶面会变多,HF 的量越多,得到的晶面越多,比表面积得到增大。在Pt/TiO2上,敏化染料也受到HF 量和比表面积的影响,当晶面为001、HF用量为3mL 时,对染料的吸附最强。当氟化氢用量为3mL 时,改性后的二氧化钛光催化材料的制氢效率达到95%以上。氟化氢的用量高于或低于3mL时,制氢效率会有明显降低。在可见光下,不含氟的二氧化钛光催化材料的制氢活性,低于3mL、含HF的光催化材料的活性。这是因为F 具有很强的吸电子性,可以与Ti 及O 发生作用,与吸附在TiO2表面的·OH 和染料中的O 形成氢键。当Pt 的沉积量达到1wt%时,材料的制氢活性达到最高,沉积量为0.02wt%时,光催化剂的制氢效率较高,原因是Pt的比表面积大,颗粒均匀,可提高光催化剂材料的制氢活性。由于此光催化剂的Pt 用量少,因此可以被广泛应用。
周美华等人[19]通过水热合成法和超声空化作用,合成了沉积薄层MoS2的TiO2,并研究了该催化剂的制氢效率。实验表明,MoS2的沉积扩宽了TiO2对可见光的吸收范围,溶剂DMF 使得MoS2的粒径变小,厚度变薄。当MoS2的沉积量为1.6 wt %,用DMF 作溶剂时,添加PVP 可使MoS2的分布更均匀。在可见光的催化下,新合成材料的制氢活性得到很大提高。溶液的pH 以及甘油的浓度会对光催化剂的制氢活性产生影响。当体系的pH 等于剥离MoS2沉积TiO2的电荷零点时,制氢效率最高。
3.2 金属离子掺杂制氢
弓莹等人[20]直接合成了TiO2掺杂Ag 的光催化材料,实验结果表明,在TiO2中掺杂Ag,可以使晶粒变细,比表面积增大,扩宽对可见光响应的范围。银离子的掺杂量为0.5%时,TiO2光催化材料的制氢效率最高,降解有机污染物的效果也最好。
彭邵琴等人[21]采用溶胶凝胶法合成了掺杂Ru的TiO2,以及掺杂Ru、SiO2的TiO2。实验研究发现,Ru 和Si 的掺入,能够阻碍TiO2的晶型转变和晶粒的聚集,降低电子和空穴的复合机会,将光的吸收范围扩大到可见光区,因此光催化材料的活性得到提高。当Ru 在TiO2中的掺杂量(质量分数)为0.014%,Ru 在复合SiO2的TiO2中的掺杂量为0.021%时,在可见光下,材料的催化制氢效率都可以达到最高,且在复合SiO2的TiO2中掺杂Ru,材料的催化活性大约比未复合的材料高5 倍。
3.3 非金属离子掺杂制氢
彭邵琴等人[22]采用溶液凝胶法和浸渍法,合成了伊红-Y 敏化掺杂S 的TiO2光催化材料,研究了其制氢效率,以评定光催化材料的化学活性。实验结果表明,染料敏化后,TiO2光催化剂对可见光的响应范围得以扩宽,在可见光区的吸收增强;S的掺杂阻碍了TiO2晶粒的聚集,增大了比表面积,材料对染料有强的吸附,因此可以提高TiO2在可见光下分解水制备氢的效率。当TiO2和S 的物质的量之比为1∶4,600℃下煅烧,伊红-Y 的浓度为0.005mol·L-1时,伊红-Y/S/TiO2在可见光下的制氢效率最大。温度过高会使晶粒聚集,S 可能会被空气氧化而脱离TiO2的表面;温度过低则不易结晶。S 掺杂量多时,会产生电子和空穴复合的缺陷。染料敏化的浓度增大会使活性升高,但达到0.005mol·L-1后,再增大浓度,活性会迅速降低。因此以上条件都需要一个最佳值。
3.4 离子共掺杂制氢
吴琛等人[23]采用溶胶凝胶法,制得了La、Eu、Nd、Tb、Er 等分别与S 共掺杂的TiO2光催化材料,研究了光催化剂的制氢效率以评价催化剂的活性。实验表明,用这些稀土元素掺杂,可以使晶体的颗粒变小,大大提高光催化剂的活性。稀土元素和S 共掺杂后改变了TiO2的活性顺序,分别是Eu >La >Nd >Tb >Er。
3.5 染料敏化制氢
刘兴等人[24]通过偶联Al3+或者Fe3+,分别制备了多层EosinY 敏化的TiO2光催化剂。采用沉积Pt的方法,研究了二者在可见光下的制氢效率和稳定性。实验结果表明,含水为0.5%(体积分数)的体系,载铂量为1.0%时,Al3+具有较高的活性和良好的稳定性。偶联Fe3+制备的多层敏化TiO2,吸附染料和吸收可见光的能力增强,传输电子的效率加快,光催化活性也有明显提高。但是该光催化材料的稳定性差,寿命短。通过对比研究,Al3+制备的敏化材料,其光催化活性和稳定性比Fe3+的敏化材料高,原因是Al3+的水解程度比Fe3+小。若在水中加入少量的甲醇,可抑制Al3+和Fe3+的水解,提高敏化材料的稳定性和光催化效率。
刘雄鹰等人[25]用SiO2改性TiO2,以染料伊红-Y作为敏化剂,制备了具有较高可见光活性的催化剂EosinY-TiO2/SiO2。采用溶胶凝胶法和浸渍法制备了Eosin Y 染料敏化光催化剂EosinY-TiO2和EosinY-TiO2/SiO2,研究了其在可见光条件下催化制氢气的效率。研究结果表明,TiO2被伊红-Y 敏化后,其对可见光有强的吸收。SiO2的复合可以减弱TiO2由锐钛矿向金红石晶相的转变,降低晶粒的聚集生长。SiO2的复合使TiO2吸附染料和吸收可见光的能力增强了,也有助于电子和空穴的分离,因此TiO2的光催化活性和稳定性都提高了。
由于染料敏化在TiO2表面的吸附量小,所以科研人员研究了一些催化剂作为辅助,以提高染料敏化光催化制氢的效率。李越湘[26]制备了石墨烯基HER 助催化剂,实验发现,镍石墨烯复合材料的HER 活性,比任何一个未复合的活性都要高,结果可归因于协同效应。形成纳米结构以及控制MoS2在石墨烯硫化镉上的负载,都可以产生协同效应。
3.6 半导体复合制氢
CdS 是常用于半导体复合TiO2的一种物质,因其对可见光不稳定,容易被光腐蚀,为了提高光催化活性,常与其他半导体复合(TiO2、SiC 等)。为了增强CdS 的活性,常用高温来煅烧,但高温会使CdS被氧化,因此在制备光催化剂时需要更高的实验条件要求,从而导致制备成本高,不能被大量应用。彭邵琴等人[27]采用不同的方法合成了CdS 复合沉积Pt 的TiO2。通过实验发现,直接机械混合后,没有煅烧的CdS 有较低的结晶度,会提高电子和空穴的捕获能力,因此可以大大提高光催化制氢的活性。与之前制备催化材料的工艺相比,机械混合的流程简单,温度较低,制氢效率更高。当TiO2和CdS 的物质的量之比为1∶4 时,在可见光下有最佳的制氢效率。即使在长时间的光照射下仍可以产生氢气,放氢速率是142μmol·h-1。
彭绍琴等人[28]采用水热法合成了晶型为单斜的CdS 复合Pt 的TiO2光催化材料,研究了其在可见光下催化纯水和海水的制氢效率,通过制氢效率来表征光催化剂的性能。实验结果表明,在海水中的制氢效率比纯水高(约为33%),原因是海水中含有无机盐,可以降低电子和空穴的复合机会,提高电子俘获空穴的能力。而且在海水中CdS 的晶型会由单斜型转变成立方及立方与六方的混合型,因此在海水中可以提高光催化材料的制氢活性。
4 影响光催化性能的因素
4.1 溶液pH
高丹等人研究了溶液pH 对以二氧化钛乙二醇为电子供体的体系的光催化降解的影响。实验结果表明,pH 在4~8 之间,光催化制氢的活性呈线性增大;pH=8~13 时,反应速率下降;pH 在等当点附近(pH=7~8)时,光催化制氢的效率最高。原因是pH影响光催化活性,是通过影响催化剂的表面特性、表面吸附和化合物存在的形态而实现的。体系存在酸碱平衡,当pH=8 时溶液中的OH-浓度较大,活性较高,促进了乙二醇被氧化,同时表面有大量的乙二醇被吸附,从而提高了光催化制氢的活性。
4.2 催化剂的晶体结构
组成上相同但晶格不同的光催化剂,其活性有很大的差异。锐钛型TiO2的光催化活性比金红型高,可能是因为锐钛矿的能带比金红石宽,处于不稳定的过渡态,所以锐钛矿的晶格价带和导带间的能极差大于金红石,氧化还原能力也大于金红石。
刘红霞和杨春[29]以TiCl4和钛酸异丙酯为原料,制备了介孔TiO2材料,以甲基橙的脱色速率来研究其光催化性能。实验结果表明,与无介孔结构的TiO2相比,有介孔的TiO2的光催化效率更高,由此可知晶型可以影响光催化活性。
如果晶体生长得不好,在内部会产生相应的晶格缺陷,也会影响光催化剂的活性。金红石型TiO2晶格产生的缺陷是氧空位,继而成为反应活性中心,同时也可能成为光生电子-空穴的结合中心。
晶粒的大小对光催化活性也会产生影响。晶体粒子的直径越小,电子和空穴在本体结合的可能性越小,量子效率就越高。此时,禁带能量隙增加,禁带边缘发生移动,加强了半导体TiO2的氧化还原作用,提高了光催化性能。颗粒直径越小,原子可以快速增多,使得反应活性增强。比表面积越大,紫外光的吸收效率加大;比表面积越小,对紫外光的吸收能力增强。
4.3 受激电子-空穴对的存活寿命
电子-空穴间的复合和水之间发生的氧化还原反应是共存的。降低电子-空穴复合的概率,延长寿命,提高光催化活性的方法,主要有以下一些。
4.3.1 贵金属沉积
TiO2负载Pt、Ru 等惰性金属后,金属本身就有可自由移动的电子,受到光激发后,金属的自由电子自然进入TiO2中,光催化活性得到提高。
4.3.2 金属或非金属离子掺杂
离子掺杂是在TiO2的价带与导带间形成一个宽的能级差,光生电子可以自由移动,受到光激发后,电子自然地由价带传输到导带,从而抑制了光生电子-空穴的复合。
4.3.3 半导体复合
在半导体复合中,具有窄带隙能量的硫化物、硒化物及其它半导体等,会与TiO2相互作用。2 种半导体之间的能量差要大,以使电子可以从一个导体传输到另一个导体中。
4.3.4 光敏化
光敏化剂吸附在光催化剂的表面,这些物质的活性大,容易被激发而产生自由电子,然后传输到半导体的导带上,有效地将电子和空穴分离,从而抑制光生电子与空穴的复合,提高光催化活性,扩大光吸收范围。
4.3.5 光催化剂的表面结构
采用一些表面修饰的方法,可增大光催化剂的比表面积,影响催化剂表面的缺陷,从而提高光催化剂的制氢效率。
4.4 光强
光照强度较低时,光催化剂的制氢效率与光的强度成线性关系;光强增强到中等强度时,制氢速率与光强的平方成线性关系。光源和反应物质之间的距离也会影响光催化活性,二者间的距离越小,相当于光强变强了,催化剂的催化活性就提高了[30]。
4.5 反应物浓度
反应物浓度的影响也有一个最佳值。浓度较低时,光催化效率与反应物的初始浓度符合Langmuir-Hinshelwood 方程式。随着浓度增加,反应速率呈线性增大,但浓度增加到一定值后,反应速率趋于平稳,几乎不再变化,即不再受反应物浓度的影响。
5 结语
采用贵金属沉积、金属离子掺杂、非金属离子掺杂、离子共掺杂、染料光敏化、半导体复合等方法对TiO2光催化材料进行改性,可以降低电子和空穴复合的机率,提高对可见光的吸收,提高光催化制氢的活性,制氢效率可达90%以上,但光量子效率只有10%左右。目前TiO2光催化制氢已取得了很大成就,但仍存在一些不足,需要通过更深入的研究加以解决。
1)寻找可提高二氧化钛光催化活性的物质,对二氧化钛进行更高活性的改性,是当前要解决的首要问题。
2)二氧化钛的能隙宽,对光的利用效率低,用于处理大量污染严重的污水时特别困难。因此光催化降解水制氢的机理有待进一步的深入研究,以提高对光子的利用率,从而可应用于生产生活的各个方面。
3)在研究二氧化钛光催化剂的制氢活性时,所用的目标降解产物不同,如甲基橙、亚甲基蓝、罗丹明B 等物质,采用的光源也多样化,如高压汞灯、自然光源等,导致科研人员在通过分析比较数据,以获得具有高催化活性的制氢材料时比较困难,今后有必要控制实验条件。
4)二氧化钛的回收及对太阳光的利用,容易受天气的影响,这些问题也需要加以考虑。
