温度和还原剂对LNT还原过程的影响
2022-08-25李志军李世龙帅石金刘世宇刘铭礼
赵 金,李志军,李世龙,帅石金,刘世宇,刘铭礼,王 妍
温度和还原剂对LNT还原过程的影响
赵 金1,李志军1,李世龙1,帅石金2,刘世宇2,刘铭礼1,王 妍1
(1. 天津大学内燃机燃烧学国家重点实验室,天津 300072;2. 清华大学汽车安全与节能国家重点实验室,北京 100084)
针对稀燃氮氧化物捕集器(LNT)还原过程中的产物和副产物,搭建了以CO和H2为还原剂的LNT还原模型,该模型包含了LNT还原过程中副产物N2O和NH3的详细产生机理.利用该模型模拟研究了温度对N2、N2O和NH3表面反应的影响,分析了温度和还原剂体积分数对LNT还原效率的影响.模拟研究结果表明,CO还原NO时,在低温下易生成N2O,在高温下生成N2,并且随着温度升高,NO和CO的转化率逐渐增加并到达最大值;H2作为还原剂时,在低温条件下会同时生成N2O和NH3,NH3生成速率更高,高温时还原的主要产物是N2;NO/H2反应中,NO转化率在低温时先升高后降低;随着CO体积分数的增加,NO和CO的转化率会先升高再降低,过高的CO体积分数会抑制NO的转化率,但是提高温度可以缓解这一问题.
稀燃NO捕集器(LNT);NO还原;还原剂;温度
与传统的按当量比工作的汽油发动机相比,稀燃汽油发动机由于其优越的燃油经济性越来越受青睐.然而,由于氧阻抑作用,在稀燃条件下传统的三元催化转化器不能有效减少发动机尾气中的NO排放.为此,必须进一步完善排放后处理技术.针对NO排放,目前研究较多且应用广泛的后处理技术主要有选择性催化还原技术、NO催化分解技术和稀燃NO捕集(LNT)技术等[1].LNT技术又被称为NO储存还原,是稀燃NO排放控制领域研究的重点之一.LNT催化器结构简单,表面含有碱土金属和贵金属,分别为NO的储存位点和还原位点[2].LNT工作原理主要分为稀燃和浓燃两个阶段.在稀燃阶段,NO以硝酸盐或亚硝酸盐形式储存在催化器载体上;在浓燃阶段,利用尾气中的还原性气体(CO、H2和HCs等)将NO脱附并还原为N2和其他产物[3].LNT催化器兼顾了发动排放性和燃油经济性,因此受到广泛关注.
国内外学者已进行了大量关于LNT的研究,提出了许多不同的机理,但尚未形成统一定论.Mulla等[4]以H2为还原剂研究了Pt/BaO/Al2O3型NO储存还原催化器的再生过程.Nova等[5]利用H2为还原剂对LNT还原机理进行了研究,发现还原过程中会产生氨气,但氨气可以进一步与硝酸盐反应生成N2.Forzatti等[6]利用CO还原再生LNT过程中发现在近等温条件下储存在Pt/Ba/Al2O3上的硝酸盐主要通过Pt催化途径还原,而不是通过硝酸盐的热分解.此前多名学者[7-9]研究还发现在CO还原氮氧化物的过程中会形成稳定的异氰酸盐或氰酸盐,之后这些物质被水解为NH3,然后与NO或在氧气存在下储存的NO反应生成N2.同时,Bion等[10]和Scholz 等[11]利用FTIR光谱在Pt/Rh/Ba/Al2O3和Ag/Al2O3催化剂上观测到了氰酸盐与氧气反应生成N2和CO2,并且在催化剂上进行了储存和还原的循环试验.在还原产物分析方面,DiGiulio等[12]研究了储存/还原循环时间对NO、CO和C3H6转化率以及NH3和N2O选择性的影响.Zhu等[13]主要从反应的发生入手,分析了以C3H6为还原剂在NO储存还原过程中N2O的形成.Li等[14]分析了LNT中HCs与NO的氧化还原反应过程.曹曼曼等[15]和刘世宇等[16]研究了不同还原剂对稀燃NO催化转化器的转化效率,并分析了CO2和水蒸气对催化器的影响.李明宣等[17]制备了Co改性水滑石基LNT催化剂,并分析了其NO还原性能.
本文采用模拟计算的方法,建立了CO和H2还原NO的化学反应动力学模型,模拟LNT还原阶段.利用文献中的试验结果对模型的合理性进行了验证,分析了温度对还原过程中基元反应反应速率的影响,研究了还原剂摩尔分数对LNT还原效率的影响及规律.
1 数值模型建立
1.1 反应器模型
完全搅拌反应器(PSR)模型是Chemkin软件中的反应模型,用于模拟LNT的NO储存还原过程和机理.它是由气相化学反应和表面化学反应组成的耦合系统,其中化学动力学过程起着主导作用.在建立模型之前,对模型有一些假设和限制.首先,模型内部气相到表面的质量传递是无限快的,即反应物到产物的转化率是由化学反应速率控制的而不是混合过程.其次,通过反应器的流量是一个标称停留时间表示的,该标称停留时间可以从气体流量和反应器体积推导出.基于以上假设,下面列出了PSR反应器模型中使用的方程式.
反应器质量守恒方程,如式(1):


表面物质的质量守恒方程,如式(2):
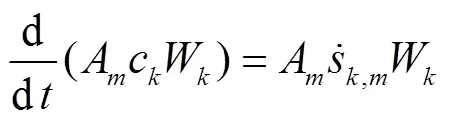
1.2 动力学方程
在表面反应中,某一组分的净生成速率为各基元反应中该组分反应速率的和,如式(3)所示:
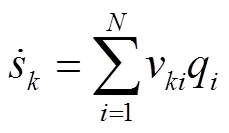

1.3 反应机理
在以往学者试验和模拟的基础上[18-21],本文以气相化学反应速率和表面化学反应速率为依据,基于Chemkin构建了包含气相和表面相,以H2和CO为还原剂的NO还原反应机理.该机理包含了10种气相组分(NO、NO2、CO、H2O、NH3、O2、H2、CO2、N2O和N2)以及14种表面组分,共计27步基元反应.下面列出了NO还原过程中的几组基元反应.
式(5)~(7)为NO吸附和解离以及N2的生成:


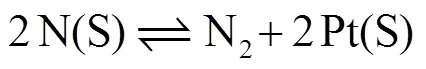
式(8)~(10)为表面N2O(S)生成和脱附反应:

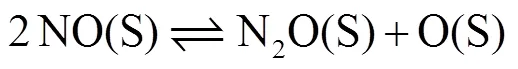
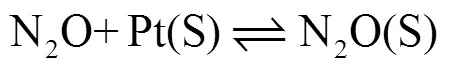
式(11)~(15)为表面NH3(S)的生成反应:

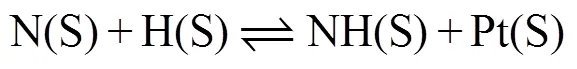
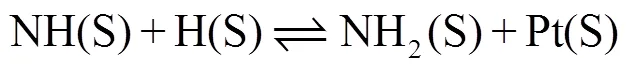
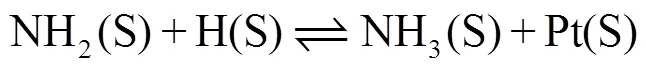

在之前的研究中,H2是还原性很强的还原剂[14],但是在实际的发动机废气中其含量不占据主导地位,一般可以由CO和H2O发生水煤气变换反应产生,如反应式(16):

在以上的所有反应中(S)表示表面吸附态.
2 模型验证
本文对Larson等[18-19]的NO还原反应试验进行了模拟,该试验在流动反应器中进行,所使用的催化剂配方为Pt/BaO/Al2O3,催化器样品来自于GDI汽油机的后处理组件.试验所用催化器参数如表1所示,详细的过程参见文献[18-19].模拟的进气组分NO、CO和H2均为500×10-6,模拟温度为75~500℃,并且所有模拟计算中都包含5%H2O和5%CO2,以N2为平衡气.
表1 LNT催化器参数

Tab.1 Parameters of LNT catalyst
图1所示的是LNT出口气体体积分数模拟结果与试验结果的对比.图1(a)中还原剂为CO,可以看出随着温度的变化,模拟的结果与试验结果尽管在数值上有一些差别,但是它们都有相同的趋势.在低温区间,NO还原会趋向于产生N2O.从图1(b)中可以看出H2为还原剂时模拟的结果和试验结果也比较吻合,模拟结果同时反映出了试验结果的一些特征.在低温条件下,模拟的还原产物体积分数偏高,是因为模型没有考虑传热和传质,还原反应速率很快.从图1中得到反应器出口NO体积分数的最大相对误差在10%以内,该模型可以应用于本文NO还原反应的研究,即验证了所建模型的正确性.

图1 模拟与试验催化器出口气体体积分数对比
3 结果分析与讨论
3.1 表面产物路径分析
如前所述,CO和H2在还原过程中会产生N2O和NH3副产物,而机理中也考虑到了副产物的生成与分解.当还原剂为CO时,表面N2O(S)和N2生成路径的反应速率随温度变化关系如图2所示.从图中可以看出温度低于175℃时,反应(9)的反应速率是高于反应(7)的,因此在这一段温度区间内,表面N2O(S)的生成占主要地位.当温度高于175℃时,反应(7)的反应速率高于其他两个反应,此时还原产物以N2为主.对于表面N2O(S)生成而言,温度低于275℃,表面反应(9)的反应速率远远高于表面反应(8),表明在这一温度区间,表面吸附态NO(S)更倾向于直接生成N2O(S).而当温度高于275℃时,表面NO解离生成的N(S)更倾向于生成表面N2O(S).

图2 表面N2O(S)和N2生成路径的反应速率随温度变化关系
当H2作为还原剂时在低温区间除了生成N2O外,还生成了NH3.图3所示为H2还原NO时表面反应(7)、(8)、(9)和(12)的反应速率随温度变化关系.表面反应(7)、(8)和(12)分别代表了表面N(S)的三种消耗途径,NH(S)是形成N2O和NH3的关键中间体[20].图中可以看出在100℃~230℃温度区间内,表面NH(S)生成的反应速率均高于生成N2和表面N2O(S)的生成反应速率,因此在这一温度区间内,表面NH3(S)的生成占主导地位.当温度高于230℃时,基元反应的反应速率随着温度的增加逐渐降低,而N2的生成速率保持不变,此时表面解离的N(S)趋向于生成N2.
此外值得注意的是,与CO还原剂不同,表面N2O(S)的生成路径有所改变.从图3可以看到,尽管在100℃之后表面基元反应(8)的反应速率逐渐增加,但是仍然处于比较低的数量级.因此,对于表面N2O(S)而言,其生成的路径更加趋向于表面吸附态NO(S)直接生成.
3.2 温度对还原效率的影响
温度对于表面催化反应至关重要,温度通过影响表面反应的速率来影响催化转化器的转化率.图4和图5分别所示的是CO和H2作为还原剂时,NO和还原剂的转化率随温度的变化.图中可以看出还原剂CO和H2对NO转化率有不同的影响.
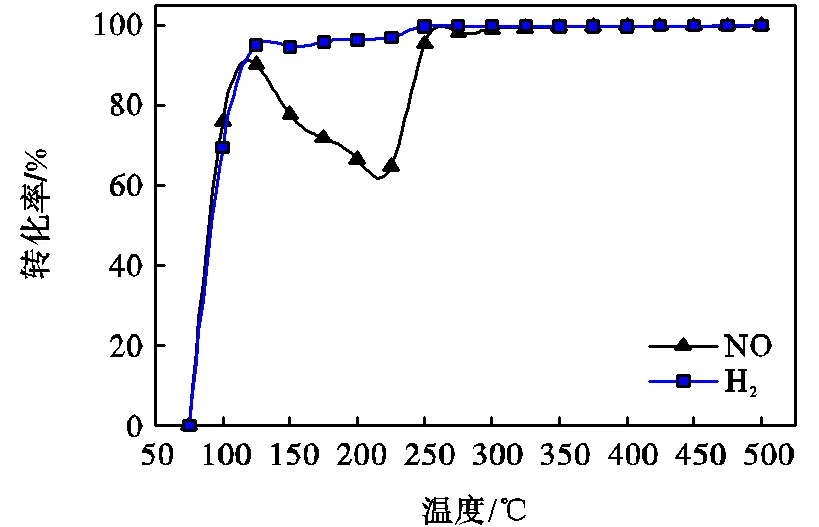
图5 温度对NO和H2转化率的影响
图4中随着温度的增加,CO和NO的转化率先是逐渐增加,在达到最高转化率后略微有所下降.在低温时,NO的转化率高于CO,这是因为在低温区间反应(8)和CO(S)对表面O(S)的竞争,使得表面吸附的CO不能有效转化为CO2.图5中NO的转化率与图4有明显差别,除了NO转化率上升比较快之外,在125℃~225℃之间,NO转化率下降了30%.出现这一变化的主要原因是表面生成的N2O(S)与H2反应又生成了NO,使NO的转化率下降.图1(b)中这一温度区间N2O的体积分数降低也可以说明这一点.
3.3 还原剂体积分数对还原效率的影响
结合学者们关于LNT催化器表面机理的研究,对表面还原反应有了更深入的了解.在还原过程中,气相物质需要先吸附在表面贵金属上,再发生解离脱附等过程.但对于催化器而言,表面的活性吸附位点的数量是一定的,因此在本研究中气相中的还原剂体积分数对催化器的转化率有一定的影响.
图6所示的是还原剂体积分数对NO和CO转化率的影响.由于H2的还原性很强,还原剂体积分数的增加对转化率的影响不大,这里只研究CO的体积分数变化.这里分别在3个温度条件下(200℃、250℃和300℃)对CO体积分数从1×10-4到1×10-3进行模拟,其他条件保持不变.

图6 CO体积分数对NO和CO转化率的影响
从图中可以看到,在200℃时,随着CO体积分数的增加,NO的转化率先是增加,之后迅速降低到43%.关于这一现象,许多学者也进行了研究.在苏庆运等[22]和Granger等[23]的研究中,CO体积分数增加并不能让NO转化率持续升高.在一般情况下,吸附在表面的CO(S)会与表面O(S)结合并脱附,为之后的反应提供活性位点.然而在低温条件下,N(S)会与O(S)结合生成N2O(S),使表面CO无法脱附,表面覆盖度随着CO体积分数升高而增大,表面活性位点变少导致NO和CO转化率降低.从图中可以看到,随着温度升高,这一现象得到缓解.这是因为随着温度的升高,表面N2O(S)生成减少,CO的脱附反应速率有所提高,表面的活性位点增加,使后续反应可以顺利进行.因此在LNT还原过程中,温度和CO体积分数对催化剂表面的影响不可忽视.
水蒸气对CO的还原过程也有影响,水蒸气可以和CO发生水汽转换反应生成H2,也可以与CO还原的中间产物异氰酸(NCO)发生水解反应生成NH2.图7所示为300℃时上述反应的表面反应速率随CO体积分数变化关系(水蒸气体积分数为5× 10-4).随着CO体积分数增加,水汽转化反应的反应速率增加,在CO和H2O体积分数比为0.9到1.1之间增加较快.另一方面,中间产物NCO(S)生成和水解反应速率也随着CO体积分数增加而增加. NCO(S)的生成使一部分CO以中间产物的形式储存在了催化剂表面,从而降低了CO的转化率.
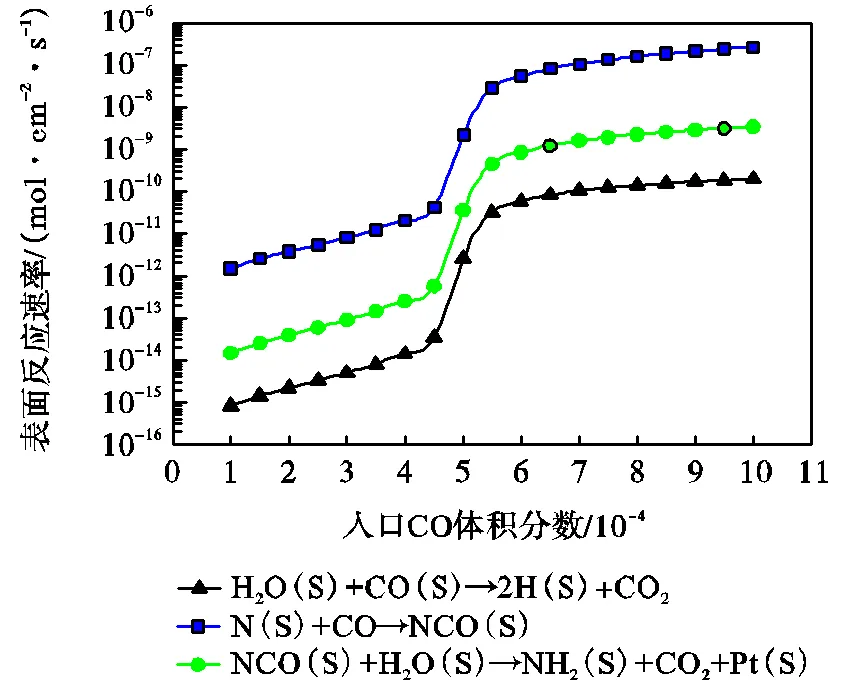
图7 CO体积分数对NCO(S)生成和水解反应速率的影响
4 结 论
(1) CO为还原剂时,在温度低于175℃时,表面N2O的生成占主导地位;温度高于175℃时,还原的产物主要是N2.此外,温度影响生成N2O的路径.当温度低于275℃时,倾向于表面NO生成表面N2O的反应路径;温度高于275℃时,则倾向于表面N(S)生成表面N2O.
(2) H2作为还原剂时,在低温度区间同时存在N2O和NH3两种副产物.在100~230℃温度区间,还原产物NH3占主导地位;在230℃之后,还原的主要产物是N2.随着温度的升高,表面N2O的生成速率逐渐降低.
(3) 随着温度增加,CO和NO的转化率逐渐增加并达到最大,H2还原NO时转化率有所不同.H2转化率在低温增加地更快,但是在125~225℃之间,NO转化率下降30%左右,这是因为在这一温度区间表面N2O(S)和H(S)反应生成NO.
(4) 在CO体积分数对NO转化率的影响模拟中,随着CO体积分数的增加,在温度200℃条件下,NO转化率先增加后降低近50%.随着温度的升高,表面CO脱附速率提高,对NO转化率有一定积极的作用.
[1] Praveena V,Martin M L J. A review on various after treatment techniques to reduce NOemissions in a CI en-gine[J].,2018,91(5):704-720.
[2] Wang P,Yi J,Sun C,et al. Evaluation of H2influence on the evolution mechanism of NOstorage and reduc-tion over Pt-Ba-Ce/γ-Al2O3catalysts[J].,2019,5(3):568-575.
[3] 曹丽娟,李志军,李世龙,等. EGR率对LNT吸附路径及净化效果的影响[J]. 燃烧科学与技术,2019,25(6):549-555.
Cao Lijuan,Li Zhijun,Li Shilong,et al. The effect of EGR rate on LNT adsorption path and purification ef-fect[J].,2019,25(6):549-555(in Chinese).
[4] Mulla S S,Chaugule S S,Yezerets A,et al. Regeneration mechanism of Pt/BaO/Al2O3lean NOtrap catalyst with H2[J].,2008,136(1/2):136-145.
[5] Nova I,Lietti L,Forzatti P. Mechanistic aspects of the reduction of stored NOover Pt-Ba/Al2O3lean NOtrap systems[J].,2008,136(1/2):128-135.
[6] Forzatti P,Lietti L,Nova I,et al. Reaction pathway of the reduction by CO under dry conditions of NOspecies stored onto Pt/Ba/Al2O3lean NOtrap catalysts[J].,2010,274(2):163-175.
[7] Unland M L. Isocyanate intermediates in the reaction nitrogen monoxide+ carbon monoxide over a plati-num/aluminum oxide catalyst[J].,1973,77(16):1952-1956.
[8] Lesage T,Verrier C,Bazin P,et al. Studying the NO-trap mechanism over a Pt-Rh/Ba/Al2O3catalyst byFT-IR spectroscopy[J].,2003,5(20):4435-4440.
[9] Szailer T,Kwak J H,Kim D H,et al. Reduction of stored NOon Pt/Al2O3and Pt/BaO/Al2O3catalysts with H2and CO[J].,2006,239(1):51-64.
[10] Bion N,Saussey J,Haneda M,et al. Study by in situ FTIR spectroscopy of the SCR of NOby ethanol on Ag/Al2O3—Evidence of the role of isocyanate spe-cies[J].,2003,217(1):47-58.
[11] Scholz C M L,Maes B H W,de Croon M,et al. Influence of reducing agent(CO,H2,and C2H4)and of H2O on NOreduction on a Pt-Ba/γ-Al2O3catalyst[J].:,2007,332(1):1-7.
[12] DiGiulio C D,Pihl J A,Choi J S,et al. NH3formation over a lean NOtrap(LNT)system:Effects of lean/rich cycle timing and temperature[J].:,2014,147:698-710.
[13] Zhu J,Shen M,Wang J,et al. N2O formation during NOstorage and reduction using C3H6as reductant[J].,2017,297:92-103.
[14] Li B,Song C,Lü G,et al. Redox reaction process between hydrocarbon and adsorbed NOover lean NOtrap catalyst[J].,2019,37(4):5455-5463.
[15] 曹曼曼,李志军,刘 磊,等. 不同还原剂对稀燃NO催化转化器转化效率的影响[J]. 西安交通大学学报,2015,49(1):34-39.
Cao Manman,Li Zhijun,Liu Lei,et al. The influence of different reducing agents on the conversion efficiency of lean-burn NOcatalytic converter[J].,2015,49(1):34-39(in Chinese).
[16] 刘世宇,李志军,史春涛,等. CO2和水蒸气对稀燃NO催化转化器的影响[J]. 西安交通大学学报,2017,51(5):134-141.
Liu Shiyu,Li Zhijun,Shi Chuntao,et al. The effect of CO2and water vapor on lean-burn NOcatalytic converter[J].,2017,51(5):134-141(in Chinese).
[17] 李明宣,宋崇林,吕 刚,等. 钴改性水滑石基LNT催化剂制备及其NO吸附-还原和碳烟催化氧化性能[J]. 燃烧科学与技术,2019,25(3):189-196.
Li Mingxuan,Song Chonglin,Lü Gang,et al. Prepa-ration of cobalt modified hydrotalcite-based LNT catalyst and its NOadsorption-reduction and soot cata-lytic oxi-dation performance[J].,2019,25(3):189-196(in Chinese).
[18] Larson R S,Pihl J A,Chakravarthy V K,et al. Microkinetic modeling of lean NOtrap chemistry under reducing conditions[J].,2008,136(1/2):104-120.
[19] Larson R S,Chakravarthy V K,Pihl J A,et al. Microkinetic modeling of lean NOtrap chemistry[J].,2012,189:134-147.
[20] Kota A S,Luss D,Balakotaiah V. Micro-kinetics of NOstorage and reduction with H2/CO/C3H6on Pt/BaO/Al2O3monolith catalysts[J].,2015,262:541-551.
[21] 王超伟,王长安,王鹏乾,等. 空气深度分级燃烧NO排放特性的CHEMKIN模拟研究[J]. 燃烧科学与技术,2020,26(1):42-50.
Wang Chaowei,Wang Chang’an,Wang Pengqian,et al. CHEMKIN simulation of NOemission of deep air-staged combustion[J].,2020,26(1):42-50(in Chinese).
[22] 苏庆运,解 亮,冯廷智,等. 柴油机LNT再生过程铂催化CO还原NO反应机理[J]. 内燃机学报,2016,34(4):339-345.
Su Qingyun,Xie Liang,Feng Tingzhi,et al. Detailed mechanism of NOreduction by CO over Pt catalyst dur-ing regeneration period of diesel LNT[J].,2016,34(4):339-345(in Chinese).
[23] Granger P,Delannoy L,Lecomte J J,et al. Kinetics of the CO+NO reaction over bimetallic platinum-rhodium on alumina:Effect of ceria incorporation into noble metals[J].,2002,207(2):202-212.
Effect of Temperature and Reducing Agent on LNT Reduction Process
Zhao Jin1,Li Zhijun1,Li Shilong1,Shuai Shijin2,Liu Shiyu2,Liu Mingli1,Wang Yan1
(1. State Key Laboratory of Engines,Tianjin University,Tianjin 300072,China;2. State Key Laboratory of Automobile Safety and Energy,Tsinghua University,Beijing 100084,China)
According to the products and by-products in the reduction process of lean NOtrap(LNT),an LNT reduction model with CO and H2as reducing agents was built. This model includes the detailed production mechanism of such by-products as N2O and NH3in the LNT reduction process. The model was used to simulate the effect of temperature on the surface reaction of N2,N2O and NH3and analyze the effect of temperature and reducing agent volume fraction on the reduction efficiency of LNT. The results show that when CO reduces NO,it is easy to generate N2O at low temperature and N2at high temperature. As temperature rises,the conversion efficiency of both NO and CO gradually increases and reaches the maximum value. When H2is used as a reducing agent,both N2O and NH3are generated at low temperature,with the rate of NH3generation being higher,while at high temperature N2is the main product. The NO conversion efficiency first increases and then decreases at low temperature in the NO/H2reaction. With the increase of CO volume fraction,the conversion efficiency of NO and CO will first increase and then decrease. Excessive CO volume fraction will inhibit the conversion rate of NO,but increasing the temperature will solve the problem to some extent.
lean NOtrap(LNT);NOreduction;reducing agent;temperature
TK411.5
A
1006-8740(2022)04-0464-07
10.11715/rskxjs.R202102015
2021-02-20
国家自然科学基金资助项目(51976136,51576140);清华大学汽车安全与节能国家重点实验室开放基金资助项目(KF1818).
赵 金(1996— ),男,硕士研究生,zhaojin1895@tju.edu.cn.
李志军,男,博士,教授,zhijunli@tju.edu.cn.
(责任编辑:梁 霞)
