异基因造血干细胞移植后巨细胞病毒感染预防治疗的进展
2022-08-23王朴英赵翔宇
王朴英, 赵翔宇, 成 娟, 刘 蓓
异基因造血干细胞移植(allo-HSCT)广泛应用于血液病治疗,术后细菌、真菌、病毒等各种病原菌感染的机会显著增加,其中巨细胞病毒(CMV)感染是最常见的感染[1]。CMV在人类血清中的阳性率为30%~97%,既往感染后可在患者体内潜伏,当免疫功能低下时再次活化,是allo-HSCT患者发生CMV感染的主要原因,从而引起CMV血症和CMV病。移植前供受者均进行CMV-DNA及CMV抗体检测,评价移植前CMV感染状态,自造血干细胞回输后开始采用实时定量聚合酶链反应(RQ-PCR)技术监测外周血中CMV-DNA拷贝数。CMV血症:仅在血液中通过RQ-PCR测定CMV-DNA>400拷贝/mL,无临床症状;CMV病:血液中CMV-DNA>400 拷贝/mL 同时具有相应的临床表现,或在特定感染器官、组织中分离到 CMV[2]。CMV血症如果进一步发展成为CMV病,侵犯肺、消化道、视网膜、脑等脏器,其中以CMV肺炎致死率最高,达到80%以上[3]。allo-HSCT后,根据供体和受体血清状态,CMV病的发生率为60%~70%,但通过预防治疗,早期发病率可降至3%~6%,晚期发病率可降至5%~8%[4-5]。既往的实验数据表明预防CMV感染是有效的,但预防药物的整体效益一直难以评估[6]。通过对一些抗病毒预防药物系统的回顾,评估抗病毒预防的整体疗效,以减少接受allo-HSCT患者感染CMV的风险,鉴于越来越灵敏的检测方法和新的抗病毒治疗的出现,抗病毒预防将会更加重要。
1 CMV
CMV是一种有包膜的双链DNA病毒,属于疱疹病毒科。CMV基因组由230 kbp线性双链DNA组成,编码形成相应的结构和功能蛋白,例如与抗CMV药物相关的UL97和UL54。CMV在上皮细胞、成纤维细胞、单核/巨噬细胞和内皮细胞都有复制位点,一旦CMV进入被感染的细胞,病毒DNA被运输到细胞核进行转录,CMV DNA聚合酶开始编码,形成一个包含多个重复基因序列的长DNA链,称为串联体,感染性病毒颗粒的产生需要将连接型DNA裂解成多个单体,这些单体最终包装成病毒衣壳,然后作为感染性病毒颗粒释放。这些成熟、包装和终止的步骤是由“CMV终止酶复合物”协同pUL89和pUL56完成,一旦终止酶复合物裂解CMV连接体,CMV DNA通过终止酶复合物与衣壳蛋白的相互作用被运输到空的病毒原壳内,最终被包裹的CMV感染颗粒释放出来[7-8]。值得注意的是,与终止酶复合物相互作用的因子可能在保护人类细胞的同时具有潜在的病毒特异性[9]。
2 抗病毒药物在预防CMV感染中的应用
2.1 更昔洛韦和缬更昔洛韦
目前,美国食品药品监督管理局(FDA)批准更昔洛韦及其缬更昔洛韦用于预防或治疗全身CMV感染。更昔洛韦是一种鸟苷类似物,经CMV UL97激酶磷酸化后,终止病毒DNA复制[10]。更昔洛韦最常见的不良反应是骨髓抑制,引起中性粒细胞显著减少[11]。缬更昔洛韦是更昔洛韦的前药,药动学研究表明,与静脉注射的更昔洛韦相比,口服的缬更昔洛韦可以达到相同甚至更高的药物暴露量,缬更昔洛韦作为预防药物的优点为组织分布好,尤其是眼睛和脑脊液[12-13]。谭栩等[11]一项关于更昔洛韦与膦甲酸钠预防allo-HSCT后CMV感染效果比较的研究显示,更昔洛韦组开始出现CMV感染的时间迟于膦甲酸钠组(P=0.015);不良反应显示,Ⅲ度粒细胞减少的发生更昔洛韦组明显高于膦甲酸钠组(P=0.016),而Ⅰ、Ⅱ度血小板减少和Ⅳ度粒细胞减少及肾功能损害在两组间并没有差异;这项研究显示两种药物在预防allo-HSCT后CMV感染的疗效相当,但不良反应有一定差异。陆铉等[2]一项关于缬更昔洛韦抢先治疗allo-HSCT后CMV血症的临床研究表明,缬更昔洛韦的治疗可有效缩短CMV-DNA转阴的时间,加速清除外周血中的CMV,在移植期间使用大剂量抗胸腺细胞球蛋白(ATG)的患者采用缬更昔洛韦疗效更为显著。根据2019年NCCN指南推荐[14]:口服缬更昔洛韦为抗CMV感染的一线预防用药,剂量为900 mg,每日1次,成人剂量应根据内生肌酐清除率(Ccr)进行调整;静脉滴注更昔洛韦预防剂量为5 mg/kg,每日1次。
2.2 膦甲酸钠
膦甲酸钠是一种无机焦磷酸盐有机类似物,选择性抑制病毒DNA聚合酶的焦磷酸盐结合位点,干扰病毒DNA链合成,对CMV蛋白激酶(CMV-PK)突变株有活性,因此对耐更昔洛韦的CMV株有效,可用于对更昔洛韦耐药的CMV感染的预防[14]。膦甲酸钠无明显骨髓抑制毒性,但具有肾脏毒性,包括肾脏损害和电解质紊乱[15]。谭栩等[11]研究中,电解质紊乱发生率膦甲酸钠组较更昔洛韦组更常见(P=0.024),用药预防期间,膦甲酸钠组有4例因不良反应停药,两药预防使用应当个体化。膦甲酸钠为抗CMV的二线药物,其疗效与更昔洛韦接近,是对更昔洛韦耐药CMV感染的首选治疗药物,但由于长期使用膦甲酸钠导致急性肾损伤的发生率较高,因而限制了其在allo-HSCT人群中的长期应用[14]。抢先治疗中,膦甲酸钠与更昔洛韦的疗效差不多[16]。
2.3 西多福韦和brincidofovir
西多福韦是一种核苷酸类似物,竞争性抑制CMV-DNA聚合酶dNTP结合位点,干扰病毒DNA链合成,它不需要病毒磷酸化来激活,具有良好的药动学特征。西多福韦已被批准用于治疗艾滋病患者的CMV视网膜炎,也可用于骨髓移植后CMV感染的预防治疗,主要用于UL97和(或)UL54基因突变型,也可用于更昔洛韦耐药CMV感染患者的治疗[14]。由于西多福韦严重的肾毒性、胃肠道和眼部损害,如葡萄膜炎、视网膜脱离和慢性眼低压,被认为是三线药物[8]。西多福韦对allo-HSCT后CMV再活化和CMV病有效,不论是抢先治疗还是挽救性治疗,用于二线治疗,尤其是更昔洛韦和膦甲酸钠治疗失败的患者[6]。brincidofovir 是西多福韦和脂质联合体,是西多福韦的前体物质,可以直接把药物缓慢释放至靶细胞,延长西多福韦抗病毒时间[17]。由于brincidofovir相关临床试验结果不一致,该药能否降低患者allo-HSCT后CMV感染风险尚不明确,因此,口服brincidofovir并没有作为抗CMV药物进一步开发。
3 新型抗CMV药物
3.1 maribavir
maribavir 是一种苯并咪唑苷酸类似物,通过直接作用于CMV蛋白酶 UL97,有效抑制CMV复制和包装,对缬更昔洛韦和西多福韦耐药的患者有效[18]。maribavir 无肾毒性、无骨髓抑制,最常见不良反应是味觉障碍[19]。maribavir 的Ⅰ期临床试验评估了600 mg每日2次的剂量,结果显示其安全且耐受性良好,最常见的不良反应是味觉障碍和头痛[20]。在maribavir预防治疗allo-HSCT受者的Ⅱ期研究中,评估3种剂量100 mg每天2次、400 mg每天1次、400 mg每天2次预防CMV感染或疾病的有效性,结果显示3种剂量均显现抗病毒效果[21]。然而,第三阶段研究(100 mg,每天2次)得出结论认为,相对于安慰剂,maribavir在预防allo-HSCT后的CMV疾病方面没有效果[22]。有人认为这一试验失败可能是由于使用了低剂量。一项评估maribavir 抢先治疗CMV感染疾病的随机Ⅱ期研究得出,在出现无症状病毒血症的成人移植患者中,maribavir治疗(较高剂量400~1 200 mg,每天2次)与缬更昔洛韦的疗效相似[23]。目前正在进行最低剂量(400 mg,每天2次)的Ⅲ期研究,目的是为了比较maribavir 与缬更昔洛韦在抢先治疗青少年(年龄≥16岁)和接受allo-HSCT的成人CMV感染中的疗效和耐受性。
3.2 letermovir
letermovir 于2017年被FDA批准用于CMV感染的初级预防,它通过作用于UL56亚基抑制病毒终止酶复合物而抑制病毒的复制,其抗病毒活性对CMV具有高度特异性,对其他病毒如HSV、EBV、HZV、HHV6和腺病毒缺乏抑制活性[24]。letermovir 最常见的不良反应是恶心、呕吐等胃肠道症状[14]。在一项Ⅰ期临床试验中,letermovir 在预防CMV感染中安全且耐受性良好[25]。Ⅱ期研究比较了每日剂量为60 mg、120 mg和240 mg letermovir 与安慰剂在预防血清阳性allo-HSCT受体中CMV再激活方面的效果,病毒学失败的发生率(定义为可检测到的CMV感染导致研究药物和抢先治疗的中断或CMV终末器官疾病的发生)在240 mg组(6%)中低于120 mg组(19%)、60 mg组(21%)和安慰剂组(36%)[26]。在Ⅲ期安慰剂对照研究中,在24周时,与安慰剂相比,letermovir 预防降低了CMV感染率(17.5%对41.8%),主要体现在高危患者中[27]。一项系统回顾和荟萃分析比较了allo-HSCT受者CMV预防的不同干预措施(阿昔洛韦、更昔洛韦、 maribavir、letermovir 等药物和疫苗)的安全性和有效性[28],这项研究的结论是更昔洛韦和 letermovir 的预防显示出对CMV病和感染的最佳相对疗效,就安全性而言,letermovir 也是预防策略的最佳选择(letermovir 的推荐预防剂量是480 mg每天1次)。尽管letermovir 已被批准用于allo-HSCT受者的CMV感染初级预防,然而需要确定其在CMV感染治疗中的最佳用途,包括难治性或对现有药物耐药的感染。
3.3 来氟米特
来氟米特通过抑制蛋白激酶活性和嘧啶合成来抑制病毒复制,可用于治疗难治性和耐药性CMV疾病,因为在一些案例报告中它被用于治疗更昔洛韦耐药或难治性CMV疾病疗效不一[29],所以来氟米特尚未被临床批准用于CMV治疗,也没有计划进行大型随机临床试验来评估其有效性和安全性。但某些情况下,来氟米特可用于对其他二线和三线抗病毒药物耐药或难治的患者[30]。
4 抢先治疗在预防CMV病中的应用
抢先治疗是allo-HSCT患者出现CMV血症但尚未进展为CMV病所采取的抗病毒治疗,因此抢先治疗能否成功主要依赖于能否灵敏检测到CMV血症。目前应用最广泛诊断CMV血症的方法是CMV抗原检测和定量PCR检测[31]。目前用于抢先治疗的药物有更昔洛韦、缬更昔洛韦、膦甲酸钠、西多福韦等,抢先治疗可以单独使用,也可以与抗病毒预防相结合[30]。根据来自2017年欧洲白血病感染会议(ECIL7)关于血液系统恶性肿瘤患者和干细胞移植后CMV感染的管理指南建议[30],基于检测全血或血浆中CMV DNA(或抗原)的预防性抗病毒治疗对预防CMV病有效,更昔洛韦或膦甲酸钠均可用于一线抢先治疗,口服缬更昔洛韦可代替更昔洛韦或膦甲酸钠,但严重胃肠道移植物抗宿主病(GVHD)患者除外,药物的选择取决于allo-HSCT后的时间、不良反应的风险和是否接触过抗病毒药物,不推荐使用膦甲酸钠和更昔洛韦一半剂量的组合,所有剂量均要考虑患者的肾功能,更昔洛韦治疗的药物监测有助于减少不良反应指导治疗;可考虑使用更昔洛韦(或缬更昔洛韦)和膦甲酸钠的替代药物,西多福韦可考虑作为二线或三线抢先治疗(5 mg/kg/周),但需要仔细监测肾功能,更昔洛韦和膦甲酸钠的一半剂量组合被考虑用于二线或三线抢先治疗,对于所有二线和三线治疗,应尽可能减少免疫抑制方法的使用,来氟米特可用于对其他二线和三线抗病毒药物耐药或难治的患者,不建议在二线或三线治疗中加入静脉注射免疫球蛋白。见表1。
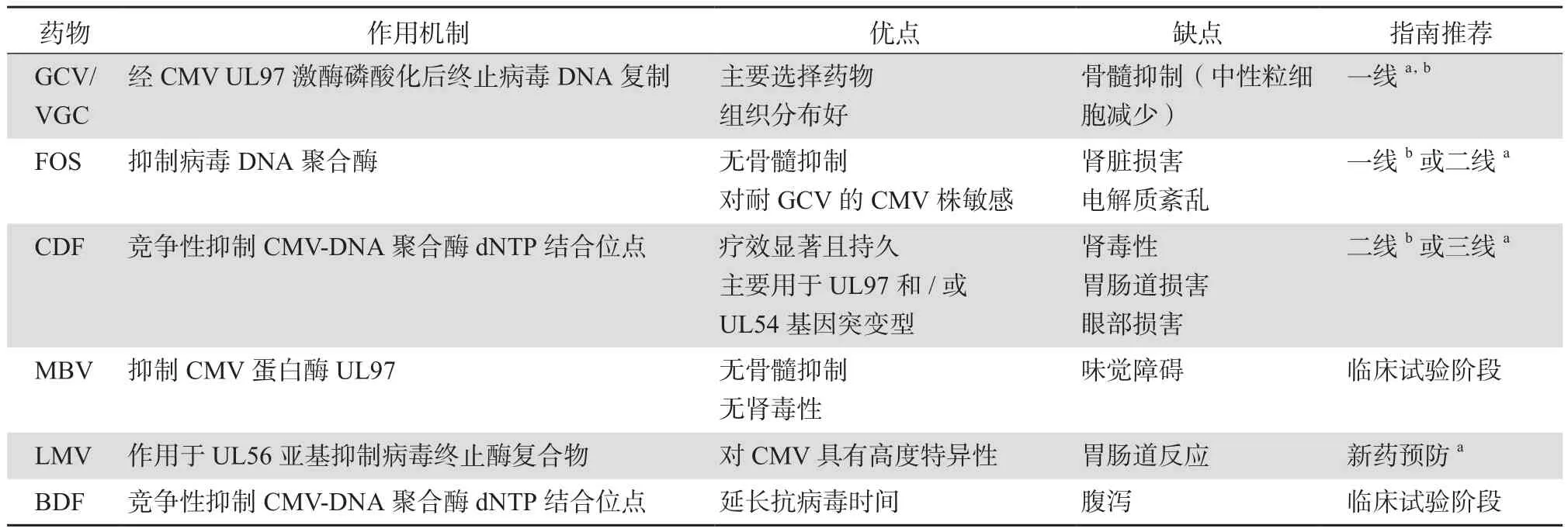
表1 抗CMV药物在普遍性预防和抢先治疗中的总结
5 新型预防CMV感染的方案
5.1 过继免疫疗法
过继免疫疗法是指通过分离、体外繁殖和向受体输注供体T细胞来重建CMV特异性T细胞反应[13]。随着细胞免疫治疗的开展,CMV 感染的高危患者可以通过输注CMV特异性细胞毒性T淋巴细胞获益,有研究显示过继免疫疗法作为抗病毒治疗的辅助手段,可用于抢先治疗和难治性CMV感染的治疗以及allo-HSCT后的预防治疗,并取得了较好的效果[32]。在一项研究中,在allo-HSCT的第28天或之后,将来源体外产生的供体CMV特异性细胞毒性T细胞预防性过继转移给9例CMV D+/R+(供体血清CMV阳性/受体血清CMV阳性)和D+/R-(供体血清CMV阳性/受体血清CMV阴性)的allo-HSCT受体,9例患者中有6例在输注一周后出现可检测到的CMV特异性T细胞,虽然有2例CMV R+患者出现了CMV血症,但他们都不需要抗病毒治疗,没有观察到不良事件的发生[33]。另一项研究检测了在缺乏CMV特异性免疫反应的31例患者中,将供体的记忆性T淋巴细胞输注给allo-HSCT受体,供体淋巴细胞输注使20例患者(64.5%)在100 d内实现CMV特异性T细胞扩增,因此,输注低剂量供体记忆性T淋巴细胞可能是预防移植后CMV感染的一项有效措施[34]。此外,第三方供体病毒特异性T细胞输注对其他病毒(BK病毒、人类疱疹病毒6型、爱泼斯坦-巴尔病毒和腺病毒)的感染治疗也有益处[35]。过继性CMV特异性T细胞免疫疗法正在继续进行CMV疾病预防或预防性治疗试验,虽然目前不推荐细胞疗法作为标准的抗病毒治疗方案,但在临床试验范围内,可以使用供体或第三方抗CMV特异性T细胞的实验性过继免疫疗法[32]。
5.2 CMV疫苗
CMV疫苗是一种与佐剂联合的实验性多肽疫苗,CMV疫苗通过诱导免疫与免疫原性化合物以降低高危患者的CMV再活化率或CMV疾病发生率[31]。疫苗种类包括重组蛋白疫苗(DNA疫苗)、载体疫苗和肽疫苗,目前研究较多的DNA疫苗是ASP0113和 CSJ148[10]。其中关于ASP0113的研究并没有取得较好的效果。CSJ148也是研究较多的一种疫苗,研究表明其安全且耐受性良好,人体免疫球蛋白的药动学符合预期,第2阶段研究的结果目前正在审查中[21]。最近,疫苗开发的重点是整合五聚体复合物,通过此疫苗引发有效的中和抗体反应,阻止CMV进入相关细胞[36]。最近,在一项Ⅰ期研究中,发现这种疫苗对CMV血清阴性的受试者是安全的,并能引起稳定水平的中和抗体和T细胞反应[37]。其他几种候选疫苗目前正在成人和儿童allo-HSCT受体的Ⅰ期和Ⅱ期试验中进行评估。1999年美国国家医学研究院将CMV指定为疫苗开发的优先事项,但目前还没有获得许可的抗CMV疫苗,仍需要进一步的研究和开发。
6 讨论
CMV感染一直是allo-HSCT和CMV血清阳性患者面临的一项难题,在过去的几十年里,一些研究已经评估了不同的抗病毒药物,试图找到一种安全和有效的药物作为普遍预防或抢先治疗。常用预防抗CMV或抢先治疗的药物有更昔洛韦、缬更昔洛韦、膦甲酸钠和西多福韦(见表1),其中目前应用最多的是更昔洛韦和缬更昔洛韦。具有更好作用的新型药物的需求导致了一些有前景的预防抗病毒药物的开发,其中最有效的药物是maribavir、 letermovir、brincidofovir (见表1),letermovir 已于2017年被FDA批准用于CMV感染的预防,成为近年来CMV感染预防的一大突破,其他新药都处于正在开发研究中,需更好地评估其安全性和有效性。随着对移植受者免疫重建和CMV生物学研究的深入和更新,免疫学策略越来越受到人们的关注,其中,过继T细胞治疗已在临床实验中取得了很好的疗效,免疫治疗作为CMV治疗的一种新技术,近年来正在发展和探索中。疫苗一直是预防CMV感染的研究重点,虽然目前仍没有针对CMV感染有效的疫苗,但关于疫苗的研究从未停止。尽管CMV感染预防或抢先治疗使疾病的发生率降低,但CMV感染仍然是一个重要的临床挑战。
