基于真实世界研究对依拉环素治疗中重度感染的疗效与安全性的系统综述与荟萃分析
2022-08-23肖婷婷王雪婷肖永红
肖婷婷, 喻 玮, 王雪婷, 肖永红
复杂性腹腔感染(cIAI)是累及腹腔或腹膜后间隙,伴或不伴有脓肿形成,具有全身感染中毒症状和体征的感染。cIAI是临床常见病,容易发展为多器官功能障碍综合征(MODS),病死率高达10. 5%,耗费大量医院资源和医疗费用[1-3]。不同的cIAI诊治指南显示,患者特征、诊断标准、治疗方式存在较大差异[4-5]。通过外科手术控制感染源是cIAI治疗成败的关键环节,包括清除坏死的感染组织、充分引流渗液或脓液。及时启动恰当的抗菌治疗是治疗cIAI的重要组成部分。经验性抗菌治疗应依据流行病学特征和微生物学结果选择适当的抗菌药物。然而,近年来,细菌耐药形势日益恶化,我国cIAI中产超广谱β内酰胺酶(ESBL)的肠杆菌目细菌持续处于较高水平,由此导致碳青霉烯类抗生素的广泛使用,增加了细菌对这类抗生素的耐药风险,2020年CHINET监测显示我国美罗培南耐药肺炎克雷伯菌检出率高达22.4%[6]。cIAI常见病原体包括革兰阴性肠杆菌、兼性厌氧菌以及肠球菌等,我国和其他地区致病菌的分布没有明显差异[7-8]。面对严峻的耐药形势,临床迫切需要新型的治疗耐药菌感染的抗菌药物。
依拉环素是新一代全合成氟环素类抗菌药物,属于四环素大类,对革兰阴性和革兰阳性需氧菌、兼性厌氧菌和专性厌氧菌及其耐药菌株都有高度的抗菌活性;在动物感染模型中表现出良好的治疗效果。全球Ⅱ期和Ⅲ期临床研究结果证明依拉环素在cIAI受试者中具有良好的疗效和耐受性,临床疗效非劣效于厄他培南或美罗培南,没有观察到四环素类抗菌药物常见不良反应以外新的安全性问题,最常见不良反应为消化道和输注部位反应[8]。依拉环素于2018年分别在美国和欧洲批准上市用于治疗cIAI,并于2020年4月获得新加坡批准用于治疗cIAI。2020年美国感染病学会(IDSA)发布的治疗耐药革兰阴性菌感染指南推荐依拉环素作为治疗包括碳青霉烯类耐药肠杆菌目细菌感染的药物选择[9]。
本文旨在通过文献检索、系统综述以及荟萃分析的方式,收集和汇总目前为止已发表的真实世界研究数据,以了解依拉环素在真实世界情况下治疗包括cIAI在内的各种中重度感染的疗效和安全性。
1 资料与方法
1.1 检索策略
以“eravacycline or xerava or TP-434 or 7-fluoro-9-pyrrolidinoacetamido-6-demethyl-6-deoxytetracycline” 和“effectiveness or efficacy or safety or real world”在“篇名”“摘要”及“关键词”中检索PubMed和Medline数据库中收录的全部文献。为了避免遗漏尚未发表的文献,以同样的检索策略检索“clinicaltrials. gov”网站。检索时间为建库至2021年1月。
1.2 纳入标准
文献纳入标准:①研究对象为依拉环素临床应用数据;②研究内容应包括临床疗效和安全性信息;③研究类型为非干预性真实世界研究,以减少对临床结局影响。
1.3 排除标准
排除不符合以上标准的文献,以及:①重复发表的文献,或该文献为某研究的阶段性报告,而另有其他发表的文献已经报告该研究更完整结果;②实验室基础研究或没有临床资料的分析;③文中提及依拉环素临床信息,但实际是引用其他研究的文献;④综述、评论或讲座。
1.4 数据提取
对纳入的文献数据进行提取,包括文献第一作者、发表时间、文献类型,样本量、患者平均年龄、性别、感染类型,依拉环素用药剂量和频次、平均用药时间,临床疗效、不良事件/不良反应等。
1.5 终点指标
考察的疗效终点指标为依拉环素临床有效率,以文献定义的“治疗期间临床感染症状消失或恢复”为准。安全性终点指标为报告的不良事件发生率。
1.6 统计学方法
将提取出的数据按不同文献输入电子表格,采用R软件(3.6.2版)进行数据汇总和统计学分析。
对疗效终点指标进行荟萃分析计算合并的疗效,提供各文献中疗效终点估计及95% 置信区间(CI)的森林图,并采用卡方检验对不同文献疗效数据的统计学异质性进行评估。当纳入文献之间的统计学异质性检验P≥0.05,I2≤50%时,说明纳入的文献之间异质性无统计学意义。根据文献间的统计学异质性检验结果,采用固定效应模型或随机效应模型分别计算研究水平数据合并的临床有效率。
对于安全性终点指标及患者数据(如性别、感染类型),将不同文献的可追溯数据进行简单合并,计算合并后的描述性统计量。
2 结果
2.1 纳入文献的基本情况
依据检索策略,共检索到文献109篇,其中101篇为无关或重复文献(图1)。共收集8篇真实世界研究报告,但其中3篇为同一研究的阶段性报告(第一作者均为Sara Alosaimy,且与通信作者确认)[10-14],故按筛选标准,取最新发表的也是最完整结果那一篇,以剔除重复数据。经过上述筛选,最终纳入本研究文献为5篇,其中正式发表的论文2篇,会议简报3篇。
2.2 基本信息汇总
纳入分析5篇文献全部为回顾性研究,包含3个单中心和2个多中心研究。共有265例不同类型感染患者的数据,包含的病例就诊时间不一,总体时间跨度为在依拉环素获FDA批准后,即2018年到2020年底。通过异质性分析,除了Van Hise等[14]的研究外,其他4项研究不存在显著异质性,可以合并分析。因此,在以下对疗效终点的分析中将Van Hise等[14]的研究进行单独描述,对其他4个研究进行荟萃分析以评估其合并的疗效。
不同研究中,由于研究目的的差异,患者基本情况数据的呈现方式各有不同,报道依拉环素治疗疗程最短为3 d,最长为73 d,见表 1。

表1 各研究中依拉环素治疗用药信息Table 1 Details about the dose, treatment duration, and combination regimen of eravacycline in each study
2.2.1 共同分析的4篇文献基本情况 4个研究共包含215例患者,单个研究样本量最大为165例,最小为8例。所有研究均包含cIAI,也同时包含其他感染类型,如肺部感染、血流感染、皮肤软组织感染等(表2)。最常见的为腹腔感染(63例,29.3%)、呼吸道感染(54例,25.1%)和皮肤与软组织感染(36例,16.7%)。

表2 纳入荟萃分析的4篇文献中患者感染类型分布Table 2 Site of infections reported in the 4 studies included in this meta-analysis
Carr等[10]的研究中23例患者急性生理与慢性健康评分(APACHE Ⅱ)平均值为20±11,其中14例患者微生物培养显示多种致病原,4例伴有血流感染,依拉环素疗程中位时间为8 d( 范围3~30 d),19例患者联合使用其他抗菌药治疗,治疗期间4例(19%)死亡。Lunsted等[13]的研究中,重点描述了患者感染类型,耐药致病菌和合并用药情况,8例患者的致病菌包括碳青霉烯类耐药肠杆菌目细菌(CRE)、万古霉素耐药肠球菌(VRE)各2例,碳青霉烯类耐药鲍曼不动杆菌(CRAB) 1例,依拉环素治疗剂量为1 mg/kg 每12小时1次或1.5 mg/kg 每24小时1次(有1例患者合并使用了CYP3A 诱导剂扑米酮,按说明书调整给药方式),治疗平均时间为16 d(范围4~30 d),1例为感染疾病导致死亡。Alosaimy等[11]研究中,165例患者的APACHE Ⅱ和综合并发症指数(CCI)中位值分别为14.0(四分位数10.0,20.2)和3.0(四分位数1.5,5.5),其中146例患者(88.5%)有多重耐药(MDR)风险因素,93例(56.4%)依拉环素联合其他抗菌药治疗,79例(55.2%)为医院获得性感染,30 d病死率为20.0%,90 d病死率为29.9%。Hwang等[12]报道了其研究的19例患者中的合并症情况,其中18例(94.7%)有合并症,平均CCI评分3(0~8),13例(68.4%)患者存在耐药危险因素(近期住院使用抗菌药物),依拉环素治疗剂量为1 mg/kg 每12小时1次或1.5 mg/kg 每24小时1次,治疗时间平均为24 d(范围4~73 d)。
2.2.2 单独分析的1篇文献基本情况 研究中50例接受依拉环素治疗的感染患者均在院外接受最后一剂治疗,最常见的为腹腔感染(17例,34%)、呼吸道感染(9例,18%)和糖尿病足感染(6例,12%)。大多数(88%)患者合并2种或以上基础疾病,包括慢性阻塞性肺疾病(COPD)、肿瘤、肾功能不全等,仅3例无合并症,平均CCI评分3.3(范围0~6)。依拉环素治疗剂量为1.5 mg/kg每24小时1次,疗程5~26 d[14]。
2.3 疗效结果的荟萃分析
5篇文献均对临床有效率给予了描述。对可合并分析的4篇文献的临床有效率进行荟萃分析,结果以及按文献列举的临床有效率森林图见图2。4篇文献间的异质性检验结果(P=0.22,I2=33%)说明各研究间没有明显异质性,故荟萃分析将采用固定效应模型的分析过程。4个研究的临床有效率在52%~73%,采用固定效应模型的荟萃分析汇总的临床有效率为69%(95%CI:62%~75%)。Van Hise等[14]研究中患者临床有效率为94.0%(47/50),明显高于上述4篇文献报道的疗效结果。
2.4 安全性结果汇总
采用描述性统计学方法,对全部5篇文献报告的不良事件发生情况进行汇总(表3)。265例患者中,共29例(10.9%)发生不良事件,最常见为胃肠道反应。有11例(4.2%)患者因不良事件提前停用依拉环素治疗,但导致提前停药的不良事件全部文献均未做详细说明。
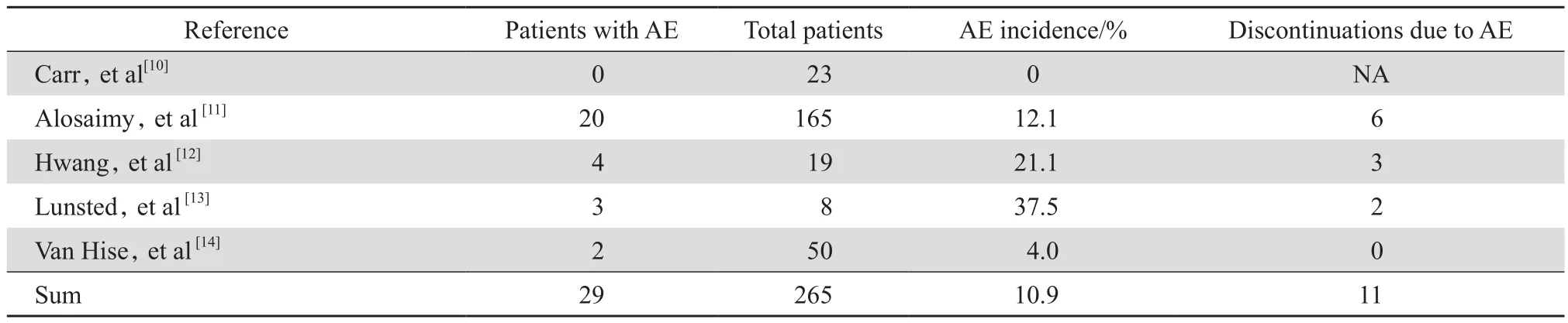
表3 患者的不良事件发生率Table 3 Incidence of adverse events in each study
3 讨论
依拉环素是全球第一个全合成的氟环素类抗菌药物,对革兰阳性和革兰阴性需氧菌、厌氧菌,如耐甲氧西林金黄色葡萄球菌(MRSA)、VRE、产ESBL和CRE与多重耐药鲍曼不动杆菌(MDRAB)等具有良好的体外活性[15]。2018年在欧美批准用于治疗18岁及以上患者中由下列敏感细菌引起的cIAI:大肠埃希菌、肺炎克雷伯菌、弗劳地枸橼酸杆菌、阴沟肠杆菌、产酸克雷伯菌、粪肠球菌、屎肠球菌、金黄色葡萄球菌、咽峡炎链球菌、产气荚膜梭菌、类杆菌属和狄氏副拟杆菌,推荐的给药方案为1 mg/kg,每12小时1次,推荐的疗程为4~14 d,并应根据感染严重程度和部位以及患者临床应答情况,选择疗程。本文纳入分析的5篇资料均来自美国的真实世界的报道。
本次纳入荟萃分析的4篇研究的215例患者,多数为严重感染患者,其中有3篇报告了研究期间的患者病死率在12.5%~20.0%,1篇报道了90 d死亡率接近30%。所观察患者具有耐药菌感染(包括CRE和CRAB)或有耐药风险因素,伴随多种基础疾病或合并症,APACHE Ⅱ评分多数在10分以上,CCI在3分左右或类似合并症评分达到6分,整体给药时间也普遍比较长(3篇报道中有超过14 d的疗程)和/或合并其他抗菌药物使用;所有患者中腹腔感染最常见,其次为肺部感染,这两者占超过50%的病例数,另外还包括血流感染、皮肤软组织感染等。对治疗终点临床有效率进行荟萃分析结果显示,4篇涉及病情较重的患者接受依拉环素治疗后的总体临床有效率为69%(95%CI:62%~75%),提示依拉环素治疗耐药菌感染和严重感染患者(包括腹腔感染)具有良好的临床疗效。由于样本量较小以及缺乏文献数据的支持,未能分别针对不同的感染部位单独进行汇总分析。另一研究入选的50例患者部分为社区获得性感染,临床有效率则高达94%。以上研究中依拉环素治疗剂量为1 mg/kg 每12小时1次或1.5 mg/kg 每24小时1次,研究中虽未明确区分两种治疗方案的疗效数据,总体疗效结果提示依拉环素不同给药方案在真实医疗环境下治疗不同部位感染、包括耐药菌所致的严重感染均具有良好的临床疗效。依拉环素在国外已开展2项Ⅲ期研究用于验证在cIAI的疗效和安全性,分别选择厄他培南与美罗培南作为对照药。研究结果显示依拉环素在改良意向治疗(MITT)人群中的治愈率分别为86.8%和90.8%,达到了预先设定的非劣效界值,证明依拉环素治疗cIAI的疗效与碳青霉烯类相当。与依拉环素治疗cIAI的Ⅱ期和Ⅲ期注册研究人群相比,依拉环素在真实世界中的使用场景更加广泛,包括住院患者与门诊患者。此外,治疗的感染类型也不局限于cIAI,其他常见的包括肺部感染、血流感染、皮肤软组织感染等也显示出良好的疗效。对比注册临床研究和真实世界研究的入组人群,注册研究的患者经过入排标准的筛选,病情相对较轻(参考APACHE Ⅱ评分),具有更高的临床治愈率[16-18]。
安全性合并分析结果显示患者治疗不良事件发生率为10.9%,主要为胃肠道反应,因不良事件提前停用依拉环素的发生率较低(共11例,占4.2%),表明依拉环素在真实医疗环境中的临床应用具有良好的安全性和耐受性。在注册临床试验中,依拉环素总体安全耐受性良好,胃肠道反应包括恶心、呕吐以及输注部位反应是常见的不良反应,四环素类药物常见不良反应以外新的安全性问题,与真实世界研究结果基本一致[16-18]。
本次纳入分析的研究均为真实世界回顾性数据,纳入分析的数据量有限,数据的分析和报告标准不一,患者的感染类型、基线情况等分布各异,给数据的合并分析带来一定的挑战,导致其结果的解读存在一定的局限性。但这些研究提供了依拉环素在真实世界的应用情况及其有效性/安全性数据,在以新药上市为目的的随机对照研究提供的数据之外,为依拉环素实际应用于临床提供了宝贵的数据支持和有效证据。随着依拉环素临床应用的逐步推广,未来会积累更多来自于真实世界的患者数据,将进一步为依拉环素实际临床应用的疗效与安全性提供更为全面的证据支持。
