口腔清洁护理用品 牙膏用羟基磷灰石(QB/T 5637—2021)
2022-08-22
前言
本文件按照GB/T 1.1-2020《标准化工作导则 第1部分:标准化文件的结构和起草规则》的规定起草。
本文件由中国轻工业联合会提出。
本文件由全国口腔护理用品标准化技术委员会牙膏分技术委员会(SAC/TC 492/SC1)归口。
本文件起草单位:重庆登康口腔护理用品股份有限公司、上海紫临实业有限公司、云南白药集团健康产品有限公司、无限极(中国)有限公司、上海美加净日化有限公司、广州薇美姿实业有限公司、好来化工(中山)有限公司、狮王日用化工(青岛)有限公司、淮安纵横生物科技有限公司、福建爱洁丽日化有限公司、中山市多美化工有限公司、西安泰荣新型材料有限公司、黑龙江省轻工科学研究院。
本文件主要起草人:邓全富、张小为、陈凤、宫敬禹、潘建、高鹰、高艳、俞晓燕、陈敏珊、何琪莹、刘婧、陈万金、郭婷婷、雷锡全、冯菊华、丁恺、陈梦军。
本文件为首次发布。
1 范围
本文件规定了牙膏用羟基磷灰石的要求、检验规则、标志、包装、运输、贮存和保质期,描述了相应试验方法,给出了分子式和相对分子量的信息。
本文件适用于牙膏(粉)中主要用作抗牙本质敏感、美白等活性成分的羟基磷灰石粉料的生产、检验和销售。
本文件不适用于纳米级羟基磷灰石。
2 规范性引用文件
下列文件中的内容通过文中的规范性引用而构成本文件必不可少的条款。其中,注日期的引用文件,仅该日期对应的版本适用于本文件;不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T 191包装储运图示标示
GB/T 601化学试剂 标准滴定溶液的制备
GB/T 602化学试剂 杂质测定用标准溶液的制备
GB/T 603化学试剂 试验方法中所用制剂及制品的制备
GB/T 1875磷矿石和磷精矿中灼烧失量的测定 重量法
GB/T 6682分析实验室用水规格和试验方法
GB/T 8170数值修约规则与极限数值的表示和判定
GB/T 9724化学试剂 pH值测定通则
GB 23101.3外科植入物 羟基磷灰石 第3部分:结晶度和相纯度的化学分析和表征
QB/T 2317口腔清洁护理用品 牙膏用天然碳酸钙
QB/T 2477牙膏用二水磷酸氢钙
YY 0303医用羟基磷灰石粉料
JJF 1070-2005定量包装商品净含量计量检验规则
《化妆品安全技术规范》(2015版)
《中华人民共和国药典》(2020年版四部)
《定量包装商品计量监督管理办法》(国家质量监督检验检疫总局令[2005]第75号)
3 术语和定义
本文件没有需要界定的术语和定义。
4 分子式和相对分子质量
4.1 分子式
Ca10(PO4)6(OH)2
4.2 相对分子质量
1004.636(按2013年国际相对原子质量)
5 要求
5.1 鉴别
5.1.1 X射线衍射图谱
样品的X射线衍射图谱,应符合相应的标准粉末衍射峰卡片(pdf)图谱规定。
5.1.2 红外吸收图谱
样品的红外吸收图谱,应显示羟基吸收峰:3573cm-1,632cm-1;磷酸根吸收峰:571cm-1,601cm-1,959cm-1,1047cm-1,1090cm-1;无碳酸根、羰基、氨基或其他杂质峰出现。
5.2 感官、理化指标
应符合表1规定。
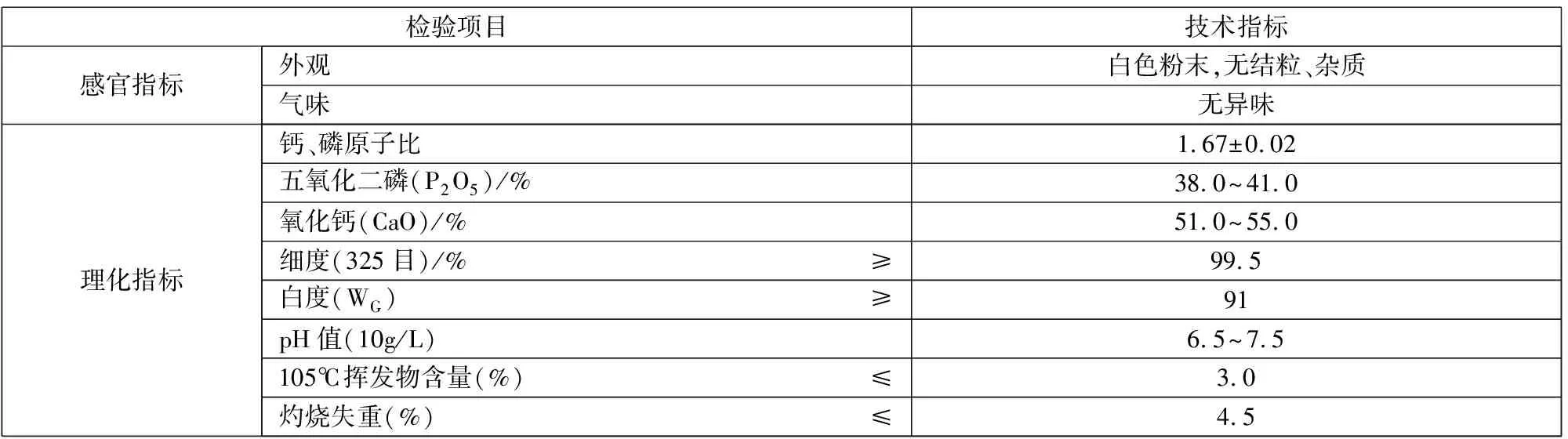
表1 感官、理化指标
5.3 卫生指标
应符合表2规定。

表2 卫生指标
5.4 净含量
应符合《定量包装商品计量监督管理办法》的规定。
6 试验方法
6.1 通则
本文件所用试剂和水,在没有注明其他要求时,均指分析纯试剂和GB/T 6682中规定的三级水。
试验中所需的各种溶液、制剂或制品,在没有注明其他要求时,均按GB/T 601、GB/T 602、GB/T 603规定制备。
6.2 鉴别
6.2.1 X射线衍射图谱,按GB 23101.3中规定的方法进行鉴别。
6.2.2 红外吸收图谱,按YY 0303中规定的方法进行鉴别。
6.3 外观
取适量样品,置于清洁、干燥的表面皿或白瓷板上,在自然光线下,用目测法判定。
6.4 钙、磷原子比
按照QB/T 2477中规定的方法,根据(6.6)测定的氧化钙质量分数,换算出钙质量分数;根据(6.5)测定的五氧化二磷质量分数,换算出磷质量分数。钙和磷质量分数的比值,即为钙、磷原子含量比。
6.5 五氧化二磷(P2O5)
按QB/T 2477中规定的方法进行。
6.6 氧化钙(CaO)
按QB/T 2477中规定的方法进行试验。
6.7 细度(325目)
6.7.1 仪器
6.7.1.1 标准筛:筛孔宽度45μm(325目),筛面材质为不锈耐酸钢。
6.7.1.2 恒温干燥箱:精度±2℃。
6.7.2 测定程序
称取试样10g(精确至0.1g),置于预先用水润湿的筛孔宽度45μm(325目)标准金属筛中。用水流冲洗筛内试样(水流不宜过大以防样品溅失,且水中不应含机械杂质),同时倾斜着转动筛体,直至无细度料通过为止。然后将筛上物料冲至带滤纸(已恒重)的漏斗内进行过滤,滤渣连同滤纸在105℃恒温下烘干至恒重。
6.7.3 结果表示
以质量分数表示的细度S,按公式(1)计算:
(1)
式中:S——细度,单位为质量百分数(%);
m——试样质量,单位为克(g);
m1——筛余物(金属标准筛筛后的余物)及滤纸(恒重后)质量,单位为克(g);
m2——经105℃烘至恒重的滤纸质量,单位为克(g)。
6.8 白度(WG)的测定
6.8.1 仪器
自动白度计:可测定甘茨白度,分度值不应大于0.2。
6.8.2 测定程序
按QB/T 2317中规定的白度检测法,测试3次,读取甘茨白度值。
6.8.3 结果计算
3次读取甘茨白度值,计算其平均值为白度值。
6.9 pH值(10g/L)
称取1.0g试样,精确至0.1g,置于100mL烧杯中,加入99.0mL无二氧化碳的水,搅拌15min。其余按GB/T 9724中规定的方法进行。
6.10 105℃挥发物含量
按《中华人民共和国药典》(2020年版四部)中干燥失重规定的方法进行。
6.11 灼烧失重
按GB/T 1875中规定的方法进行。
6.12 微生物指标
按《化妆品安全技术规范》(2015版)中规定的方法进行。
6.13 重金属(以Pb计)
按《化妆品安全技术规范》(2015版)中理化检验方法中规定的方法进行。
6.14 砷(As)
按《化妆品安全技术规范》(2015版)中理化检验方法中规定的方法进行。
6.15 净含量
按JJF 1070-2005执行。
7 检验规则
7.1 出厂检验和型式检验。
7.1.1 出厂检验
本文件规定的感官、理化指标、菌落总数、霉菌与酵母菌总数列为出厂检验项目。
7.1.2 型式检验
本文件规定的全部项目,正常生产情况下每3个月进行1次型式检验,有下列情形之一时也应进行型式检验:
a)新产品或老产品转厂生产的试制定型鉴定;
b)正常生产后,如原料、生产工艺有较大改变,可能影响产品性能时;
c)产品长期停产后恢复生产时;
d)出厂检验结果与上次型式检验有较大差异时;
e)国家质量监督检验机构提出进行型式检验要求时。
7.2 组批、抽样和采样
7.2.1 生产企业采用相同材料,基本相同的生产条件,在同一生产过程中的同等级产品为1批。
7.2.2 检验取样方法:应从每批桶(袋)数的3%中抽取试样,小批时不得少于2桶(袋)。从选取的桶(袋)中,用取样管伸入至3/4处,取出不少于50g的试样,将选取的试样迅速混匀,分别装于两个清洁、干燥的密闭样品容器中并贴上标签,注明:生产厂名、产品名称、生产批号、采样日期和采样者姓名。样品一份用于检验,另一份保存备查。样品放置室温阴凉、干燥处密闭保存。
7.3 判定规则
检验结果按GB/T 8170修约至规定位数,对照要求限定值确定检验的产品是否可以验收。检验结果如不符合要求时,应重新自两倍包装中采样复验,复验结果仍不符合要求时,则整批产品不能验收。
7.4 仲裁
如交收双方对产品检验结果发生异议时,双方可协商解决,必要时,可共同选定仲裁机构按本文件检验裁定。
8 标志、包装、运输、贮存、保质期
8.1 标志
包装袋、箱或桶上应有下列标志及符合GB/T 191规定:
a)产品名称;
b)毛重及净含量;
c)生产批号和包装日期;
d)生产厂名、厂址;
e)产品标准编号;
f)保质期;
g)防雨、防晒、防钩等文字或标志、堆码层数限制。
8.2 包装
本产品包装应保证容器清洁,可选用塑料桶(袋)或适合的金属桶包装,各种包装应封口严密不渗漏,适合长途运输和贮存。
8.3 运输
产品不应与有毒有害物质混运,搬运时注意小心轻放,避免包装桶变形或破裂。
8.4 贮存
本产品应贮存于通风干燥的仓库内,堆放应离地、离墙10cm以上,不应露天堆放,应避免包装物积尘、积水,不应与有毒、有害或其他污染物品混放,贮存期间应做到先进先出,尽量缩短库存期。
8.5 保质期
在符合本文件包装、运输和贮存条件下,自生产之日起保质期为24个月,超过保质期应作报废处理。
