H 2 O和SO2对钙循环捕集CO2碳酸化过程协同效应的研究
2022-08-19戴文浩王春波闫广精
戴文浩, 王春波, 陈 亮, 方 远, 袁 峰, 闫广精
(1.华北电力大学动力工程系,河北省低碳高效发电技术重点实验室,河北保定 071003;2.中国城市建设研究院有限公司,北京 100120)
2019年使用化石能源产生的二氧化碳达到了380亿t当量[1],世界各国制定了碳减排路线[2]。我国也提出2030年前碳达峰、2060年前碳中和的目标,这对于能源电力行业打造清洁高效、低碳环保的现代能源体系有着重要的指导意义。
碳捕集、利用与封存(CCUS)技术是燃煤电厂降低碳排放的关键解决方案,在推进电力系统低碳化、实现碳中和目标中发挥了重要作用。钙循环捕集CO2技术作为一种燃烧后碳捕集技术,受到了广泛关注[3]。在煅烧炉内,CaCO3在高温下煅烧生成多孔CaO,同时释放出高浓度的CO2;在碳酸化炉内,燃煤烟气中的CO2与CaO发生如下的碳酸化反应,从而将CO2固定到CaCO3中。
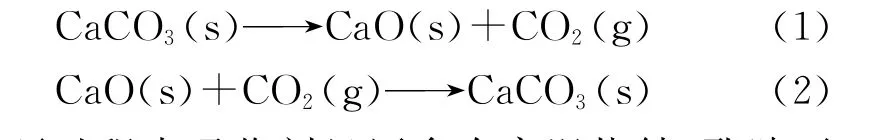
循环过程中吸收剂经历多次高温烧结,孔隙不断减少而失活,导致碳捕集能力下降[4]。研究表明,在碳酸化气氛中加入H2O能够提高钙基吸收剂的碳捕集效率[5],在一定程度上克服了吸收剂失活的缺陷。王春波等[6]发现当碳酸化气氛中H2O的体积分数从0%增加至20%后,第8次循环的转化率仍提高了约10%,推测是H2O与CaO生成了瞬态的中间产物Ca(OH)2,对碳酸化反应起到催化作用。李泽华等[7]认为中间产物Ca(OH)2的连续生成与分解形成了孔径发达的CaO颗粒。Donat等[8]认为碳酸化过程中H2O降低了CO2在产物层中的扩散阻力,使吸收剂反应活性增加。Wang等[9]发现当碳酸化气氛中H2O的体积分数从0%增加到10%时,CaO吸收剂性能显著提高。
燃煤烟气中存在一定量的SO2,会显著影响钙基吸收剂捕集CO2。Ridha等[10]对碳酸化/硫化行为进行了测试,发现随着循环的进行,SO2与CaO生成CaSO4,减弱了吸收剂对CO2的吸收性能。SO2的负面影响会随着循环累积,Wang等[11]在碳酸化阶段加入SO2后,发现硫化转化率几乎随循环次数增加线性增长。此外,碳酸化反应和硫化反应是竞争反应,并且在煅烧/碳酸化循环过程中吸收剂形成了更有利于SO2反应的形貌[12],导致吸收剂碳捕集能力下降。
目前,多数研究主要集中于H2O或SO2对钙循环捕集CO2的单独影响,虽有少量研究探讨了H2O和SO2在碳酸化过程中的协同效应,但作用机理尚不清楚。He等[13]在热重分析仪(TGA)和管式炉中进行了钙循环实验,发现高浓度SO2条件下,H2O对硫化的促进效果比对碳酸化的促进效果强,虽然结合微观吸附能解释了CO2和SO2竞争吸附的机理,但并未体现碳酸化和硫化反应过程,且无法反映SO2浓度的影响。Coppola等[14]在一个双流化床内发现0.007 5%φ(SO2)下,H2O对捕集CO2的促进作用强于SO2对捕集CO2的不利影响。
综上可知,烟气中H2O和SO2在钙循环捕集CO2过程中起到重要作用,也得到了很多有价值的结论,但在实验方法上仍需改进。在实际应用中,吸收剂通常直接喷入炉内,突然置于高温环境中,而TGA需要采用逐步升温的方式,对CaCO3的分解特性影响较大,且在煅烧与碳酸化环境气氛切换时,管道残留气氛会影响实验结果;循环流化床虽能够模拟工业环境,但难以对具体的反应动力学进行分析,不能有效评估炉内各因素的影响。为解决以上问题,笔者采用自制的恒温热重系统研究了碳酸化气氛中H2O和SO2对钙循环转化率以及反应过程的影响,探讨了H2O和SO2的协同作用,同时从微观孔结构上对反应特性进行分析,为CO2捕集技术的发展提供参考。
1 实验部分
1.1 实验系统与材料
钙循环恒温热重系统主要由碳酸化炉、煅烧炉、质量传感器和配气系统组成,如图1所示。该装置已经进行过大量的反应动力学实验,精度和准确度都可以得到保证[4]。
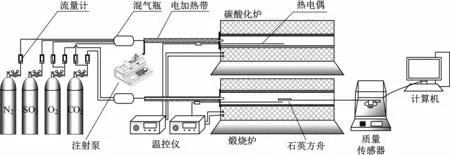
图1 恒温热重系统Fig.1 Thermostatic thermogravimetric system
选用保定石灰石,粒径为150~250μm,其成分如表1所示。每次称取150 mg石灰石放置于石英方舟中,实验时以恒定的速度送入煅烧炉中,煅烧完成后,通过滑轨将样品转移到碳酸化炉内进行碳酸化反应,以此进行循环测试。实验开始前,将煅烧炉和碳酸化炉升至所需温度,并且保温2 h以实现炉体温度稳定。混气体积流量为1.2 L/min,预先实验证实该流量能够充分消除碳酸化反应的外扩散阻力。

表1 石灰石各成分的质量分数Tab.1 Mass fraction of limestone composition%
实验工况如表2所示,笔者着重研究碳酸化阶段中H2O和SO2对钙循环捕集CO2的影响,因此煅烧气氛固定为80%体积分数的CO2和20%体积分数的O2。每组进行10次煅烧/碳酸化循环,每次煅烧和碳酸化时间均设置为4 min,之前的实验证实石灰石可以在该时间内煅烧完全。每组实验进行3次,并对结果取平均值以保证实验结果的准确性。

表2 实验工况Tab.2 Experimental condition
1.2 实验数据处理
实验开始时称量质量为m0的样品,进行N次煅烧后样品质量为mcal,N,经过碳酸化炉后的质量为mcar,N,则第N次碳酸化的转化率X N为:
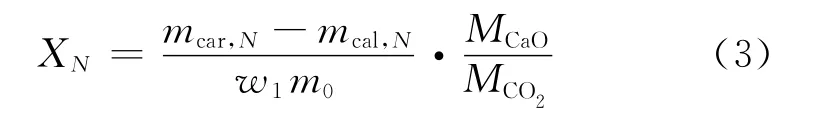
式中:w1为CaO在石灰石中的质量分数;MCaO和MCO2分别为CaO和CO2的摩尔质量。
由于硫化产物CaSO4在900℃煅烧温度下不会分解,一直存在于吸收剂中且随着循环次数增加而累积,循环中的硫化转化率Xsul为:
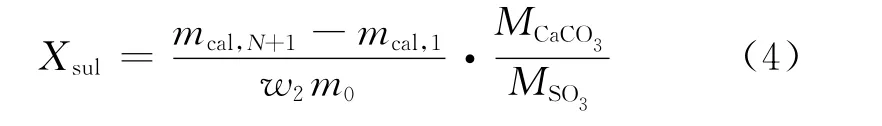
式中:w2为石灰石中CaCO3的质量分数;MCaCO3和MSO3分别为CaCO3和SO3的摩尔质量。
2 实验结果与讨论
2.1 碳酸化阶段中H2 O对钙循环的影响
不同H2O体积分数下的碳酸化转化率如图2所示。由图2可知,当碳酸化过程含H2O时,循环过程中的碳酸化转化率较无H2O时明显提升,并在多次循环后提升效果仍显著。随着H2O体积分数的增加,H2O对反应过程的促进作用会随之增强,但促进效果减弱,如10%φ(H2O)工况下首次碳酸化转化率比无H2O工况提升了3.27%,而20%φ(H2O)工况下仅提升了4.46%。这表明随着H2O体积分数增加,H2O对碳酸化转化率的促进效果并未线性增强。为了进一步探明H2O的作用,对第1和第5次碳酸化阶段中的样品质量变化进行了分析,结果见图3。

图2 不同H 2 O体积分数下的碳酸化转化率Fig.2 Carbonation conversion rate at different H2 O volume fractions

图3 不同H 2 O体积分数下碳酸化过程中的样品质量Fig.3 Sample mass during the carbonation process at different H 2 O volume fractions
通常认为,碳酸化反应包含快速反应和慢速反应2个阶段,且碳酸化转化率主要取决于快速反应阶段的转化程度。由图3可知,在240 s的碳酸化反应时间内,H2O加速了碳酸化反应快速反应阶段的反应速度,20%φ(H2O)工况下第1次碳酸化反应在170 s左右进入到慢速反应阶段,大约比10%φ(H2O)和无H2O工况下进入慢速反应阶段的时间提前20 s和60 s,第5次碳酸化过程也呈现了相同的趋势。同时,由于慢速反应阶段对最终的碳酸化转化率影响较小,因而H2O通过加速快速反应阶段的反应速度,提高了CaO吸收剂的CO2捕集能力。
H2O对碳酸化反应可能存在多种影响途径。一方面,H2O可能与CaO生成Ca(OH)2,加速了碳酸化反应。量子化学和分子动力学研究表明,在典型碳酸化条件下,H2O在CaO表面解离形成H+和OH-,能够与CaO形成类似Ca(OH)2结构的瞬态产物,进而与CO2反应生成CaCO3(见反应式(5))[13,15]。Blamey等[16-17]也发现相较于CaO的碳酸化反应,反应式(5)具有更快的反应速度。因此,加入H2O后,可能在碳酸化阶段生成了瞬态的Ca(OH)2,改变了碳酸化反应路径进而加速碳酸化反应速度。另一方面,H2O可能改变了CaO颗粒孔隙结构从而影响碳酸化反应速度。
2.2 碳酸化阶段中SO2对钙循环的影响
由于烟气中的SO2与CaO发生硫化反应,生成CaSO4而堵塞吸收剂孔隙,造成CO2捕集能力迅速下降。因此,分别对无SO2、0.05%φ(SO2)和0.1%φ(SO2)工况下的碳酸化过程进行了研究,结果如图4所示。

图4 不同SO2体积分数下的转化率Fig.4 Conversion rate at different SO2 volume fractions
由图4可知,在碳酸化阶段分别加入0.05%和0.1%体积分数的SO2后,首次循环中碳酸化转化率较无SO2工况分别下降了4.23%和6.29%,且随着循环的进行在第10次循环后碳酸化转化率下降幅度分别达到9.37%和13.36%。由图4(b)可知,硫化转化率随循环次数增加几乎呈线性增长趋势,增长速率随着SO2体积分数的增加而增加。由此可见,随着SO2体积分数的增加,硫化转化率升高,而碳酸化转化率下降较为明显。
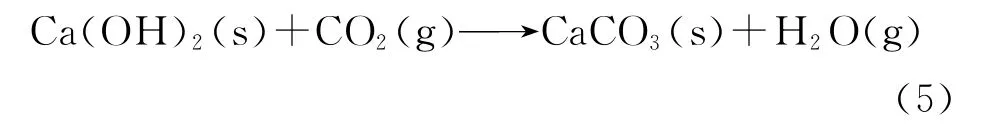
为了深入了解SO2在循环捕集CO2过程中的影响,研究了第1和第5次碳酸化阶段的样品质量变化,如图5所示。由图5可知,随着SO2体积分数的增加,硫化反应对碳酸化反应的负面影响更加明显。第1次碳酸化过程0.1%φ(SO2)工况下吸收剂质量增幅比0.05%φ(SO2)工况大,这并非是吸收剂在碳酸化过程中捕获了更多的CO2,而是生成了较多的CaSO4,如第1次循环中0.1%φ(SO2)工况下的硫化转化率较0.05%φ(SO2)工况提高了1.23%。此外,循环中累积的CaSO4会持续对钙循环特性造成影响。在第5次循环中,含SO2时的吸收剂质量增长缓慢,这是由于在经历了多次煅烧/碳酸化后,在CaO颗粒孔内生成的CaSO4不断累积,阻碍了CO2进入吸收剂内部,导致吸收剂的CO2捕集能力下降。因此,随着SO2体积分数和循环次数的增加,SO2对碳酸化反应的抑制作用更加明显。
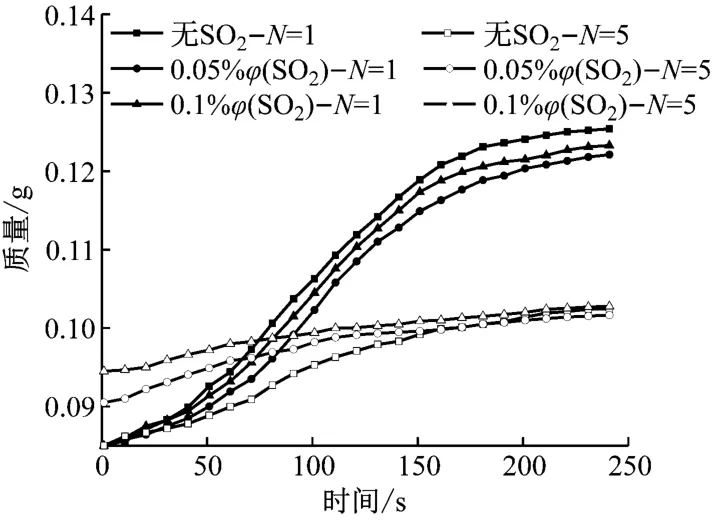
图5 不同SO2体积分数下碳酸化过程中的样品质量Fig.5 Sample mass during the carbonation process at different SO2 volume fractions
2.3 H2 O和SO2在碳酸化阶段的协同效应
以上探讨了H2O和SO2单独作用对碳酸化过程的影响。但是,作为影响CO2捕集的主要因素,烟气中H2O和SO2将共同作用于碳酸化过程。因此,本节通过改变H2O和SO2体积分数来探讨两者在碳酸化阶段的协同效应。
为探究H2O体积分数对碳酸化和硫化反应过程的影响,测试了在碳酸化阶段加入0.05%体积分数的SO2后H2O体积分数变化对钙循环特性的影响。如图6(a)所示,在碳酸化阶段0.05%φ(SO2)工况的基础上,加入H2O后能明显提升10次循环内的碳酸化转化率,这与H2O单独作用时类似。但是,气氛中0.05%体积分数的SO2对循环捕集CO2的抑制作用仍较为明显。
H2O的加入会使CaO硫化反应增强[18]。但如图6(b)所示,20%φ(H2O)工况下的硫化转化率却低于10%φ(H2O)工况,即硫化转化率随着H2O体积分数增加反而下降。这可能与碳酸化反应与硫化反应之间的竞争机制有关:碳酸化和硫化反应同时消耗CaO,二者之间存在竞争关系[12]。在15%φ(CO2)和0.05%φ(SO2)工况下,当H2O体积分数由10%增加到20%时,碳酸化反应速度增加,因而消耗了更多的CaO,导致参与硫化反应的CaO浓度降低、反应面积减小,由此造成的硫化反应减缓程度大于H2O体积分数增加对硫化反应带来的促进作用,从而使硫化反应速度下降,硫化转化率降低。

图6 H2 O在协同效应中的影响Fig.6 Influence of H2 O on synergistic effect
碳酸化阶段中的SO2导致吸收剂活性下降,但加入H2O后会明显改善钙基吸收剂的循环活性,表现为H2O减弱了SO2对碳酸化反应的抑制作用。由图6(a)可知,无H2O时第5次循环中0.05%φ(SO2)使碳酸化转化率较无SO2工况下降了11.68%,而加入20%体积分数的H2O使碳酸化转化率仅下降了6.17%。
此外,考虑到不同燃煤烟气中的SO2体积分数不同,对10%φ(H2O)工况下无SO2、0.05%φ(SO2)和0.1%φ(SO2)时CaO吸收剂的循环煅烧/碳酸化特性进行了分析,如图7所示。
由图7(a)可知,随着SO2体积分数增加,SO2对碳酸化反应的抑制作用更加明显,但10%φ(H2O)仍能使钙基吸收剂保持较高的碳酸化转化率。由图7(b)可知,随着SO2体积分数的增加,硫化转化率升高,且在加入10%体积分数的H2O后,硫化转化率进一步提升。此外,在碳酸化阶段加入10%体积分数的H2O和0.1%体积分数的SO2后,硫化转化率每次增长约为1.2%,几乎比0.05%φ(SO2)工况下的0.64%高出一倍,这会导致碳酸化转化率明显下降。但由图7(a)还可知,加入10%体积分数的H2O和0.1%体积分数的SO2后,碳酸化转化率仍高于0.05%φ(SO2)工况下的碳酸化转化率。这表明10%体积分数的H2O对碳酸化反应的促进作用强于对硫化反应的促进作用,使吸收剂在硫化转化率较高的同时仍能保持较好的CO2捕集能力。
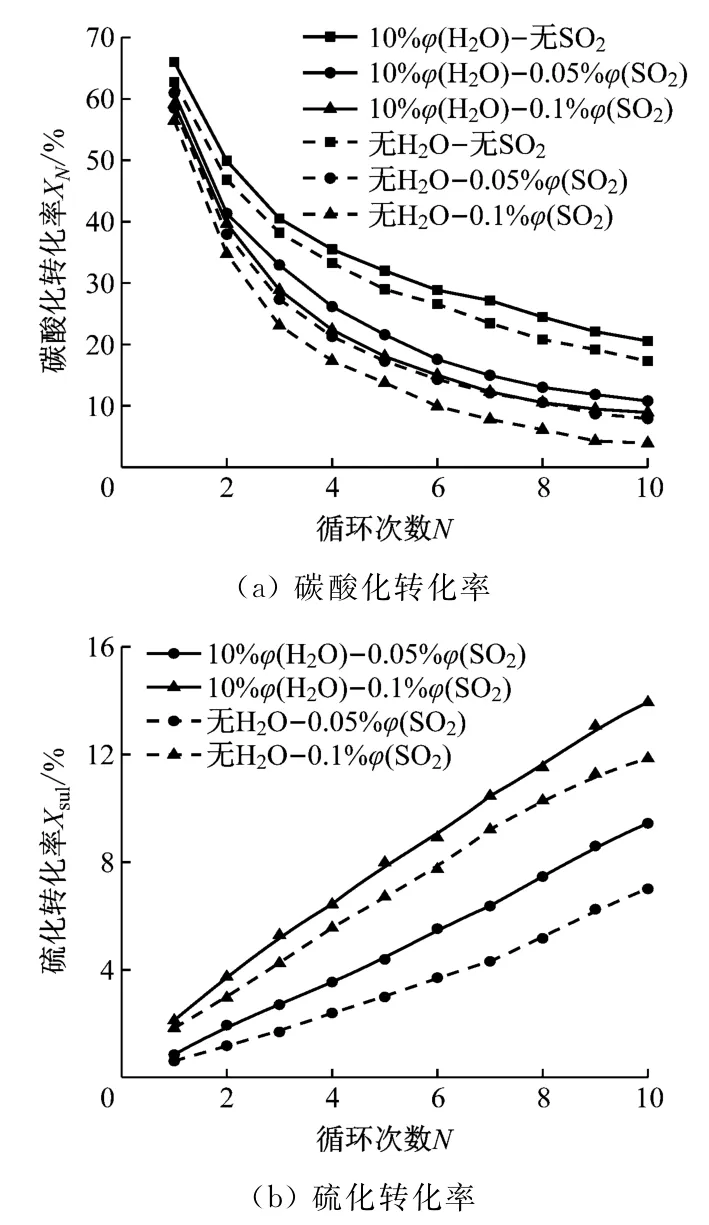
图7 SO2在协同效应中的影响Fig.7 Influence of SO2 on synergistic effect
2.4 孔结构分析
为了进一步探讨H2O和SO2在碳酸化阶段的影响,采用氮气吸附方法测量了不同工况下的孔结构。考虑到H2O和SO2持续对循环过程产生影响,选用第5次煅烧后的CaO吸收剂进行孔结构特性分析。
2.4.1 H2O和SO2对CaO颗粒孔结构的影响
如图8(a)所示,CaO吸收剂在10%φ(H2O)工况下经过5次煅烧后,比表面积和孔容积分别为4.89 m2/g和16.13 mm3/g,较无H2O工况下分别提升了23.8%和19.3%,同时,图8(b)(V为比孔容积,W为孔隙宽度)中介孔(2~<20 nm)和大孔(20~100 nm)的孔隙体积较无H2O工况均有所提升。当单独加入0.05%体积分数的SO2后,比表面积和孔容积降低至3.77 m2/g和8.77 mm3/g,且孔隙体积明显小于无SO2工况,这表明持续积累的CaSO4破坏了CaO颗粒的孔结构。
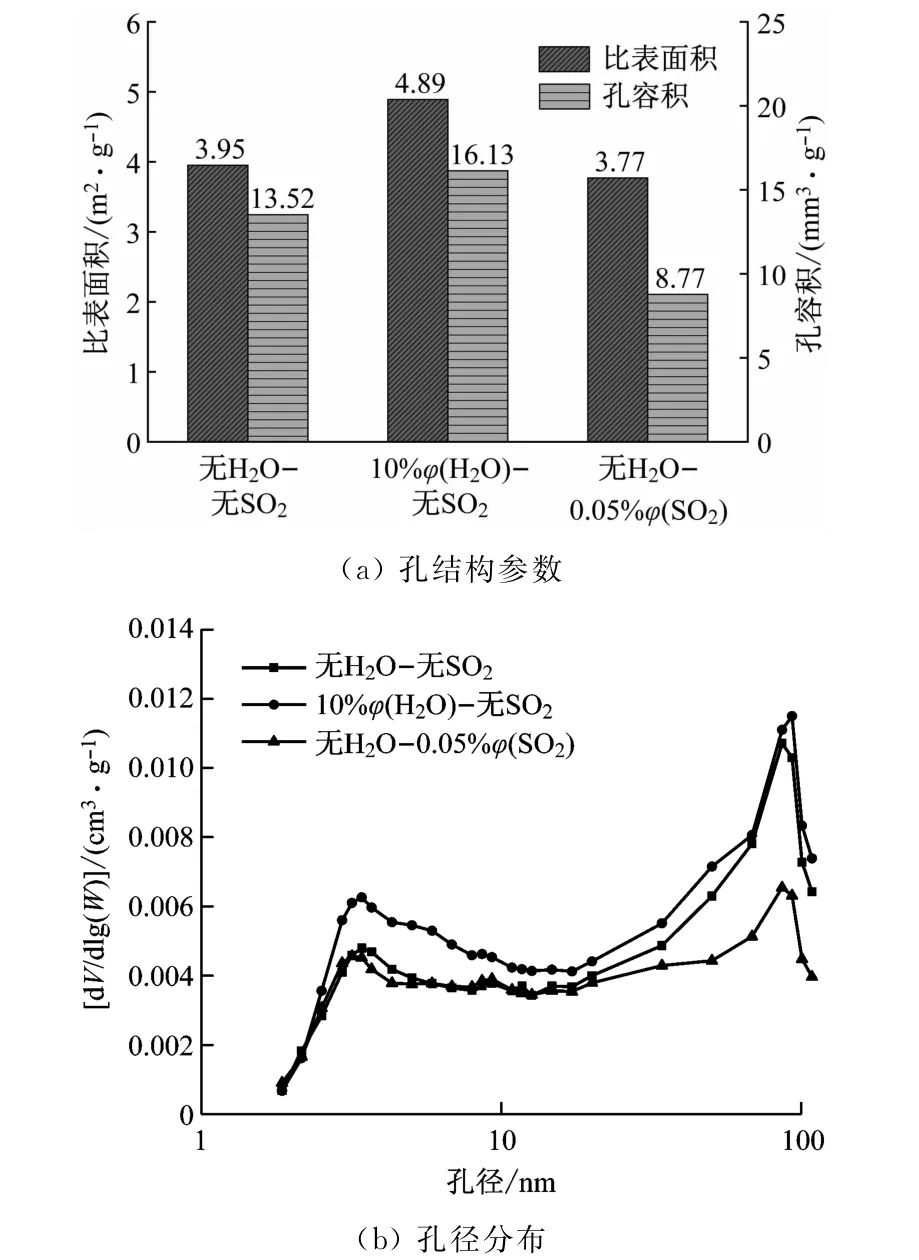
图8 H 2 O和SO2单独作用时第5次煅烧后吸附剂孔结构参数和孔径分布Fig.8 Pore structure and size distribution of adsorbent after the fifth calcination when H 2 O and SO2 acting alone
通常情况下,反应气体通过扩散方式进入固体孔内。因此,采用有效扩散系数De对不同工况下CO2在固体孔内的扩散特性进行分析。对于煅烧后钙基吸收剂颗粒,有效扩散系数的计算方法[19]如下:

式中:Dg为固体孔内的气体扩散系数;ε为孔隙率。
Dg由分子扩散系数DM和Knudsen系数Dk构成:

分子扩散系数的计算公式[20]为:
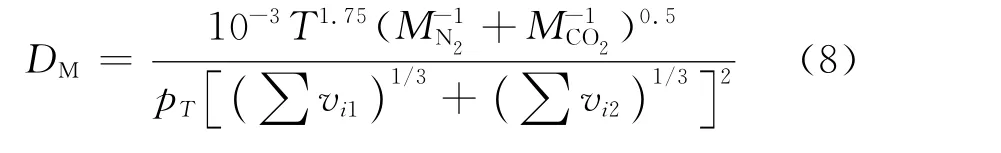
式中:T为碳酸化反应的热力学温度;MN2为N2的摩尔质量;p T为反应系统的压力;Σv i1和Σv i2分别为N2和CO2的扩散容积。
Knudsen扩散系数为:

式中:¯d为平均孔径,可由氮吸附测试结果计算得出。
假设CaO颗粒内孔径呈圆柱形,则平均孔径为:

式中:S为比表面积。
式(10)可用于单峰孔径分布的平均孔径计算。观察图8(b)可知,CaO颗粒的实际孔径分布呈双峰状特点,因此分别计算小于20 nm和大于等于20 nm的平均孔径(以下简称孔径)的CO2有效扩散系数,结果见表3和表4。
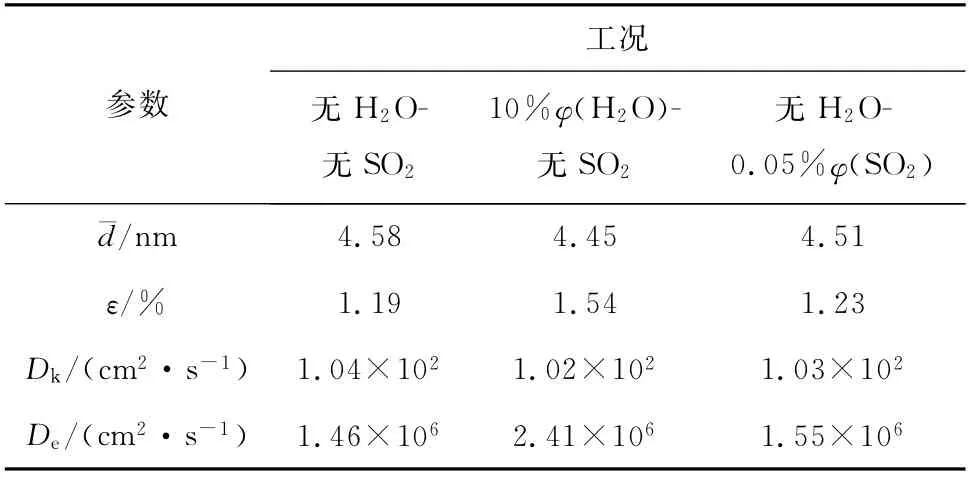
表3 CO2在CaO颗粒孔(孔径<20 nm)内的有效扩散系数Tab.3 Effective diffusion coefficient of CO2 in CaO particle with pore size<20 nm

表4 CO2在CaO颗粒孔(孔径≥20 nm)内的有效扩散系数Tab.4 Effective diffusion coefficient of CO2 in CaO particle with pore size≥20 nm
对比表3与表4可知,孔径小于20 nm的孔的有效扩散系数远小于20 nm以上孔径的孔的有效扩散系数,因此可以忽略孔径小于20 nm的孔对有效扩散系数的作用。由表4可知,10%φ(H2O)工况下的有效扩散系数大于无H2O工况。结合图8可知,H2O的加入改善了吸收剂的孔结构,使CaO吸收剂在多次循环后仍能保持较高的碳酸化转化率。此外,单独加入0.05%体积分数的SO2后,CaO颗粒孔内CO2的有效扩散系数仅为无SO2工况下的22.5%,这表明CaO颗粒孔内生成CaSO4堵塞孔隙,CO2扩散阻力增加,导致碳酸化转化率下降。
2.4.2 H2O和SO2对碳酸化反应的协同作用机理
由实验结果可知,H2O的加入显著提高了钙循环煅烧/碳酸化捕集CO2的性能,且在一定程度上减弱了硫化所带来的负面效果。因此,当H2O和SO2协同作用时,吸收剂的孔结构将发生进一步的转变。
如图9(a)所示,在碳酸化阶段加入0.05%体积分数的SO2后,当H2O体积分数从0%增加至20%时,CaO吸收剂比表面积虽无明显变化,但孔容积却显著提升。图9(b)进一步表明随着H2O体积分数增加,孔径分布的峰值升高。这表明在SO2作用于碳酸化阶段时,增加H2O体积分数仍能改善吸收剂的多孔性能。
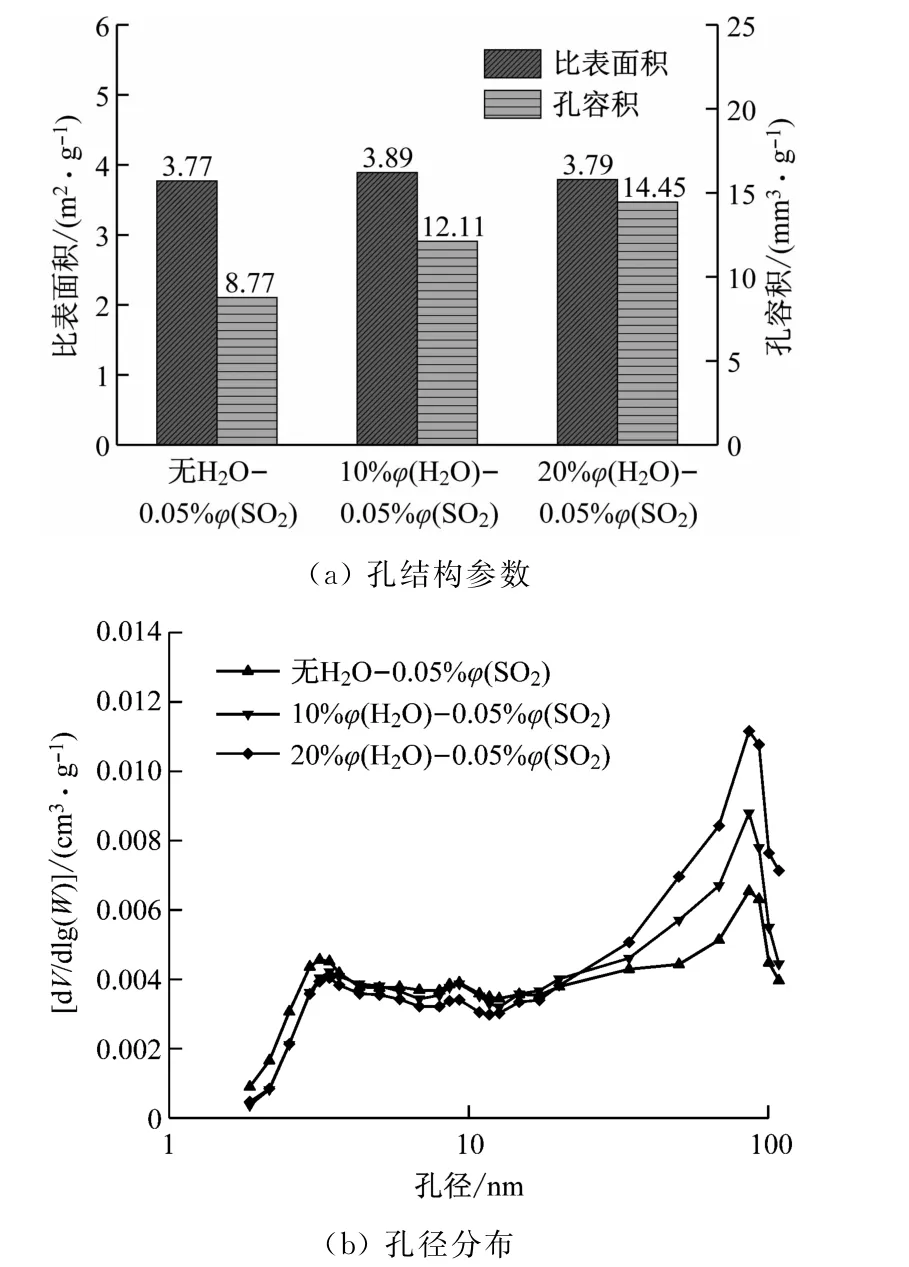
图9 H 2 O体积分数在协同作用中的影响Fig.9 Influence of H2 O volume fraction on synergistic effect
由图10(a)可知,10%φ(H2O)工况下CaO吸收剂比表面积和孔容积均随着SO2体积分数的增加而下降,且图10(b)中孔隙体积也随之明显下降。这说明尽管H2O的加入改善了吸收剂孔结构,使碳酸化转化率升高,但随着SO2体积分数的增加,仍会持续堵塞吸收剂孔隙。
基于图9与图10中的孔结构数据,计算了不同工况下CO2在CaO颗粒孔内的有效扩散系数(见表5)。由表5可知,0.05%体积分数的SO2单独作用时CO2在CaO颗粒孔内的有效扩散系数最小,但当H2O体积分数从0%增加至10%再增加至20%时,有效扩散系数分别升高了2.08倍和5.46倍,CO2在CaO吸收剂孔内的扩散能力增强。结合图6可知,随着H2O体积分数的增加,SO2对碳酸化反应的抑制效果减弱。这表明当SO2存在时,H2O仍使CaO吸收剂保留较好的孔结构,改善了吸收剂的CO2捕集能力,且改善效果随H2O体积分数增加而更加明显。由表5还可知,10%体积分数的H2O单独作用时,有效扩散系数最大,但随着SO2体积分数的增加,有效扩散系数迅速下降。这说明尽管H2O改善了吸收剂孔结构,但SO2的负面影响仍存在。因此,在进行钙循环捕集CO2之前,要尽可能地去除燃煤烟气中的SO2。

图10 SO2体积分数在协同作用中的影响Fig.10 Influence of SO2 volume fraction on synergistic effect

表5 H2 O和SO2的协同作用对CO2有效扩散系数的影响Tab.5 Influence of H2 O and SO2 synergistic effect on CO2 effective diffusion coefficient
3 结 论
(1)当H2O单独作用于碳酸化阶段时,显著提升了循环过程中的CO2捕集效率,但碳酸化转化率不会随着H2O体积分数的增加而线性增长。
(2)当SO2单独存在时,由于硫化反应生成CaSO4而堵塞孔隙,阻碍CO2扩散到CaO颗粒内部,导致碳酸化反应减缓,CO2捕集能力下降。
(3)当H2O和SO2协同作用时,H2O体积分数增加明显减弱了SO2对碳酸化反应的负面影响,从而提升碳酸化转化率,即H2O对碳酸化反应的促进作用大于对硫化的负面效应;在碳酸化阶段加入10%体积分数的H2O后,CO2捕集能力随着气氛中SO2体积分数的增加而持续下降,但与相同体积分数的SO2单独作用时相比,H2O对碳酸化反应的促进作用仍较为显著。
