TiO2/GO-Fe3O4复合材料的制备及性能研究
2022-08-11刘晨浩姜承志
刘晨浩,姜承志
(沈阳理工大学 环境与化学工程学院,沈阳110159)
环境污染和能源短缺是现代人类社会所面临的两大问题,其中环境污染是当今世界突出的问题,除了节能减排、优化产业结构外,治理环境污染问题仍是尤为重要的研究内容[1]。对纺织材料(纤维、纱、线和织物)进行以化学处理为主的工艺过程称为染整,染整过程中染料并不会完全附着在材料表面,其中10%~15%的染料因未固定而流失[2]。目前工业环境中有近10万种染料,每年约有1000吨不可降解的染料被释放到水资源中[3],全国染织厂每年废水排放量占整个纺织行业废水排放量的80%[4-5],印染废水是难以降解的工业废水之一。
光催化水处理技术因具有较低的能耗、操作简便、效率高、无二次污染等优点[6],与传统的催化方法相比,具有显著的优势[7],被公认为解决全球能源和环境问题的主要方法之一,是去除废水中有机污染物的理想选择,具有广阔的发展前景[8]。
二氧化钛(TiO2)是一种成本低和环境友好的半导体材料,因其具有稳定的化学性质、较好的耐酸碱性等特性,在光催化方面备受关注[9]。目前研究最多的锐钛矿型TiO2,其禁带宽度约为3.2eV,在可见光和近红外区利用太阳能的效率相对较低。另外由于光生电子和空穴复合几率很高,导致TiO2光生载流子利用效率低。通过对TiO2进行掺杂、修饰、复合等拓宽TiO2的禁带宽度,可改善TiO2半导体材料的光催化活性。
氧化石墨烯(GO)为石墨烯的氧化产物,是石墨烯最重要的衍生物之一。GO是一种多分散的材料,为非晶态[10],在很多方面都具有优异的性能,因其具有极大的比表面积和较低的生产成本,非常适合开发高性能的光催化复合材料[11]。同时,其优异的导电性可大大提高光生电子和空穴的传输速率,解决复合率高的问题,从而大大提高光催化效率[12-13]。
许文涛等[14]采用溶胶凝胶法制备了复合光催化剂GO/TiO2,经过2h的光催化反应,对甲基橙的降解率达到了92.7%。由于分离过程复杂,单独的TiO2很难在水溶液中重复使用,因此开发一种易于回收的光催化材料很有必要。王瑞萌等[15]将Fe3O4加入光催化剂中,制备得到复合材料,该材料既具有光催化性能,又具有磁性,有利于光催化反应后的固液分离。
本文采用共沉淀法制备磁性氧化石墨烯(GO-Fe3O4),采用水热法制备二氧化钛/磁性氧化石墨烯复合材料(TiO2/GO-Fe3O4),研究GO用量、异丙醇用量、钛酸四丁酯用量、水热反应温度、反应投加量等对TiO2/GO-Fe3O4复合材料光催化性能的影响。
1 实验部分
1.1 实验试剂及仪器
1.1.1 实验试剂
氧化石墨烯水溶液,苏州碳丰石墨烯科技有限公司;钛酸四正丁酯(化学纯)、异丙醇(分析纯)、无水乙醇(分析纯),国药集团化学试剂有限公司;三氯化铁(FeCl3·6H2O)、硫酸亚铁(FeSO4·7H2O)、氨水(25%)、亚甲基蓝,均为分析纯,天津市大茂化学试剂厂。
1.1.2 实验仪器
JJ-4型六联电动搅拌器、HH-2数显恒温水浴锅,常州国华电器有限公司;101-0BS型电热鼓风恒温干燥箱,上海力辰邦西仪器科技有限公司;20W紫外灭菌灯,广东雪莱特光电科技股份有限公司;78-1型磁力加热搅拌器,郑州博科仪器设备有限公司;QUANTA250扫描电子显微镜,美国FEI公司;FT-IR/FIR中远红外光谱仪,美国PE公司;ASAP 2460多站扩展式全自动比表面与孔隙度分析仪,麦克默瑞提克仪器有限公司;D8 Advance X射线衍射仪,德国布鲁克公司。
1.2 材料的制备
1.2.1 GO-Fe3O4的制备
将2mg/mL的GO溶液分别稀释成浓度不同的GO溶液,各取50mL,分别加入0.8745g FeCl3·6H2O和1.797g FeSO4·7H2O,超声分散30min;加氨水调节pH值至10~11;在60℃水浴下机械搅拌2h;抽滤后,用蒸馏水洗涤至中性,50mL无水乙醇洗涤一次;在烘箱中50℃干燥4h,将干燥后的固体研磨成粉,制备得到GO-Fe3O4。
1.2.2 TiO2/GO-Fe3O4的制备
将4mL钛酸四丁酯溶于异丙醇44mL中,磁力搅拌30min;加入20mL蒸馏水,称取0.128g GO-Fe3O4加入上述混合溶液中,超声分散2h,转入100mL反应釜中;将反应釜放入干燥箱,在80℃温度下反应8h;自然冷却至室温,抽滤,用蒸馏水洗涤至中性,50mL无水乙醇洗涤一次;在烘箱中50℃干燥4h,将干燥后的固体研磨成粉,制备得到TiO2/GO-Fe3O4。
1.3 材料的性能分析与测试
1.3.1 光催化性能
光催化实验装置为实验室自行搭键,亚甲基蓝溶液置于距光源15cm处,将30mg的TiO2/GO-Fe3O4样品放于100mL浓度为6mg/L的亚甲基蓝溶液中,暗吸附30min,然后在20W紫外灯下照射2h,每隔20min取样,用滤膜过滤后,在波长664nm处测定吸光度。TiO2/GO-Fe3O4样品对亚甲基蓝溶液的光催化降解率D计算式为
(1)
式中:A0为光照前亚甲基蓝溶液的吸光度;At为光照时间为t时亚甲基蓝溶液的吸光度。
1.3.2 材料表征
采用红外光谱(FT-IR)分析样品,将样品压片后,放于样品室,在波数400~4000cm-1范围内扫描。根据谱图中吸收峰的位置判断化学键和官能团的相关信息。
通过对材料进行X射线衍射(XRD),获得其衍射图谱,通过MDI Jade软件对衍射图谱进行物相检索获取材料成分的相关信息。X射线衍射仪采用40kV工作管电压和40mA工作管电流,步长0.02,扫描速度10°/min,扫描范围20~90°。
利用扫描电子显微镜(SEM)对TiO2/GO-Fe3O4样品进行观测,获得各样品的粒径大小及表面形貌图片。
采用全自动比表面积和孔径分析仪对样品进行N2吸-脱附实验,得到各样品的N2吸-脱附曲线,采用BJH模型和BET模型进行分析,获得材料的比表面积和孔结构。
2 结果与讨论
2.1 GO浓度对降解率的影响及光催化材料的表征
2.1.1 GO浓度对降解率的影响
在不同GO浓度下制备TiO2/GO-Fe3O4,通过光催化实验得到GO浓度对亚甲基蓝降解率的影响趋势,如图1所示。
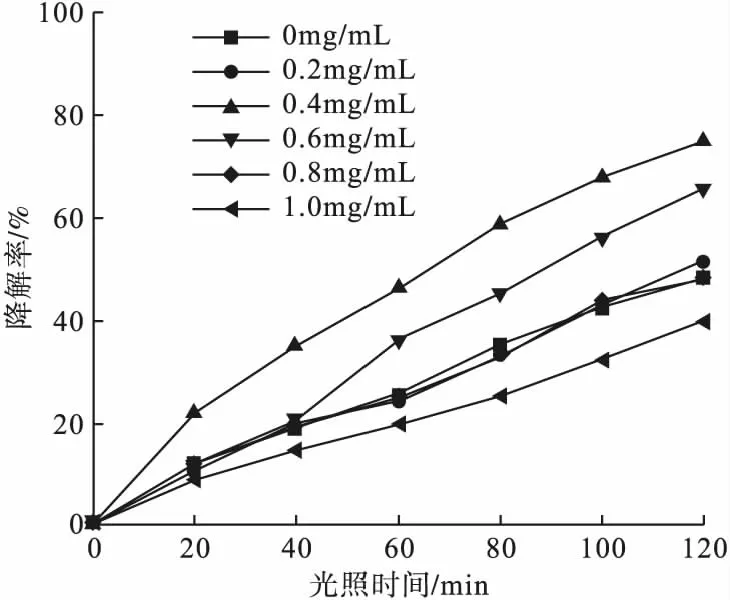
图1 GO浓度对亚甲基蓝降解率的影响
由图1可见,随着光照时间延长,降解率逐渐增大;经过2h紫外光光照后,随着GO浓度的增加,光催化降解率先增加后减少;当GO浓度为0.4mg/mL时,制备样品对亚甲基蓝的降解率最高,达到75%。由于GO浓度增大,即其用量增多,TiO2/GO-Fe3O4复合材料的比表面积增加,更多的亚甲基蓝分子能够被吸附在材料表面,有利于提高光催化效率;GO用量增多,也会使TiO2产生的光电子更好地通过GO进行转移,进一步提高电子-空穴的分离效率,阻碍光电子的复合,使得TiO2/GO-Fe3O4复合材料的光催化性能显著提高;若继续增加GO用量,由于石墨烯材料具有很强的疏水特性,容易聚集结块,反而会降低材料的比表面积,使光催化效率下降。因此,GO用量是制备光催化材料的一个比较重要的影响因素,本实验选用适宜的GO浓度为0.4mg/mL。
2.1.2 红外光谱(FT-IR)分析
将不同GO浓度下制备的样品进行红外光谱分析,得到不同样品在中红外区内的光吸收情况,如图2所示。
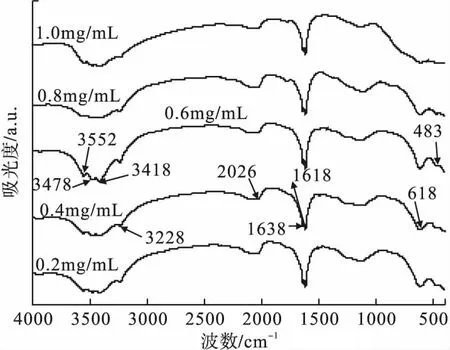
图2 TiO2/GO-Fe3O4的FT-IR光谱
由图2可见,GO用量的增加并没有引起TiO2/GO-Fe3O4复合材料官能团的增加或减少,所有样品的红外吸收谱图基本一致。波数3418cm-1和1618cm-1处分别对应—OH伸缩振动峰和弯曲振动峰,说明TiO2/GO-Fe3O4样品表面都含有羟基或者被吸附的水分;波数1638cm-1处的吸收峰是C=C伸缩振动峰;波数483cm-1的吸收峰归属于TiO2的Ti—O—Ti伸缩振动和Ti—O的弯曲振动;波数618cm-1的吸收峰归属于Fe3O4中Fe—O键的特征吸收峰。文献[16]的研究表明,Fe3O4中Fe—O键的吸收峰在586cm-1处,低于本文制备的复合材料中Fe—O键吸收峰对应的波数,说明Fe—O键发生了红移,有利于该材料对可见光的吸收,增强光催化效果。
2.1.3 XRD分析
对不同GO浓度下制备的TiO2/GO-Fe3O4样品进行XRD分析,获得衍射图谱如图3所示。

图3 TiO2/GO-Fe3O4的XRD谱图
由图3可见,不同GO用量下制备的TiO2/GO-Fe3O4复合材料的X射线衍射光谱图基本一致,所有样品的X射线衍射峰与锐钛矿TiO2(标准卡片编号为PDF#73-1764)和磁性Fe3O4(标准卡片编号为PDF#75-0449)的衍射峰匹配度一致,说明本文制备的材料为锐钛矿TiO2和磁性Fe3O4的复合物。
2.1.4 SEM分析
利用扫描电子显微镜对不同GO浓度下制备的TiO2/GO-Fe3O4样品进行观测,获得其形貌照片如图4所示。

图4 TiO2/GO-Fe3O4的SEM图片
由图4可见,不同GO浓度下制备TiO2/GO-Fe3O4复合材料的SEM照片有所不同。当GO浓度为0.2mg/mL(图4a)和0.6mg/mL(图4c)时样品因团聚呈小颗粒状;当GO浓度为0.8mg/mL(图4d)时,样品形貌虽然平坦,但由于GO用量大,会造成样品孔径增大,反而不利于提高光催化效率;当GO浓度为0.4mg/mL(图4b)时,样品中无较大的团聚颗粒,且分布均匀,可提供更多的活性点位,有利于提高光降解效率。该结果与图1结论一致。
2.1.5 比表面积与孔径分析
采用全自动比表面积和孔径分析仪对不同GO浓度下制备的TiO2/GO-Fe3O4样品进行分析,得到各样品的N2吸-脱附曲线如图5所示,孔径分布图如图6所示,同时获得材料的比表面积和孔结构参数如表1所示。
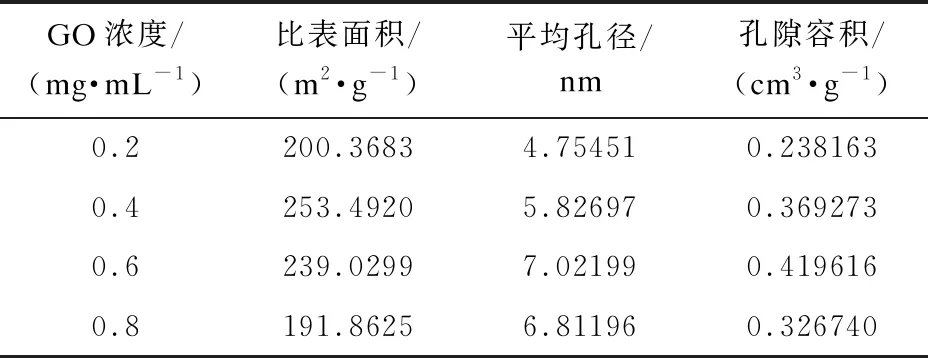
表1 TiO2/GO-Fe3O4的比表面积和孔结构参数

图5 TiO2/GO-Fe3O4的N2吸-脱附曲线

图6 TiO2/GO-Fe3O4的孔径分布图
根据国际纯粹与应用化学联合会(International Union for Pure and Applied Chemistry,IUPAC)对吸附等温线的分类[17],图5中样品的吸附等温线符合Ⅳ型吸附等温线特征,说明样品中存在介孔;根据IUPAC对回滞环的分类,回滞环分为六种,本文制备的所有样品中均具有回滞环,且属于H3型回滞环;等温线没有明显的饱和吸附平台,表明孔结构很不规整。
由图6可见,GO浓度为0.2mg/mL时制备的TiO2/GO-Fe3O4复合材料的孔径分布在0~60nm范围内;GO浓度为0.4mg/mL时制备的TiO2/GO-Fe3O4复合材料的孔径分布在0~95nm范围内;GO浓度为0.6mg/mL时制备的TiO2/GO-Fe3O4复合材料的孔径分布在0~80nm范围内;GO浓度为0.8mg/mL时制备的TiO2/GO-Fe3O4复合材料的孔径分布在0~75nm范围内。故随着GO浓度的增加,TiO2/GO-Fe3O4复合材料的孔径范围先增宽再减小。
光催化材料孔径大小会影响其光催化效果,当孔径大小在合适的范围内时,有机分子更容易进入孔内,利用孔内表面积,占据更多活性点位,有利于提高光催化降解效率;但材料孔径过大,会增大被降解物在孔道内的扩散阻力,反而使其降解效率下降[18]。结合图1结论,当GO浓度为0.4mg/mL时,样品的光催化效率最高,由图6可知,当GO浓度为0.4mg/mL时,样品的孔径大小主要分布在10~70nm,说明在适宜的孔径尺寸范围内,可达到较高的光催化效率。
由表1可知,当GO溶液浓度为0.4mg/mL时,制备出的TiO2/GO-Fe3O4复合材料的比表面积最大,为253.4920m2/g。比表面积越大,单位质量材料吸收的亚甲基蓝分子越多,降解效率越高。
2.2 异丙醇用量对降解率的影响
在不同异丙醇用量下制备TiO2/GO-Fe3O4复合材料,通过光催化实验得到异丙醇用量对亚甲基蓝降解率的影响,如图7所示。

图7 异丙醇用量对亚甲基蓝降解率的影响
由图7可见,随着异丙醇用量的增加,经过2h紫外光光照后,TiO2/GO-Fe3O4对亚甲基蓝溶液的降解率先升高后降低;当异丙醇用量为44mL时,TiO2/GO-Fe3O4复合材料对亚甲基蓝的光催化降解率最高,为75.57%。当异丙醇用量从36mL增加到44mL时,TiO2/GO-Fe3O4对亚甲基蓝的降解率提升了17%左右,说明异丙醇用量对TiO2/GO-Fe3O4的光催化活性具有较大影响。由于异丙醇的加入会抑制钛酸四丁酯的水解速度,并且对TiO2的成型过程产生影响,从而导致不同异丙醇用量下TiO2/GO-Fe3O4降解亚甲基蓝效率的差异。本实验选用适宜的异丙醇用量为44mL。
2.3 钛酸四丁酯用量对降解率的影响
在不同钛酸四丁酯用量下制备TiO2/GO-Fe3O4复合材料,通过光催化实验得到钛酸四丁酯用量对亚甲基蓝降解率的影响,如图8所示。

图8 钛酸四丁酯用量对亚甲基蓝降解率的影响
由图8可见,随着钛酸四丁酯用量增加,经过2h紫外光光照后,TiO2/GO-Fe3O4对亚甲基蓝的降解率呈现上升的趋势;当钛酸四丁酯的用量增至12mL时,降解率达到90.77%;当钛酸四丁酯从2mL增加到6mL时,TiO2/GO-Fe3O4对亚甲基蓝的降解率提升程度较大,从67.68%升高到87.26%,其用量从6mL增加到12mL时,光催化降解率仅提高3.51%,同时磁铁吸引实验表明,钛酸四丁酯用量为12mL时制备的TiO2/GO-Fe3O4比钛酸四丁酯用量为6mL时制备的TiO2/GO-Fe3O4的磁性明显降低,这可能是钛酸四丁酯水解生成大量的TiO2包覆GO-Fe3O4,导致其磁性降低。综合考虑材料对亚甲基蓝的降解率和材料的磁性,选择适宜的钛酸四丁酯用量为6mL。
2.4 水热反应时间对降解率的影响
改变水热反应时间制备TiO2/GO-Fe3O4复合材料,通过光催化实验得到水热反应时间对亚甲基蓝降解率的影响,如图9所示。
由图9可见,随着水热反应时间的增加,经过2h紫外光光照后,TiO2/GO-Fe3O4对亚甲基蓝的降解率先升高后降低;当水热反应时间为8h时,TiO2/GO-Fe3O4对亚甲基蓝的降解率最高,为86%。由于水热反应时间会影响材料晶体的生长速率,改变晶体的结构尺寸,从而对其光催化活性造成影响。本实验选择适宜的水热反应时间为8h。

图9 水热反应时间对亚甲基蓝降解率的影响
2.5 磁性分析
在上述适宜条件下制备TiO2/GO-Fe3O4复合材料,采用振动样品磁强计测试其磁滞回线,结果如图10所示。
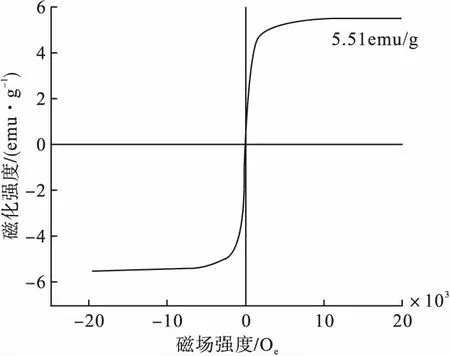
图10 TiO2/GO-Fe3O4的磁滞回线
由图10可知,TiO2/GO-Fe3O4的饱和磁化强度为5.51emu/g,说明TiO2/GO-Fe3O4具有磁性,有助于磁性回收。
2.6 催化剂投加量对降解率的影响
TiO2/GO-Fe3O4投加量分别取为10、20、30、40、50、60mg(以100mL亚甲基蓝溶液为基准),通过光催化实验得到投加量对亚甲基蓝降解率的影响,如图11所示。
由图11可见,随着TiO2/GO-Fe3O4投加量的增加,经过2h紫外光光照后,亚甲基蓝降解率先升高,然后稳定在最高值;当投加量为30mg时,TiO2/GO-Fe3O4复合材料对亚甲基蓝的降解效率达到86%;投加量再继续增加,光催化降解率不再提高,保持在86%左右。随着TiO2/GO-Fe3O4投加量的增加,更多的光催化剂粒子参与到反应中,故降解率提高。随着投加量继续增加,光催化降解率不再增加,其原因有两点:其一,投加量为30mg时,TiO2/GO-Fe3O4对所设光源的利用效率已经达到饱和,此时继续增加投加量,TiO2/GO-Fe3O4对亚甲基蓝的降解率不再增长;其二,随着投加量增多,溶液中一部分TiO2/GO-Fe3O4粒子占据了有效光照面积,掩蔽了光照,导致另一部分TiO2/GO-Fe3O4材料颗粒无法接收到光子能量,价带中的电子无法发生跃迁,阻碍了这部分材料的光催化反应发生。因此,当投加量达到一定值后,TiO2/GO-Fe3O4对亚甲基蓝溶液的光催化降解率基本稳定。
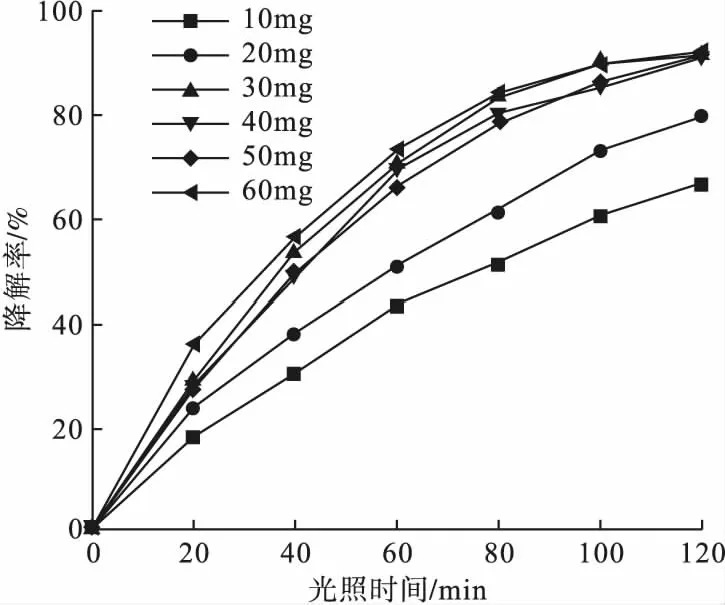
图11 TiO2/GO-Fe3O4投加量对降解率的影响
3 结论
采用共沉淀-水热法制备了TiO2/GO-Fe3O4复合材料光催化剂。以光照2h的降解率为目标,确定适宜的制备条件为:GO浓度0.4mg/mL、异丙醇用量44mL、钛酸四丁酯用量6mL、水热反应时间8h,适宜的催化剂投加量为30mg,此时TiO2/GO-Fe3O4对亚甲基蓝的光催化降解率可达86%。
复合材料的性能和结构测试结果显示,GO浓度的变化影响材料的表面形貌、比表面积及孔径尺寸,进而影响其光催化性能;在实验选取的GO浓度变化范围内,均能获得锐钛矿TiO2和磁性Fe3O4的复合物;GO的加入使Fe3O4中Fe—O键发生了红移;TiO2/GO-Fe3O4复合材料中含有Fe3O4,具有磁性,可利用其磁性进行分离回收。
本文所用石墨烯为氧化石墨烯水溶液,为提高复合材料光催化效率,可采用石墨烯。本文采用共沉淀法制备的磁性氧化石墨烯粒径偏大,团聚较明显,且分布不均,对于磁性氧化石墨烯的制备可尝试采用其他方法,以期能制备出粒径均一的颗粒,进一步提高其光催化活性。
