中医禁食疗法对超重/肥胖2型糖尿病患者的临床疗效
2022-08-11张汀滢刘桃丽胡建国张丽叶智裕李志铃陈洪达秦鉴
张汀滢,刘桃丽,胡建国,张丽,叶智裕,李志铃,陈洪达,秦鉴
(中山大学附属第七医院中医科,广东深圳 518107)
2 型糖尿病目前已经被视为人类健康的重要威胁,据2020 年最新数据统计,我国糖尿病患病率已达到12.8%[1],因此寻找2 型糖尿病更有效的治疗方法迫在眉睫。越来越多研究表明,热量限制可以逆转或缓解2 型糖尿病,且逆转效果与体质量减轻的程度密切相关[2-3]。作为热量限制的一种特殊形式,中医禁食疗法结合了西方热量限制与中医药,形成了一套独具中医特色的、适合中国人体质的热量限制方法,已在临床运用[4]。既往研究表明,1 次中医禁食疗法可降低2 型糖尿病患者的空腹血糖、OGTT 2 h 血糖、糖化血红蛋白以及体质量和BMI[5-6],但随访期较短。因此,本研究拟通过纳入超重∕肥胖2 型糖尿病患者,进行1 次为期7 d 的中医禁食疗法,后随访6 个月时间,并通过空腹血糖、空腹胰岛素、HOMA-IR、糖化血红蛋白以及其他代谢性指标,评估中医禁食疗法对超重∕肥胖2型糖尿病的短期以及中远期临床疗效。
1 材料与方法
1.1 研究对象
本研究于2019年5月至2019年12月于中山大学附属第七医院招募超重∕肥胖2型糖尿病患者,所有患者均已在首次入院时签署知情同意书,并同意使用相关病例及随访资料。本研究方案遵从《赫尔辛基宣言》,已通过中山大学附属第七医院医学伦理委员会审批,审批编号:2019SYSUSH-009。
1.2 纳入及排除标准
1.2.1 纳入标准 年龄18~65岁;诊断2型糖尿病(诊断标准参见《中国2 型糖尿病防治指南(2017版)》);超重∕肥胖:BMI≥24 kg∕m2;心肝肾功能正常;符合《赫尔辛基宣言》并签署知情同意书。
1.2.2 排除标准 ①使用过胰岛素治疗者;②近期糖化血红蛋白≥12%;③妊娠、哺乳期妇女;④恶性肿瘤或血液疾病;⑤精神疾病;⑥严重胃出血的溃疡;⑦过度消瘦、营养不良;⑧合并严重并发疾病;⑨3 月内使用药物或手术以减轻体质量者;⑩不能配合治疗、依从性差;○1 研究者判断不适合入组的其他情况。
1.2.3 纳入情况 根据纳入标准,本研究筛选40名超重∕肥胖2 型糖尿病患者,其中4 名因使用过胰岛素治疗而排除,最终36 名超重∕肥胖2 型糖尿病患者接受中医禁食疗法,疗程7 d。其中2 名患者因痛风性关节炎急性发作终止疗程,退出研究,完成中医禁食疗法共34名患者。
1.3 临床干预方法
本研究为单中心、前瞻性、自身前后对照研究。本研究以超重∕肥胖2型糖尿病患者为研究对象,使用中医禁食疗法治疗1 周,对所有患者的临床疗效进行评估,对所有患者进行随访追踪6 月,于禁食前、禁食结束、禁食后3 月、禁食后6 月,对体质量、BMI、糖化血红蛋白、空腹血糖、空腹胰岛素、HOMA-IR 等指标进行检测,观察中医禁食疗法对超重∕肥胖2型糖尿病的短期及中远期疗效。
1.3.1 中医禁食疗法实施步骤 所有受试者完成为期7 d 的中医禁食疗法治疗1 次,分别在干预前1 d及干预后1 d早晨留取血液标本,治疗期内停用口服降糖药、降压药、利尿药、抗凝药等。具体流程分为缓冲期、禁食期和恢复期3个阶段[4]。
缓冲期(第1 日):通过水果餐进行正常饮食至禁食的过渡。第1日以1 500 g水果分为三餐服用,选用升糖指数较低的水果。饮3 L矿泉水。禁食期间戒茶、酒精、咖啡等饮品。
禁食期(第2 日至第6 日):禁食期共5 d,为治疗期。治疗第2日晨8:00~9:00进行肠道清洁,使用玄明粉20 g,以温开水500 mL 冲服,以站立姿势在10 min内服用完毕。禁食期间放松心情,每日进行2~3 h 轻体力活动。每日饮用3 L 矿泉水。药物:加味苓桂术甘汤1剂,冲服;碳酸氢钠片2.0 g 口服,每日3 次;葡醛内酯0.2 g,口服,每日3 次;左旋肉碱2.0 g 静脉推注每日2 次。治疗第3~6 日,除不做肠道清洁外,药物、饮水和运动均同第2日。
恢复期(第7 日):通过流质饮食或半流质饮食完成禁食向均衡膳食的过渡。饮水、运动不限。
1.3.2 中药药物组成及依据 中医禁食疗法过程中所使用的加味苓桂术甘汤,茯苓、桂枝、白术、炙甘草、黄芪、党参、山药、陈皮、白扁豆、淫羊藿、巴戟天,其中茯苓健脾利水,桂枝温阳化气,白术、炙甘草、山药益气健脾,黄芪、党参大补元气,陈皮、白扁豆理气化痰,淫羊藿、巴戟天温补肾阳,全方可健脾化饮、益气温阳,因此可减轻禁食过程中由于痰浊困脾、气不运化导致的一系列临床症状[7-8]。
本研究采用广州一方制药有限公司所生产的中药配方颗粒,每日1剂,以600 mL温水冲泡,全天感到饥饿时随时服用。
1.3.3 随访期管理 随访期为6 个月,要求2 型糖尿病患者持续停用口服降糖药物,每周监测体质量、空腹指尖血糖、餐后2 h 指尖血糖,并依照患者目前饮食及运动情况对患者进行相应生活方式指导以及糖尿病宣教。
在随访节点3个月、6个月留取血液标本,复查糖化血红蛋白指标。复诊时,若空腹血糖>7.0 mmol∕L,餐后两小时血糖>10 mmol∕L,则1 周后复测,若仍超过以上标准,则视为高血糖症复发,启动复发管理策略[9]——按照中国2型糖尿病指南指导用药。
对于禁食期间停用降压药、降脂药的患者,在随访期内密切观察血压,定期复查血脂情况,并在医师指导下调整药物用量。
1.4 观察指标
主要观察指标:糖化血红蛋白、空腹血糖(fasting plasma glucose,FPG)、空腹胰岛素(fasting insulin,FINS)、HOMA-IR、体质量、BMI。
次要观察指标:腰围、臀围、腰臀比、体脂率、收缩压、舒张压、丙氨酸氨基转移酶(alanine transaminase,ALT)、天冬氨酸氨基转移酶(aspartate transaminase,AST)、γ-谷氨酰转肽酶(γ-glutamyl transpeptidase,GGT)、尿酸、β-羟丁酸等。
1.5 统计学方法
2 结果
2.1 一般资料
完成中医禁食疗法疗程的34 名超重∕肥胖2 型糖尿病患者中,男性18 名(52.9%),女性16 名(47.1%)。年龄30 至45 岁者占52.9%,46 至60 岁者 占35.3%。诊断超重(BMI≥24 kg∕m2)16 人(47.1%),诊断肥胖(BMI≥28 kg∕m2)18 人(52.9%)。确诊2 型糖尿病病程小于12 月者占44.1%,病程12至36 月者占32.4%。糖化血红蛋白小于6.5%者占41.2%,6.5%至7.5%者占41.2%。合并高血压病者8 人(23.5%),合并脂肪肝者25 人(73.5%),合并高脂血症者27 人(79.4%),合并糖尿病酮症0人(表1)。
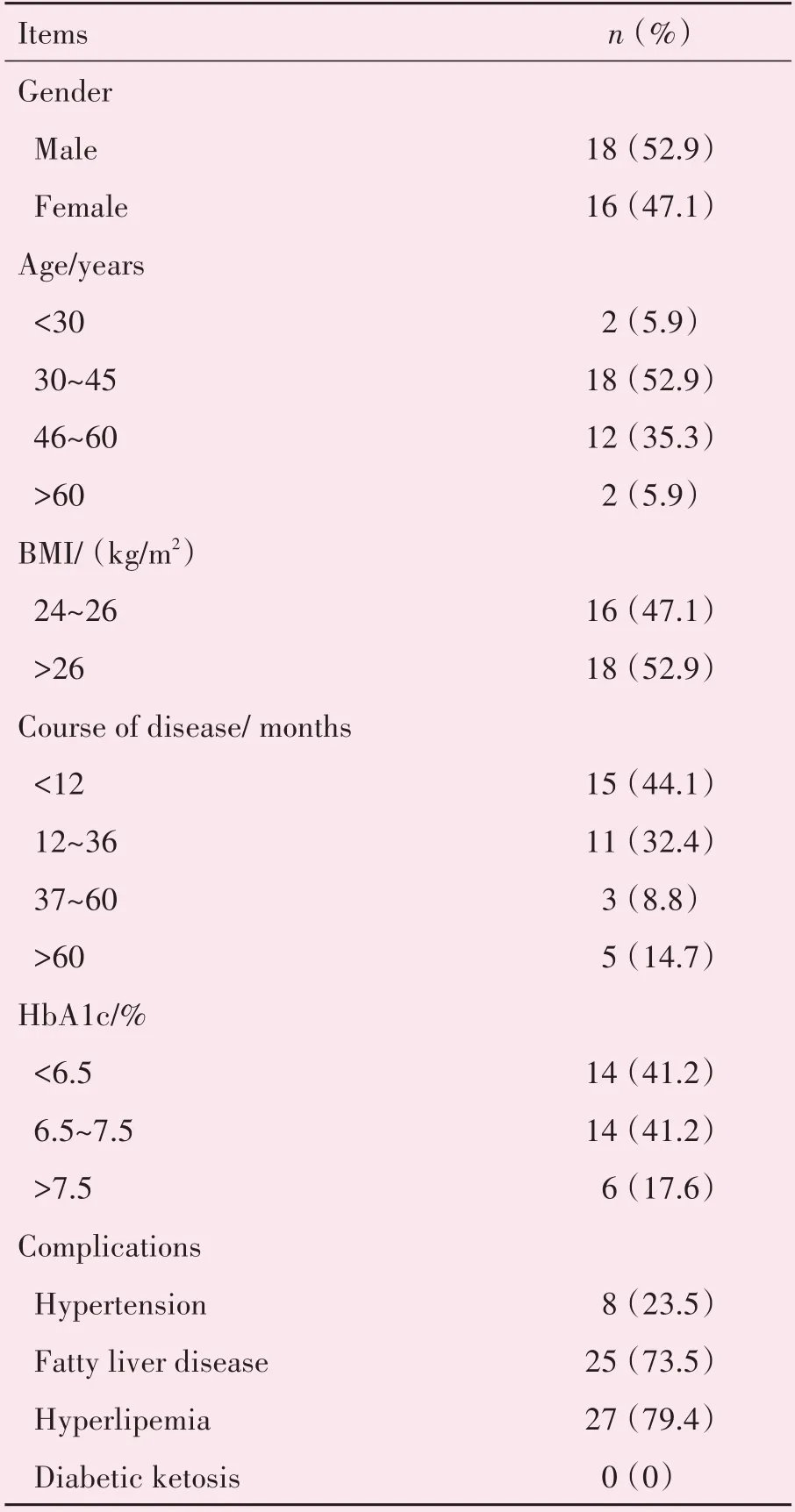
表1 34名患者一般情况及疾病相关资料Table 1 Demographic and clinical characteristics of 34 patients
2.2 血糖和胰岛功能
完成中医禁食疗法后随访3 月和随访6 月时,超重∕肥胖2 型糖尿病患者糖化血红蛋白均显著低于基线值水平(t=4.353,P<0.001;t=4.456,P<0.001)。空腹血糖在禁食后显著降低(t=4.289,P<0.001),但在随访3月和随访6月时与基线值比较差异无统计学意义(t=1.927,P=0.064;t=1.662,P=0.108)。患者HOMA-IR值在禁食后、随访3月和随访6月时较基线值均显著降低(z=-3.353,P=0.001;z=-2.819,P=0.005;z=-2.511,P=0.012),且随访3月和随访6月时较禁食后水平差异无统计学意义(z=-1.786,P=0.074;z=-0.914,P=0.346;表2)。
表2 禁食前后及随访血糖和胰岛功能比较Table 2 Comparison of HbA1c,FPG,FINS,and HOMA-IR among baseline,post-fasting and follow-up[(),M(P25~P75)]

表2 禁食前后及随访血糖和胰岛功能比较Table 2 Comparison of HbA1c,FPG,FINS,and HOMA-IR among baseline,post-fasting and follow-up[(),M(P25~P75)]
HbA1c:glycosylated hemoglobin;FPG:fasting plasma glucose;FINS:fasting insulin;HOMA-IR:homeostasis model assessment-insulin resistance.1)versus baseline;2)versus post-fasting.3)showed by,compared by t-test;4)showed by M(P25~ P75),compared by Wilcoxon test.
2.3 体质量及人体测量学指标
从禁食第2 天起,禁食期间每日体质量与BMI对比基线值均显著下降,至随访3 月和随访6 月体质量(t=9.105,P<0.001;t=7.174,P<0.001)与BMI(t=9.247,P<0.001;t=6.996,P<0.001)对比基线值差异均有统计学意义(图1A-B)。
患者禁食后及随访3 月体脂率较禁食前均显著下降(t=7.314,P<0.001;t=7.462,P<0.001),且随访3月较禁食后同样显著下降(t=2.557,P=0.017;图1C)。
中医禁食疗法治疗后,超重∕肥胖2型糖尿病患者腰围显著下降(t=3.331,P=0.003),臀围差异无统计学意义(t=1.704,P=0.104),但腰臀比显著下降(t=2.381,P=0.027;图1D-F)。

图1 体质量、BMI和人体测量学指标Fig.1 Weight,BMI and anthropometric indices
2.4 安全性指标
在安全性方面,对于2 型糖尿病患者进行热量限制,众多研究者顾虑在于低血糖风险、血压、肝功能及酮体情况。
首先,在中医禁食疗法治疗期间,7 d 时间内,超重∕肥胖2 型糖尿病患者空腹指尖血糖在第3 日较基线值显著降低(t=3.778,P=0.001),且在第4日和第5日继续降低,在第5日达到目标水平,但血糖水平不会进一步下降,而是在第6 日和第7 日稳定在目标值水平。且在随访3 月和随访6 月时,患者空腹指尖血糖水平仍显著低于禁食前血糖水平(t=3.023,P=0.005;t=3.063,P=0.004;图2A)。
禁食期间第2、4、6 日患者收缩压显著低于基线值水平(t=2.326,P=0.026;t=2.844,P=0.008;t=2.193,P=0.035),而舒张压则在每日保持稳定水平,每日较基线值差异均无统计学意义(图2B-C)。
禁食期间,患者ALT、AST 开始升高,但至随访3 月和随访6月时,ALT(t=3.255,P=0.003;t=2.517,P=0.017)、AST(t=3.625,P=0.001;t=3.457,P=0.002)较禁食后均显著下降(图2D-E)。患者GGT 在禁食开始后则开始降低,治疗期第4 天、禁食后、随访3月和随访6月时,GGT均显著低于基线值(t=3.155,P=0.003;t=4.613,P<0.001;t=4.133,P<0.001;t=4.042,P<0.001;图2F)。
禁食期间,患者血尿酸水平升高,至禁食结束显著高于基线值水平(t=-2.695,P=0.011),但在随访3月和随访6月时较禁食后显著降低(t=2.231,P=0.033;t=2.366,P=0.024),且可回落至基线值水平,较基线值水平差异无统计学意义(t=-1.238,P=0.225;t=-0.925,P=0.362;图2G)。
中医禁食疗法治疗期间,患者血液β-羟丁酸水平迅速升高,治疗第4 天及禁食结束时均显著高于基线值水平(t=-5.462,P<0.001;t=-9.074,P<0.001;图2H)。

图2 空腹指尖血糖、血压、肝功能、尿酸及β-羟丁酸Fig.2 Fingertip fasting glucose,blood pressure,liver function,uric acid and β-hydroxybutyric acid
3 讨论
3.1 主要发现
中医禁食疗法脱胎于欧洲禁食疗法(fasting therapy),属于热量限制的一种特殊形式,它是在一段时间内(5~28 d),在保证正常生命活动需要的前提下,除了适量饮水和极低热量供应之外,不食用任何日常食物,以达到预防或治疗疾病目的的饮食疗法[10]。而中医禁食疗法则结合了西方热量限制与祖国医学特色,是中山大学秦鉴教授于2008年引进欧洲禁食疗法后,结合国人体质进行改良的一种特色疗法,其在临床应用过程中减重效果佳、不良反应发生率低,安全性良好[8]。目前中医禁食疗法已临床运用14 年,已形成一套完整、标准化的操作流程和规范,收治2 000余例临床患者,发表相关学术论文60 余篇,同时在全国数十家医院推广开展,发表《中医禁食疗法专家共识(征求意见稿)》[4]。
禁食疗法作为一种养生、治疗疾病的手段在近年来愈加受到重视,在国外存在较多临床研究及相关专家共识[11],且已有临床研究表明其可缓解2 型糖尿病[12-13],但独具中医特色的中医禁食疗法治疗2 型糖尿病则存在较少证据,因此本研究为目前国内少有的中医禁食疗法治疗2 型糖尿病的循证医学证据,且具有相对较大的样本量和较长的随访期,具有一定创新性。
与本研究结果一致,8周热量限制使8名肥胖2型糖尿病青少年糖化血红蛋白平均由8.1%降至6.6%[14]。14 名重度肥胖2 型糖尿病患者进行1 周热量限制,并使用高葡萄糖钳夹技术结果显示,空腹血糖、胰岛素第一时相分泌和第二时相分泌均得到显著改善[12]。发表于Lancet杂志的DiRECT研究显示,3 个月的热量限制配合后期生活方式干预的体质量管理,可通过减少内脏脂肪含量和改善胰岛素抵抗等[15],使2 型糖尿病患者在1 年内和2 年内的缓解率分别达到46%和36%,而常规治疗对照组仅为4%和3.4%[2-3]。可见对2 型糖尿病患者进行一段时间的热量限制可降低血糖,并改善胰岛素抵抗。
3.2 可能机制
发表上述DiRECT 研究的Roy Taylor 教授认为2 型糖尿病与体质量增加和肝脏、胰腺内的脂肪堆积密切相关,据此提出了双恶性循环假说[16]。他认为,饮食不当导致的能量摄入过多是第一步,能量过多导致肝脏脂质沉积,引发胰岛素抵抗,导致肝脏葡萄糖合成功能失调。为调节葡萄糖合成,胰岛素浓度相应上升,但由于胰岛素可促进肝脏脂肪合成,又进一步加剧肝脏脂质沉积,从而形成恶性循环。同时,肝脏脂质沉积导致甘油三酯分泌,而胰腺更易受到甘油三酯积聚的影响,导致胰腺脂肪累积,β 细胞去分化,两者共同作用导致。因此,热量限制是通过一段时间的负能量平衡,从源头上打破双恶性循环,减轻肝脏和胰腺脂质沉积,改善胰岛素抵抗,进而缓解2型糖尿病[15]。
同时,2 型糖尿病缓解可能与减重相关,一项纳入867 名2 型糖尿病患者随访5 年的研究结果显示,在未进行任何干预的情况下,患者减重比例越高,糖尿病缓解率也越高,疾病早期减重超过10%的患者在随访5 年时缓解率达到77%[17]。而Di-RECT 研究中同样显示类似结果,糖尿病缓解率在体质量下降10 kg 至15 kg 的受试者中,1 年缓解率为57.1%,2 年缓解率为60.0%,而体质量下降大于15 kg的受试者中,1年缓解率高达86%,2年缓解率也达到70%[2-3]。指南推荐,超重∕肥胖2 型糖尿病患者体质量减轻3%~5%是体质量管理的基本要求[13],而在本研究中,受试者6 月随访时体质量平均下降4.82 kg,下降幅度为自身体质量的6.03%,考虑中医禁食疗法能够达到超重∕肥胖2 型糖尿病患者体质量管理要求,且血糖缓解与体质量下降可能存在关联。
除此之外,其他研究表明,热量限制缓解2 型糖尿病可能与改善肠道菌群结构及数量[18]、调节胰岛素信号通路(AKT∕AS160∕GLUT4)[19-20]等有关。
3.3 结论
总体上,本研究评估了中医禁食疗法对超重∕肥胖2 型糖尿病患者的短期及中远期临床疗效,发现中医禁食疗法可显著降低超重∕肥胖2 型糖尿病患者血糖水平,改善胰岛素抵抗,且在6 个月的随访期内效果持续,且可显著降低超重∕肥胖2型糖尿病患者体质量和BMI,具备一定的安全性。但本研究为单中心自身前后对照研究,未设立对照组,若在进一步研究中设置2 型糖尿病常规治疗对照组及健康受试者对照组则研究将更为完善。
