复发/转移宫颈癌患者应用PD-1抑制剂卡瑞利珠单抗联合阿帕替尼治疗的患者报告结局
2022-08-11赖月容姜月黄欣欧玉兰
赖月容,姜月,黄欣,欧玉兰
(中山大学肿瘤防治中心妇科,广东广州 510060)
宫颈癌是常见的女性生殖道恶性肿瘤,2020年我国宫颈癌新发病例11.0万,死亡病例5.9万,均较2018 年显著增长[1]。一项宫颈癌疾病负担的数据分析显示2007-2017 年东亚地区宫颈癌负担大幅增加,其中2017 年我国宫颈癌发病例数及死亡例数均为东亚最高[2]。早期宫颈癌患者可以通过手术或放疗获得有效的治疗,但仍有11%~22%的复发率[3]。同时约有10%~15%的患者在疾病诊断时即为晚期(FIGO 分期IVB 期),伴有肿瘤的全身转移且易复发,即便经过综合治疗,其复发率仍高达30%~50%[4]。对于复发性宫颈癌的二线治疗,NCCN 指南建议采用的药物包括帕博利珠单抗贝伐单抗、多西他赛、吉西他滨、托泊替康等[5-8]。然而,上述二线化疗方案的疗效极其有限,客观有效率大约为10%~30%,中位OS 仅约为7~11 个月[5-8]。因此,针对复发性宫颈癌患者迫切需要新的治疗模式和药物,以延长患者生存时间,改善生活质量[9]。免疫检查点抑制剂(immune checkpoint inhibitors,ICIs)治疗是近几年的研究热点,在肿瘤领域的治疗中不断获得重大突破[10]。研究表明,ICIs 联合抗血管生成靶向治疗具有协同增效的作用[11]。这一联合治疗模式已在肾癌、肝癌、宫颈癌等多个癌种中取得成功[12-14]。中山大学肿瘤防治中心蓝春燕等在2019 年开展了程序性细胞死亡蛋白1(programmed death-1,PD-1)抑制剂卡瑞利珠单抗联合抗血管生成药物阿帕替尼治疗复发性宫颈癌的一项多中心、单臂的Ⅱ期临床研究(以下简称CLAP 研究),显示卡瑞利珠联合阿帕替尼具有良好的抗肿瘤活性,客观有效率(ORR)为55.6%[15]。既往研究显示,抗血管生成药物,如索拉非尼、舒尼替尼等会导致患者严重疲劳的发生率显著增加,造成患者更多的心理和生理困扰[16-17]。在CLAP 中,研究者采用患者报告结局(patient-reported outcome,PRO)评估了患者接受卡瑞利珠单抗联合抗血管生成药物阿帕替尼治疗后健康相关生活质量(Health Related Quality of Life,HRQoL)的变化。患者报告结局(patient-reported outcome,PRO)指直接来源于患者对自身健康状况、功能状态以及治疗感受的报告,是评价疗效和药物安全性的重要组成部分[18]。在本研究中,我们将报告CLAP 研究宫颈癌患者接受卡瑞利珠单抗联合阿帕替尼治疗的PRO结果。
1 材料与方法
1.1 研究对象
CLAP 研究是一项前瞻性、开放标签、多中心、单臂的Ⅱ期临床研究,其入组标准在既往文献已详细描述,概括如下:18~70 岁组织学确诊为转移性、复发性或持续性宫颈癌,接受过至少一线全身治疗后进展;根据RECIST 第1.1 版有可测量的病灶;美国东部肿瘤协作组体能状态评分为0 或1。患者还必须具有足够的骨髓、肾、凝血、心脏和肝功能。本研究已获本中心伦理委员会批准(伦理批号为:B2018-169-01)。所有参与研究患者均已签署知情同意书。
在CLAP 研究中,对符合入组条件的患者给予卡瑞利珠单抗联合阿帕替尼治疗。卡瑞利珠单抗给药剂量为200 mg 静脉注射,每2 周1 次。阿帕替尼起始剂量为250 mg 口服,每天1 次,连续4 周为1个治疗周期(卡瑞利珠单抗治疗最长24 个月)。治疗持续至疾病进展、出现不可接受的毒性或撤回知情同意。当发生治疗相关毒性而给予支持性治疗无法缓解时,可调整给药剂量。如发生明确与阿帕替尼相关的不良事件(adverse events,AEs),如高血压、蛋白尿、手足综合征等,允许阿帕替尼剂量中断和剂量下调(最多下调2次),首次阿帕替尼剂量下调可减少至250 mg 每日一次,给药2 d,停药1 d;第二次阿帕替尼剂量下调可减少至250 mg 隔日一次。试验期间出现免疫相关毒性,允许卡瑞利珠单抗剂量暂停,针对用药期间体质量下降至50 kg以下的受试者,卡瑞利珠单抗可酌情下调至3 mg∕kg给药。
本研究纳入的患者为CLAP 研究中,至少使用过一次研究药物,并且至少完成一次问卷的受试者。
1.2 观察指标
本研究应用宫颈癌【Functional Assessment of Cancer Therapy-Cervix v4.0,FACT-Cx(v4.0)】问卷作为PRO 的评估工具。FACT-Cx 量表由一个测量癌症病人生命质量共性部分的量表(Functional Assessment of Cancer Therapy-Generic Scale,FACTG)和宫颈癌分量表(Cervical cancer score,CxCS)两部分组成[19]。FACT-G 包含27 个条目,分为4 部分:生理状况(Physical,GP1-7;7 条)、社会∕家庭状况(Social∕family,GS1-7;7 条)、情感状况(Emotional,GE1-6;6 条)及功能状况(Functional,GF1-7;7条)[20]。宫颈癌分量表(CxCS)包含15个子条目,包括是否有阴道出血、异味、阴道狭窄对生育状况及性生活是否感到担忧等。既往研究显示,该问卷在测量癌症患者生活质量方面具有良好的信效度[21]。在研究期间由经过统一培训的研究员按研究制定的流程按时对纳入研究的患者进行面对面调查与跟踪随访,患者将在第一周期第1 天治疗前及每1个治疗周期进行影像学评估时进行完成FACT-Cx量表,直至退组或结束治疗。本研究中患者按照过去7 d 的感受、出现症状的频率勾选,采用Likert5级评分,每个条目按“一点也不”、“有一点”、“有些”、“相当”、“非常”分别记为0~4 分,逆向条目为GP1-GP7、GE1、GE3-GE6,进行4~0 分反向计分。FACT-G 得分范围为0-108 分,CxCS 得分范围0~60分。得分越高,生活质量越好。
1.3 统计学方法
本研究描述所有统计数据由SPSS 20.0 软件完成。符合正态分布的计量资料用均数±标准差(xˉ±s)描述,多组比较进行单因素方差分析(ANOVA)和校正的单因素方差分析(ANOVA);非正态分布计量资料用中位数及四分位距M(P25~P75)描述,多组比较采用秩和检验,多组率的比较采用卡方检验,并根据需要采用Bonferroni 法校正法或采用Fisher 确切概率法。以P<0.05 为差异有统计学意义。多组率的比较采用卡方检验,并根据需要采用Bonferroni 校正或采用Fisher 确切概率法。多组均数比较,各组定量资料都呈正态分布并且方差齐性采用One way-ANOVA 进行分析,不满足方差齐性的情况时,使用Welch's anova。以P<0.05 为差异有统计学意义。
2 结果
2.1 一般临床资料
本研究共有41 例患者接受治疗且至少完成一次AEs 评估与生活质量FACT-Cx 问卷,其中位年龄为54(33~67)岁。75.61%的患者ECOG 评分为1 分。常见的转移部位为肺(41.46%)、淋巴结(51.21%)、和肝(21.95%)。有41.46%的患者既往接受过二线系统治疗,14.63%的患者接受了三线或以上的系统治疗。截至2020年10月12日,32例患者(71.1%)发生治疗相关3~4 级AEs,其中最常见的是高血压(24.4%)、贫血(20.0%)和疲劳(15.6%)。
根据研究方案规定,试验期间发生治疗相关毒性时可调整给药剂量。33 例患者(73.3%)因出现药物毒性而下调阿帕替尼剂量,其中4 例(12.1%)发生1 次剂量下调,29 例(87.9%)发生了2 次剂量下调。未有患者需要卡瑞利珠单抗剂量下调。所有阿帕替尼的剂量下调均发生在前6 个用药周期。在前6 个用药周期,3~4 级AEs 发生率为71.11%,其中高血压发生率为77.78%,疲劳为48.89%。而在治疗6 个周期后,3~4 级AEs 发生率显著下降至25.0%,高血压发生率为50.0%,疲劳为3.57%。所有患者人口学特征与治疗前FACT-Cx 量表得分见表1。

表1 ICIs联合抗血管生成靶向治疗宫颈癌患者人口学特征与基线FACT-Cx量表Table 1 Demographic characteristics and baseline FACT-Cx scale of cervical cancer patients treated with ICIs combined with antiangiogenic targeted therapy
2.2 FACT-Cx量表得分及其变化
本研究中41 例患者在第一次用药前测得的基线生活质量均分为114.53±18.23,95%CI 为(108.78,120.29)。在前6个用药周期,共有33例患者完成了FACT-Cx 量表,测得生活质量均分为124.08±15.23,95%CI为(119.84,128.32)。在治疗6个周期后,截止至本研究问卷收集截止时间,共有20 例患者完成了FACT-Cx 量表,测得生活质量均分为132.82±21.97,95%CI 为(126.29,139.34)。本研究生活质量总分的数据不满足方差齐性,故应用校正的单因素方差分析,采用Welch 方差分析法,判断各阶段患者生活质量是否存在差异。结果显示,在基线、前6个用药周期、治疗6个周期后,患者的生活质量评分随治疗周期的增加而升高,差异具有统计学意义(P<0.001;表2)。

表2 ICIs联合抗血管生成靶向治疗各用药阶段FACT-Cx量表评分单因素方差分析Table 2 One-way analysis of variance for FACT-Cx scale scores of ICIs combined with anti-angiogenic targeted therapy in each medication stage
应用Games-Howell 检验方法将患者用药各阶段生活质量进行对比,结果显示患者生活质量评分在前6 个用药周期较基线升高,差值具有统计学意义(P=0.023;表3)。与此相似,治疗6 个周期后患者的生活质量评分也较基线显著升高(P<0.001;表3)。我们进一步比较前6 个用药周期和治疗6个周期后患者的生活质量评分,发现生活质量评分在治疗6 个周期后较前6 个周期升高,差值具有边际统计学意义效应(P=0.068;表3)。

表3 ICIs联合抗血管生成靶向治疗各用药阶段FACT-Cx量表评分的两两比较Table 3 Pairwise comparison of FACT-Cx scale scores of ICIs combined with antiangiogenic targeted therapy in each medication stage
2.3 治疗期间FACT-Cx量表各维度得分的变化
我们对患者用药阶段生活质量各维度得分进行对比。结果显示,在FACT-Cx 量表的生理状况、情感状况、功能状况及附加关注等四个维度中,用药后各维度的均分显著高于用药前各维度的基线均分,差异具有统计学意义(P<0.05;表4)。
各维度两两对比结果显示,在生理状况维度、功能状况维度和附加关注维度这三个维度中,前6个用药周期的评分与基线水平相比差异不显著,而治疗6 个周期后的评分显著高于基线水平(P<0.05;表5)。在情感状况维度,前6 个用药周期和治疗6 个周期后评分都显著高于基线水平,其中治疗6 个周期后的评分分为最高(P<0.05;表5)。社会∕家庭状况维度在各用药阶段得分变化差异不明显(表4,表5)。
表4 ICIs联合抗血管生成靶向治疗各用药阶段FACT-Cx各维度得分对比Table 4 Comparison of FACT-Cx scores for each dimension of ICIs combined with anti-angiogenic targeted therapy in each medication stage()

表4 ICIs联合抗血管生成靶向治疗各用药阶段FACT-Cx各维度得分对比Table 4 Comparison of FACT-Cx scores for each dimension of ICIs combined with anti-angiogenic targeted therapy in each medication stage()
1)Welch's anova was used.
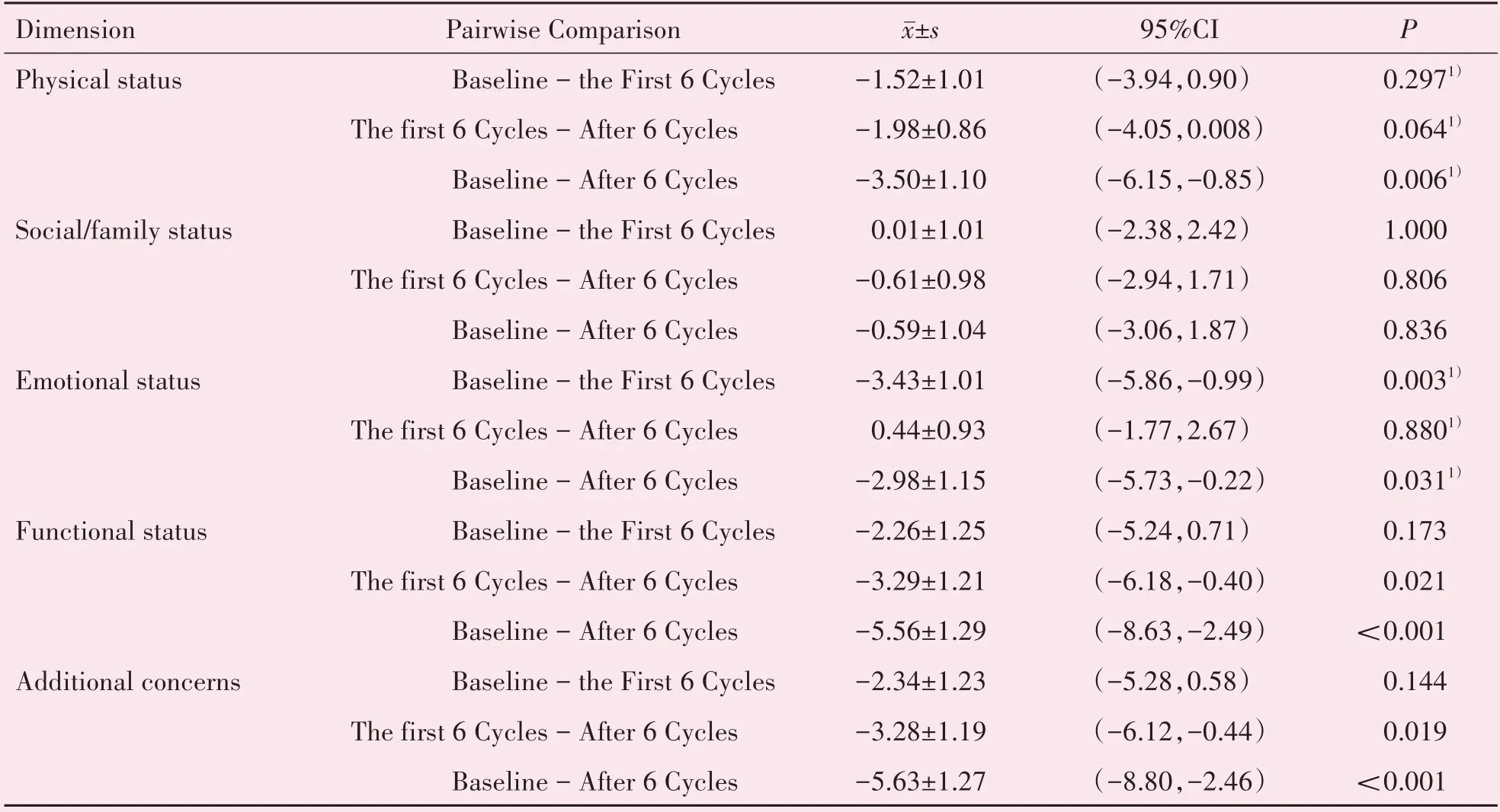
表5 不同治疗阶段FACT-Cx量表各维度得分的两两比较Table 5 Pairwise comparison of the scores of each dimension of the FACT-Cx scale in different treatment stages
2.4 不同治疗效果的患者FACT-Cx 量表的得分情况
本研究41 例患者中,根据方案经实体肿瘤疗效评价标准RECIST1.1 版评价,23 例治疗效果评估为有效即完全缓解(complete response,CR)及部分缓解(partial response,PR),14例治疗效果评估为无效即疾病稳定(stable disease,SD)及疾病进展(progressive disease,PD),4 人疗效无法评估。对比有效与无效患者的基线生活质量评分,结果显示生活质量评分差异不显著。然而,与基线相比,治疗后生活质量评分在有效患者中较无效患者明显升高(P<0.001;表6)。

表6 ICIs联合抗血管生成靶向治疗不同疗效患者的FACT-Cx量表评分Table 6 FACT-Cx scale scores of patients with different efficacy of ICIs combined with anti-angiogenic targeted therapy
3 讨论
既往CLAP[15]研究评估了一线治疗失败的复发性宫颈癌患者接受PD-1抑制剂卡瑞利珠单抗联合抗血管生成药物阿帕替尼的有效性和安全性。本研究报告了该研究队列患者的PRO 分析结果。目前认为,对癌症患者的治疗提高其生存率和改善生活质量同等重要[22]。本研究是首个关于接受PD-1抑制剂联合抗血管生成治疗的复发性宫颈癌患者队列的PRO报告。
本研究显示患者在接受卡瑞利珠联合阿帕替尼治疗后,无论是在前6 个用药周期还是治疗6 个周期后,患者的生活质量评分均较基线有明显的改善。此外,本研究中对治疗方案有效的患者其生活质量评分明显高于无效的患者(P<0.05)。结合CLAP 研究观察到的“免疫+抗血管”治疗方案对患者预后的改善,本研究结果提示卡瑞利珠单抗联合阿帕替尼的治疗在改善患者预后的同时提高了患者的生活质量。
一直以来,化疗是复发性宫颈癌患者重要的抗肿瘤手段之一。然而,研究表明,随着使用周期的增加,化疗引起的毒副作用随之增加,患者的躯体、社会等功能下降,总体生活质量降低[23]。区别于既往化疗方案对患者生活质量的影响,本研究中,患者接受超过6 周期卡瑞利珠单抗联合阿帕替尼的治疗后,其生活质量评分显著高于用药前患者的基线生活质量评分,P<0.05;同时亦较前6 个用药周期的生活质量评分高,虽然其P值仅具有边际统计学意义效应,但我们考虑是因为本研究样本量较小而未能显示出显著的统计学差异。我们的结果显示了这一“免疫+抗血管”的“去化疗”方案对改善患者生活质量的持续性,提示临床“免疫+抗血管”这一联合治疗方案给转移∕复发的宫颈癌患者带来的整体的生存获益。
在CLAP 研究中已报道过本研究队列观察到最常见的治疗相关AEs为高血压、疲倦、口腔炎等,这些毒性考虑主要与抗血管生成药物阿帕替尼相关。在本研究中,我们发现严重的(3~4级)AEs的发生率在前6 个治疗周期远远高于治疗6 个周期后。结合阿帕替尼的剂量下调均发生在前6 个用药周期的情况,我们考虑由于阿帕替尼给药剂量的下调,使6 个治疗周期后的患者对治疗方案的耐受性增高,毒副作用发生率减少。这也从另一方面解释了,本研究中患者接受超过6周期治疗后,其生活质量评分较基线和前6个用药周期均有持续的提高。
FACT-Cx 量表中的生理状况维度,包括恶心、疼痛、身体不适等,直接反映了患者躯体症状在接受抗肿瘤治疗中的变化。本研究中,患者的生理状况维度在接受治疗后较基线时明显改善,表明PD-1 抑制剂联合抗血管生成药物方案良好的耐受性显现出持久性[24]。同时,在FACT-Cx 量表中的情感状况维度,患者用药后得分较基线显著增加,提示患者的负向情绪明显减少。我们考虑,一方面本研究治疗方案疗效出现令人鼓舞的55.6%的客观有效率,明显高于既往单药疗效及既往复发性宫颈癌二线化疗方案,使患者对疾病治疗更有信心;另一方面,该治疗方案未损害患者的躯体功能给患者增加情绪的负担,这些获益均改善了患者的情感状况。此外,FACT-Cx 量表的功能状况维度与附加关注维度,在患者用药后得分亦较基线得分显著增加,这与患者治疗后肿瘤缩小,疾病得到控制相关。需要指出的是,以上各个维度的改善均随着治疗周期的延长,评分改善持续显著,表明了患者生活质量改善的稳定性。另外,本研究中患者生活质量中社会∕家庭状况这一维度在治疗各阶段变化不显著,研究显示宫颈癌患者对其承担家务方面及日常工作状态的改变感到无力[25]。有研究表明有工作的宫颈癌患者其生活质量评分相对更高[26],提示临床工作者对复发∕转移的宫颈癌患者应重视其社会∕家庭属性的改变,及时对患者进行心理疏导。
需要指出的是,由于本研究样本例数较少,结果可能存在偏倚,后期需要加大样本量进行进一步研究。
综上所述,复发性宫颈癌患者接受PD-1 抑制剂卡瑞利珠单抗联合抗血管生成药物阿帕替尼治疗后,FACT-Cx 调查量表在生理状况、情感状况、功能状况及附加关注等多个维度的评分均有升高,生活质量明显提高。并且,生活质量评分在治疗6个周期后较前6 个治疗周期仍有升高,提示生活质量改善时间持久。值得大样本量的研究进一步验证本结论。
