股动脉联合无名动脉 左颈总动脉插管在手术治疗急性A型主动脉夹层患者中的临床效果分析
2022-08-11葛建军
王 琛,葛建军
急性A型主动脉夹层(acute type A aortic dissection,ATAAD)是一种外科急症,手术治疗虽并发症发生率、死亡率高[1],但若不进行手术治疗,患者的病死率更高[2]。有研究表明,ATAAD的住院病死率为22%[3],而动脉内膜撕裂切除后移植物置换被认为是治疗ATAAD的金标准[4]。与接受手术治疗的患者相比,未接受手术治疗患者的存活率显著降低。在手术过程中需建立体外循环(cardiopulmonary bypass,CPB),动脉插管策略取决于各种临床因素,包括分支血管的夹层累及程度、不良灌注、血管钙化和血流动力学稳定性,以及外科医师的技能水平等。理想策略是快速建立插管,最大限度地减少任何器官灌注不良,防止夹层或主动脉破裂的进展,并在需要低温停循环(hypothermic circulatory arrest,HCA)时提供最佳的脑保护干预[5]。股动脉联合腋动脉插管是常用的方法,不仅在停循环期间可以通过上半身进行顺行脑灌注,避免了单纯的股动脉插管逆行灌注的风险,保证了脑灌注,减少了脑部并发症的发生,同时可以改善下半身重要器官如肾脏的血流灌注,降低术后肾损伤的发生。目前也有临床医师采用双侧脑灌注的插管方法,即腋动脉、无名动脉或右颈总动脉联合左颈总动脉插管,该方法被认为可以降低术后脑卒中发生的风险[6]。综合上述各种插管方法的优缺点,本课题组采用股动脉+无名动脉+左颈总动脉[若无名动脉受累则采用股动脉+腋动脉(或右颈总动脉)[7]+左颈总动脉]的三动脉插管的方法建立CPB,取得了较好的临床效果,现报道如下。
1 对象与方法
1.1研究对象 选择2021年4月至2022年4月在安徽医科大学附属省立医院行手术治疗的ATAAD患者62例。根据术前胸腹主动脉血管造影(computed tomography angiography,CTA)结果及术中动脉情况决定插管方法,26例左颈总动脉未受累者采取股动脉+无名动脉+左颈总动脉[若无名动脉受累则取股动脉+腋动脉(或右颈总动脉)+左颈总动脉]三动脉插管方法建立CPB(观察组),36例采用股动脉+无名动脉的双动脉插管方法建立CPB(对照组)。两组基线资料比较差异无统计学意义(P>0.05),具有可比性。见表1。研究获医院伦理委员会批准(2022-RE-186),患者知情同意参与。
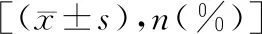
表1 两组基线资料比较
1.2纳入与排除标准 纳入标准:(1)根据临床表现、心电图、胸腹主动脉CTA以及心脏彩超结果明确诊断ATAAD;(2)患者及其家属同意手术治疗并签署知情同意书。排除标准:(1)患者或家属要求保守治疗,拒绝手术;(2)住院期间夹层破裂死亡者;(3)手术过程中死亡者。
1.3插管方法及CPB建立
1.3.1 观察组 麻醉满意后,患者取平卧位,消毒皮肤,铺巾,右侧腹股沟上方纵切口,分离右股动脉,套绕阻断带。取胸骨正中位切开皮肤及皮下组织,锯开骨止血,撑开胸骨,心包外分离出无名静脉、无名动脉、左颈总动脉、左锁骨下动脉,头臂三分支血管均无夹层累及[根据术前胸腹主动脉CTA及术中直视下判断无名动脉累及情况,若受累及则在开胸前取右锁骨下切口,分离出右侧腋动脉,套带备用激活全血凝固时间(activated coagulation time,ACT)>280 s后插入14号动脉插管并固定]。切开悬吊心包,全量肝素化,分离主肺动脉间隔,右心房缝置房腔静脉插管荷包,右上肺静脉缝制左心引流管荷包。ACT>280 s后行股动脉插管(管道型号视患者股动脉内径而定,宜尽可能选择较大口径保证灌注)并固定。经无名动脉远端插16号动脉插管并固定,经左颈总动脉插14号动脉插管并固定,保证术中充足脑部血供。右心房插入34号房腔静脉插管并固定,建立CPB,转流。
1.3.2 对照组 麻醉满意后,患者取平卧位,消毒皮肤,铺巾,右侧腹股沟上方纵切口,分离右股动脉,套绕阻断带。取胸骨正中位切开皮肤及皮下组织,锯开骨止血,撑开胸骨,心包外分离出无名静脉、无名动脉、左颈总动脉、左锁骨下动脉,无名动脉远端5-0 Prolene缝荷包备用,切开悬吊心包,全量肝素化,ACT>280 s后,右侧股动脉插管并固定,右心房插入34号房腔静脉插管并固定,无名动脉14号插管,建立CPB,转流。
1.4观察指标 (1)手术相关指标:手术时间、CPB时间、主动脉阻断时间、停循环时间、术中出血量(计算方法为血纱布重量-干纱布重量+吸引瓶中血量)等。(2)术后相关指标:术后苏醒时间(手术结束至意识恢复所用的时间)、术后呼吸机停用时间、2次或多次气管插管情况、重症监护时间、术后住院时间、术后当日引流量(所有引流管引流量之和)、胸部引流管留置时间、术后并发症[如肺部感染、脑部并发症(包括新发脑梗死、术后癫痫发作、术后谵妄等)]、切口愈合不良,以及术后红细胞、血浆输注量等。(3)疗效指标:二次开胸手术及术后30 d死亡情况。
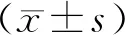
2 结果
2.1两组手术相关指标比较 观察组停循环时间较对照组短,术中出血量较对照组大,差异均有统计学意义(P<0.05)。见表2。
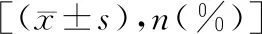
表2 两组手术相关指标比较
2.2两组术后相关指标比较 观察组术后苏醒时间、呼吸机停用时间、胸管拔除时间均快于对照组,重症监护时间、术后住院时间均短于对照组,脑部并发症、肾功能不全发生率均低于对照组,而术后当日引流量多于对照组,差异均有统计学意义(P<0.05)。见表3。
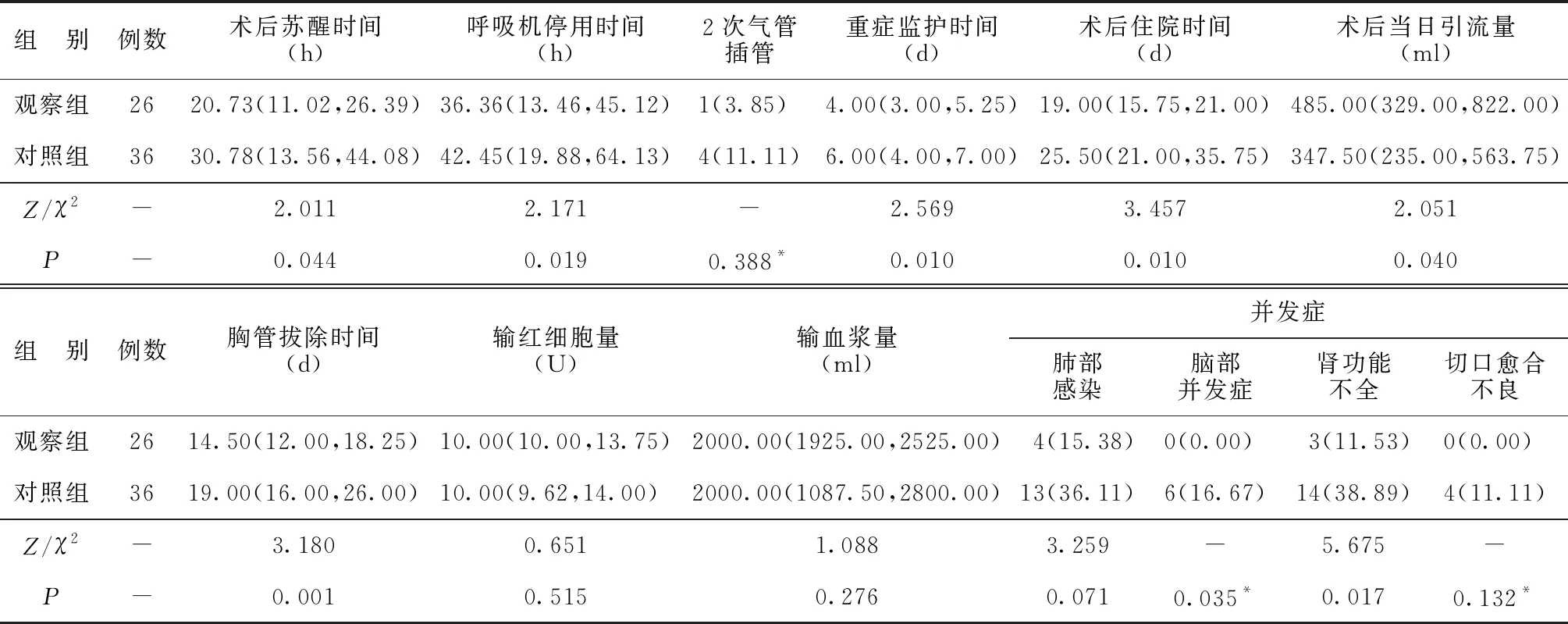
表3 两组术后相关指标比较[M(P25,P75),n(%)]
2.3两组术后二次开胸止血及术后30 d死亡情况比较 对照组术后二次开胸止血3例(8.33%),术后30 d内死亡3例(8.33%);观察组无术后二次开胸止血病例,术后30 d内死亡1例(3.85%),两组比较差异无统计学意义(Fisher确切概率法:P=0.258;P=0.633)。
3 讨论
3.1ATAAD病情较重,因其起病急、进展快,且极易出现误诊、漏诊等情况,从而危及患者的生命安全[8]。患者手术风险较高,尽管在术前诊断、手术技术和围手术期护理方面有所改进,但ATAAD仍然是心脏大血管外科医师面临的挑战,围手术期死亡率为8%~34%[9-11]。患者围手术期死亡的最重要原因是由于术中需要深低温停循环而导致器官灌注不良[12],因此,手术中最佳的插管策略对患者的生存至关重要。在插管方法选择上,通过建立维持足够的全身血流灌注的CPB对防止手术中终末器官低灌流是必不可少的。由于灌注不良所导致的相关并发症与较长的住院时间和较高的病死率有关[13]。本课题组在成熟的股动脉及腋动脉插管的基础上对多种插管方法进行探讨,从中吸取经验从而达到改善患者预后的效果。本研究中两组患者在主动脉近端及远端的处理方法上无显著差异。1995年开始腋动脉逐步替代股动脉成为主动脉夹层手术中最常用的动脉插管部位[14],但是无名动脉较腋动脉在手术过程中游离简单,易于暴露。有研究表明,使用无名动脉插管与腋动脉或股动脉插管一样安全,并且可以较为迅速建立CPB[7],避免了额外皮肤的切开以及有可能损伤腋神经造成肢体麻木等并发症的发生,同时可更快地恢复下半身灌注。因此,在无名动脉未被夹层累及时可首选其进行动脉插管。本研究观察组术中主动脉阻断时间、CPB时间以及手术时间虽然短于对照组,但差异不显著。观察组术中出血量比对照组增多,可能是在置入以及拔除左颈总动脉插管时所造成的损失。患者都采取自体回输方法,两组术后输注红细胞及血浆量并无显著差异,提示自体回输减少了因术中出血可能导致的容量不足、血红蛋白低下等相关并发症。笔者将继续完善插管技术,最大限度地减少术中出血量。
3.2本研究结果显示,观察组术中停循环时间显著短于对照组,HCA已被证实可通过诱导内皮功能障碍、细胞凋亡和坏死对中枢神经系统产生有害影响,接受长时间HCA的患者术后发生出血、呼吸衰竭和急性肾功能不全的风险更高[15]。本研究观察组术后肾功能异常发生率显著低于对照组,由于观察组停循环时间短,可以迅速恢复体外循环,从而降低了下半身器官灌注不良导致缺血、缺氧及其相关并发症的风险。另外,本研究结果显示观察组术后苏醒时间、呼吸机停用时间以及重症监护时间均短于对照组,且脑部并发症的发生率也更低。提示在停循环期间保证充足的脑灌注有利于减少脑部并发症的发生,这与相关研究结果相似[16-17]。
3.3本研究共有4例患者在术后30 d内死亡,原因主要是术前多器官灌注不良,术后需长时间机械通气、透析纠正内环境稳态等生命支持措施依然无法改善患者症状,进而导致呼吸、循环衰竭。三动脉插管虽然面临着术中出血较多的风险,但与双动脉插管相比,由于术中脑灌注充足,停循环时间短,降低了患者术后脑、肾等重要器官并发症的发生风险,进而缩短了患者的术后住院时间,改善患者预后。本研究中观察组术后无需行二次开胸止血的病例,且术后30 d内死亡的病例数也较对照组更少。
综上所述,对比股动脉联合无名动脉插管,股动脉联合无名动脉、左颈总动脉插管同样是一种安全、有效的建立CPB的方式,在保证术中充足脑部血供的同时降低停循环时间,有效改善重要器官灌注,在一定程度上降低术后并发症发生率,缩短住院时间,值得临床推广。
