外科手术治疗年龄≥75岁的高龄肾细胞癌合并静脉癌栓患者的临床经验
2022-08-09朱国栋唐世英张启鸣李丽伟陈志刚王滨帅杨飞龙葛力源孙争辉张树栋王国良田晓军张洪宪马潞林
刘 茁,朱国栋,唐世英,洪 鹏,赵 勋,张启鸣,李丽伟,彭 冉,陈志刚,王滨帅,张 丽,杨飞龙,葛力源,孙争辉,张树栋,王国良,田晓军,张洪宪△,马潞林△
(北京大学第三医院 1.泌尿外科,2.超声诊断科,3.肿瘤放射治疗科,北京 100083)
肾细胞癌(肾癌)是泌尿外科常见的恶性肿瘤,在局部进展期的肾癌中合并下腔静脉癌栓的患者占4%~10%[1]。根治性肾切除及肾静脉或下腔静脉癌栓取出术是治疗肾癌伴静脉癌栓的标准治疗方法,并能有效改善预后,其5年肿瘤特异性生存率为40%~65%[2],但无论是腹腔镜或机器人等微创途径,还是传统的开放途径,根治性肾切除和静脉癌栓取出术都是泌尿外科中难度最大的手术之一。随着中国人平均寿命的延长, 在临床工作中可见高龄肾癌合并静脉癌栓患者逐年增多。根据世界卫生组织定义和我国中老年人年龄段的划分标准,将75岁及以上定义为老年人[3]。高龄患者身体的各个方面(包括器官功能、组织代谢等)功能都在衰减,且较多同时患有肾癌以外合并症, 如心、肺、脑等重要脏器的疾病,其手术的危险因素增加, 术后并发症发生率较高,以往列为相对手术禁忌证, 诊治经验较少。目前伴随手术条件和技术的进步, 北京大学第三医院高龄肾癌伴静脉癌栓患者数目和手术成功数目不断增多,本文回顾性分析2015年5月至2018年11月北京大学第三医院收治的年龄≥75岁的肾癌伴随静脉癌栓患者的临床资料,探讨高龄患者行根治性肾切除术及静脉癌栓取出术的安全性和有效性。
1 资料与方法
1.1 一般资料
本研究12例患者均为男性。年龄75~83岁,平均(77.67±3.03)岁。体重指数17~30 kg/m2,平均(23.56±3.02) kg/m2。肾肿瘤位于右侧8例(66.67%), 左侧4例(33.33%)。采用美国麻醉医师协会(American Society of Anesthesiologists,ASA)分级评估患者麻醉风险[4],采用卡氏功能状态(Karnofsky performance status,KPS)评分评估患者的体力状况[5],采用Mayo分级评估肾静脉或下腔静脉癌栓等级。收集患者临床资料,包括有无局部症状(如血尿、腰痛、腹部肿块等)或全身症状(如消瘦、发热、乏力、贫血等)。所有患者术前均行泌尿系B超检查,评估肿瘤的侧别、部位、直径、与肾血管及集合系统的关系等。行胸部CT扫描和腹部CT扫描对肾肿瘤进行TNM分期。行下腔静脉增强磁共振成像(magnetic resonance imaging,MRI)扫描,以测量肿瘤癌栓的长度、癌栓是否同时合并血栓、癌栓是否侵犯下腔静脉或肝静脉血管壁[6-7]。行超声心动图检查以评估心脏功能及是否存在心房癌栓。检测术前血肌酐及术后1周血肌酐以评估肾脏功能。术前行肺部CT以评估有无肺转移,行腹部超声和CT以评估有无腹部脏器转移。对有相关症状的患者可行头颅MRI或骨扫描以除外中枢神经系统转移或骨转移。
本研究患者的纳入标准:(1)术前泌尿系增强CT和/或下腔静脉增强MRI等影像学检查提示为肾恶性肿瘤伴随下腔静脉癌栓;(2)患者年龄≥75岁;(3)全身评估一般情况可,ASA评分1至3级,KPS评分≥80分;(4)向患者交代不同的治疗方式,患者及家属同意行手术治疗,且手术意愿强烈。排除标准为:(1)存在严重心肺功能不全、凝血功能异常等绝对或相对手术禁忌证或麻醉禁忌证;(2)选择单纯非手术治疗方式,例如酪氨酸激酶抑制剂药物治疗、放射治疗、等待观察等;(3)术后病理证实为非肾细胞癌。
1.2 手术方法
根据高龄患者肾癌癌栓的Mayo分级制定相应的手术策略[8]。对于Mayo 0级的肾静脉癌栓,处理方法同肾根治性切除术,完整切除患侧肾及含癌栓的肾静脉[9]。对于凸入腔静脉内长度短的Ⅰ级癌栓,可尝试采用Milking技术将癌栓挤回肾静脉再行肾根治性切除术,对于长度长的癌栓或有腔静脉壁侵犯建议采用Satinsky心耳钳阻断下腔静脉后取栓,术中切除受侵犯的下腔静脉血管壁,并对下腔静脉进行血管重建[10]。对于Ⅱ级癌栓,如癌栓高度未超过第一肝门,一般无需翻肝,依次阻断癌栓远心端下腔静脉、对侧肾静脉(左侧肾癌伴癌栓需同时阻断右肾动脉)及癌栓近心端腔静脉后切开下腔静脉取栓;如癌栓高度达肝后,未侵及腔静脉壁者可用气囊尿管法取出,多数则需离断部分肝短静脉及右侧肝韧带,翻起肝右叶,游离肝后段腔静脉至瘤栓顶端之上,于癌栓近心端阻断后切开下腔静脉取栓[11]。对于癌栓超过肝静脉的Ⅲ级癌栓,需要离断肝韧带,将肝脏自膈肌向下游离,显露并游离出肝上、膈下段的下腔静脉,于膈下阻断下腔静脉,同时Pringer法游离并阻断第一肝门后取栓[12-13]。对于Ⅳ级癌栓,手术难度及风险极高,本组1例患者癌栓达到膈肌以上,但尚未进入心房,且未侵犯静脉壁,采用气囊尿管法轻柔推挤将癌栓挤入下腔静脉[14],使癌栓由膈上变为膈下,进一步取出癌栓[15]。对于有肾门淋巴结转移的患者(患者编号2、5、7),术中采用肾门淋巴结清扫术。
1.3 术后并发症及随访
在并发症方面,采用Clavien分级系统统计患者并发症的发生率、类型、处理方式及预后[16-17]。在手术难度评估及预后方面,统计术中出血量、术中输注悬浮红细胞的容积、术后重症监护室(intensive care unit,ICU)住院天数、术后住院天数。术后5年内每6个月随访1次,5年后每年随访1次。随访检查内容主要包括生化(肾功能)、腹部B超和/或泌尿系增强CT、胸片或胸部增强CT等,以除外局部复发或转移。
1.4 统计学分析
采用Spss 18.0统计软件进行分析,连续变量采用“均数±标准差”表示,分类变量用例数和百分比表示。生存时间的计算是从手术日至死亡或最后一次随访(确认患者存活)之日。
2 结果
本组12例高龄肾癌合并肾静脉或下腔静脉癌栓患者的肿瘤直径2~10 cm,平均(7.16±2.40)cm。ASA 评分2分者8例,3分者4例。KPS评分80~100分,平均(96.25±6.08)分。临床表现方面,无症状者2例(16.67%), 仅有局部症状者7例(58.33%), 仅有全身系统症状者2例(16.67%),同时合并局部症状和全身症状者1例(8.33%)。既往合并症方面,仅合并高血压者3例(25%), 仅合并糖尿病者2例(16.7%), 仅合并冠心病者1例(8.3%),同时合并高血压及糖尿病者1例(8.3%), 否认合并症者5例(41.7%)。TNM分期方面,T3bN0M0者7例(58.33%), T3bN1M0者3例(25.00%), T3cN0M0者1例(8.33%), T4N1M0者1例(8.33%)。静脉癌栓Mayo分级方面,Mayo 0级者4例(33.33%),Mayo Ⅰ级者4例(33.33%),Mayo Ⅱ级者2 例(16.67%),Mayo Ⅲ级者1例 (8.33%), Mayo Ⅳ级者1例 (8.33%)。术前平均血红蛋白为(94.50±27.58) g/L(75~114 g/L),平均白蛋白为(39.70±0.85) g/L(39.1~40.3 g/L),平均总蛋白为(77.15±5.02) g/L(73.6~80.7 g/L), 见表1。
12例患者手术均顺利完成,无术中死亡病例,无围术期死亡病例。采用腹腔镜途径手术者9例(75%), 采用开放途径手术者3例(25%)。手术时间174~567 min,平均(329.29±127.37) min。术中出血量400~800 mL,平均(566.67±208.17) mL。输注红细胞0~2 000 mL,平均(600.00±910.54) mL。输注血浆量0~1 600 mL,平均(233.33±496.04) mL。4例因肿瘤侵犯血管壁(33.33%)切除下腔静脉壁。术后ICU住院时间0~6 d,平均(1.00±1.71) d。术后住院时间5~13 d,平均(7.92±2.71) d。术前血肌酐60~134 μmol/L,平均(93.92±22.35) μmol/L。术后1周血肌酐62~161 μmol/L,平均(100.83±24.76) μmol/L。病理诊断为肾透明细胞癌11例(91.67%),乳头状肾细胞癌2型者1例(8.33%)。在11例肾透明细胞癌中病理分级2级6例(54.55%), 3级3例(27.27%), 4级2例(18.18%)。患者术中及术后资料见表2。
本组12例中,有1例(8.33%)发生术后早期并发症,其并发症为改良Clavien分级Ⅱ级,具体表现为双下肢肌间静脉血栓,采用低分子肝素抗凝治疗后好转。12例未见明显术后大出血、肾周脏器损伤(如肝、脾、胰腺、胃肠道)、胸膜损伤、肺栓塞等并发症。12例中11例(91.6%)获得随访,1例失访。11例获得随访的患者中,随访时间为5~44个月,中位随访时间25个月,有3例患者分别于随访5、14和23个月出现肿瘤特异性死亡。本组12例患者中,患者编号2术后3个月复查时肺部CT提示肺转移,采用舒尼替尼靶向药物治疗,术后5个月发生肿瘤特异性死亡;患者编号9术后3个月复查时出现骨痛症状,行骨扫描提示为肾癌骨转移,采用舒尼替尼靶向药物治疗,本次研究结束随访时患者仍然存活;其余10例患者术后随访均未发现远处转移。本组12例患者术后随访均未发现肿瘤局部复发。
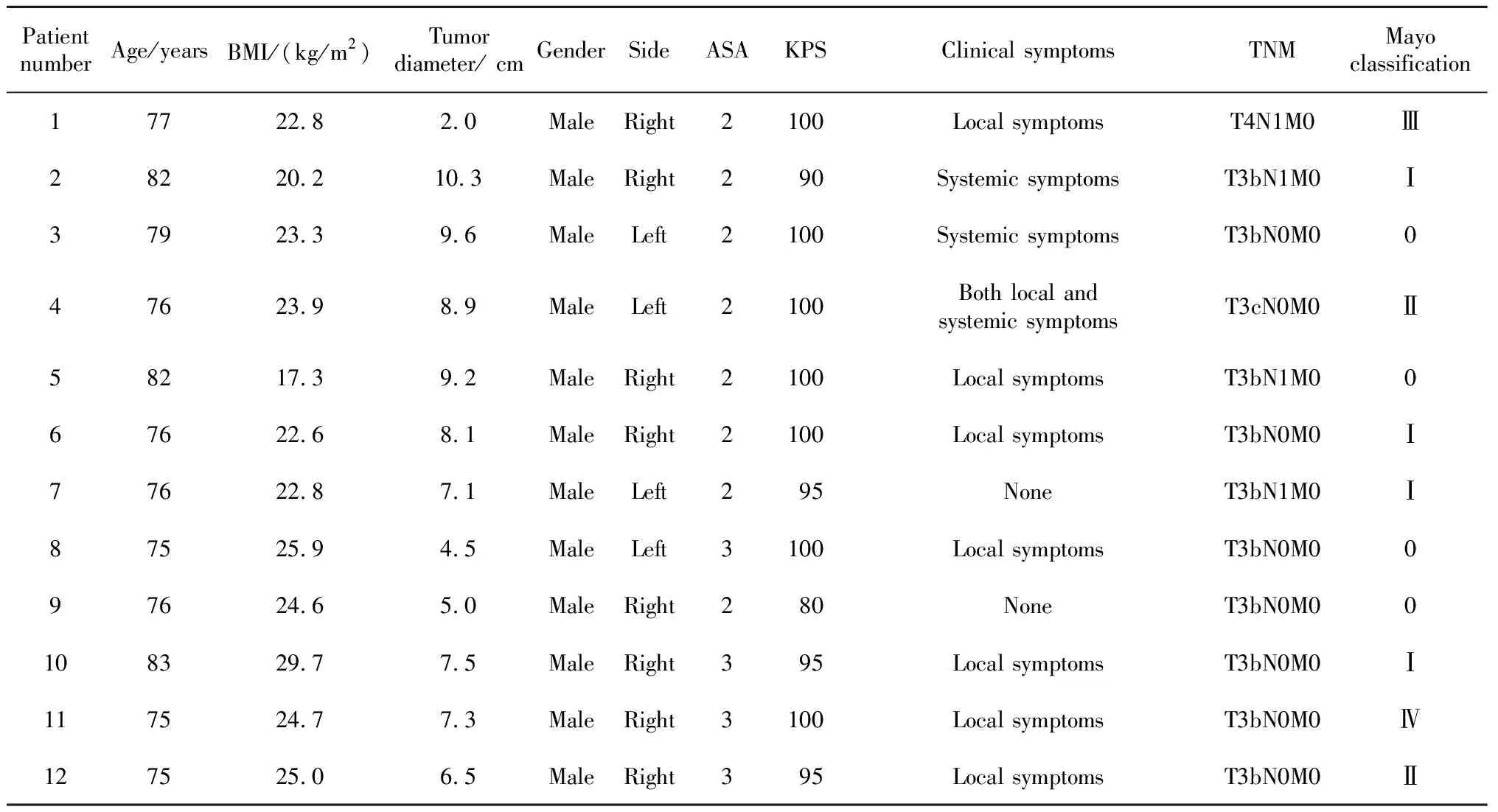
表1 高龄肾癌伴静脉癌栓患者术前资料Table 1 Preoperative data of elderly patients with renal cancer and venous tumor thrombus
3 讨论
肾癌是泌尿系统常见的恶性肿瘤,无论是腹腔镜方式还是开放手术方式,手术切除对于大多数患者来说是唯一可以实现的治愈方式[18]。肾根治性切除+下腔静脉瘤栓取出术具有以下特点:(1)手术损伤大,术中出血多;(2)下腔静脉阻断和阻断开放时术中血流动力学波动;(3)术中癌栓脱落或癌栓上附着血栓脱落,可导致肺栓塞发生。由此可见肾癌癌栓的手术治疗具有手术麻醉难度较大的特点,但是,高龄肾癌患者手术数量具有增加趋势。由于生活水平提高, 人群平均寿命延长,人口老龄化明显。同时, 社会保健意识增强,以及医学影像诊断技术的发展, 越来越多的高龄肾癌癌栓患者被及时发现。对于这些高龄肾癌癌栓患者,手术治疗给泌尿外科医生带来较大挑战。
对于初步诊断肾癌伴静脉癌栓的高龄患者,其初步治疗方式的选择如下:(1)以外科手术治疗为主导的综合治疗模式;(2)单纯的药物治疗,例如酪氨酸激酶抑制剂[19];(3)放射治疗[20];(4)血管介入栓塞治疗[21];(5)等待观察;(6)其他治疗方式。高龄肾癌癌栓患者如何选择适合的个体化治疗方案,需要结合患者本身及肿瘤特点,权衡利弊综合判断。姑息性切除可以降低肿瘤负荷,外科手术可一定程度上减轻患者的心理负担,但是高龄肾癌癌栓患者的身体机能减退,代偿能力降低;术前常合并心脑血管及呼吸系统等老年慢性病,可能给麻醉和手术带来较大的风险;术后易发生并发症,如伤口预后延迟、肺部感染、下肢静脉血栓及压疮等。北京大学第三医院严格把控高龄肾癌癌栓的手术适应证,具体如下:(1)患者及家属有较强的手术治疗意愿;(2)全身评估一般情况可,ASA评分1至3级,KPS评分≥80分;(3)无明显手术或麻醉禁忌证。在决定手术前,充分告知手术风险。
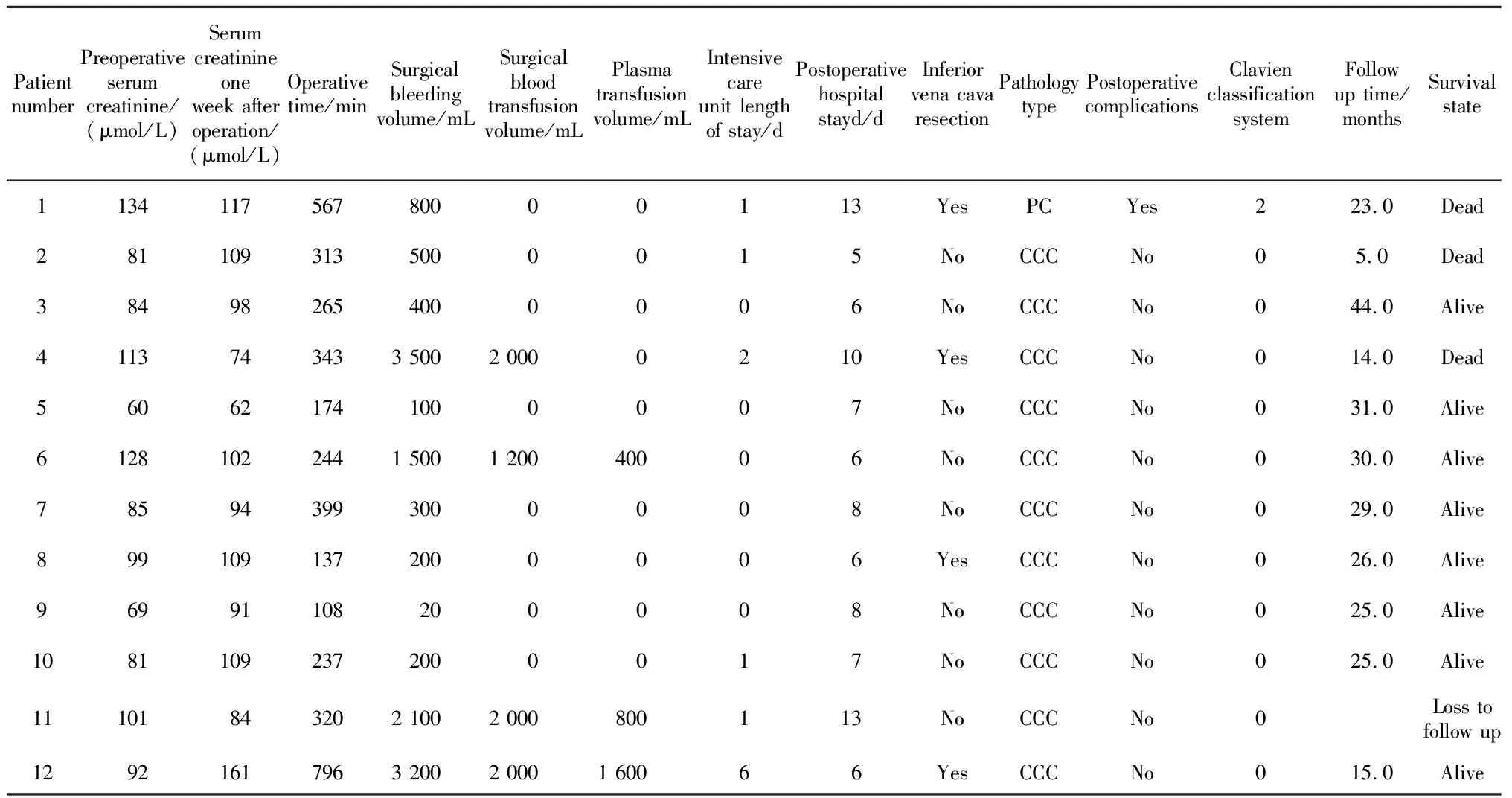
表2 高龄肾癌伴静脉癌栓患者术中及术后随访资料Table 2 Intraoperative and postoperative follow-up data of elderly patients with renal cancer and venous tumor thrombus
对于高龄状态可能给外科手术带来的弊端方面,我们的经验是:(1)高龄肾癌癌栓患者的身体机能减退,代偿能力降低,可以采用ASA评分及KPS评分等准确及时地评估患者对手术的耐受程度。(2)术前常合并心脑血管及呼吸系统等老年慢性病,在术前需要完善常规的化验和检查,明确心、肺、肝、肾等重要脏器的功能,对合并糖尿病、高血压、心脏病、慢性支气管炎等基础病的患者,积极完善相关科室会诊及多学科团队会诊(multi-disciplinary team,MDT)[22],将指标控制在相对稳定的状态,能够满足手术的要求。麻醉前应做好充分准备,慎重选择麻醉药物,麻醉中严密监测,积极预防麻醉中和麻醉后可能出现的并发症。(3)术后易发生并发症,如伤口预后延迟、肺部感染、下肢静脉血栓及褥疮等,需要对高龄患者进行围手术期的护理,术前做好健康宣教,术后严密观察病情,及时采取正确的预防性护理措施,使患者顺利度过围手术期,降低并发症的发生率。
本组12例患者在经过谨慎的术前评估及全面细致的术前准备后选择了手术治疗。在临床表现方面,本研究患者无症状者仅有占16.67%,其余患者均有局部症状(如血尿、腰痛、腹部肿块等)或全身症状(如消瘦、发热、乏力、贫血等)。手术后患者临床症状缓解或消失,可提高患者的生活质量。另外,外科手术一定程度上可减轻患者的心理负担,例如对疾病的恐惧感和焦虑感,但同时应当注意高龄癌栓患者围术期的心理波动性,及时发现并帮助患者由于手术治疗本身产生的恐惧感,稳定患者不良的情绪,提高患者的依从性和配合度,以确保手术能顺利进行。
本研究存在以下缺陷:(1)只统计了高龄肾癌癌栓患者行外科手术治疗的临床资料,而对于选择其他治疗方式的患者因缺乏完整的随访资料,未纳入研究;(2)为回顾性研究,其结论需要前瞻性对照研究进一步明确;(3)样本量少,需要大样本量长期的随访资料。
综上所述,对于手术意愿强烈、全身评估一般情况可、体能状态良好的高龄肾癌伴静脉癌栓患者,在经过谨慎的术前评估及全面细致的术前准备后选择手术治疗安全、有效。
