RCDs-Fe(III)复合荧光碳点的合成及检测氟离子的应用
2022-08-05唐帅罗亚雄李永生
唐帅,罗亚雄,李永生
(1.四川大学 化学工程学院,四川 成都 610065;2.四川大学 基础医学与法医学院,四川 成都 610065)
氟是人体必需的微量元素之一,在人体中分布广泛[1]。体内氟离子含量失衡会对健康产生影响[2]。氟化物被世界卫生组织列入3类致癌物清单中,我国卫生标准规定[3],饮用水中氟浓度应小于1.0 mg/L。迄今,常见氟离子检测方法有离子选择电极法[3-4]、离子色谱法[5-6]、比色法[7-8]和荧光法等[9-10]。荧光法具有灵敏度高、重现性好、抗干扰能力强的优点[11-16],尤其是碳点(CDs)荧光法检测氟离子[17-18]。因此,本研究基于复合荧光碳点[RCDs-Fe(III)],开发了一种氟离子分析方法。
1 实验部分
1.1 试剂与仪器
柠檬酸(CA)、乙二胺(EDA)、水杨酸(SA)、36%醋酸(HAc)、三水醋酸钠(NaAc·3H2O)、六水氯化铁(FeCl3·6H2O)、氟化钠(NaF)均为分析纯;实验用水为纯水(电导率:~1.0 μS/cm)。
RF-5301PC荧光光度仪;KL-UP-IV-10型艾柯超纯水器;82-5型恒温磁力搅拌器;AUW型电子天平;UV-1800pc紫外-可见分光光度计;pXJ-1C离子计;7102复合氟电极。
1.2 试剂配制
1.2.1 0.1 mol/L醋酸 取36%的乙酸溶液8.3 mL 至500 mL容量瓶内,用水定容。
1.2.2 0.1 mol/L醋酸钠 溶解6.80 g三水醋酸钠,转移至500 mL容量瓶中,用水定容。
1.2.3 150 mg/L Fe(III)标液 用pH 2的盐酸溶解0.720 g FeCl3·6H2O,转移至100 mL容量瓶,用水定容。
1.2.4 0.1 g/L F-标液 用水溶解0.221 g NaF,转移至100 mL容量瓶中,用水定容。
1.2.5 0.5% CA/EDA/SA-CDs 取0.5 mL的CA/EDA/SA-CDs碳点母液,pH 5.0的溶剂稀释至100 mL。
1.2.6 复合碳点 40 mL的0.5% CA/EDA/SA-CDs溶液与10 mL的150 mg/L Fe(III)溶液混合后,用于F-的测定。
1.3 RCDs-Fe(III)复合碳点的制备
100 mL烧杯中,用纯水溶解2 g柠檬酸和0.2 g水杨酸。边搅拌,边加入2 mL乙二胺[19]。混合液放入通风橱内的微波炉中加热4 min,生成荧光碳点(CA/EDA/SA-CDs)。用250 mL纯水溶解,得到碳点母液。将碳点母液稀释到一定浓度后,与Fe(III)溶液混合反应5 min,得到测定氟离子的复合碳点(RCDs-Fe(III))。
1.4 氟离子测定
常温下,取4 mL 氟离子样品液,与1 mL RCDs-Fe(III)混合反应1 h。以3 000 r/min离心10 min。取上清液进行检测,由于F-络合能力较强,能与RCDs-Fe(III)表面Fe(III)络合反应形成FeF3,碳点被释放,且荧光得到恢复,根据荧光恢复程度(ΔF)间接定量氟离子。
2 结果与讨论
2.1 碳点原料的影响
2.1.1 碳点原料对荧光量子产率的影响 称取2 g能与Fe(III)反应的多种原料(AsA、EDTA、KSCN、草酸、CA)和2 mL EDA混合,采用微波法(800 W,中档,4 min)合成一系列荧光碳点(EDTA/EDA-CDs、AsA/EDA-CDs、OC/EDA-CDs、CA/EDA-CDs、CA/KSCN-CDs),随后比较并筛选出荧光量子产率φ(φ=k·F/A;F为待测物的积分荧光强度,A为待测物质的吸光度,k为与溶剂折射率等因素相关的校正系数)最大的碳点,结果见图1。

图1 碳点原料对量子产率的影响Fig.1 The influence of carbon dot raw materials on quantum yield
由图1可知,各种CDs荧光量子产率不同,相对于参比物质硫酸奎宁(φ=0.54),5种碳点中量子产率最高的是EDTA/EDA-CDs(φ=0.32),其次为CA/EDA-CDs (φ=0.31),最低的是AsA/EDA-CDs(φ=0.05)。
2.1.2 碳点原料对复合碳点的影响 为筛选出与Fe(III)反应最灵敏的碳点,将上述5种碳点分别稀释至荧光强度相同的浓度,然后加入2 mg/L Fe(III),根据荧光猝灭值(ΔF)评价碳点与Fe(III)的络合能力,结果见图2。
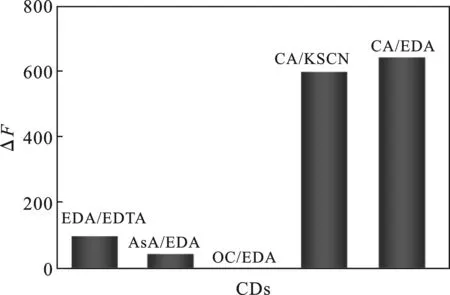
图2 碳点原料对复合碳点的影响Fig.2 The effect of carbon dot raw materials on composite carbon dot
由图2可知,不同碳点对Fe(III)的猝灭程度不同,仅有OC/EDA-CDs不与Fe(III)发生反应,其余碳点荧光均能被Fe(III)猝灭;其中2 mg/L Fe(III)对CA/KSCN-CDs和CA/EDA-CDs猝灭程度最大,但由于前者合成时,KSCN高温分解,产生有害气体,污染环境。因此,选定CA/EDA-CDs作为初始碳点进行研究。
2.2 水杨酸的影响
2.2.1 水杨酸对复合碳点检测氟离子的影响 为了增强CA/EDA-CDs对Fe(III)的敏感度,提高复合碳点检测氟离子的灵敏度,本研究在合成CA/EDA-CDs时添加了水杨酸(SA)。在0.05%的CA/EDA/SA-CDs、CA/EDA-CDs中加入1 mL 150 mg/L Fe(III),形成两种复合碳点,再加入不同浓度F-恢复荧光,根据响应曲线的斜率,对比氟离子检测灵敏度,实验结果见图3。

图3 水杨酸对复合碳点检测氟离子的影响Fig.3 The effect of salicylic acid on the detection of fluoride ion by composite carbon dot
由图3可知,CA/EDA/SA-CDs形成的复合碳点对F-响应更为灵敏,因此,本研究选择在合成CA/EDA-CDs时加入一定量的SA。
2.2.2 水杨酸加入量对复合碳点检测氟离子的影响 在相同条件下,合成不同SA含量的碳点,并稀释至0.05%,再添加150 mg/L Fe(III),形成复合碳点,之后加入不同浓度氟离子,并比较响应曲线斜率,结果见图4。
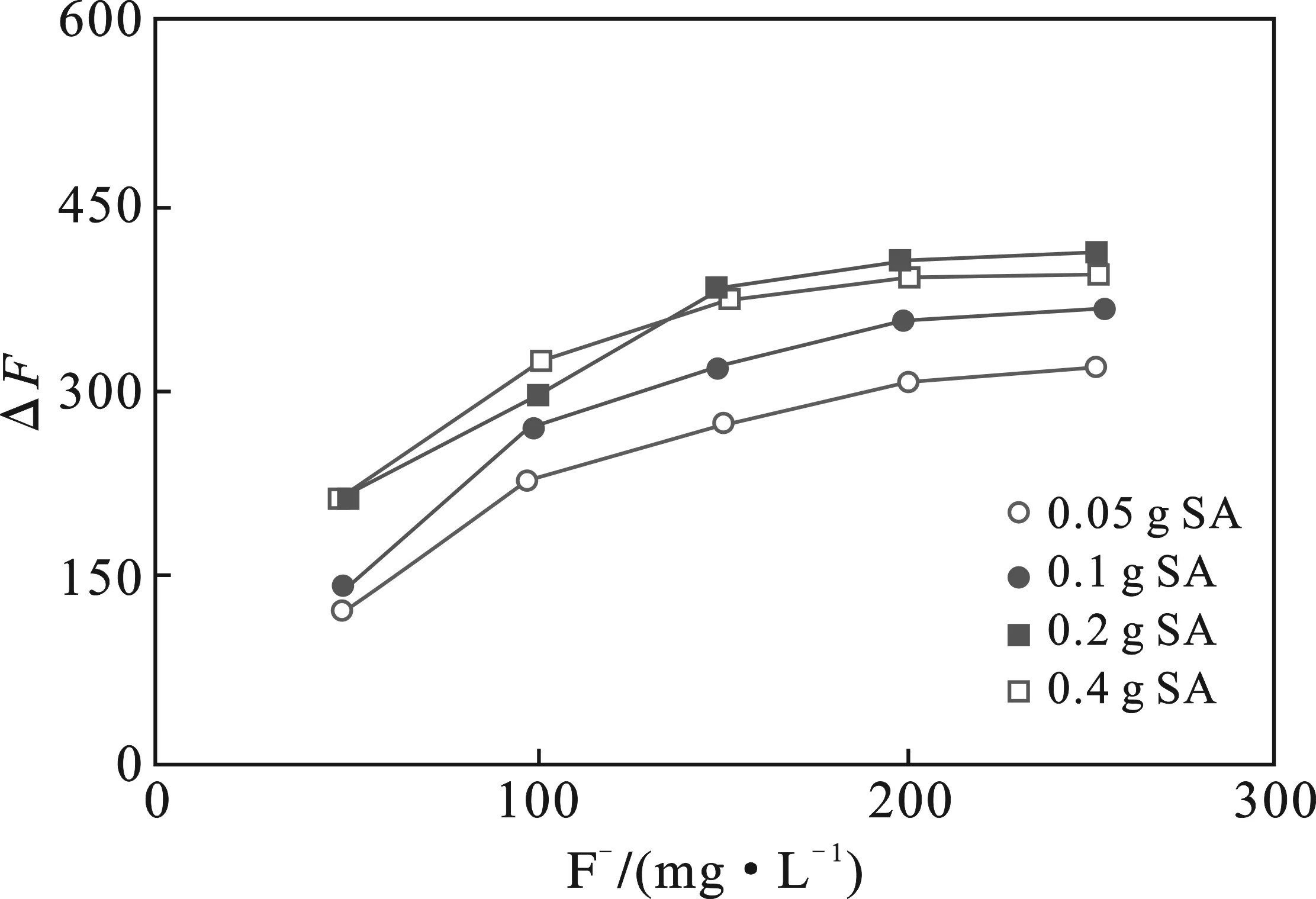
图4 水杨酸加入量对复合碳点检测氟离子的影响Fig.4 The influence of the addition of salicylic acid on the detection of fluoride ion by the composite carbon dot
由图4可知,在复合碳点/氟离子反应体系中,水杨酸加入量为0.2 g时,氟离子检测线性响应范围较宽,且灵敏度较高。因此,选定CA/EDA-CDs中水杨酸加入量为0.2 g。
2.3 CA/EDA/SA-CDs的光谱扫描
图5是碳点CA/EDA/SA-CDs的紫外吸收光谱及荧光光谱。
图中紫外吸收光谱曲线(Abs)表明,该碳点在237,350 nm处有特征吸收,分别是来自于碳点表面官能团碳碳双键的π→π*跃迁和羧基的n→π*跃迁。荧光光谱曲线表明,该碳点的最大激发和最大发射波长分别为370,460 nm。该荧光碳点的最大激发峰与其吸收峰基本重合,这与理论相符。
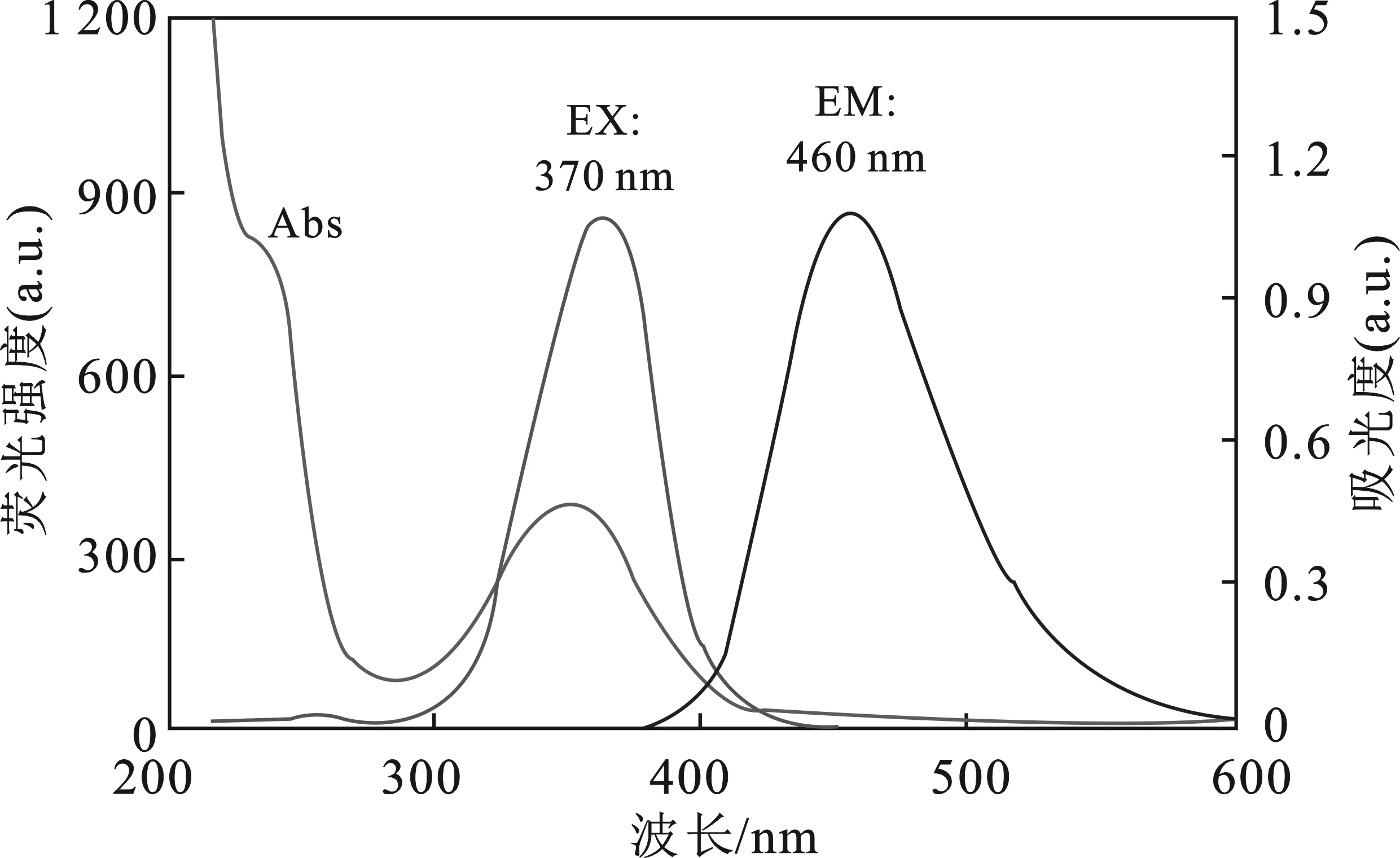
图5 CA/EDA/SA-CDs的分子光谱Fig.5 Molecular spectra of CA/EDA/SA-CDs
2.4 复合碳点溶剂对氟离子检测的影响
0.1 mol/L醋酸-醋酸钠缓冲液和盐酸溶液(pH 5.0) 作为溶剂时,对0.5% RCDs-Fe(III)检测氟离子的影响,见图6。

图6 复合碳点溶剂对氟离子检测的影响Fig.6 The influence of composite carbon dot solvent on fluoride ion detection
由图6可知,当盐酸溶液作为体系溶剂时,RCDs-Fe(III)检测氟离子的灵敏度高。其原因可能是醋酸-醋酸钠缓冲液作为溶剂时,部分醋酸根与RCDs-Fe(III)表面的Fe(III)反应,形成醋酸铁,影响了复合碳点荧光的恢复程度(ΔF)。因此,本方法选定盐酸溶液(pH 5.0)作为体系的反应溶剂。
2.5 Fe(III)浓度对氟离子检测的影响
影响RCDs-Fe(III)检测氟离子的主要因素是碳点表面与Fe(III)络合的基团数量及络合能力;基团数量影响F-检测范围,络合能力影响氟离子检测的灵敏度。因此,考察了Fe(III)浓度对RCDs-Fe(III)检测氟离子的影响。将0.5% CA/EDA/SA-CDs与不同浓度(25~200 mg/L)的Fe(III)形成RCDs-Fe(III)后,再取4 mL RCDs-Fe(III)与1 mL不同浓度(15~80 mg/L) F-溶液混合,检测该混合液荧光强度的变化,结果见图7。
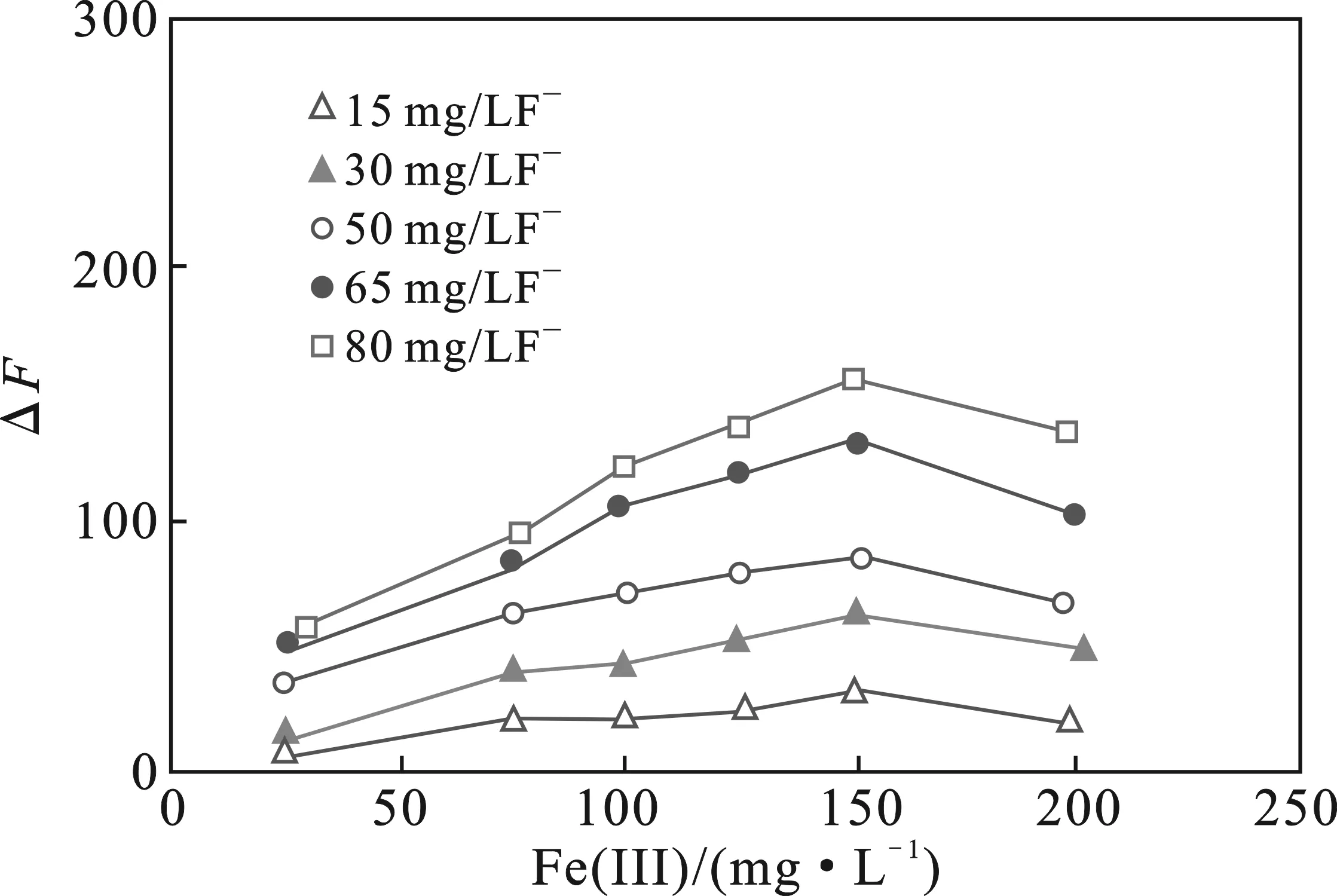
图7 Fe(III)浓度对氟离子检测的影响Fig.7 The influence of Fe(III) concentration on the detection of fluoride ion
由图7可知,Fe(III)浓度为150 mg/L时,氟离子恢复碳点荧光最强,即RCDs-Fe(III)检测氟离子的灵敏度最高。因此,选定检测氟离子时Fe(III)浓度为150 mg/L。
2.6 复合碳点浓度对氟离子检测的影响
在上述选定条件下,考察了RCDs-Fe(III)浓度对氟离子检测的影响。首先,将5个不同浓度(0.01%,0.05%,0.1%,0.3%,0.5%)的CA/EDA/SA-CDs与150 mg/L Fe(III)按4∶1比例混合,得到5个RCDs-Fe(III)溶液(以CDs计);然后,再与不同浓度的氟离子标液混合,实验结果见图8。

图8 RCDs-Fe(III)浓度对氟离子检测的影响Fig.8 The influence of RCDs-Fe(III) concentration on the detection of fluoride ion
由图8可知,随着RCDs-Fe(III)浓度的增大,荧光恢复值也逐渐增加;根据曲线斜率可知,当RCDs-Fe(III)浓度为0.5%时,氟离子检测的灵敏度相对较高。因此,选择该浓度作为检测氟离子时RCDs-Fe(III)的浓度。
2.7 复合碳点检测氟离子的干扰评价
在选定的实验条件下,评价了多种常见阴离子对0.5% RCDs-Fe(III)检测F-(5,10 mg/L)的影响。在4 mL的0.5% RCDs-Fe(III)中分别添加不同种类的阴离子(5,10 mg/L)并检测其荧光强度,其中纯水作为空白组进行对照,结果见图9。
由图9可知,这两个浓度下,只有氟离子能显著恢复RCDs-Fe(III)的荧光,其他阴离子几乎不能恢复复合碳点的荧光,RCDs-Fe(III)对氟离子表现出很强的选择性,其余阴离子对氟离子的检测不产生干扰(RSD<5%)。
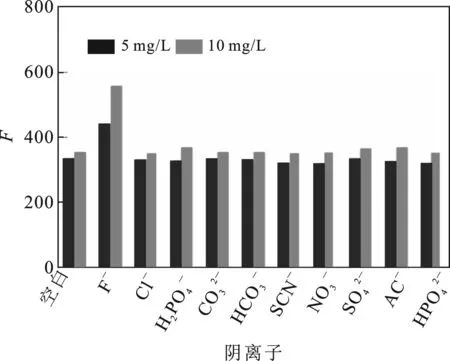
图9 阴离子对RCDs-Fe(III)检测氟离子的干扰实验Fig.9 Interference experiment of anion on RCDs-Fe(III) detection of fluoride ion
2.8 氟离子的线性检测范围及实样测定
在上述优化条件下,先评价了检测试剂RCDs-Fe(III)复合碳点荧光强度的重现性。分别取11次0.5% RCDs-Fe(III)复合碳点液作为样品,并进行检测(328.0,335.3,329.4,330.7,325.8,338.2,336.5,331.3,330.6,335.7,334.6,332.4±3.92),求出检测结果RSD为1.2%。然后,评价了RCDs-Fe(III)荧光恢复程度(ΔF)与氟离子浓度之间的相关性得到氟离子检测标准曲线,见图10。
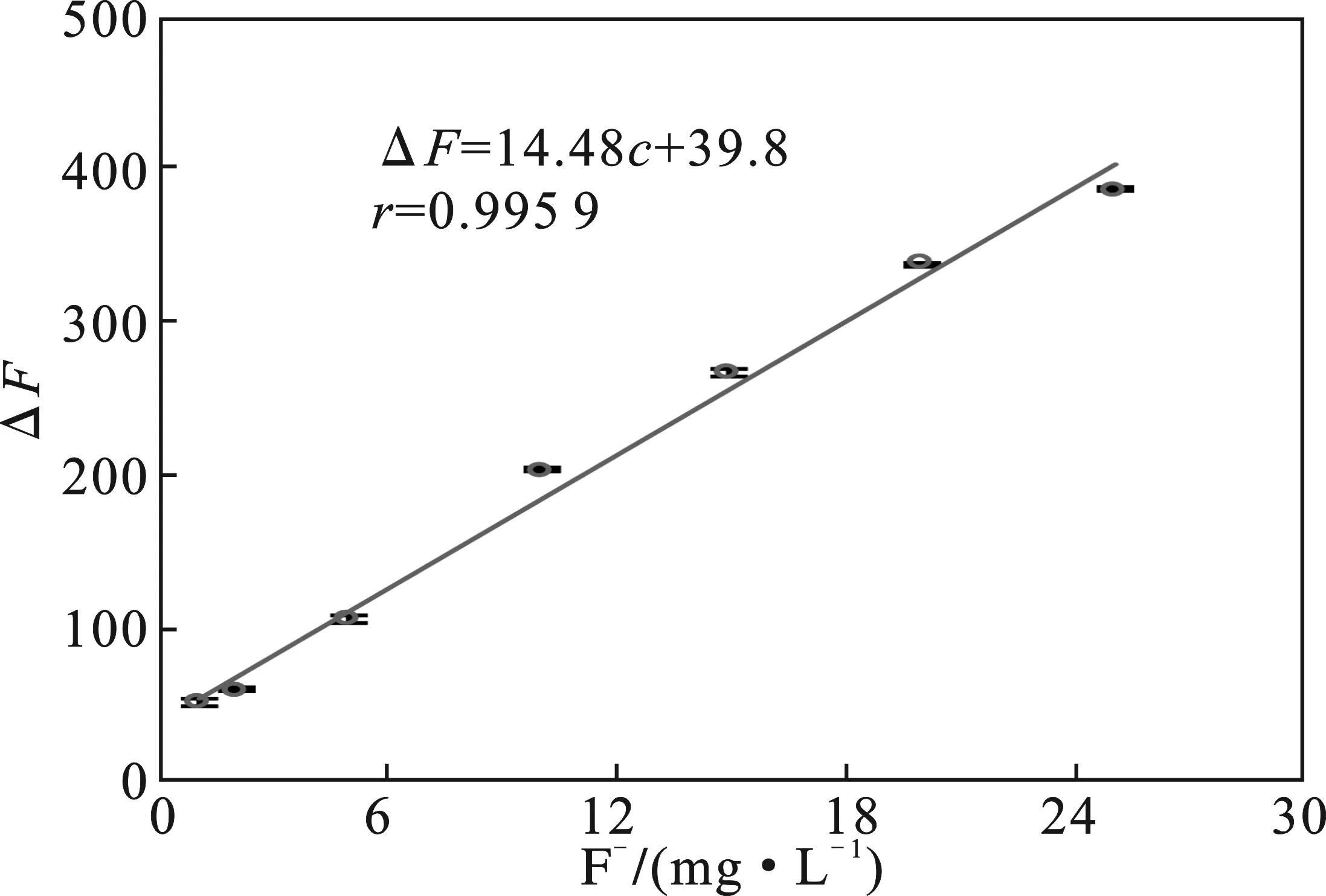
图10 复合碳点法检测氟离子的线性范围Fig.10 Linear range of RCDs-Fe(III) detecting fluoride ion
由图10可知,该复合碳点检测氟离子的线性响应范围为1~25 mg/L (ΔF=14.48c + 39.8,r=0.995 9)。根据荧光强度的偏差及上述相关曲线方程的斜率,求出的最小检出限(LOD=3 SD/k)为0.82 mg/L。
选择佳洁士清甜樱花香型(No.1)、舒克椒样薄荷香型(No.2)、黑人专研亮白牙膏(No.3)、高露洁360°长效清新牙膏(No.4)和欧乐B抗敏护龈牙膏(No.5)(购于当地沃尔玛超市)。在测定前,样品进行了以下预处理:用100 mL纯水溶解1.0 g牙膏,超声30 min后,在10 000 r/min转速下离心30 min,上清液作为测试样品。RCDs-Fe(III) 法及电极法测定结果见表1。
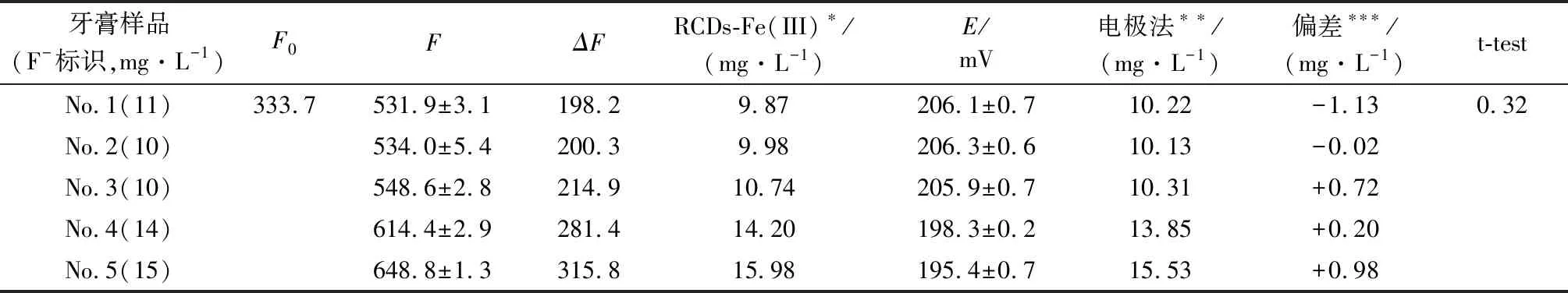
表1 RCDs-Fe(III)法及对照法的测定结果
由表1可知,RCDs-Fe(III)法测定牙膏中氟离子含量的结果与电极法基本一致,与牙膏标识值也相同;t检验结果表明两种方法无显著性差异。因此,本方法可用于牙膏中氟离子的准确测定。
3 结论
以柠檬酸、乙二胺、水杨酸和Fe(III)为原料,合成了一种对氟离子敏感的RCDs-Fe(III)复合碳点,并对合成和检测条件进行了优化。通过对溶剂、Fe(III)和RCDs-Fe(III)浓度等因素优化,建立了检测范围为1~25 mg/L的氟离子分析方法,检出限为0.82 mg/L。最后对5种牙膏样品中氟离子含量进行了检测,测定结果准确、可靠。本方法具有重现好、抗干扰、快速方便等优点,在磷化工、茶叶和高氟水等领域中氟离子的检测具有较好的应用前景。
