有机聚合物和生物材料用于HMIs电化学检测的研究进展*
2022-08-02郑明明张晓臣
王 珏,付 东,郑明明,张晓臣,阚 侃
(黑龙江省科学院 高技术研究院,黑龙江 哈尔滨 150020)
前 言
重金属离子(HMIs)被认为是低密度高毒性的化学物质的代表。由于其具有富集性和不可降解性,导致其对生态环境和人类健康有巨大的威胁[1-3]。HMIs可以在生物圈中积累,并通过食物链汇入人体,从而恶化人类健康。当HMIs进入细胞后,会改变身体内组织和器官的生命周期并造成不可逆损
伤[4-6]。
在绝大多数情况下,一些微量的HMIs是生物体所必须的,如镁、铁、钴、锌、铜、锰等。他们是合成生物体必要成分的主要元素,如叶绿素、血红蛋白等[7,8]。这对于生物细胞的功能性很重要,如能量转化、转运和细胞信号传递等[9]。当这些HMIs浓度很高时会脱离其所在的成分,并与其他的普通蛋白质作用,从而导致生物毒性。HMIs的毒性机制表现为抑制酶作用、氧化应激和抗氧化代谢受损等。这些机制通过自由基生成导致DNA损伤、脂质过氧化、蛋白质巯基耗竭从而影响人类健康[10]。而镉、铬、铅、汞、砷等HMIs,即使在极低浓度下也会对生物产生很强的毒性。他们会导致神经、免疫、生殖和消化系统的各种紊乱和病变[11]。
因此对环境和食品的HMIs含量监测尤为重要。这就需要发展高灵敏性、高选择性的HMIs检测方法测定水体环境、生物样本、土壤样本等复杂基质中的有毒有害HMIs。
电化学传感器具有灵敏、快速、可同时检测多种HMIs的特点。尤其电化学检测设备轻便便宜、测试方法简单、操作难度低、预处理过程少及可以实现HMIs的原位检测,因此成为一种重要的HMIs检测手段[12,13]。电化学检测的关键在于工作电极。目前,玻碳电极(G C E)已经逐渐取代传统的滴汞电极和贵金属电极,因为GCE更为便宜、稳定、且不会造成二次污染。但是GCE也存在一定的弊端就是G C E对HMIs的选择性和敏感性较差,无法应对痕量HMIs的检测。科研工作者们针对G C E改性进行了大量的研究工作。这其中有机材料与生物材料由于具有丰富的富电子原子和富电子基团,可以与HMIs发生配位和螯合作用,提高GCE电极的灵敏度并降低检测极限,从而备受关注。本文综述了有机与生物材料制备的电化学传感器用于HMIs的检测及其检测增强机理。
1 有机聚合物改性电极
有机聚合物材料是优异的HMIs电化学检测材料。这些有机聚合物材料由于含有大量的N、S等富电子原子及-NH2、-SH等富电子基团,通过孤对电子与HMIs发生配位或螯合作用,增强改性电极对HMIs的吸附和捕集效果,被广泛应用于HMIs的电化学检测工作[14]。
1.1 导电聚合物改性电极
导电聚合物(CP)是一类特殊的有机聚合物材料。他们的单体经过掺杂聚合后能够使聚合物导电,因此可以用于制备改性电极材料。常用的C P包括聚乙炔(PAc)、聚苯胺(PANI)、聚吡咯(PP y)和聚噻吩(PT h)[15]。CP价格低廉、制备工艺简单、导电性好,是优异的改性电极材料。但是CP在聚合的过程中容易团聚,这也是C P作为电极材料所面临的主要问题[16]。而设计CP的结构,往往成为这类研究的关键。因此静电纺丝法与硬模板法成为解决这一问题的主要手段。通过静电纺丝或是让C P沿模板原位聚合赋予CP一定的结构,可以有效地避免CP的团聚。Promphet[17]采用静电纺丝法,以石墨烯、PANI、聚苯乙烯(PS)为原料,通过调控溶剂T H F和DM F的比例,制备了G/PA NI/P S多孔纳米纤维。石墨烯和PA NI良好的导电性能够显著提高多孔纤维对Pb2+和Cd2+的电化学敏感性。此外多孔结构有利于HMIs的吸附,使G/PA NI/P S对Pb2+和C d2+检测的LOD分别为3.30和4.43μg·L-1,检测范围为10~500μg·L-1。Deshmukh[18,19]以H2SO4掺杂PA NI,并采用循环伏安法将PA NI沉积到ITO玻璃上制备PANI/ITO电极。PA NI/I T O电极可以用于检测Cu2+离子,而且具有电致变色的特点。在Cu2+的检测过程中,电位为-0.5~1.4V的区间内,PA NI/I T O电极材料在氧化过程中由浅黄色变为绿色又逐渐变为蓝色,在还原过程中由蓝色逐渐变为黄色。同时,他们还用H2SO4掺杂的PA NI包覆单壁碳纳米管(SWNTs)。以SWNTs为硬模板,赋予了PA NI管状形貌。在PA NI循环检测过程中,重复的嵌入脱出HMIs会导致PA NI的体积变大,机械稳定性降低。而SWNTs机械强度高、导电性好、比表面积大,但是对金属离子HMIs的敏感性和选择性较低。以SWNTs作为导电骨架,采用螯合剂E D TA对PA NI改性,发挥E D TA对HMIs的螯合作用,使制备的E DTA-PA NI/SWNTs用于D P V检测,且不受Pb2+、C d2+、Ni2+、C o2+等离子的干扰。EDTA-PA NI/SWNTs对Cu2+的LOD为1.4μM,灵敏度为189 mA/μM。Suvina[20]在还原氧化石墨烯(rGO)水溶液中,原位聚合了吡咯单体,得到了PPy/rGO水凝胶复合材料。他们将HCl加入到检测溶液中,作为PP y的掺杂剂,增加PP y的导电性。由于PP y本身具有大量的N原子,可以与HMIs产生配位作用。因此这种PPy/rGO复合材料对HMIs有较好的检测效果。PP y/rGO水凝胶复合材料对Pb2+的L O D为0.3 n M,检测范围为0.5~5000 n M。
也有一些研究者将研究的重点放在如何进一步增加C P的活性位点,使其对痕量HMIs有更好的检测效果。他们通过筛选具有特定基团的聚合物单体或搀杂剂,使C P对HMIs有更灵敏的响应。Dai[21]以植酸(PA)掺杂PP y中,再通过静电吸引复合氧化石墨烯(GO)制备HMIs传感器。其中带负电荷官能团的PA对HMIs能够产生静电吸引,同时发挥PP y与GO的导电性能,将HMIs吸附在复合材料表面,并通过DPV进行检测。测得Pb2+和Cd2+的L O D分别为0.41和2.13μg·L-1,检测范围为5~150μg·L-1。
1.2 非导电聚合物改性电极
非导电聚合物含有大量的与导电聚合物不同的活性位点与基团,如羟基、酮基等,也可用于HMIs的吸附与捕集[22]。但是非导电聚合物的电导率较导电聚合物低,通常非导电聚合物检测HMIs的应用为光化学传感器。通过非导电聚合物的孤对电子吸附HMIs,降低孤对电子的跃迁效应,从而改变其紫外-可见光区的吸收峰强度,获得被检测HMIs的种类与浓度等信息[23]。如果将非导电聚合物应用于电化学传感器则需要将非导电聚合物涂覆在导体基材上或对非导电聚合物进行表面改性来增强其导电性能。同时利用非导电聚合物的基团效应,实现其对HMIs的电化学检测。杨婷[24]将超支化的聚苯硫醚溶解在四氢呋喃中并滴于铂片电极表面,形成超支化聚苯硫醚单层膜电极。将该电极作为工作电极在不同种类和浓度的HMIs溶液中测试其电容,利用电容数值的变化来反映离子浓度的变化。该电极对Cu2+、Z n2+和Pb2+均有响应,且离子浓度变化可用电容的定量变化标定,因此可用于HMIs的定量检测。许春萱[25]将G O分散在DM F中滴在GCE表面制备了GO/GCE电极。然后将GO/GCE电极在苏木精溶液中进行循环伏安扫描,通过电沉积法得到聚苏木精/氧化石墨烯修饰电极(HMGO/GCE)。利用聚苏木精大量的-OH,提高了C d2+和Pb2+的电化学响应。其对C d2+和Pb2+的检测范围为0.01~1μM,检测极限分别为1和8 n M。杨澜[26]将G O溶液滴涂于G C E表面形成GO/GCE电极,然后采用吸附自聚法,将GO/GCE电极插入多巴胺溶液,使多巴胺在GO/GCE电极表面自聚合,干燥成膜后得到P D A-GO/GCE改性电极。利用多巴胺的亲水性与高粘附性,增强了P D A-GO/GCE改性电极与HMIs的结合能力。 DA-GO/GCE改性电极测得Cu2+的检测极限为0.02μg·L-1,检测范围为0.1~30μg·L-1。Hassan[27]以1,2-二氨基蒽醌单体为原料合成聚1,2-二氨基蒽醌(P1,2-D AAQ)。P1,2-D AAQ具有大量的-N H2和酮基,因此P1,2-D AAQ对HMIs具有强力的螯合作用,如图1。所以P1,2-D AAQ对H g2+、Cu2+、Pb2+和C d2+均有较好的检测效果。其LOD分别为0.26、1.94、0.58和0.3μg·L-1,检测范围为0~120μg·L-1。

图1 P1,2-DAAQ与HMIs的相互作用机理[27]Fig.1 The interaction mechanism of P1,2-DAAQ and HMIs[27]
近几年,石墨相氮化碳(C3N4)作为一种半导体聚合物材料被广泛关注,由于C3N4含有大量的N活性位点及残存的-N H2,非常适用于HMIs的检测[28]。C3N4通常采用热聚合法将尿素、双氰胺等富氮前驱体经高温煅烧而制得。但是C3N4直接热聚合通常得到块体材料,这导致C3N4的活性位点无法完全暴露而使C3N4的电化学活性降低。此外,C3N4的导电性能较差,活性位点与HMIs吸附后无法快速的转移电子。这些都是制约C3N4成为改性电极材料的关键问题。一些研究者针对C3N4体积效应的缺点,将C3N4剥离成薄片状,这在一定程度上缓解了C3N4的导电性能差的问题[29]。为了增加C3N4的活性位点,他们采用B i[30]、PA NI[31]、E D TA[32]等活性材料修饰C3N4,或是直接将C3N4官能化[33]等手段,增强C3N4对HMIs的吸附能力。为了进一步增强C3N4的利用率,杂原子掺杂和纳米结构设计成为C3N4的主要研究方向。
Wang[34]以三聚氰胺和三聚硫氰酸为原料,采用诱导蒸发辅助超分子自组装法制备了三聚氰胺-三聚硫氰酸前驱体。通过调控热聚合反应的条件,得到了S掺杂多孔管束状的C3N4(STB)。三聚硫氰酸在热聚合过程中会保留一定的S原子和-S H基团,有效地增加了STB的活性位点。此外,为了改善STB导电性差的问题,将质子化的石墨烯纳米片(Gs)与STB静电组装得到STB/Gs复合材料,如图2。他们发现STB呈现介孔-微孔的分级孔结构。这种分级孔结构中的介孔有利于电解液在STB/Gs之间的快速渗透,微孔有利于HMIs的捕集。并发现了沉积与溶出过程中三嗪单元内电子的转移规律。STB表面的G s,在STB捕集HMIs后能够快速转移STB的电子,实现HMIs在材料表面的快速氧化还原,因此具有优异的HMIs检测性能。
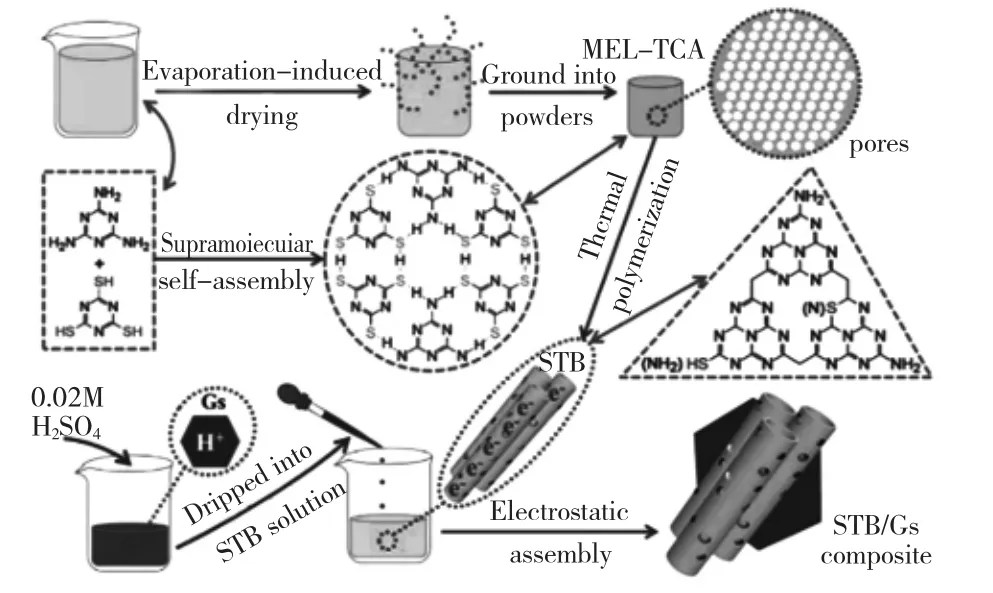
图2 STB/Gs复合材料的制备流程[34]Fig.2 The preparation process of STB/Gs composite[34]
Xiao等[35]以三聚氰胺为原料,在500℃下热聚合制备了C3N4。然后他们将C3N4研磨成粉末后放入N2保护的管式炉中,520℃又处理了3h。从而获得了具有N缺陷的C3N4(N-deficien t-C3N4)。为了进一步增加活性位点,他们采用经典的柠檬酸还原法,将N-deficien t-C3N4溶于HAuCl4中,并用柠檬酸钠和NaBH4的混合溶液还原H A uC l4,得到表面具有约5 nm Au颗粒修饰的N-deficient-C3N4,记为Au/N-deficien t-C3N4。与通过掺杂增加活性位点不同的是,他们通过制造缺陷增加C3N4的活性位点。C3N4表面分散的纳米A u粒子,一方面起到活性位点的作用,另一方面增加了C3N4的电子转移路径。通过A u与N-deficien t-C3N4协同机制,实现了Pb2+的电化学检测。他们还针对Au与N-deficient-C3N4协同机制的机理进行了深入的研究,如图3[35]。
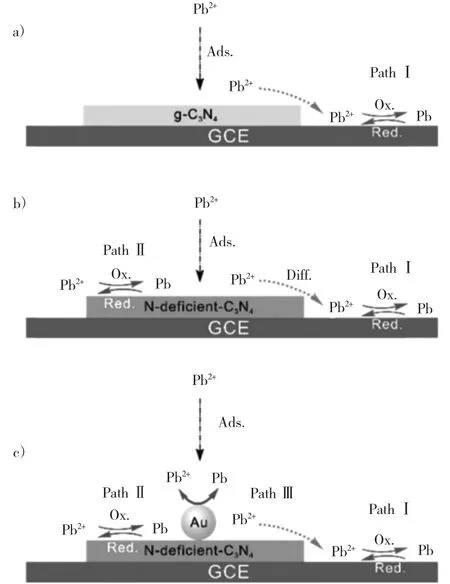
图3 Pb2+在Au/N-deficient-C3N4表面的协同催化机制Fig.3 Synergistic catalysis mechanism of Pb(II)on the surface of Au/N-deficient-C3N4
2 生物材料改性电极
氨基酸、肽、核酸、蛋白质、酶等生物材料由于含有丰富的氧、氮、硫等原子,以及含氧、含氮、含硫的官能团,它们可以通过金属-配体之间的配位和螯合作用识别HMIs[36,37]。根据软硬酸碱理论,N、S、P等软碱对于C d2+、Pb2+、Cu2+、H g2+等软酸具有较强的亲和力,因此可以用于HMIs检测。
Guo[38]以rGO、壳聚糖(CS)和聚-L-赖氨酸(PLL)通过循环伏安法电聚合制备rGO-CS/PLL改性电极。rGO起到导电剂的作用,能够增强rGO-C S/PLL的电子传输速率;CS不但能够起到粘接剂的作用,而且大量的-N H2,能够与HMIs发生配位作用;PLL分散在rGO表面上,使其具有较大的活性面积、较强的吸附能力和独特的络合能力,能够为HMIs靶向吸附提供一个优异的平台,因此rGO-CS/PLL改性电极对HMIs具有优异的检测性能。经过D PA S V测试,rGO-CS/PLL对Cd2+、Pb2+、Cu2+的L O D分别为0.01、0.02和0.02μg·L-1,检测范围为0.05~10μg·L-1。此外他们还对rGO-C S/PLL复合材料对C d2+、Pb2+、Cu2+三种离子的最大吸附量进行了考察,分别为47.14、18.96和16.33 m g·g-1。静态吸附试验证明G O-C S/PLL复合材料不仅可以用于HMIs检测,还可以用作HMIs去除。
Zhang[39,40]课题组采用冻干法制备三维rGO,然后用苯胺单体原位聚合在3D-rGO表面制备3D-rGO@PA NI。他们将3D-rGO@PA NI滴在Au电极表面后,将A u电极浸没在含DNA的磷酸缓冲溶液中12 h,将DNA锚定在3D-rGO@PA NI复合材料的PA NI表面,最终得到3D-rGO@PA NI-DNA分子探针。通过DNA的双螺旋结构及胸腺嘧啶(T)的碱基对可以与H g2+实现特异性结合,形成T-H g2+-T金属介导碱基对,从而实现对H g2+的高灵敏性和高选择性检测,如图4[35]。虽然DNA对于H g2+离子具有高灵敏性和高选择性,但是同时DNA也降低了阻滞层上的电子传递,导致电化学活性下降。与3D-rGO@PA NI相比,3D-rGO@PA NI-DNA分子探针的电子转移电阻从0.65增加到0.75 kΩ。吸附10nMHg2+后,DNA中富含的游离T形成T-Hg2+-T双链结构,导致构象发生变化,使电子传递电阻增加到1.62 kΩ。其对H g2+的LOD为0.035 n M,检测范围为0.01~100 n M,且对H g2+检测具有高度的再现性,检测浓度的标准偏差值为4.5%。同时,他们以3D-rGO作为导电基体材料,利用3D-rGO比表面积大、电子传递快,传质速度快等特点,采用CS包覆rGO形成CS@3D-rGO复合材料。然后将DNA锚定在C S@3D-rGO表面形成C S@3D-rGO@DNA分子探针。核酸杂化的电化学DNA传感器,具有特异性、选择性、灵敏性、可重复性等优点。CS的加入将配位作用引入分子探针,进一步地提高其对H g2+的选择性和灵敏性。C S@3D-rGO@DNA分子探针对H g2+的L O D降低至0.016 n M,检测范围为0.1~10 n M。

图4 CS@3D-rGO@DNA电化学生物传感器检测Hg2+的原理图Fig.4 Schematic diagram of Hg2+detection using electrochemical biosensor based on CS@3D-rGO@DNA
Seenivasan[41]以羰基二咪唑为交联剂,通过酰胺键和氨基甲酸酯键将半胱氨酸(CySH)与GO交联形成CySH改性氧化石墨烯(sGO)。对然后采用循环伏安法将s GO和P y单体沉积到丝网印刷电极(SPE)上,得到sGO/PPy-SPE改性电极。CySH作为一种天然生物材料具有-COOH和-OH基团,能够与Pb2+发生配位作用形成金属-配体配位键结构,而GO/PPy具有比表面积大、传电、传质速度快、电催化性能强、溶液电阻低、信噪比高等特点,因此可以作为CySH的载体材料。将CySH对Pb2+的强亲和力、PP y的层状孔结构及GO导电能力复合,得到的到s G O/PP y复合材料对Pb2+具有高的选择性和灵敏性。经过E I S测试,GO-SPE、sGO-SPE和s GO/PP y-SPE的电子传递电阻分别为12.17、5.2和0.763 kΩ。G O-SPE的电子传递电阻较大归因于G O表面的-COOH、-OH和C-O-C等官能团阻碍了电子传递。加入PPy使sGO/PPy-SPE的电子传递电阻降到了最低。以DPASV法检测Pb2+,检测范围为1.4~14000 pp b,LOD可达0.07 ppb。
3 展望
有机聚合物与生物材料由于具有丰富的富电子原子和富电子基团可与重金属离子发生配位和螯合作用,因此十分适合于制备重金属离子检测修饰电极。但是有机聚合物与生物材料也存在着一定的弊端,即导电性能较差、材料的规整度和可设计性较差。因此如何在不破坏生物材料功能的情况下对生物材料复合改性提高其导电性能是生物材料用于重金属离子检测的关键。而有机聚合物材料由于其容易团聚,也会影响其重金属离子的检测性能,如何分散聚合物材料并设计聚合物材料的结构也将是有机聚合物材料用于重金属离子电化学检测工作的研究重点。有机与生物材料克服这些弊端以后,也将获得更加优异的重金属离子电化学检测性能。
