半纤维素及其衍生物转化为γ-戊内酯及其动力学研究进展
2022-08-01庄雨婷王建华向智艳赵娟徐琼刘贤响尹笃林
庄雨婷,王建华,向智艳,赵娟,徐琼,刘贤响,尹笃林
(1 湖南师范大学化学化工学院,湖南 长沙 410081;2 湖南师范大学石化新材料与资源精细利用国家地方联合工程实验室,湖南 长沙 410081)
在碳达峰及碳中和目标愿景下,能源发展迎来了新的阶段,意味着以化石能源为主的发展时代逐渐向非化石能源时代过渡。为了改善日益严重的环境污染和全球能源危机问题,研究人员一直在探索新的绿色和可再生资源利用策略。在众多可再生资源中,生物质是唯一可以替代化石资源转换合成化学品及液体燃料的可再生资源。木质纤维素作为地球上最丰富的生物质资源,取之不尽用之不竭,可转化为糠醛(FAL)、5-羟甲基糠醛(HMF)、糠醇(FOL)、乙酰丙酸(LA)、-戊内酯(GVL)、甘油、山梨醇等平台分子(见图1),进而转化为高附加值的化学品和燃料。
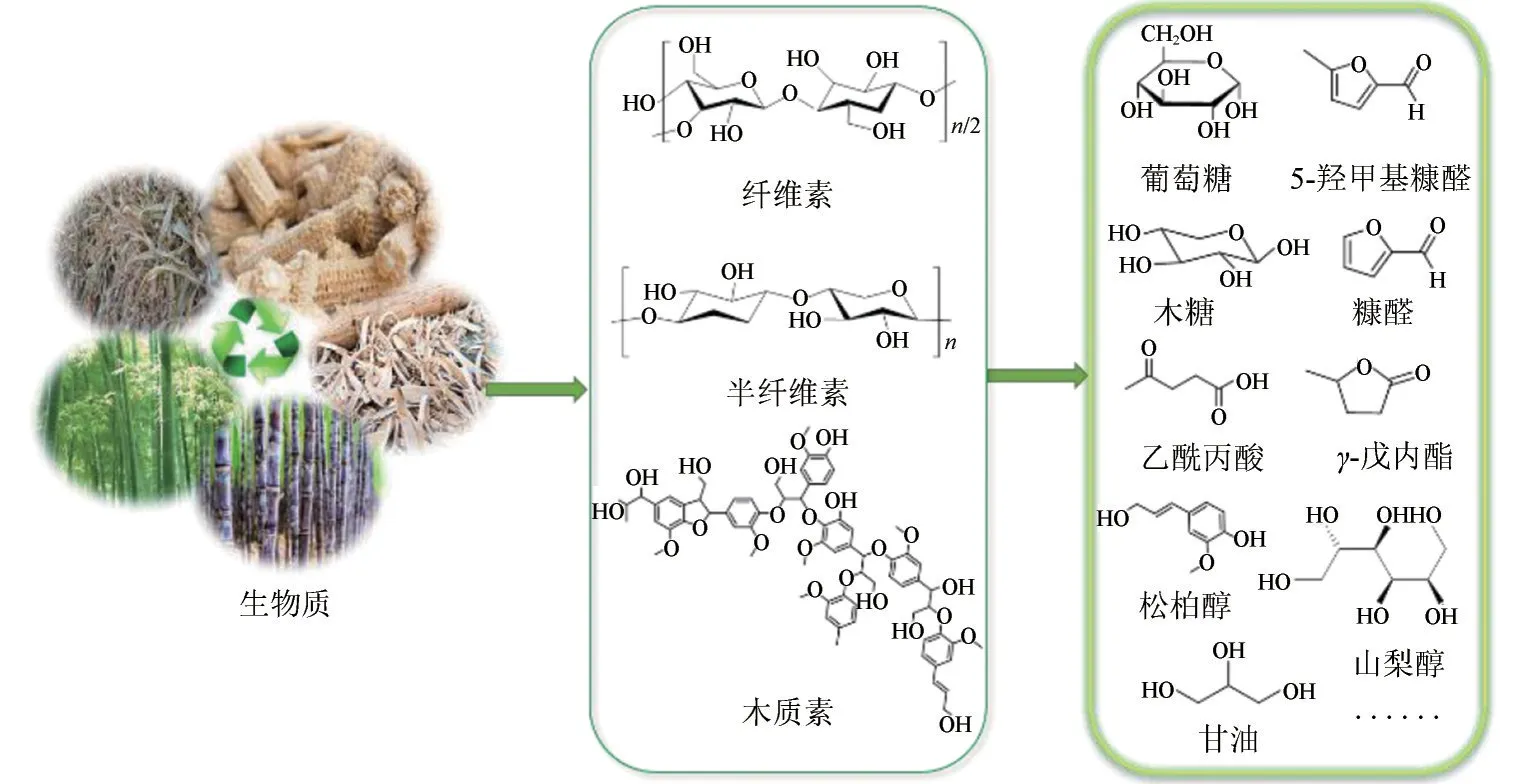
图1 木质纤维素类生物质的组成及其高价值衍生物
GVL 是一种C环酯,不仅是环境友好的天然产物,也是生物质衍生物中最具价值的化合物之一。GVL 具有高沸点(207~208℃)、高闪点(96℃)、低挥发和高热值,同时还具有优良的稳定性、低温流动性、易降解性、低毒环保性和便于存储运输的特点,种种优势使其应用广泛。GVL能够溶解纤维素从而提高纤维素的转化效率,是极佳的生物质转化反应的绿色溶剂。例如以GVL为溶剂,可以将玉米芯和毛竹等生物质原料高效转化为FAL。GVL 的重要作用还在于它作为一个重要的平台分子可以参与多种反应,转化为燃料添加剂、聚合物前体和其他高附加值化学品(见图2)。例如它可与乙酰丙酸酯(LEV)在汽油-乙醇共混物中形成可持续的液体运输燃料,取代汽油-乙醇混合物中的乙醇。
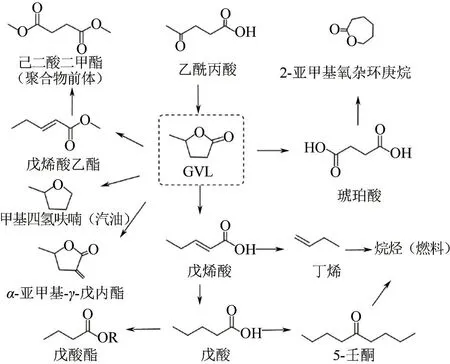
图2 GVL转化为燃料和高附加值化学品的途径[19-20]
由于GVL 在制备能源化合物、高分子材料等领域有着广泛应用,因此以可再生生物质原料制备GVL 的研究也成为热点。以LA 及其酯类为原料转化为GVL 取得了较好的成绩,已有不少报道综述了这方面的成果。直接催化转化生物质原料、纤维素、半纤维素为GVL 的研究有较大挑战,但从原料成本和制备工艺的经济性来看,有突出优势。不少学者从这些初始原料出发,采用一步或多步反应制备GVL,近年来也取得较大进展。与纤维素相比,具有五碳单体的半纤维素制备GVL 具有更好的原子经济性。从半纤维素制备平台化合物FAL已实现工业化,FAL转化为GVL的研究也层出不穷。因此,本文重点综述半纤维素及其衍生物转化为GVL反应中的高效催化剂体系。由于生物质制备GVL 的串联反应中包含关键的加氢反应步骤,不同氢源的反应体系适宜的催化剂和反应条件不一样,故而总结了不同氢源反应体系的特点和溶剂对反应的影响。此外,对GVL 合成反应的动力学研究有助于了解反应条件对各串联反应速率的影响、揭示反应历程、确定速率控制步骤和研究催化反应机理,从而为催化剂设计提供可行建议,为GVL 工业化生产奠定基础。鉴于动力学研究的重要意义,本文也对木糖转化为FAL以及FAL转化为GVL的反应动力学研究进行了综述。
1 生物质转化为GVL的反应路径
生物质原料制备GVL 的研究主要有半纤维素路径和纤维素路径。生物质中的半纤维素和纤维素在酸性条件下解聚为单糖,并进一步衍生为制备GVL的平台化合物FAL和HMF。
从半纤维素出发制备GVL,反应路线如图3所示,主要包括以下串联反应:半纤维素在酸催化下形成了以木糖为主的五碳糖,木糖脱水生成FAL;FAL 经加氢还原为FOL,FOL 在酸催化下醚化形成糠基醚(FE),进而生成LEV,或经-当归内酯(-AL)和-当归内酯(-AL)中间体开环生成LA,再酯化为LEV;LEV 经加氢还原生成中间体4-羟基戊酸酯(4-HPE),4-HPE不稳定快速环化生成GVL。
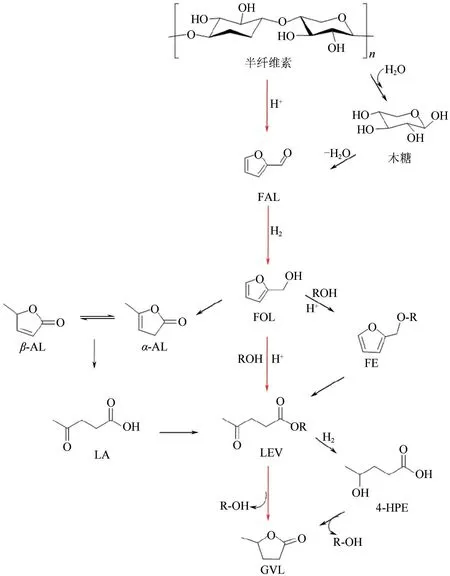
图3 半纤维素合成GVL的路线图
纤维素路线主要包括以下串联反应:纤维素在酸性条件下解聚得到葡萄糖,葡萄糖异构为果糖,果糖脱水得到HMF 中间体,HMF 在高温酸性水溶液中不稳定重排为LA 和当量的副产物甲酸,LA 经过加氢还原和乳糖化生成GVL。由于纤维素路线中生成了当量的甲酸导致碳流失,因此半纤维素路线显得更符合原子经济性。另外,半纤维素具有分支结构和较短的分子链,比纤维素更具反应性,更易从木质纤维素生物质中分离,因此半纤维素水解所需的条件比纤维素温和。在这一点上,半纤维素路线也具有更好的工业应用前景,这也是近年来半纤维素及其衍生物转化制备GVL 受到广泛关注的原因。
2 合成GVL的高效催化剂
新型高效、高选择性催化剂的设计和开发是制备GVL 的关键,也是最具有挑战性的工作。近年来,研究者在半纤维素及其衍生物一步或多步串联合成GVL的研究中做了大量工作。多步反应路径长,存在的副反应多,中间产物的分离操作成本高,延缓了GVL 生产工业化进程。一锅法制备GVL 免去了中间产物的分离,若能开发出高效绿色的催化体系以获得高产率GVL,则可进一步降低GVL生产成本,这无疑是其工业化的首选。
2.1 糠醛和糠醇合成GVL的高效催化剂
FAL 是木糖的脱水产物,经加氢还原可获得FOL。FAL 和FOL 均是重要的生物基平台化合物,是连接生物质和GVL 之间的桥梁化合物。从FAL和FOL 制备GVL 将成为生物燃料生产的一种新的替代途径。FAL 和FOL 一锅制备GVL 的研究有很多,已开发的催化剂有分子筛催化剂、离子液体催化剂、金属有机框架(MOFs)催化剂、二氧化硅基催化剂等,尤其是以分子筛催化剂和醇为氢源的催化转移加氢(CTH)体系更是发展迅速。表1列出了FAL和FOL一锅转化GVL的研究情况。
2.1.1 分子筛催化剂
分子筛具有独特的规整晶体结构和孔道体系,其表面具有较强的酸中心,是一种优良的催化剂和载体。近年来分子筛催化合成GVL 的研究获得了广泛的关注,典型的催化剂如ZSM-5、沸石、钛硅分子筛、HY、USY、SAPO-34 等报道较多。在这些报道中,分子筛或作为混合催化体系的酸中心,或经过负载改变酸性酸强度促进GVL的合成。
分子筛作为酸中心与金属催化剂构成混合催化体系。利用分子筛自身的Brønsted 酸进行开环反应,金属催化剂完成FAL 和LEV 的还原反应。Wang 等以ZSM-5 催化剂结合多相壳聚糖负载型金属配合物Chitosan-Ru/PPh催化剂,乙醇为溶剂,甲酸为氢源,在160℃反应30h,GVL 产率达到79%(表1,条目1)。Chitosan-Ru/PPh催化剂将甲酸分解成H和CO。Chitosan-Ru 中的Ru和N均可用作可能的活性催化位点。在PPh存在下,Chitosan-Ru 催化FAL 转化为FOL 时,带负电的N原子作为碱,把甲酸吸附到催化剂表面,捕获甲酸中的H,HCOO与Ru配位形成Ru-H,同时释放CO。PPh可作为电子给体添加剂,与Ru有微弱的相互作用,可以促进甲酸的分解,因此有利于氢化过程。当不存在PPh时,GVL产率只有30%。经5次循环实验后GVL 的产率急剧下降,这归因于Ru的流失。Zhu 等报道了ZSM-5 分子筛和Au/ZrO催化剂在2-丙醇溶剂中催化FAL一锅转化为GVL。该工艺在120℃下反应30h实现了FAL的完全转化,获得较高的GVL产率(表1,条目2)。其突出的性能主要归因于活性金属和ZSM-5 酸中心之间的有效协同作用以及有效地受阻路易斯对的形成。
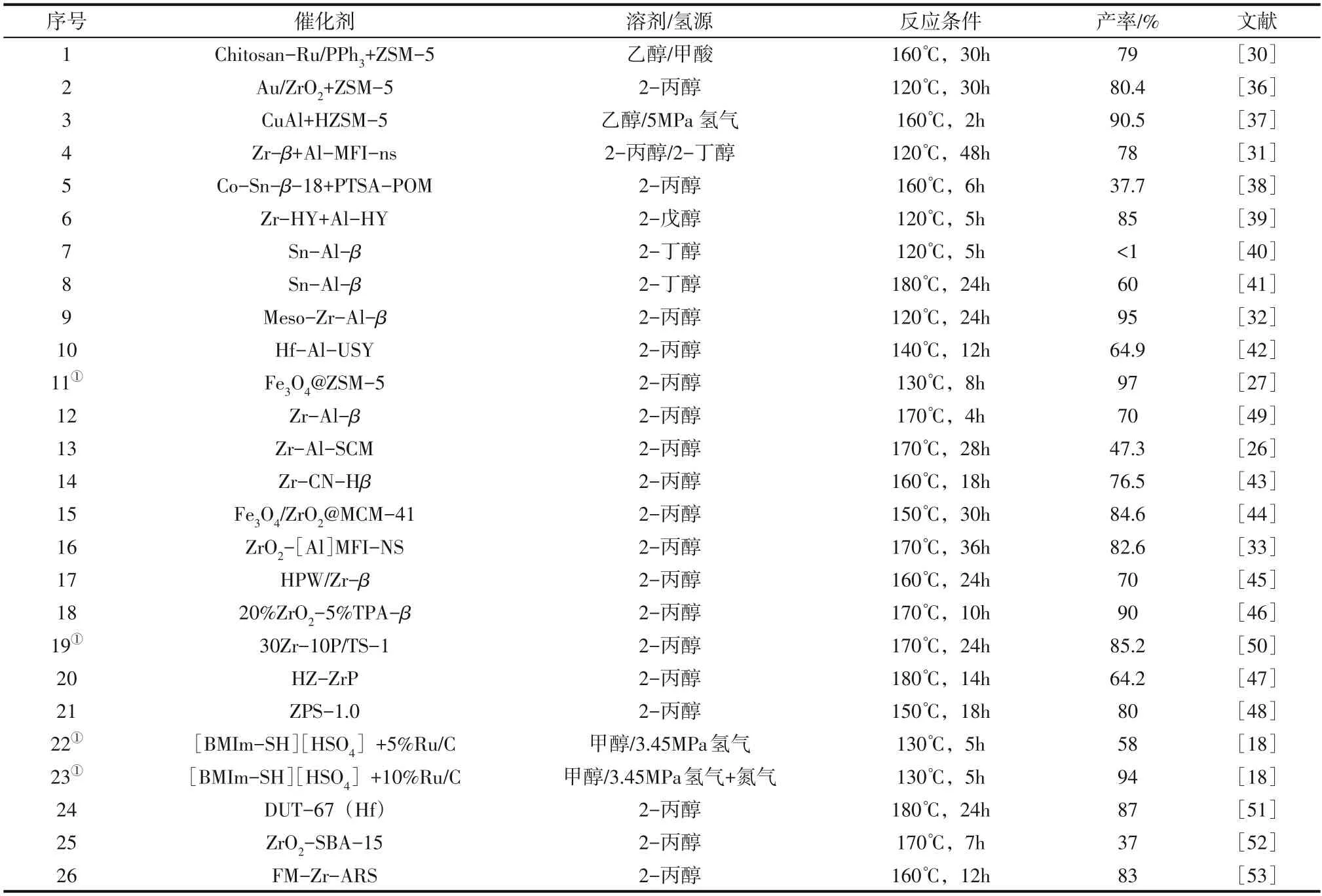
表1 FAL/FOL一锅合成GVL的研究情况
贵金属的高成本和稀缺性限制了其大规模应用。因此,非贵金属催化剂因其在加氢反应中的高活性而受到广泛关注。最近,胡勋课题组以HZSM-5为酸催化剂,非贵金属CuAl为加氢催化剂,在乙醇溶液中催化FAL 一锅合成GVL。在5MPa 氢气压力、160℃和2h的反应条件下实现了FAL的完全转化,GVL 产率高达90.5%(表1,条目3)。催化剂的Lewis 和Brønsted 酸位点的协同作用以及相对丰度决定了FAL 的转化效率和GVL 的选择性。但该催化体系中催化剂用量远大于底物且在反应过程中易积炭导致稳定性不好。
分子筛负载金属以引入适量Lewis 酸位点,通过转移加氢反应促进FAL和LEV的转化。分子筛是具有三维十二元环孔结构的中孔沸石,其孔道介于ZSM-5 型分子筛与Y 型分子筛之间,具有较好的热稳性。2013年,Bui 等通过水热法将Zr 掺入到沸石中,首次以Zr-和Al-MFI-ns 为Lewis 和Brønsted 酸催化剂,2-丁醇为氢供体,在120℃反应24h,GVL 产率达到78%(表1,条目4)。这种沸石组合与用于半纤维素转化为FAL 的工艺兼容,因此该催化剂体系提供了将五碳糖转化为GVL 的简化策略。Lu 等通过简单的后合成法制备了双金属掺杂的沸石Co-Sn--18,并将其与PTSAPOM 催化剂用于催化FAL 制备乙酰丙酸异丙酯(IPL)和GVL,160℃下反应16h,IPL 和GVL 产率分别为48.3%和37.7%(表1,条目5)。Zhang 等采用两步后合成方法制备了Zr-HY,先对沸石脱铝,后用湿法浸渍将Zr填充到骨架以产生Lewis酸位。以2-戊醇为氢源,在120℃、5h的反应条件下,Zr-HY 与Al-HY 的组合催化FAL 一锅转化为GVL的产率高达85%(表1,条目6)。Zr-HY比Zr-具有更大的孔径,因此,在Meerwein-Ponndorf-Verley(MPV)反应中具有更高的活性。
除了混合催化剂系统外,为了避免多种催化剂难以分离的问题,研究人员开始探索具有Lewis 和Brønsted酸位点的双功能催化剂。2015年,Antunes等率先报道了一种采用脱铝和固态离子交换法制备、兼具Lewis酸和Brønsted酸的双功能催化剂Sn-Al-分子筛,并将其用于FAL 到GVL 的转化。但GVL产率很低,主产物为糠基异丁醚(表1,条目7)。2016 年,Winoto 等通过调整脱铝程度和Si/Sn 比例优化了Sn-Al-催化剂,GVL 产率提高到60%(表1,条目8)。这可归因于该催化剂具有合适的Brønsted 酸位点,且与Lewis 酸位点的位置非常接近,从而具有协同作用,提高级联反应的催化效率。在前人的不断探索下,具有Lewis 和Brønsted酸的双功能催化剂在FAL 向GVL 的转化方面显示出良好的前景。沸石固有的微孔性会阻碍大分子与活性位点的相互作用以及大分子的扩散,覆盖活性位点并堵塞通道,导致催化活性低和快速失活,因此中孔结构的沸石应运而生。2017年,Song等在Zr-Al-沸石上引入介孔后,GVL 产率达到95%(表1,条目9)。该项研究通过碱处理控制脱硅和脱铝的程度改变沸石的孔道结构,成功制备了分级的Meso-Zr-Al-沸石。引入的中孔结构进一步增强了活性位点的可及性并加快反应物和产物转移和扩散。Tang等通过后合成工艺,精确控制母体H-USY 的脱铝和骨架Hf 位点的引入,成功制备了具有平衡Brønsted和Lewis酸位点的分级双功能Hf-Al-USY 沸石。Al 位的Brønsted 酸位点催化的开环反应,Hf位的Lewis酸位点催化的MPV反应,两者之间的协同效应以及传质的改善(通过沸石脱铝诱导的层次结构),Hf-Al-USY 催化剂在FAL 一锅法制备GVL中表现出非常高的性能。在回收实验中,Hf-Al-USY 沸石经热煅烧处理后显示出良好的回收性能(表1,条目10)。
Zhang 等采用浸渍法制备了Zr-CN-H催化剂,以2-丙醇为氢源,在160℃、18h 反应条件下实现了FAL的完全转化,GVL产率达76.5%(表1,条目14)。该催化剂制备简单,成本低且催化效果优异,提升了产业应用潜力。然而,Zr-CN-H催化剂稳定性差。这归因于多次循环后Lewis 酸和Brønsted酸催化位点的逐渐流失。Gao等通过浸渍法制备了磁性多功能催化剂FeO/ZrO@MCM-41,在150℃、30h 反应条件下,GVL 产率高达84.6%(表1,条目15),该催化剂可重复5 次。类似地,Kim 等制备的ZrO-[Al]MFI-NS 具有优异催化活性和稳定性(表1,条目16)。这归因于其具有非常接近的Brønsted 和Lewis 酸位点及比Zr-CN-H孔道更大的中孔结构。
在分子筛上引入适量Brønsted酸位点以增强酸强度,可加快FOL的开环速率。2019年,Winoto等通过浸渍法将杂多酸负载到Zr-沸石上,开发了一种新型的双功能催化剂HPW/Zr-。该催化剂催化FAL 高效地一锅转化为GVL,产率达70%(表1,条目17)。Rao等制备了一系列沸石负载金属氧化物(ZrO、AlO、SnO、TiO和NbO)和磷钨酸(TPA),并对FAL 一锅选择性转化为GVL 的催化体系进行评价。结果表明,20%ZrO-5%TPA-催化剂的催化活性最高。在170℃、10h条件下,实现了FAL 的完全转化,GVL 产率高达90%(表1,条目18),高Lewis 酸密度和碱基位置是催化剂具有优异催化活性的原因。
磷酸锆作为一种环境友好材料,具有可调节的Lewis 酸和Brønsted 位点。Ye 等通过沉淀法将磷酸锆负载到HZSM-5 分子筛上,制备了Brønsted 和Lewis 酸比可调的HZ-ZrP 催化剂。在180℃、14h下,GVL产率为64.2%(表1,条目20)。该催化剂经过4次循环后活性明显降低,失活主要原因为炭沉积覆盖了活性位点,堵塞孔道,经焙烧处理可恢复到第一次活性。Li等采用沉淀法制备SAPO-34负载磷酸锆催化剂(ZPS-1.0),通过调节Zr/P比得到适宜的Lewis 和Brønsted 酸比例,在150℃、18h下2-丙醇介质中一锅转化FAL 为GVL,GVL 产率高达80%(表1,条目21)。该催化剂具有较高的稳定性,循环6 次无明显活性降低。相比HZ-ZrP催化剂,ZPS-1.0 具有更大的比表面积和孔道,有利于FAL 的吸附和扩散,从而具有更高的活性和稳定性。上述报道也说明载体的选择对催化剂的活性和稳定性有重要影响。
2.1.2 离子液体催化剂
离子液体以其溶解能力强、热稳定性和可设计性好等优点,被广泛用作溶剂和催化剂。在酸功能化的离子液体催化FOL合成LEV取得较大进展的基础上,有研究开始报道将酸结合金属催化剂串联转化为GVL。2013 年,Hengne 等首次将酸性离子液体和金属催化剂相结合的方法用于FOL 一锅合成GVL。以[BMIm-SH][HSO]和5%Ru/C 为催化剂,氢气为氢源,在130℃条件下反应5h,实现了FOL的完全转化,GVL选择性达58%。在加氢条件下,呋喃环加氢制四氢糠醇(THFA)是一个竞争反应,不利于GVL 的形成。因此,第一阶段醇解在N氛围下进行,然后转换为H氛围以避免THFA 的形成。随着Ru 负载量增加到10%,GVL的选择性提高到94%(表1,条目22、23),这表明金属活性位点的有效性在LEV 醇解和加氢串联反应中更为显著。该催化剂可有效循环使用5 次,但离子液体存在回收困难和黏性大的问题,增加了工艺成本。
2.1.3 MOFs催化剂
MOFs 是由金属离子或金属簇节点和有机配体通过配位键连接而成的新型多孔材料,具有高比表面积、孔隙率和结构可控的特性,因此在催化领域有广泛应用。Li 等首次报道了双功能金属有机骨架Hf 基DUT-67 催化剂对FAL 一锅高效转化为GVL(表1,条目24)。通过水热法合成DUT-67(Hf)再硫酸化以引入Brønsted 酸。在2-丙醇溶剂下180℃反应24h,GVL 产率高达87%。但催化剂的制备周期长且存在硫酸根在反应过程中容易脱落的问题,其酸度在反应前后由1.578mmol/L 降至0.732mmol/L。
2.1.4 其他催化剂
多孔二氧化硅和杂化材料等在催化领域也有广泛应用。Iglesias 等通过调节SBA-15 表面的ZrO厚度制备了ZrO-SBA-15 催化剂,在170℃下反应7h,GVL 产率为37%(表1,条目25)。由于催化剂的酸强度不足,仍有许多中间产物FE和IPL未转化。另外,利用天然有机配体制备的功能化催化杂化材料,与金属离子配位后,可提供丰富的功能位点,形成稳定的多孔骨架。Peng等采用水热法合成了多功能含锆催化剂FM-Zr-ARS。在制备过程中引入甲酸作为酸调节剂,改善了传统水热法造成的低比表面积和孔隙率的缺点,使底物更有效地接近活性位点。FM-Zr-ARS 中酸碱中心之间的有效协同作用对MPV反应表现出显著的催化活性。茜素红S(ARS)中—SOH 的Brønsted 酸位点在呋喃开环反应中起关键作用。以2-丙醇为氢源,在160℃、12h 条件下实现了FAL 的完全转化,GVL产率高达83%(表1,条目26)。该催化剂可稳定循环6次,这归因于ARS分子结构中的对醌基团和相邻的羟基与Zr进行配位形成六元环,从而产生丰富的酸碱位点,提高了催化剂的活性和热稳定性。
FAL 和FOL 一锅合成GVL 的催化体系主要从分子筛催化剂、2-丙醇为氢源和溶剂方面展开探索。具有Brønsted 酸和Lewis 酸的双功能多相催化剂的开发给FAL 和FOL 转化为GVL 的串联反应提供了有效方法,具有光明前景。设计具有Brønsted酸和Lewis 酸的双功能多相催化剂是当前高效转化为GVL反应的研究热点。
2.2 生物质原料、半纤维素和木糖合成GVL 的高效催化剂
尽管从半纤维素或生物质原料转化为GVL 的研究困难重重,在下游衍生物转化获得了良好转化效果的基础上,生物质原料、半纤维素和木糖一锅转化制备GVL 的工作也开始有报道,已开发的催化剂主要为分子筛催化剂。水解和脱水是生物质原料和半纤维素转化为有价值的化学品和燃料的两个关键步骤:半纤维素在酸催化下转化为五碳糖和六碳糖,得到木糖、阿拉伯糖和葡萄糖等混合物,经过脱水形成呋喃类化合物和乙酰丙酸,再经加氢得到GVL。
2.2.1 分子筛催化剂
木糖一锅合成GVL 的研究集中在改性分子筛催化体系上,在分子筛表面引入Lewis 酸,促进C=O 的转移加氢,表2 列出了近年来木糖一锅转化为GVL 的研究情况。Hernández 等报道了以2-丙醇为氢源、双功能Zr-Al-沸石为催化剂直接从木糖一锅生产GVL 的研究。Zr-Al-沸石Al/Zr 比为0.22,木糖在170℃反应48h 后完全转化,GVL产率为35%(表2,条目1)。随后,该课题组以Z1r(NO)为锆源制备了Zr-Al-,仅10h 得到34%GVL 产率(表2,条目2),极大缩短了反应时间。其主要原因是Zr(NO)比ZrOCl有更好的水溶性,在浸渍过程中锆可以更好地分散到载体上。而Zr位点活性的增强促进了两个MPV 还原反应,进而提高了级联反应速率。虽然GVL产率不高,但却为半纤维素直接催化转化为GVL 提供了拓展性思路。Clara 等对H-USY 进行脱铝后采用湿法浸渍掺入锆,成功制备了锆改性沸石Zr-USY 催化剂,并将其用于木糖一锅合成GVL。该研究确定了木糖在2-丙醇中转化的两种竞争反应:GVL 的形成和木糖的逆羟醛缩合。这两个竞争反应的程度强烈依赖于催化剂的锆负载量。
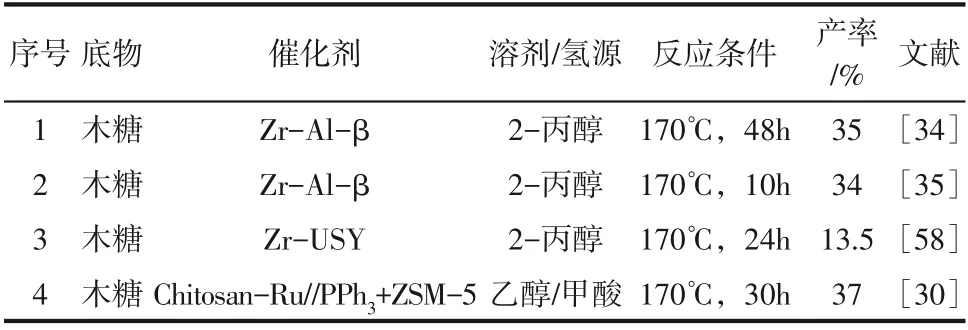
表2 木糖一锅转化为GVL 的研究情况
从生物质原料制备GVL 涉及了多步反应,相应的催化剂需要多功能化。一锅法虽然更加绿色经济,但难以制备出促进每一步反应高选择性转化的理想催化剂。在现有研究中,从生物质原料和半纤维素多步转化合成GVL 级联反应的各关键反应都得到了关注。这里对生物质原料和半纤维素多步转化为GVL的催化体系进行归纳总结。
Wang 等以甲酸为氢源、壳聚糖负载型金属配合物Chitosan-Ru/PPh与ZSM-5 为催化剂,催化半纤维素转化为GVL,其产率为30(表3,条目1)。半纤维素先在ZSM-5 存在下水解得到FAL;然后,壳聚糖中带负电的N原子捕获甲酸中的H,H与Ru-H进攻FAL 的羰基,从而得到FOL。FOL在ZSM-5 催化下开环得到EL,EL 加氢得到产物GVL。Zhu 等以半纤维素为原料,首先在ZSM-5催化剂上水解,FAL 产率高达81.8%。然后在Au/ZrO和ZSM-5 的共同作用下将FAL 转化为GVL(表3,条目2)。结果证明,Au/ZrO催化剂具有极高的催化活性,在温和的条件下实现了半纤维素的完全转化,GVL产率高达61.5%。其优异的性能主要归因于Au 与ZrO的强界面作用,ZSM-5 上大量的中强酸位点以及活性金属与酸位之间的有效协同作用。该催化体系通过简单的两步法将半纤维素转化为GVL。其高效的催化性能避免了副产物的分离操作,降低了整个反应过程的能耗和成本消耗。这为在温和条件下合成GVL 提供了一条简便的途径,且无需使用液体酸和外部H。
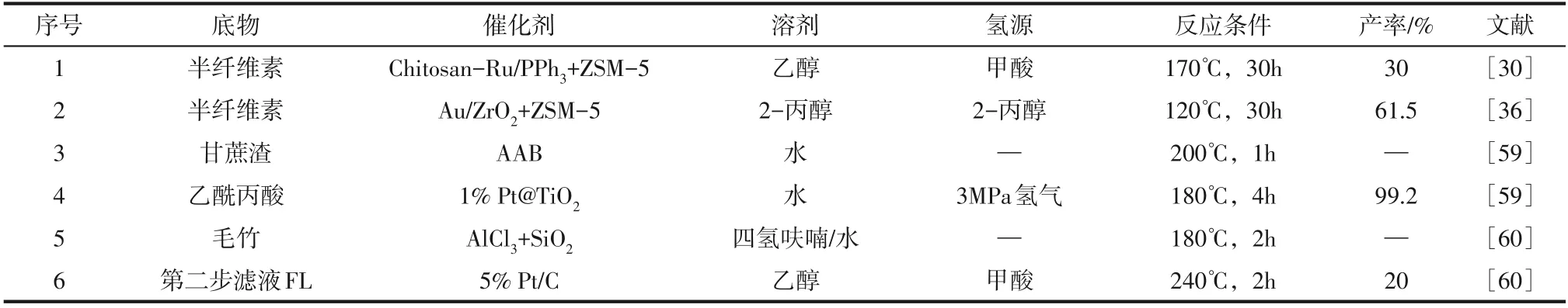
表3 植物原料和半纤维素转化为GVL 的研究情况
2.2.2 其他催化剂
利用金属盐、酸活化膨润土(AAB)等催化剂将生物质原料转化为LA,再加入金属催化剂催化LA为GVL,从而实现生物质原料的转化。Putro等提出将甘蔗渣转化为GVL的绿色策略(表3,条目3、4)。第一步,在AAB 固体酸催化剂作用下促进甘蔗渣中的纤维素和半纤维素水热转化为LA;第二步,以浸渍法制备的1% Pt@TiO为催化剂,AAB 为助催化剂,H为氢源,催化第一步得到的LA 水溶液加氢得到高选择性的GVL。该催化剂可循环5次无明显活性下降,而催化剂中毒主要为活性位点上的焦炭沉积所致。Luo 等以甲酸为内部氢源,采用三步法实现了毛竹多步转化为GVL(表3,条目5、6)。首先,AlCl促进了毛竹中的半纤维素的选择性溶解;然后加入四氢呋喃(THF)和SiO,进一步促进了半纤维素低聚物和单体转化为FAL、LA 和甲酸;最后,在第二步含甲酸的滤液(FL)中加入浸渍法制备的Pt/C 催化剂,半纤维素转化为GVL 的产率为20%。这个过程无需外加氢源且避免了随后的分离步骤。
3 氢源
半纤维素制备GVL 的串联反应中包含关键的加氢反应步骤,直接(氢气)和间接(甲酸和醇类)加氢制备GVL 都有显著的效果,特别是以醇类作为氢源的MPV反应近年来取得了较快的发展。下面对不同氢源体系的优缺点进行归纳。
3.1 分子H2
分子H是常用的氢源,从LA制备GVL使用分子H作为氢源的报道较多,分子H一般需在高温高压的条件下反应,以金属为催化剂作用下才能表现出高效的还原能力,如5%Ru/C、CuAl和1%Pt@TiO[等催化体系。由于使用分子H的反应条件苛刻,且存在安全隐患,在半纤维素及FAL制备GVL的反应中报道不多。
3.2 甲酸
近年来,间接加氢受到学者们的广泛关注,其中,甲酸被证明是有用的外部氢源。在2005 年,甲酸被报道可作为氢源用于醛酮化合物的还原。在生物质合成GVL 的反应中,纤维素水解理论上可得到等摩尔的LA 和甲酸。因此,利用反应生成的甲酸作为内部氢源实现GVL 的合成,有较好的原子经济性,避免外部H的使用,最大程度地降低转化过程的分离能耗,有望成为生物质原料直接转化为GVL 的最便捷的工艺之一。Chitosan-Ru/PPh+ZSM-5催化半纤维素及其衍生物转化为GVL 的反应和Pt/C催化毛竹转化为GVL 的反应,都证明了以甲酸为氢源可以得到良好的催化效果,表明甲酸是一种极具前景的氢源。另一方面,甲酸常用于贵金属催化剂如Ru 和Pt 催化体系,加之甲酸本身具有较强的腐蚀性,对反应设备要求较高,甲酸的使用会给环境带来一定的负担,这些弊端使其在应用上受到很大程度的限制。
3.3 醇类化合物
MPV 反应以醇类化合物为氢供体,对羰基化合物进行转移加氢具有高度选择性。MPV反应由Lewis 酸催化,可以避免贵金属使用。2013 年,Bui等提出将酸驱动与MPV 还原反应结合用于FAL合成GVL。具有高Lewis酸活性的Zr和Sn改性的沸石催化剂常被用于FAL/FOL 级联反应一锅转化为GVL的CTH反应。在没有外部H的情况下,以醇为氢源,通过CTH 将FAL 和LA 分别还原为FOL和GVL;同时,醇在此过程中转化为酮。
4 溶剂的影响
溶剂在生物质及其衍生物的转化中也占据重要地位。生物质转化为FAL 的反应中常以水与有机物作溶剂,在FAL/FOL 转化为GVL 的反应中常以醇作溶剂。溶剂不仅影响底物的分散性和溶解性,还在产物的形成、分布、降解和分离等方面发挥着关键作用,甚至参与到反应过程。
第一,溶剂参与到反应过程中影响产物分布。在CTH 反应中,醇作为氢源,也扮演着溶剂的角色,与普通工业溶剂相比,对人类健康和环境的毒性较低;与分子H体系相比,反应所需压力更低,反应条件更温和,因而受到了更多关注。Lima等开发合成了具有核-壳型结构的磁性FeO@ZSM-5催化剂,在130℃、8h 条件下,FOL 完全转化,以2-丙醇为溶剂时得到产率为97%的CVL,当以2-丁醇和1%水为溶剂时可得到高产率的乙酰丙酸-2-丁酯,当加入20%水为溶剂时得到LA。通过简单地改变溶剂便可实现对GVL、LA 和LEV 这些高价值的平台化学品可调控选择性的催化体系。
第二,溶剂影响FOL 的醇解。FOL 在酸催化剂的作用下发生醇解生成LEV。Hao等报道了在Keggin 型杂多酸及杂多酸离子液体催化FOL 合成LEV 中,随着醇链长度的增加,其给电子效应增强,相应的羟基活性增强。因此,醇的烷基链越长,LEV的产率越高。Amol等研究发现,FOL醇解随着溶剂醇链长度的增加,LEV的选择性反而降低,选择性的降低与相应的中间体FOL 醚的形成有关,取决于所用的醇。此外,空间位阻效应在FOL的醇解过程中也起到很重要的作用,正丙醇的空间位阻比异丙醇小,因而乙酰丙酸丙酯的产率比乙酰丙酸异丙酯高。
第三,溶剂影响产物的降解和产率。在生物质转化为FAL 的反应中,向水相中添加有机溶剂或者使用有机溶剂可提高FAL 的产率,如甲苯/水、GVL/水、GVL和-丁内酯/水催化体系。在纯水中进行反应时,由于其极性较强,木糖和FAL 在酸性水溶液中倾向于聚合生成胡敏素等副产物,且FAL 在高温水溶液中容易降解生成有机酸。随着有机层的引入,胡敏素的形成受到抑制,表明GVL 在酸性条件下能有效溶解胡敏素,抑制木糖和FAL 的聚合并减少副产物的形成,有效促进生物原料合成FAL。Zhu 等报道了在半纤维素一锅合成GVL 研究中,在木糖和半纤维素转化的第一步反应中引入-丁内酯后,木糖在ZSM-5上脱水时,FAL 产率从47.7%显著提高到75.3%。半纤维素在ZSM-5上脱水时,FAL产率从54.6%显著提高到81.8%。表明-丁内酯可以溶解腐殖质,抑制FAL 的降解反应,提高FAL 的产量。Li和Yang等的研究也说明了有机层的引入明显降低了生成腐殖质的速率,有利于FAL 的形成,证实了两相系统的优越性。
5 半纤维素及其衍生物合成GVL 的反应机理和动力学
使用多功能催化剂将半纤维素及其衍生物一锅转化为GVL具有一定挑战性,因为涉及各种反应,难以控制所有反应以实现高转化率和选择性的目标。基于动力学分析,设计出用于该反应体系的改进型多功能催化剂,在可持续的化学过程中至关重要,为寻找高效、环保、经济的GVL 催化合成体系提供思路与参考。
5.1 FAL合成GVL的动力学
根据文献报道,FAL 合成GVL 的反应一般有两条路径,如图4 所示。第一条路径主要以糠醚为中间产物,即FAL—FOL—FE—LEV—GVL(,,,,图4);第二条路径以乙酰丙酸为中间产物,即FAL—FOL—FE—-AL—LA—LEV—GVL(,,,,,,图4)。普遍认为,第一条路径为反应的主要路径。
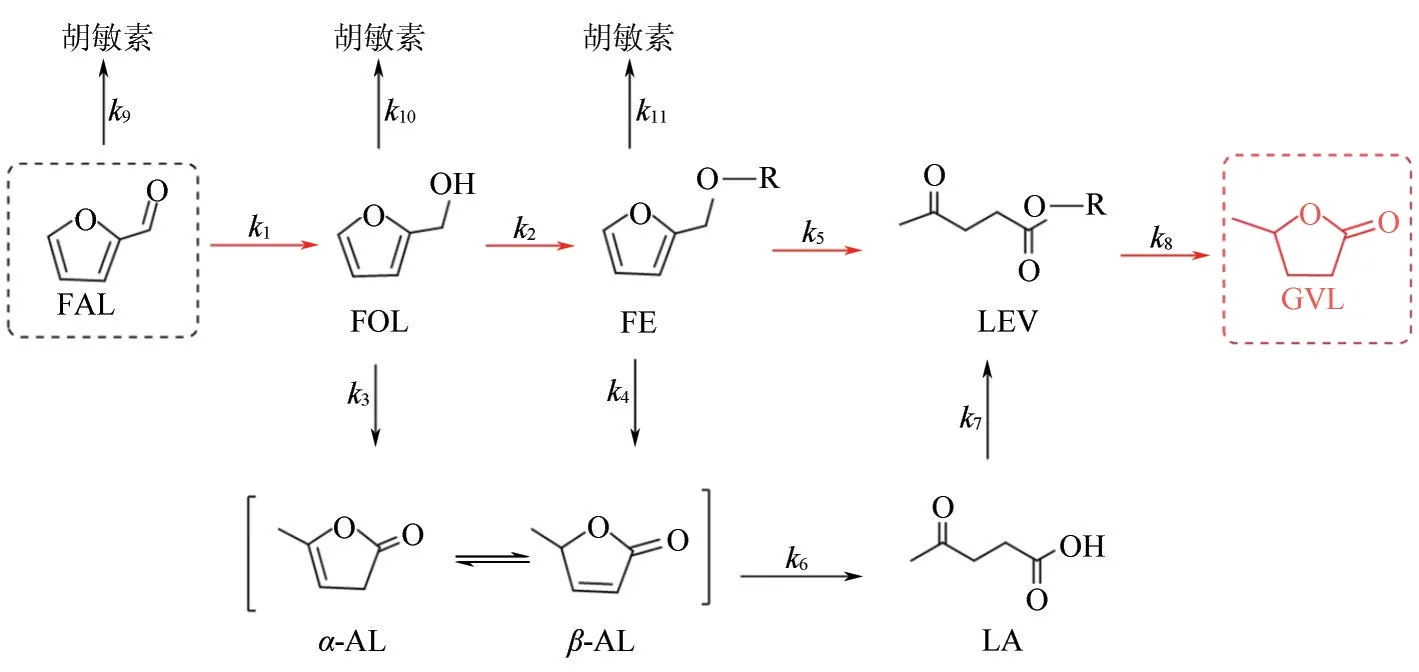
图4 FAL在仲醇介质中一锅转化为GVL的拟定反应网络[79]
Antunes 等采用后合成法将Zr 引入沸石骨架得到Zr-Al-催化剂,以2-丁醇为氢源和溶剂,催化FAL 级联转化为GVL,基于上述两条反应路径,考虑反应过程产生的腐殖质,展开了动力学研究。假设每个步骤都符合一级方程式,根据图4的反应网络建立以下模型方程[式(1)~式(8)]。

式中,为各组分的物质的量浓度;k为表观速率常数。
实验结果证明了两条路径的存在。以当归内酯(-AL或-AL)为底物时,生成LA的产率高于乙酰丙酸-2-丁酯(2-BL)。以FAL和FOL为底物时,2-BL 最初产率高于LA,说明2-BL 不仅由LA 生成,即由FAL到2-BL的反应中存在两条平行途径。Zr-Al-催化剂的Zr 位点在FAL 到FOL 和2-BL 到GVL的CTH反应中起作用,而Al位点作为Brønsted酸促进FOL 的醚化和呋喃环的开环反应。增加Al/Zr比例能促进Brønsted酸催化的同时也有利于副反应的发生(糠醛-糠醛、糠醛-醇、糠醚-醇、醇-醇等之间的缩合反应)。FOL与2-丁醇的醚化反应[=(0.8832±0.1123)h]是级联反应的快速步骤。由于LA 的反应活性较低,LA 到2-BL 的反应严重受限[=(5.625±0.947)×10h],证明第二条路线为次要反应路线。
Iglesias等提出了在ZrO-SBA-15的2-丙醇溶剂中FAL 级联转化为GVL 的合理反应途径。其动力学分析表明,FAL 的CTH 反应(=2.126h)和FOL 与2-丙醇的醚化反应(=4.548h)是级联反应的快速反应,醚化产物FE 到IPL 的开环反应(=0.192h)是限速反应。FAL 到FOL 和IPL 到GVL(=0.421h)的CTH 反应都需要弱Lewis 酸碱催化,中间步骤醚化和异构化反应则依赖于Brønsted 酸和强Lewis 酸。另外,ZrO分子膜越厚,值越大,L 酸位点越多,有利于提高FAL 和IPL的MPV 还原反应活性。但同时,ZrO-SBA-15 催化剂的B酸位点会减少(和值减小),导致级联反应的中间步骤(醚化和异构化反应)活性极低。腐殖质的生成速度与B 酸强度和反应温度呈正相关。因此,可通过调整ZrO分子膜层的厚度和酸强度以加速FE 转化为IPL 和减少副产物的形成,优化整个级联反应。
Ye等对HZ-ZrP在2-丙醇介质中催化FAL转化为GVL的反应进行了动力学研究。结果表明,ln(c/)与反应时间呈线性关系,属于一级反应,FE 到LEV的开环反应是速控步。
第二条反应路径也有相关报道。Antunes 等采用后合成法将Sn 和Al 引入脱铝沸石骨架得到Sn-Al-催化剂,并对FAL一锅转化为GVL的反应进行动力学研究。研究表明,FE—-AL 的反应速度[=(2.394±0.086)×10h]比FE—2-BL[=(8.069±0.064)×10h]快。缩合反应生成的少量水可促进FOL和α-AL转化为LA。因此,在Sn-Al-催化剂的2-丁醇溶剂中FAL 级联转化为GVL 主要按照第二条路线反应。Sn 位点促进了FAL 到FOL 的反应,Al 和Sn 位点都促进了FOL 的转化。FOL 在酸的作用下醚化为FE 在总反应中最快[=(2.066±0.080)h],2-BL形成的限速步骤与Brønsted酸强弱有关(和值较小)。Winoto等在Sn-Al-优化条件研究中发现MPV 反应是快反应,FE 和-AL转化为IPL 是需要Brønsted 酸催化的慢反应。在Sn-Al-催化下,-AL 先水解为LA 和IPL 再转化为GVL。而LA 转化为GVL 的速度比EL 慢,这归因于LA必须被酯化为IPL,IPL形成GVL在能量上更有利。提高温度有助于-AL向GVL转化,但竞争性的副反应也在加剧,腐殖酸也在增加。
另外,醇类化合物的选择对MPV 反应效果有较大差别。Luo 等以不同醇类化合物对乙酰丙酸甲酯转化为GVL 的MPV 反应进行了动力学研究,结果表明,伯醇的表观活化能比仲醇高,在仲醇介质下的反应速率常数较高,其中在2-丙醇中的值最低为46.3kJ/mol(:2-丙醇<2-丁醇<环己醇<乙醇≈丙醇<丁醇)。因此在MPV 还原中,常使用仲醇,尤其是2-丙醇和2-丁醇作为氢源。2-丙醇由于具有较小的动力学直径有利于沸石通道的扩散,是最佳的氢源选择。
综述以上FAL 转化为GVL 的级联反应的动力学案例研究,普遍认为由FE 开环形成LEV 是整个反应的速控步。催化剂的结构、酸强度以及溶剂影响着每一步反应速率。因此,设计催化剂时应着重提高催化剂的Brønsted 酸位点以促进FE 向LEV 的转化,从而提高GVL的产率。
5.2 木糖转化为FAL的动力学
Choudhary等以CrCl和HCl分别作为Lewis酸和Brønsted 酸催化剂,在甲苯/水溶剂中催化木糖级联转化为FAL。其反应路径和活化能如图5 所示,木糖首先在CrCl下异构化为木酮糖和来苏糖,然后在HCl 催化下脱水为FAL。Brønsted 酸催化木糖直接转化为FAL 的途径比级联途径需要更高的活化能,表明Lewis 和Brønsted 酸位点的联用可提高木糖反应效率和产物的选择性。Chatterjee等采用硫酸对粉煤灰进行酸浸制备了FAS-4 固体酸催化剂,在GVL/水介质中催化木糖转化为FAL。其动力学研究表明,相较于液体酸催化剂HCl(=133.9kJ/mol),该Brønsted酸型催化剂可将木糖脱水制FAL的活化能降低至83.36kJ/mol(表4,条目2)。
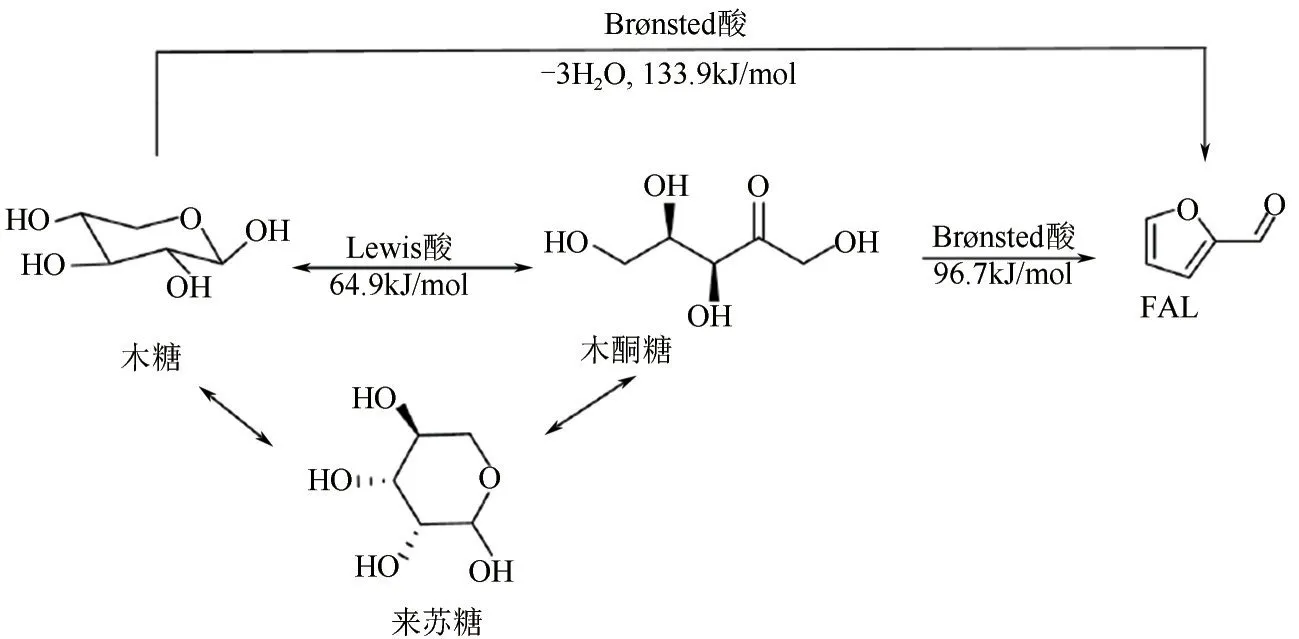
图5 酸在木糖脱水机理中的作用[72]
Sener 等对液体酸催化剂HCl 在GVL/水介质中的木糖脱水反应进行动力学研究,其反应路径如图6所示,包括木糖一步脱水制备FAL、木糖降解和FAL降解反应。
木糖脱水制备FAL的反应动力学分析基于图6所示的反应网络,其模型方程见式(9)~式(11)。
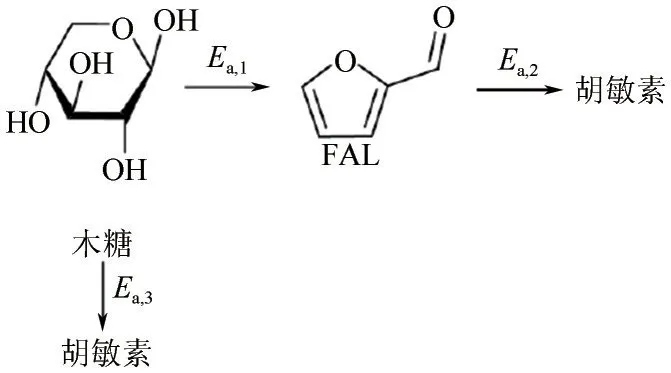
图6 木糖脱水的反应网络
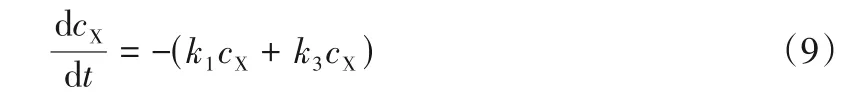
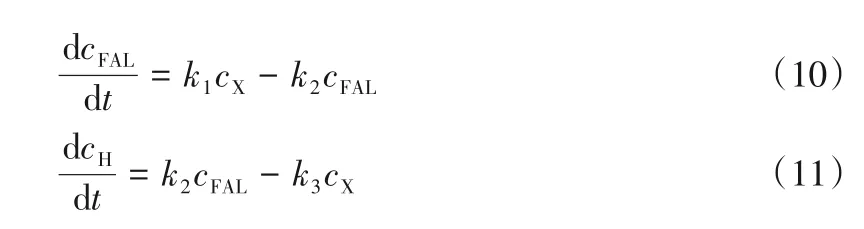
式中,X表示木糖;H表示胡敏素。
结果表明,木糖和FAL的反应级数在反应网络中的所有反应步骤均遵循表观一级动力学。在225℃下得到木糖脱水的活化能为(74.7±2.9)kJ/mol(表4,条目3)。高温下FAL 的选择性与初始木糖浓度无关。而木糖脱水速率随着酸浓度的增加而增加,脱水速率和酸浓度对反应器设计影响显著。较高的酸浓度导致较高的反应速率,从而缩短反应时间。另一方面,酸浓度越高,腐蚀速度越快,反应器寿命越短。因此,必须明智地选择酸浓度以最大化给定反应器设置的输出。
同样地,Li 等报道的动力学研究表明,以GVL 为溶剂比纯水表现出更好的效果,GVL 能改变半纤维素转化反应的能量。以0.10%HSO为催化剂,在190℃、20min 反应条件下,木糖合成FAL的最大活化能在GVL中(101.44kJ/mol)比在纯水中(154.15kJ/mol)低,而FAL 降解的最大活化能在GVL 中(126.72kJ/mol)比在纯水中(99.42kJ/mol)高(表4,条目4、5)。这说明GVL能抑制FAL 的降解以及五碳糖和FAL 之间的缩合反应,从而降低了降解速率,提高了FAL 的产率。在高温下,木糖和FAL 双分子缩合引起的FAL 损失最小,而木糖降解引起的碳损失随温度的升高而增加。黄耀兵课题组以木聚糖为底物,使用Al(SO)催化剂,在GVL/水溶剂中,190℃、20min反应条件下,FAL 产率高达99.5%。其反应路径为:木聚糖-木糖-木酮糖-糠醛。对比纯水溶剂(=1.31×10s,=0.11×10s),有机层的引入明显降低了生成腐殖质的速率。半纤维素以Al(SO)为催化剂水解生成糠醛研究表明,木聚糖转化为FAL 途径为解聚—异构化—脱水。延长反应时间会导致FAL 产率下降,这归因于FAL 在较长的反应时间内分解或与其他副产物聚合成腐殖质。
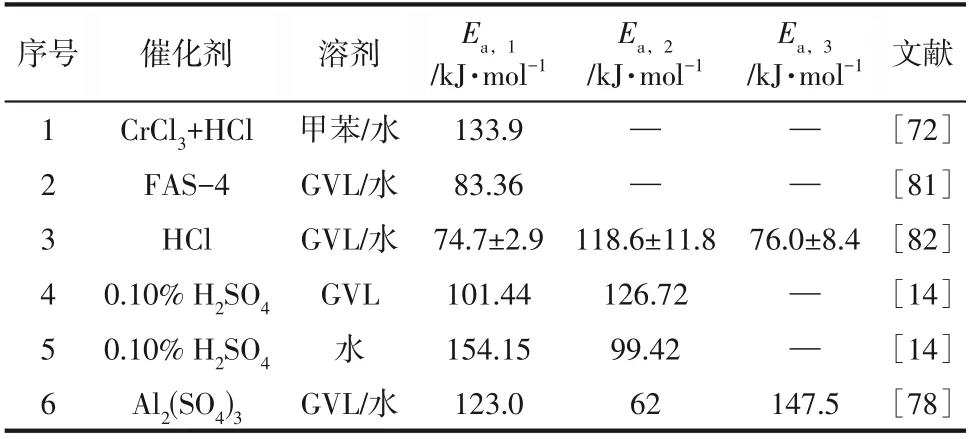
表4 木糖转化为FAL的活化能
综上发现,木糖向FAL 的转化遵循伪一级反应动力学,其最佳反应条件通常是高温短时。在GVL/水溶剂中的反应速率较快,且值较低,这可能是由于极性非质子溶剂GVL稳定了酸性质子,导致酸催化反应的活化能降低。
5.3 基于动力学分析的催化剂理性设计
木糖向FAL 的转化需要Brønsted 酸型催化剂,并且溶剂对产物选择性的影响显著,GVL/水代替纯水作溶剂可将FAL 提取到有机层以提高FAL 产率。因此,对于经济易得的木糖等原料,应着力开发对异构化和脱水反应具有高效催化作用的新型Brønsted 酸与Lewis 酸具有协同作用的固体酸催化剂或Brønsted酸型固体催化剂,在高温短时反应条件下抑制腐殖质的形成,以提高生物质原料转化率和FAL的选择性。
FAL 向GVL 的转化涉及一次酸催化和两次MPV 还原反应。反应机理和动力学分析表明,酸催化反应由Brønsted 酸位点控制,MPV 反应由Lewis 酸位点控制。中间步骤需要较强的酸催化,是未来要解决的重点问题,酸度太强容易产生腐殖质,太弱则不能达到催化效果。因此,设计合适的Lewis 和Brønsted 酸位点的催化剂是FAL 选择性合成GVL 的关键。对于FAL 到GVL 的级联反应,应着力开发具有合适Brønsted/Lewis 酸位点的双功能催化剂以高效催化半纤维素及其衍生物的转化,进一步研究有关Brønsted 和Lewis 酸性位点调控的策略和机制。另一方面,创新催化剂的合成方法,以降低生产成本和提高催化剂的稳定性,为实现GVL 的工业化开发提供基础。双金属催化剂比单金属催化剂具有更高的稳定性,可以抑制催化剂的烧结、金属浸出和炭沉积等问题。金属之间的协同作用产生令人惊奇的卓越效果,开发双金属或多金属复合协同、酸碱协同的多功能催化剂是创新催化体系的方向。
6 结语
生物质是具有替代化石能源潜力的可再生能源物质,符合当今绿色可持续发展的战略,GVL 是应用广泛的高附加值平台化合物,其工业化的应用对于改善能源短缺和环境问题具有重大现实意义,因此以可再生生物质原料制备GVL 备受广大研究者的关注。从纤维素、半纤维素、木糖和糠醛等制备GVL 的研究正广泛而深入地进行着,也获得了一些可喜的成果。从氢源角度考虑,直接(氢气)和间接(甲酸和醇类)加氢都给制备GVL 反应带来了显著的催化效果。传统的以氢气为氢源时体系通常处于高压状态,反应耗时较长。为降低直接加氢带来的高压危险和高成本,反应体系中生物质水解产生的甲酸可作为内部氢源,这更符合原子经济性。但甲酸通常搭配贵金属催化剂进行高温长时的反应。在这种苛刻条件下,甲酸的腐蚀性对反应器和环境不利。醇类化合物的出现,MPV 反应结合酸催化反应使得反应条件趋于温和,避免了高压氢和贵金属的使用,成为更符合绿色化学发展的催化剂模式。
半纤维素合成FAL 以及FAL 合成GVL 的研究已走向成熟阶段,以生物质碳水化合物为原料直接高效转化为GVL 仍是艰巨的挑战,尚有待进一步研究。选择具有高比表面积和孔隙率的材料为载体,提供更多可接近性的活性位点,同时有助于底物的扩散,增强活性位点与载体的作用力以提高催化剂的稳定性。以Zr、Sn、Ni、Cu 等非贵金属为活性中心,分子筛等为载体有望开发出催化效果优异的低廉催化剂。根据动力学的研究建议,设计具有合适的Lewis 和Brønsted 酸位点的双功能催化剂是提高GVL 选择性的有效方法。生物质原料和半纤维素制备GVL是一个十分复杂的多步反应过程,研究者也应着力于反应机理的探索和动力学的分析,为优化制备工艺提供理论指导。
