丙泊酚对过氧化氢诱导的大鼠肝Kupffer细胞氧化应激损伤及磷脂酰肌醇-3激酶/蛋白激酶B信号通路的影响▲
2022-07-31郭志强李钰艳李洪亮许斌兵
郭志强 李钰艳 李洪亮 张 敏 何 勇 许斌兵
(四川省遂宁市中心医院1 麻醉科,2 内分泌科,遂宁市 629000,电子邮箱:guozhiqiang384@163.com)
氧化应激与心力衰竭、心律失常和心肌梗死等疾病密切相关,其过度激活容易导致心血管疾病的发生[1]。活性氧簇是一组活性小分子,在调节细胞的各种功能和生物过程中发挥着重要作用,对心血管的稳态至关重要,但活性氧簇的失衡会造成心血管损伤,多种心脑血管疾病的发生都与氧化应激有关,而心血管疾病是导致死亡的主要疾病[2-3]。因此,从氧化应激方面开展心血管疾病的防治研究,成为近年来的新趋势。在临床上丙泊酚常作为快速短效的静脉麻醉药,除催眠与镇静作用外,其还具有降低动脉血压、抑制炎症反应和细胞凋亡、改善细胞能量代谢障碍等功能[4-5]。研究表明,丙泊酚具有抗心肌细胞氧化损伤的作用,能够降低心肌细胞中的活性氧簇含量,减少氧化应激条件下心肌细胞的凋亡[6]。磷脂酰肌醇-3-激酶(phosphatidylinositol-3 kinase,PI3K)/蛋白激酶B(protein kinase B,Akt)信号通路与氧化应激反应密切相关,而丙泊酚能够通过激活PI3K/Akt信号通路减轻炎症反应和氧化应激,从而抑制肾缺血再灌注损伤,以及改善蛛网膜下腔出血引起的早期脑损伤[7-8]。本研究探讨丙泊酚对过氧化氢诱导的大鼠肝Kupffer细胞氧化应激损伤和PI3K/Akt通路的影响,现报告如下。
1 材料与方法
1.1 材料
1.1.1 实验动物:10只SD大鼠,10~12周龄,雌雄均可,体重260~300 g,购自重庆医科大学实验动物中心[许可证号SCXK(渝)2019-0003],于本院动物房常规饲养,环境温度22 ℃~24 ℃,相对湿度50%,12 h光照/12 h黑暗交替,自由饮水进食。本研究符合国家实验动物伦理保护标准及相关法律规定。
1.1.2 主要试剂和仪器:丙泊酚注射液购自四川国瑞药业责任有限公司(规格10 mL ∶0.1 g,批号:20190815);含10%胎牛血清的杜氏改良伊格尔培养基(Dulbecco′s modified Eagle medium,DMEM)/F12培养基购自美国Gibco公司(批号:17502-048);30%过氧化氢溶液、二甲基亚砜(dimethyl sulfoxide,DMSO)、MTT、结合缓冲液和兔抗鼠β-actin单克隆抗体均购自美国Sigma公司(批号:SD0617M、SL5519K、SD3019、SD7123、SD5413K);蛋白提取试剂盒、ECL显色试剂盒和二氨基联苯胺显色试剂盒均购自北京中杉金桥生物科技有限公司(批号:hz-3101-1、hz-5102-3、hz-4105-6);膜联蛋白Ⅴ-异硫氰酸荧光素(annexin Ⅴ-fluorescein isothiocyanate,Annexin V-FITC)/碘化丙啶(propidium iodide,PI)细胞凋亡检测试剂盒购自嘉美生物技术有限公司(批号:s112);乳酸脱氢酶(lactate dehydrogenase,LDH)检测试剂盒、活性氧簇检测试剂盒、过氧化氢酶(catalase,CAT)检测试剂盒均购自上海碧云天生物技术有限公司(批号: SC0191-25、S0033M、S0101M);96孔培养板购自上海生工生物工程有限公司(批号:F603204);二喹啉甲酸蛋白定量试剂盒购自上海源叶生物科技有限公司(批号:R21250)兔抗鼠PI3K、Akt、磷酸化PI3K(phosphorylated PI3K,p-PI3K)和磷酸化Akt(phosphorylated Akt,p-Akt)单克隆抗体和辣根过氧化物酶标记羊抗鼠IgG二抗均购自美国Abcam公司(批号:ab01364、ab50113、ab56189、ab70142、ab0019);SpectraMax iD5型多功能酶标仪购自上海美谷分子仪器有限公司;VersaDoc 3000型蛋白凝胶成像仪购自美国Bio-Rad公司;CKX41型倒置显微镜购自日本Olympus公司;FACSCanto型流式细胞仪购自美国BD公司。
1.2 实验方法
1.2.1 Kupffer细胞的分离与培养:参照相关文献[9]的方法,使用梯度离心结合选择性贴壁法分离大鼠Kupffer细胞。使用0.3%的戊巴比妥钠以30 mg/kg的剂量进行腹腔注射,麻醉大鼠后固定、消毒,于腹部做十字切口,经腹主动脉推注肝素(100 U/kg),结扎下腔静脉;切开胸腔并夹闭主动脉,剪开心脏,使血液流入胸腔,灌注不含钙离子的Hank′s液,使肝脏逐渐变成黄白色;仔细分离切取肝脏,于无菌操作台上使用不含钙离子的Hank′s液冲洗,然后用注射器抽取0.05%胶原蛋白酶反复灌洗肝脏,使肝脏组织松散,呈泥状;剥离肝包膜,经200目网过滤,除去未消化的组织,得到肝细胞悬液。将肝细胞悬液在4 ℃下1 000 r/min离心3 min,取上清;然后4 ℃下10 000 r/min离心5 min,取沉淀;使用不含血清的DMEM/F12培养基重悬,同时加入1.065 g/mL细胞分离液,在4 ℃下10 000 r/min离心15 min,取沉淀;再次使用不含血清的DMEM/F12培养基重悬,在4 ℃下1 000 r/min离心5 min,取沉淀。加入含10%胎牛血清的DMEM/F12培养基,同时使用倒置相差显微镜鉴定Kupffer细胞,若细胞折光性强、呈圆形、体积小,15min后开始贴壁、细胞呈扁圆形、变薄、边界模糊,4 h后大部分贴壁、胞膜伸展、体积增大、形状不规则,24 h后细胞完全伸展、出现伪足、呈多边形等不规则形状,则该细胞为Kupffer细胞。对Kupffer细胞进行原代培养,然后使用含10%胎牛血清的DMEM/F12培养基,置于37 ℃、5% CO2、饱和湿度培养箱中培养,取对数生长期细胞并调整密度为1×106个/mL用于后续实验。
1.2.2 氧化应激损伤细胞模型的建立及分组处理:参照相关文献[10-12]的方法,使用100 μmol/L过氧化氢诱导Kupffer细胞,建立氧化应激损伤细胞模型。将Kupffer细胞按照2×104个/孔接种至96孔板中,37 ℃、5% CO2培养24 h后,加入100 μmol/L过氧化氢作用24 h。取正常Kupffer细胞作为对照组(用不含丙泊酚的DMEM/F12培养基培养),将模型细胞随机分为模型组(不含丙泊酚的DMEM/F12培养基培养)、丙泊酚低浓度组(含5 μmol/L丙泊酚的DMEM/F12培养基培养)、丙泊酚中浓度组(含25 μmol/L丙泊酚的DMEM/F12培养基培养)、丙泊酚高浓度组(含50 μmol/L 丙泊酚的DMEM/F12培养基培养)和阳性对照组(含0.1 μmol/L盐酸右美托咪定的DMEM/F12培养基培养)。6组细胞均于37 ℃、5% CO2的培养箱中培养12 h。每组均设6个平行孔。
1.2.3 MTT法检测细胞活性:收集1.2.2中培养12 h后的细胞,加入10 μL的MTT继续孵育4 h,吸取上清,加入150 μL的DMSO,充分震荡混匀15 min后用多功能酶标仪检测各孔570 nm处吸光度值(即OD570)。细胞活性=(实验组OD570/对照组OD570)×100%。实验重复6次。
1.2.4 流式细胞法检测细胞凋亡:收集1.2.2中培养12 h后的细胞,1 200 r/min离心5 min,弃培养基并收集细胞,用磷酸缓冲盐溶液洗涤2次,每次2 min,用400 μL结合缓冲液悬浮细胞,加入5 μL Annexin Ⅴ-FITC染液,轻轻混匀后于2 ℃~8 ℃避光孵育15 min;加入10 μL PI后轻轻混匀,于2 ℃~8 ℃避光孵育5 min;使用流式细胞仪检测细胞凋亡情况,统计细胞凋亡率。实验重复6次。
1.2.5 检测细胞LDH释放量:收集1.2.2中培养12 h后的细胞,严格按照乳酸脱氢LDH试剂盒说明书进行操作,使用多功能酶标仪测定490 nm处各孔吸光度值(即OD490),计算LDH释放量。LDH释放量(%)=(培养液OD490+细胞匀浆OD490)/培养液OD490×100%。实验重复6次。
1.2.6 检测细胞活性氧簇含量:收集1.2.2中培养12 h后的细胞上清液,按照活性氧检测试剂盒说明书进行操作,使用多功能酶标仪测量各孔的荧光强度,即调整最佳激发波长为488 nm、最佳发射波长为525 nm时显示的荧光强度,以细胞培养基的上清液作为空白组。活性氧簇含量=(实验组荧光强度-空白组荧光强度)/(对照组荧光强度-空白组荧光强度)×100%。实验重复6次。
1.2.7 检测CAT活性:收集1.2.2中培养12 h后的细胞上清液,按照CAT检测试剂盒说明书进行操作。以25 ℃反应1 minOD240减少0.1的CAT量为1个CAT酶活单位,计算CAT活性。CAT活性(U/mg)=(ΔOD240×VT)/(0.1×VS×t×W),其中,ΔOD240代表反应时间内吸光度的变化,VT代表提取酶液总体积(mL),W代表样品重量(mg),t代表反应时间(min),VS代表测定时所取酶液体积(mL)。实验重复6次。
1.2.8 Western blot检测PI3K、Akt的磷酸化水平:收集1.2.2中培养12 h后的细胞,使用蛋白提取试剂盒提取细胞中的总蛋白。使用二喹啉甲酸蛋白定量试剂盒对蛋白进行定量,然后进行聚丙烯酰胺凝胶电泳、转膜、封闭,将1 ∶500浓度稀释后的兔抗鼠PI3K、Akt、p-PI3K、p-Akt和β-actin一抗4 ℃过夜孵育,以辣根过氧化物酶标注的羊抗鼠IgG二抗(1 ∶5 000)室温孵育2 h,用ECL显色试剂盒显色,凝胶成像仪拍照,分析灰度值,以β-actin为参照进行半定量分析,PI3K、Akt磷酸化水平分别以p-PI3K/PI3K比值、p-Akt/Akt比值表示。实验重复6次。
1.3 统计学分析 采用SPSS 22.0软件进行统计分析。计量资料以(x±s)表示,多组间比较采用单因素方差分析,进一步两两比较采用SNK-q检验,以P<0.05为差异具有统计学意义。
2 结 果
2.1 各组Kupffer细胞活性的比较 与对照组相比,模型组Kupffer细胞活性降低(P<0.05);与模型组相比,阳性对照组、丙泊酚低浓度组和丙泊酚中浓度组Kupffer细胞活性升高(均P<0.05),而丙泊酚高浓度组Kupffer细胞活性差异无统计学意义(P>0.05);与阳性对照组、丙泊酚低浓度组和丙泊酚中浓度组比较,丙泊酚高浓度组Kupffer细胞活性降低(均P<0.05);阳性对照组、丙泊酚低浓度组和丙泊酚中浓度组Kupffer细胞活性差异无统计学意义(P>0.05)。见表1。
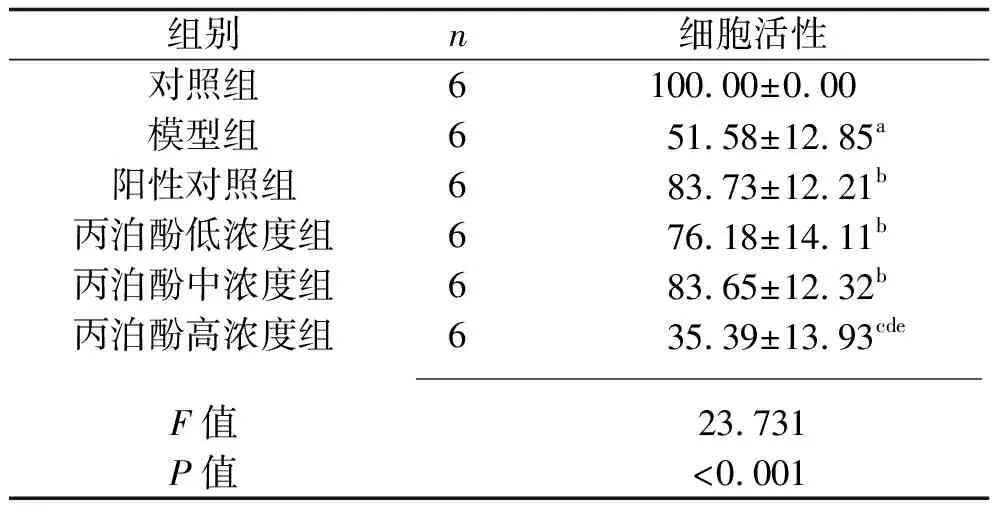
表1 各组Kupffer细胞活性的比较(x±s,%)
2.2 各组Kupffer细胞凋亡率的比较 与对照组相比,模型组Kupffer细胞凋亡率升高(P<0.05);与模型组相比,阳性对照组、丙泊酚低浓度组和丙泊酚中浓度组Kupffer细胞凋亡率降低(均P<0.05),而丙泊酚高浓度组Kupffer细胞凋亡率升高(P<0.05);与阳性对照组相比,丙泊酚低浓度组和丙泊酚中浓度组Kupffer细胞凋亡率差异无统计学意义(均P>0.05),丙泊酚高浓度组Kupffer细胞凋亡率升高(P<0.05);丙泊酚中浓度组、丙泊酚低浓度组、丙泊酚高浓度组Kupffer细胞凋亡率依次升高(均P<0.05)。见表2。

表2 各组Kupffer细胞凋亡率的比较(x±s,%)
2.3 各组Kupffer细胞LDH释放量、活性氧簇含量及CAT活性的比较 与对照组相比,模型组Kupffer细胞LDH释放量和活性氧簇含量升高,CAT活性降低(均P<0.05);与模型组相比,阳性对照组、丙泊酚低浓度组和丙泊酚中浓度组Kupffer细胞LDH释放量和活性氧簇含量降低,CAT活性升高(均P<0.05),而丙泊酚高浓度组Kupffer细胞LDH释放量和活性氧簇含量升高,CAT活性降低(均P<0.05);与阳性对照组比较,丙泊酚低浓度组Kupffer细胞LDH释放量差异无统计学意义(P>0.05),活性氧簇含量升高、CAT活性降低(均P<0.05),丙泊酚中浓度组Kupffer细胞LDH释放量、活性氧簇含量、CAT活性差异均无统计学意义(均P>0.05),丙泊酚高浓度组Kupffer细胞LDH释放量和活性氧簇含量升高、CAT活性降低(均P<0.05);与丙泊酚低浓度组相比,丙泊酚中浓度组Kupffer细胞LDH释放量和CAT活性差异无统计学意义(均P>0.05),活性氧簇含量降低(P<0.05),丙泊酚高浓度组Kupffer细胞LDH释放量和活性氧簇含量升高,CAT活性降低(均P<0.05);与丙泊酚中浓度组相比,丙泊酚高浓度组Kupffer细胞LDH释放量和活性氧簇含量升高,CAT活性降低(均P<0.05)。见表3。

表3 各组Kupffer细胞LDH释放量、活性氧簇含量及CAT活性的比较(x±s)
2.4 各组Kupffer细胞PI3K和Akt磷酸化水平的比较 与对照组相比,模型组Kupffer细胞PI3K和Akt的磷酸化水平降低(均P<0.05);与模型组相比,阳性对照组、丙泊酚低浓度组和丙泊酚中浓度组Kupffer细胞PI3K和Akt的磷酸化水平升高(均P<0.05),而丙泊酚高浓度组Kupffer细胞PI3K和Akt的磷酸化水平降低(均P<0.05);与阳性对照组、丙泊酚低浓度组和丙泊酚中浓度组相比,丙泊酚高浓度组Kupffer细胞PI3K和Akt的磷酸化水平降低(均P<0.05);阳性对照组、丙泊酚低浓度组和丙泊酚中浓度组Kupffer细胞PI3K和Akt的磷酸化水平差异无统计学意义(均P>0.05)。见表4和图1。

表4 各组Kupffer细胞PI3K和Akt磷酸化水平的比较(x±s)

图1 蛋白条带图
3 讨 论
氧化应激损伤与心血管疾病的发生存在密切的关系:氧化应激反应导致活性氧簇含量增多,耗尽抗氧化酶,使自由基损害心血管,导致心血管细胞线粒体内电子传递链受影响,引起线粒体功能障碍,诱导细胞凋亡[13]。因此,减少氧化应激逐渐成为治疗心血管疾病的重要研究方向,但是,目前并没有特定的抗氧化治疗方法来预防或治疗心血管疾病。
当离体细胞受到损伤时,LDH会由细胞释放至培养液中,所以可用LDH释放量来评估细胞受损程度。另外,活性氧簇过量会产生大量自由基,损害细胞,诱导细胞凋亡。丙泊酚是临床常用的静脉麻醉剂,可清除自由基,具有显著的抗氧化作用[5]。Yu等[14]研究发现,丙泊酚能够通过减少脑缺血再灌注损伤过程中琥珀酸盐的积累来防止氧化应激的发生。Guo等[15]研究发现,丙泊酚可在临时载瘤动脉夹闭手术后7 d内防止大脑发生氧化应激损伤,从而保护神经,促进认知功能的恢复。Yoon等[16]研究发现,丙泊酚能够诱导细胞自噬来减少氧化应激损伤所致的COS-7细胞凋亡。丙泊酚作为一种临床使用的静脉麻醉药,高浓度易对人体造成损害。本研究使用过氧化氢干预Kupffer细胞后,细胞活性降低,凋亡率升高,LDH释放量和活性氧簇含量增加,CAT活性降低,提示成功建立氧化应激损伤细胞模型。本研究结果显示,低、中浓度的丙泊酚均可抑制LDH的释放,提高活性氧簇的清除能力和CAT活性,增强细胞活性,减少细胞凋亡,但高浓度丙泊酚(50 μmol/L)却加重过氧化氢诱导的Kupffer细胞氧化应激损伤。这提示中、低浓度丙泊酚可通过增强细胞CAT活性,提高细胞清除活性氧的能力,减少LDH的释放,从而发挥其抵抗氧化应激损伤的作用,以维持细胞活性、减少细胞凋亡,但其作用机制仍需进一步研究。
氧化应激与PI3K/Akt信号通路密切相关,PI3K是一种胞外的磷脂酰肌醇激酶,PI3K活化后可诱导Akt磷酸化,p-Akt进一步活化下游信号因子,调节细胞活性,抑制细胞凋亡[7]。杨莎莎等[17]研究发现,白藜芦醇通过激活PI3K/Akt通路抑制高糖致肾小管上皮细胞凋亡;Lim等[18]研究发现,抗衰老蛋白能够通过负调控PI3K/Akt信号通路,提高抗氧化物酶活性,从而保护他克莫司诱导的氧化应激;Zhang等[19]研究发现,氢气通过PI3K/Akt信号通路抑制核因子E2相关因子2的激活,从而保护细胞免受紫外线辐射诱导的氧化应激损伤;Zhao等[20]研究发现,芪苈强心胶囊可能通过PI3K/Akt信号通路来减少氧化应激诱导的心肌细胞凋亡。上述研究表明,PI3K/Akt通路与细胞的氧化应激损伤及细胞凋亡密切相关。本研究结果显示,低、中浓度的丙泊酚能够提高Kupffer细胞PI3K和Akt的磷酸化水平,这提示丙泊酚可能通过激活PI3K/Akt信号通路来减轻氧化应激损伤,抑制细胞凋亡。
综上所述,低、中浓度(5 μmol/L、25 μmol/L)的丙泊酚可减轻过氧化氢诱导的Kupffer细胞氧化应激损伤,增强细胞活性,抑制细胞凋亡,其机制可能与PI3K/Akt通路有关。
