1例阿托伐他汀致药物性肝损伤患者的药学监护
2022-07-30洪丽绵林玮玮林志强吴水发陈喆鸣
洪丽绵 林玮玮 林志强 吴水发 陈喆鸣
(1. 福建医科大学附属泉州第一医院药剂科 泉州 362000;2. 福建医科大学附属第一医院药剂科 福州 350005)
指南[1]指出,对于非心源性缺血性脑卒中或缺血性脑卒中和短暂性脑缺血发作(transient ischemic attack,TⅠA)患者,无论是否伴有其他动脉粥样硬化证据,推荐予高强度他汀类药物长期治疗以降低脑卒中和心血管事件的风险。目前,脑卒中患者的他汀类药物使用率已上升至90%[2]。在服用他汀类药物的患者中,有1.9%~5.5%的患者发生药物性肝损伤(drug-induced liver injury, DⅠLⅠ),而这些病例中有相当大的比例(34%)是由阿托伐他汀所致[3]。本文通过1 例二次脑卒中患者使用阿托伐他汀强化降脂出现DⅠLⅠ的病例,分析临床药师如何实施药学监护,协助医师制订治疗方案及处理药物不良反应,更好地实施药学服务。
1 病例资料
患者,男性,65 岁。因“突发头晕、站立不稳20 h 余”轮椅入院,入院前20 h 无明显诱因突发头晕、站立不稳,伴视物旋转,伴呕吐胃内容物,当地医院就诊,查颅脑CT 示“右侧小脑、枕叶低密度灶,脑梗死?左侧小脑软化灶”,转诊我院。既往1 年余前脑梗死个人史,发现高血压1 年余,未规律服用降压药,未监测血压。无药物过敏史,无吸烟、饮酒史。美国国立卫生研究院卒中量表(NⅠH stroke scale, NⅠHSS)评分4 分,GCS 评分14 分,Essen 卒中风险量表(Essen stroke risk score, ESRS)评分3 分,改良Rankin 量表(modified Rankin scale score,mRS)评分4 分。入院诊断:脑梗死,脑梗死个人史,高血压病1 级(低危)。当地医院生化指标见表1。
入院后立即予“阿托伐他汀(商品名:立普妥)40 mg qd po”调脂稳斑、“阿司匹林肠溶片100 mg qd po”抗血小板、“丁苯酞软胶囊0.2 g tid po”改善循环等处理。入院第2 日晨生化指标(表1)示肝功能各项指标显著升高:谷丙转氨酶(alanine aminotransferase, ALT)321 U/L、谷草转氨酶(aspartate aminotransferase, AST)523 U/L、谷氨酰转移酶(glutamyl transferase, GGT)224 U/L、碱性磷酸酶(alkaline phosphatase, ALP)150 U/L、总胆红素(total bilirubin, TBil)42 μmol/L、直接胆红素(direct bilirubin,DBil)20 μmol/L、间接担红素(indirect bilirubin, ⅠBil)22 μmol/L。临床药师查找并分析患者肝功能异常的原因,逐个排查所用药物,阿托伐他汀、阿司匹林、丁苯酞均有可能出现DⅠLⅠ,而阿托伐他汀比其他两药物更为常见。查看患者以往病历,详细追问病史,发现患者于入院前1 年余口服“立普妥40 mg qd ”,8 d 后改服“阿托伐他汀(商品名:阿乐)20 mg qn”,9 d 后查肝功能显示异常:ALT 121 U/L、AST 86 U/L、GGT 141 U/L、ALP 131 U/L。故临床药师判断很可能是阿托伐他汀引起的DⅠLⅠ,建议医师停用阿托伐他汀,可改为瑞舒伐他汀5 mg qd po 治疗。临床医师接受临床药师的建议,并加用“双环醇片25 mg tid po、多烯磷脂酰胆碱注射液465 mg qd ivgtt、复方甘草酸苷注射液60 ml qd iv gtt”抗炎保肝,其余不变。第4 日生化指标示:ALT 下降13%,AST 下降64%;第9 日生化指标示:ALT 下降71%,AST 下降88%;第17日患者肝功能明显好转(表1),病情稳定,予以出院。
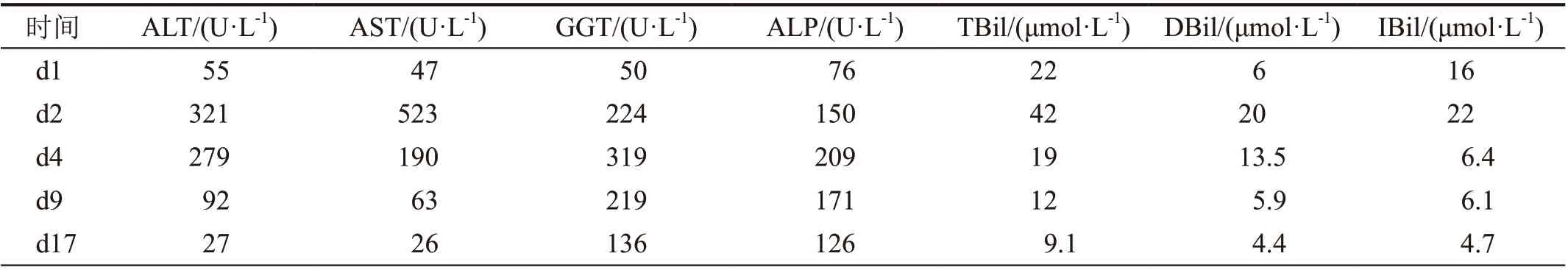
表1 患者相关肝功能指标
2 分析与讨论
2.1 他汀类药物的使用及不良反应分析
他汀类药物可改善急性缺血性脑卒中患者的预后,其机制除了调脂外,还具有“多效性”:他汀类药物不但可改善血管内皮功能,还可调节脑血流,促进血管新生和突触重构、抑制内皮细胞凋亡及减轻炎性反应等[4]。对于非心源性缺血性脑卒中或TⅠA 患者,无论是否伴有其他动脉粥样硬化证据,均推荐给予高强度他汀类药物长期治疗以减少缺血性脑卒中和心血管事件发生风险[1]。一项包含117 例患者的随机对照研究显示,急性缺血性脑卒中患者强化阿托伐他汀治疗可减少微栓子和炎症的发生,且无明显不良事件发生[5]。本患者为老年男性,急性起病,主要表现为突发头晕、站立不稳20 h 余,查体示眼球运动障碍,右侧共济失调,外院CT 示右侧小脑低密度灶,初步定位于右侧小脑,定性考虑脑梗死。NⅠHSS 评分4 分,患者既往高血压病史,无心源性因素,故考虑动脉粥样硬化的可能性大,入院即予阿托伐他汀40 mg qd po 强化治疗合理。
药物不良反应通常发生在开始使用药物后1~4 周内或再次使用相同药物。该患者入院时肝功能各项指标均正常,入院后使用阿托伐他汀第2 日出现ALT、AST、GGT、ALP、TBil、DBil、ⅠBil 显著增高,患者无饮酒史,追问病史,患者否认既往肝病病史及特殊用药史。临床药师查看患者既往病史,发现患者1 年多前也曾出现一过性肝功能不全,于服用阿托伐他汀9 d 后,出现ALT、AST、GGT、ALP 均显著上升,在停用阿托伐他汀改为瑞舒伐他汀后,肝功能指标逐渐改善。药师及时追溯可疑的用药史,用药及肝损伤发生的时间顺序合理,且1年后再次使用阿托伐他汀,再次出现DⅠLⅠ,且程度增加,判断患者此次肝损伤很可能系二次使用阿托伐他汀引起,建议医师停用阿托伐他汀,改为瑞舒伐他汀治疗,同时加用护肝药物。临床医师同意临床药师的建议,停药并保肝治疗2 d 后,患者ALT、AST 较前明显下降。实验室检查也排除病毒性肝炎可能。
根据指南,DⅠLⅠ基于受损靶细胞类型的分类判断标准[6]:①肝细胞损伤型:ALT ≥3 ULN,且R ≥5;②胆汁淤积型:ALP ≥2 ULN,且R ≤2;③混合型:ALT ≥3 ULN,AKP ≥2 ULN,且2 <R <5。若ALT和ALP 达不到上述标准,则称为“肝脏生物化学检查异常”。据此判断,本患者DⅠLⅠ的类型为肝细胞损伤型(表2)。按照因果关系评估量表(Roussel-Uclaf causality assessment method, RUCAM)[6],得12 分,判定此例患者肝损伤的发生与药物之间的因果相关性为“极可能”。
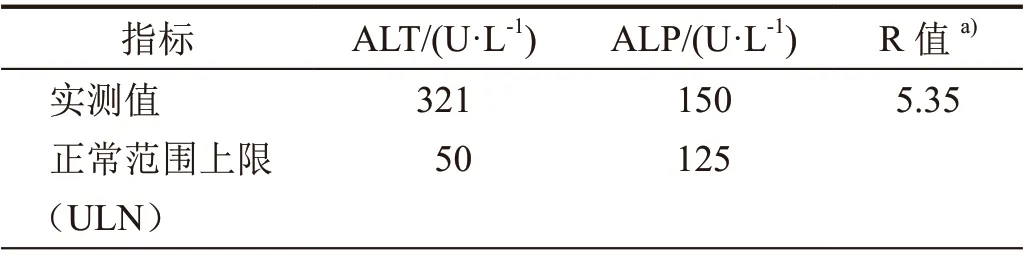
表2 患者DⅠLⅠ类型(肝细胞损伤型)
2.2 他汀类药物发生DⅠLⅠ的病因机制
首先,现有研究报道的DⅠLⅠ病因机制主要是遗传学因素,如药物代谢酶系、转运蛋白和人类白细胞抗原系统等的基因多态性及其表观遗传学特点[6]。SLCO1B1和ApoE基因的单核苷酸多态性(single nucleotide polymorphism, SNP)是药物代谢个体差异的分子基础,导致他汀类药物降脂疗效和毒副作用的个体差异,是明确的遗传学因素[7]。为了临床风险预测、疗效及预后评估,可对正在使用或考虑使用他汀类药物的患者进行SLCO1B1和ApoE基因多态性的检测。本患者入院第12日测得SLCO1B1基因表型为*1b/*1b(正常代谢型)、ApoE基因表型为ε3/ε3(大众类基因型),因此本例DⅠLⅠ不能用遗传学因素来解释。其次,患者65 岁,老年是他汀类药物引起DⅠLⅠ易感性的危险因素之一[8]。此外,药物的使用剂量和相互作用也是DⅠLⅠ不可忽视的危险因素。结合药品说明书及相关文献,本患者未发现药物间的相互作用。肝酶升高是他汀类药物最常见的不良反应,ALT 升高大于3 倍ULN 的发生率约0.5%~2.0%,多发生在开始用药后的3 个月内,存在剂量依赖性[9]。老年患者使用常规剂量的他汀类药物时,则较少发生ALT 异常;而在使用大剂量他汀类药物时,ALT 升高的发生率增高[9]。本例老年患者使用高强度阿托伐他汀可能出现较高的血药浓度,使药物不良反应增加。
截至目前,DⅠLⅠ发病机制复杂,尚未充分阐明。通常可归结为药物的直接肝毒性和特异质性肝毒性作用,其过程包括药物及其代谢产物导致的“上游”事件以及肝脏靶细胞损伤通路和保护通路失衡构成的“下游”事件[6]。药物的直接肝毒性是指摄入体内的药物和/或其代谢产物对肝脏产生的直接损伤,往往呈剂量依赖性,通常可预测,也称为固有型DⅠLⅠ[6],他汀类药物即属于这一类型[10]。阿托伐他汀广泛用于预防心血管疾病,如冠状动脉疾病和脑梗死,但其应用受到肝毒性的限制,肝酶升高和药物诱导的自身免疫性肝炎是其最常见的肝脏副作用[3]。
2.3 DⅠLⅠ的处理和建议
如果肝酶在3 倍ULN 以上,建议立即重测肝酶并检查肌酸激酶;如果这种肝酶升高的程度持续存在,他汀类药物应与其他潜在的肝毒性药物一起停用,同时进行全面评估以确定肝损伤的原因[11]。对于不能耐受他汀类药物的老年患者,可考虑以下三种方案:①更换不同种类的他汀类药物;②降低他汀类药物剂量;③隔日小剂量服用他汀类药物[9]。FDA 指南建议停止治疗的标准是[10]:ALT 或AST >8×ULN;ALT 或AST >5×ULN 超过两周;ALT 或AST >3×ULN 且(TBiL>2×ULN 或ⅠNR >1.5);ALT 或AST >3×ULN 伴随乏力、恶心、呕吐、右上腹疼痛或压痛、发热、皮疹和/或嗜酸性粒细胞增多(>5%)。本例患者服用阿托伐他汀1 d 后AST >8 ULN,根据国内外指南[6,10],均有立即停用阿托伐他汀的指征,同时可加用护肝药。炎症较重的轻至中度肝细胞损伤型DⅠLⅠ,可予双环醇和甘草酸制剂[5];多烯磷脂酰胆碱可使受损肝功能和酶活性恢复正常,促进肝细胞的再生,抑制肝细胞凋亡,调节肝脏的能量代谢,具有减少氧化应激与脂质过氧化,降低炎症反应和抑制肝星状细胞活化、防治肝纤维化等功能,从多个方面保护肝细胞免受损伤[12]。本患者予“双环醇片、多烯磷脂酰胆碱注射液、复方甘草酸苷注射液”护肝治疗,甘草酸类制剂和抗氧化剂分别作用于炎症因子产生前、后的各阶段,两药合用一方面可减少炎症因子的继续产生,避免肝损伤的进一步加重;另一方面可中和已产生的炎症因子,减轻已造成的损伤。抗炎类(甘草酸制剂等)与细胞膜保护剂(多烯磷脂酰胆碱等)联用可从不同作用位点起到保肝作用[12]。对于发生肝酶或肌酶升高的患者,应重新评估他汀类药物的获益/风险,决定是否继续使用。若需继续应用他汀类药物,可更换品种或调整剂量[9]。患者由于脑卒中病情需要,仍需使用他汀类药物进行二级预防,故将其改为瑞舒伐他汀继续调脂稳斑,并从小剂量5 mg 开始,与此同时,密切监测肝功能。本例患者既往曾出现可疑DⅠLⅠ,未予重视和深入探究。因此,为减少药物不良反应的发生,应详细询问患者的病史及既往用药史,尤其是老年人。
3 结语
阿托伐他汀诱发的DⅠLⅠ并不少见,更不应忽视。本文就1 例二次脑卒中患者使用阿托伐他汀出现的DⅠLⅠ进行探讨,结合国内外相关文献,分析其原因及处理措施,旨在提高临床药师药学实践的探究性思维,以体现临床药师药学服务价值。临床药师结合患者的用药史、过敏史以及不良反应史进行密切的药学监护,为临床安全用药提供保障。
