双胎妊娠孕妇妊娠期甲状腺功能指标参考区间的探讨研究
2022-07-30张超龙燕付溪娜
张超,龙燕,付溪娜
妊娠合并甲状腺功能异常可引起流产、早产、胎盘早剥等不良妊娠结局[1],影响胎儿神经系统发育,导致子代智力、体格发育落后[2]。双胎妊娠孕妇甲状腺功能受胎盘分泌激素的影响,促甲状腺激素(thyroid stimulating hormone,TSH)水平低于单胎妊娠孕妇,而游离甲状腺素(free thyroxine,FT4)水平却高于单胎妊娠孕妇[3]。如采用单胎妊娠实验室检查标准判断双胎妊娠孕妇的甲状腺功能状况,可能导致妊娠合并甲状腺疾病的误诊和漏诊。因此,有必要建立适用于双胎妊娠孕妇甲状腺功能判断标准。本研究对妊娠期双胎健康孕妇的甲状腺功能及甲状腺过氧化物酶抗体(thyroid peroxidase antibody,TPOAb)进行了检测,分析妊娠期甲状腺功能的变化特点,建立其特异性的甲状腺功能指标参考范围,并对甲状腺功能异常在双胎妊娠中的患病情况进行探讨,旨在为双胎妊娠孕妇妊娠期甲状腺疾病的临床诊治提供参考。
1 资料与方法
1.1 一般资料 回顾性选取2009 年1 月至2019 年9月在首都医科大学附属北京友谊医院产科门诊行产前检查的双胎妊娠健康孕妇作为双胎组。
双胎妊娠健康孕妇需符合美国国家临床生化学会(National Academy of Clinical Biochemistry,NACB) 推荐的妊娠期“标准人群”的条件[3],包括:(1)妊娠期进行1 次及以上的甲状腺功能筛查;(2)TPOAb 水平在检测试剂生产厂家提供的参考范围内;(3)年龄20~40 岁;(4)妊娠6~9 周首次经超声确认为双胎妊娠,直至分娩为双活胎。
排除标准:有甲状腺疾病史(甲状腺肿大、甲状腺功能亢进或减退、甲状腺癌、甲状腺手术或放射性碘治疗史)及甲状腺疾病家族史;妊娠期服用治疗甲状腺疾病的药物;使用可能影响甲状腺功能的药物(如抗惊厥药、抗精神病药、糖皮质激素、多巴胺等);有心脏病史、慢性高血压、糖尿病、哮喘、炎症性肠病、肿瘤、肾脏疾病、肝脏疾病、自身免疫性疾病和结缔组织疾病等慢性疾病史;有血液传播疾病史;有妊娠相关并发症(包括妊娠期高血压、妊娠期糖尿病、早产或其他不良妊娠结局、滋养细胞疾病或晚期妊娠出血等);染色体异常或遗传综合征;辅助生殖术后;反复流产史;胎儿染色体或基因异常等。
回顾性选取同期在首都医科大学附属北京友谊医院产科门诊行产前检查的单胎妊娠健康孕妇作为单胎组。纳入标准:(1)年龄20~40 岁;(2)妊娠结局良好;(3)妊娠6~9 周首次经超声确认为单胎妊娠;(4)妊娠期进行1 次及以上的甲状腺功能筛查。排除标准同双胎组。
本研究经首都医科大学附属北京友谊医院伦理委员会审核通过(2001-1002-04)。
1.2 研究方法
1.2.1 资料采集 记录孕妇年龄、身高、体质量、妊娠前体质指数(BMI)、是否为初产。
1.2.2 实验室检查指标 采集孕妇清晨空腹肘静脉血3 ml 送至本院临床检验科进行检测。当日采用化学发光免疫法测定甲状腺功能指标(包括血清TSH、FT4、TPOAb 水平),TSH 和FT4测定使用美国贝克曼公司UnicelDxl 800 免疫分析系统和试剂盒,TPOAb 水平测定采用德国西门子全自动化学发光免疫分析仪(ADVID Centaur) 和试剂盒,各指标的批间变异和批内变异均<6%。生产厂家提供的TPOAb 参考范围为0~60、0~1 300 mU/L(2017 年以前试剂盒生产厂家提供的TPOAb 参考范围为0~60 mU/L;2017 年更换试剂盒,生产厂家提供的参考范围为0~1 300 mU/L)。
尿碘测定:收集两组孕妇清晨尿液5 ml,采取过氧化氢四甲基联苯胺氧化显色法测定尿碘。留取尿样的前1 d 嘱孕妇避免食用海带、紫菜等含碘较高的食物,连续测定3 d,记录平均值。妊娠孕妇尿碘参考范围为100~300 μg/L。
1.2.3 诊断标准 本研究以第2.5 百分位数(P2.5)和第97.5 百分位数(P97.5)为TSH 和FT4参考范围的下限和上限,以确定妊娠期甲状腺功能的参考区间。按照检测时的妊娠周期进行划分,妊娠早期:妊娠<12+6周,妊娠中期:妊娠13+0~27+6周,妊娠晚期:妊娠28+0周至分娩。如TSH<P2.5(总TSH),FT4>P97.5(总FT4)则诊断为临床甲状腺功能亢进(简称甲亢);TSH>P97.5(总TSH),FT4<P2.5(总FT4)则诊断为临床甲状腺功能减低(简称甲减);TSH>P97.5(总TSH),P2.5(总FT4)≤FT4≤P97.5(总FT4)则诊断为亚临床甲减;P2.5(总TSH)≤TSH ≤P97.5(总TSH),FT4<P2.5(总FT4)则诊断为低甲状腺素(T4)血症。TPOAb阳性定义为TPOAb>60 mU/L(2017 年前)和TPOAb>1 300 mU/L(2017 年及以后)。
1.3 统计学方法 采用SPSS 24.0 统计学软件进行数据分析。参考范围的测定采用 95%CI,正态性检验采用Kolmogorov-Smirnov 方法,服从正态分布的计量资料以(±s)表示,两组间比较采用成组t 检验;非正态分布的计量资料以 M(P2.5,P97.5)表示,组间比较采用秩和检验;计数资料以相对数表示,组间比较采用χ2检验。以P<0.05 为差异有统计学意义。
2 结果
2.1 基本信息 双胎组排除有甲状腺疾病史者6例,妊娠期服用治疗甲状腺疾病的药物者20例,TPOAb 水平高于参考范围上限者39例,其他疾病史及无甲状腺功能检测数据者69例,最终纳入352例孕妇。单胎组最终纳入988例孕妇。单胎组与双胎组年龄、尿碘、妊娠前BMI、初产妇所占比例比较,差异无统计学意义(P>0.05),见表1。

表1 双胎组和单胎组一般资料比较Table 1 Comparison of general data between singleton and twin groups
2.2 单胎组和双胎组不同妊娠周期时TSH 和FT4比较 双胎组孕妇妊娠早期TSH 低于单胎组,妊娠晚期TSH 高于单胎组,差异有统计学意义(P<0.05);两组孕妇妊娠中期时TSH比较,差异无统计学意义(P>0.05);双胎组孕妇妊娠早期、中期、晚期时FT4均高于单胎组,差异有统计学意义(P<0.05),见表2。

表2 双胎组和单胎组妊娠早期、中期、晚期TSH 和FT4 比较〔M(P2.5,P97.5)〕Table 2 Comparison of FT4 and TSH levels in the first,second and third trimesters of pregnancy between singleton and twin groups
2.3 双胎妊娠孕妇不同妊娠期甲状腺功能异常分布情况 分别以双胎、单胎妊娠孕妇TSH 和FT4总体数据的P2.5和P97.5为下限和上限标准,统计双胎妊娠孕妇妊娠早、中、晚期的甲状腺功能异常的患病情况,双胎妊娠孕妇不同妊娠期甲状腺功能异常患病率及累积患病率详见表3~6。
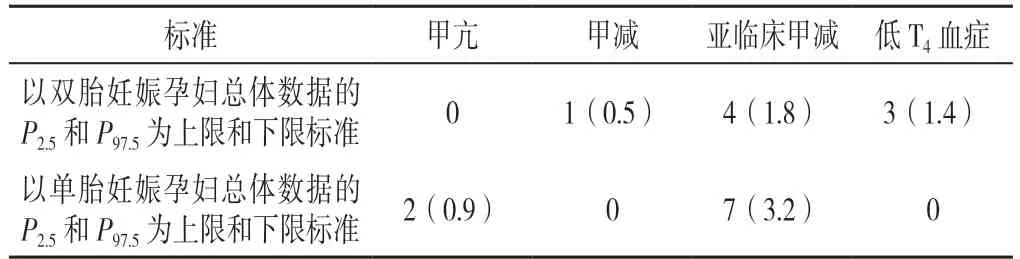
表3 双胎孕妇妊娠早期时不同诊断标准测得甲状腺功能异常的分布情况〔N=217a,n(%)〕Table 3 Distribution of thyroid dysfunction in the first trimester of pregnancy in twin pregnancy group by different diagnostic criteria

表4 双胎孕妇妊娠中期时不同诊断标准测得甲状腺功能异常的分布情况〔N=344b,n(%)〕Table 4 Distribution of thyroid dysfunction in the second trimester of pregnancy in twin pregnancy group by different diagnostic criteria

表5 双胎孕妇妊娠晚期时不同诊断标准测得甲状腺功能异常的分布情况〔N=177c,n(%)〕Table 5 Distribution of thyroid dysfunction in the third trimester of pregnancy in twin pregnancy group by different diagnostic criteria

表6 双胎孕妇妊娠期不同诊断标准测得甲状腺功能异常的分布情况〔N=352,n(%)〕Table 6 Distribution of thyroid dysfunction in the three trimesters of pregnancy in twin pregnancy group by different diagnostic criteria
3 讨论
3.1 妊娠期甲状腺功能生理性变化特点 妊娠期母体甲状腺功能受胎盘、下丘脑和垂体分泌激素的影响发生复杂的变化,主要表现在以下几个方面:(1)胎盘分泌大量雌激素,刺激肝脏合成球蛋白,血清甲状腺结合球蛋白明显升高,使妊娠早期血清总甲状腺素(TT4)升高,可达非妊娠妇女的1.5 倍;(2)胎盘分泌的人绒毛膜促性腺激素(human chorionic gonadotrophin,hCG)[4]可抑制垂体分泌TSH,且在妊娠8~10 周TSH下降至最低,妊娠12 周后逐渐恢复正常[3];(3)FT4一般在参考范围内,妊娠早期轻度升高,到妊娠中晚期较前下降[2]。本研究对352例双胎妊娠孕妇整个妊娠期甲状腺功能进行检测,结果显示TSH 和FT4变化符合上述特点。
3.2 妊娠期甲状腺功能参考范围的建立 多年来学术界对妊娠期甲状腺功能参考范围存在争议,随着相关临床研究提供了更多循证医学证据,国际有关内分泌学术团体对妊娠期甲状腺功能参考范围的建立标准不断进行修订。2007 年美国内分泌学会(the Endocrine Society,TES)曾推荐TSH 参考范围为妊娠早期≤2.5 mU/L,妊娠中期≤3.0 mU/L,妊娠晚期≤3.0 mU/L[5]。2011 年美国内分泌医师协会(American Association of Clinical Endocrinologists,AACE)指南及2017 年美国甲状腺学会(American Thyroid Association,ATA)指南均推荐,妊娠期特异性TSH 参考范围应定义如下:如有可能,应由开展研究的实验室确定妊娠期特异性TSH 参考范围(高质量的证据)[1],依据健康的TPOAb 阴性孕妇最佳的碘摄入量和没有甲状腺疾病的妊娠女性的数据来确定参考范围。当这一目标不可实现时,应从相似的患者人群中获得的妊娠期特异性TSH 参考范围和使用相似的TSH 测定法。如果没有内部或可借用的妊娠期特异性TSH 参考范围,可使用4.0 mU/L 作为妊娠早期和中期的参考范围上限[6]。目前国内关于双胎妊娠甲状腺功能参考范围的高质量、大规模研究较少,国内的指南中亦未提及关于双胎妊娠的参考范围[6],因此笔者对本院的双胎妊娠孕妇进行了相关研究,以期得到双胎妊娠孕妇甲状腺功能合理的参考范围。
妊娠第6 天滋养细胞开始分泌hCG 后,血清hCG水平即呈指数式增长,于妊娠第8~10 周时达峰值,持续约10 d 后迅速下降,至妊娠中、晚期,血清hCG水平仅为其峰值的10%[7]。与单胎妊娠相比,双胎妊娠第8~16 周时,完整和游离的β-hCG 的峰值均显著增高,且持续时间延长;一般血清hCG 水平每增高10 000 U/L,血清TSH 水平降低0.1 mU/L,整个妊娠期二者均存在联系[8]。由于hCG 急剧而持久的升高可能会导致TSH 水平下降,研究发现双胎孕妇出现TSH 水平显著下降的情况是单胎孕妇的3 倍[3]。这些发现解释了为何双胎妊娠孕妇的TSH 中位数低于单胎妊娠孕妇。在临床实践中,使用单胎妊娠的参考范围来评估双胎妊娠的甲状腺功能可能会导致甲亢和亚临床甲减的过度诊断。此外,如果使用不适当的抗甲状腺药物治疗,可能会导致孕妇白细胞减少和肝功能障碍及后代畸形。因此,建立评估双胎妊娠孕妇甲状腺功能的具体参考范围是有必要的[6]。本研究结果显示,双胎妊娠早期孕妇TSH 的中位数明显低于单胎妊娠早期孕妇,与相关文献报道一致[3]。
3.3 妊娠期甲状腺功能异常患病率评估 按照双胎妊娠甲状腺功能指标的参考区间计算,本院双胎孕妇妊娠期甲亢的患病率为0,有研究报道双胎孕妇妊娠期甲亢患病率为0.02%~0.50%[2,6],本研究结果低于相关研究报道;本研究中双胎孕妇妊娠期甲减的患病率为0.28%,美国孕妇妊娠期甲减的患病率为0.3%~0.5%[2],2019 年《妊娠和产后甲状腺疾病诊治指南(第2 版)》[6]报道中国妊娠期甲减的患病率为1.0%,本研究结果与上述结果相似;本研究中双胎孕妇妊娠期亚临床甲减的患病率为4.83%,有研究报道孕妇妊娠期亚临床甲减的患病率为2%~3%[2],本研究结果略高于上述研究结果。而按照单胎妊娠甲状腺功能的参考区间计算,本院双胎孕妇妊娠期甲亢的患病率为8.24%,明显高于文献报道,甲减的患病率为0,亚临床甲减的累积患病率为15.91%,明显高于文献报道。如以4.0 mU/L 作为TSH参考区间上限进行计算,则甲减及亚临床甲减的总患病率为11.36%(40/352),明显高于文献报道[2]。可以看出无论是以单胎参考区间或以TSH 上限4.0 mU/L 为参考区间为标准应用于双胎妊娠孕妇甲状腺功能的诊断,均导致亚临床甲减孕妇增多,从而导致一些孕妇被过度诊断,增加孕妇的思想负担,使孕妇可能接受不必要的药物治疗。此外各个实验室检查所采用的分析方法不同也会造成结果出现差异,实现分析方法国际标准化将有助于减少这种差异[9]。
3.4 潜在偏倚 由于本研究中双胎妊娠孕妇的例数有限,且存在一定的缺失数据,可能造成一定的偏倚,需要进一步、更大规模的研究。
综上所述,双胎妊娠孕妇妊娠早期、中期、晚期FT4均高于单胎妊娠孕妇,而TSH 不同,妊娠早期TSH低于单胎妊娠孕妇,随着妊娠周期增长TSH 水平升高,至妊娠晚期,双胎妊娠孕妇TSH 高于单胎妊娠孕妇。以双胎妊娠特异性甲状腺功能指标的参考范围为标准,双胎孕妇妊娠期甲状腺功能异常以亚临床甲减最常见,若以单胎妊娠参考范围为评定标准,则将造成双胎妊娠孕妇甲状腺功能异常尤其是甲亢和亚临床甲减的过度诊断,因此建议有条件的实验室建立双胎妊娠甲状腺功能指标在本实验室的特异性参考范围。
作者贡献:张超负责数据收集、论文起草、统计学分析、绘制图表等,负责最终版本修订,对论文整体负责;龙燕负责进行研究的调查与设计;付溪娜协助数据收集。
本文无利益冲突。
