DTC 患者131I 治疗后左甲状腺素钠片最佳初始剂量预测模型探究
2022-07-28岳园芳刘建井尹国戴东徐文贵
岳园芳 刘建井 尹国 涛 戴东 徐文贵,
1 天津市肿瘤医院空港医院核医学科,天津 300308;2 天津医科大学肿瘤医院分子影像与核医学诊疗科,国家肿瘤临床医学研究中心,天津市肿瘤防治重点实验室,天津市恶性肿瘤临床医学研究中心,天津 300060
近年来,DTC 的发病率呈逐年上升趋势,虽然其预后相对较好,但仍有30%左右的患者会出现复发,其病死率也呈上升态势,因此,给予患者及时且规范的治疗十分必要[1]。TSH 抑制治疗是DTC 治疗方案中不可或缺的环节,其可以有效地降低患者复发和病死的风险,提高患者的生存率、改善生存质量[2]。国内外指南皆推荐TSH 抑制治疗药物首选左甲状腺素(levothyroxine,L-T4)口服制剂,推荐剂量为1.5~2.5 μg/(kg·d),并指出起始剂量视年龄及伴随疾病而异[3-4]。由于指南对L-T4最佳初始剂量并没有较为明确的标准,在临床工作中,医师往往根据个人经验决定,这导致很多患者经历较长的调药周期后TSH 水平才能达标。调药周期过长会给患者带来一定的不良反应,如L-T4剂量不足会导致患者的甲状腺功能减退,造成患者乏力、嗜睡、水肿、血脂异常,甚至会增加肿瘤复发的风险等[5-6];L-T4 剂量过大会加重患者心血管系统的负担,引起心绞痛或心律失常,加重绝经期女性的骨质疏松,进而增加其骨折风险等[7-8]。综上,构建DTC 患者131I 治疗后L-T4 最佳初始剂量的预测模型,对于提高患者生活质量、改善预后都具有重要的临床意义。然而,截至目前尚未发现国内外有相关研究和文献报道。
本研究运用机器学习的方法为131I 治疗后的DTC 患者构建预测左甲状腺素钠片(优甲乐)的最佳初始剂量模型,提高首次达标率,有效缩短调药周期,以期减轻患者的经济负担,提高其生存质量,改善预后。
1 资料与方法
1.1 一般资料
回顾性分析2019 年11 月至2020 年11 月天津市肿瘤医院空港医院核医学科收治的266 例DTC 患者的临床资料,其中男性78 例(男性组)、女性188 例(女性组),年龄18~70(40.0±11.5)岁。纳入标准:接受131I 治疗并行TSH 抑制治疗且最终达标的患者。依据2015 年美国甲状腺协会指南,131I 治疗后TSH 抑制治疗的达标标准:TSH<0.1 mU/L(高危患者)、TSH 0.1~0.5 mU/L(中危患者),且游离T3、T4在正常范围即为达标[3]。排除标准:存在影像学检查结果证实的转移病灶;年龄<18 周岁;术后一年内妊娠;合并严重心脑血管疾病或严重肝肾功能损害。
所有患者均于治疗前签署了知情同意书。本研究符合《赫尔辛基宣言》的原则。
1.2 资料收集
收集临床、生化指标共16 项,包括年龄、性别、身高、体重、体表面积(body surface area,BSA)、体重指数(body mass index,BMI)、是否合并消化系统疾病(慢性胃炎或肝胆疾病等)、是否绝经、收缩压/舒张压、血红蛋白(hemoglobin,HB)、平均红细胞体积(mean corpuscular volume,MCV)、术后甲状旁腺激素水平、是否合并桥本氏甲状腺炎、是否合并心脑血管疾病、是否有肿瘤家族史、是否合并其他肿瘤病史。所有患者TSH 抑制治疗选择的药物均为左甲状腺素钠片,左甲状腺素钠片初始剂量的制定采取经验性给药的方式,即BMI 在正常范围内按100 μg/d 给药;超出正常范围即按1.5~2.2 μg/(kg·d)给药,老年患者适当减量。出院后患者按照推荐剂量规律服药4~6 周后复查甲状腺功能,医师根据复查结果调整左甲状腺素钠片剂量,直至TSH 水平达标。随访的相关信息通过查阅患者门诊病历及电话随访的方式收集。
1.3 特征筛选
首先,通过随机森林模型确定每个基线临床特征的重要度(数值越大,重要度越高);然后以整个数据集为基础,构建并训练另一个包含所有基线临床特征的随机森林模型,记录袋外均方误差;之后每次剔除重要度最低的基线临床特征,重新训练模型,记录袋外均方误差;最后,选择袋外均方误差最小的基线临床特征组合。由于随机森林模型构建过程中具有一定的随机性,我们进行了10 次筛选,将10 次筛选中均出现的基线临床特征用于回归模型的构建。
1.4 筛选最佳回归模型
以筛选出的指标为自变量,以左甲状腺素钠片达标剂量为因变量构建多种回归模型,包括线性回归、泊松回归、随机森林回归、使用径向基核的支持向量回归(support vector regression, SVR)、岭回归、套索回归、K 近邻回归、伽马回归。由于数据量有限,构建回归模型采用5 折交叉验证。规定左甲状腺素钠片预测剂量与达标时剂量差值的绝对值<12.5 μg 为预测正确,然后通过交叉训练验证选取预测准确率最高的回归模型。
1.5 统计学方法
应用SPSS 26.0 软件进行统计学分析。符合正态分布的计量资料以±s表示。计数资料的组间比较采用独立样本的卡方检验。P<0.05 为差异有统计学意义。所有临床特征的筛选及回归模型的构建均使用基于Python 3.7.6 的scikit-learn 0.23.2 软件(https://scikit-learn.org/stable)。
2 结果
2.1 患者的一般资料分析
266 例DTC 患者中,绝经女性45 例(16.9%);合并桥本氏甲状腺炎71 例(26.7%);合并心脑血管疾病27 例(10.2%),主要包括高血压、糖尿病、冠心病、脑梗死、心律失常等;存在慢性胃炎或肝炎等19 例(7.1%);合并其他肿瘤病史5 例(1.9%),分别为乳腺癌2 例、肾癌1 例、肺癌1 例、子宫内膜癌1 例;存在肿瘤家族史22 例(8.3%),其中存在甲状腺癌家族史6 例(2.3%)。此外,266 例患者的体重、身高、BMI、BSA、HB、MCV、收缩压/舒张压、术后甲状旁腺激素、达标时左甲状腺素钠片剂量分别为(68.4±12.9) kg、(165.8±12.8) cm、24.6±3.5、(1.9±0.2) m2、(140.1±19.1) g/L、(88.6±5.5) fl、(125.7±18.9) mm Hg/(82.7±12.4) mm Hg、(4.1±2.2) pmol/L、(117.0±30.1) μg/d。随访时间为(4.79±3.09)个月,无失访者。通过查阅门诊复查信息及电话随访结果,采取经验给药的266 例患者出院后第1 次复查结果显示,仅有40 例无需调整左甲状腺素钠片剂量,即首次达标率为15.0%。
2.2 筛选重要临床特征
经过特征筛选发现,重要度排在前6 位的临床特征依次为BSA、体重、HB、身高、BMI、年龄。其重要度均数依次为0.2805、0.1951、0.1315、0.1252、0.1080、0.0819。
2.3 不同回归模型预测左甲状腺素钠片剂量准确率的比较
套索回归、K 近邻回归、岭回归、随机森林回归、伽马回归、泊松回归、线性回归、SVR 模型预测左甲状腺素钠片剂量的准确率依次为35.3%(94/266)、44.0%(117/266)、46.6%(124/266)、47.7%(127/266)、48.1%(128/266)、48.5%(129/266)、48.9%(130/266)、53.4%(142/266)。SVR 模型预测左甲状腺素钠片剂量与真实剂量的分布如图1 所示,灰色区域内为预测正确者。

图1 266 例分化型甲状腺癌患者支持向量回归模型预测左甲状腺素钠片剂量与真实剂量分布图Figure 1 The distribution of actual and predicted levothyroxine sodium tablet dose by support vector regression model in 266 differentiated thyroid cancer patients
2.4 不同性别组SVR 模型预测左甲状腺素钠片剂量准确率的比较
SVR 模型在男性组和女性组中的预测准确率分别为35.9%(28/78)和60.6%(114/188),且两者之间的差异有统计学意义(χ2=13.51,P<0.001)。这提示该模型对女性患者的预测效能更好。SVR 模型在男性组、女性组中预测左甲状腺素钠片剂量与真实剂量分布情况如图2 所示,灰色区域内为预测正确者。
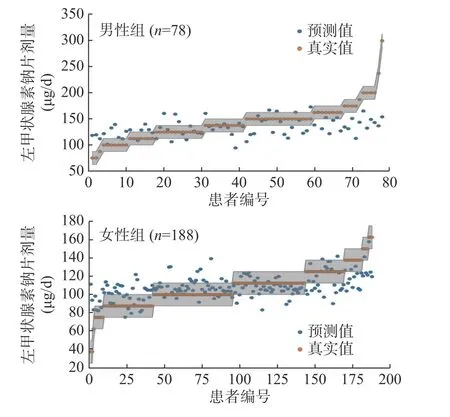
图2 不同性别分化型甲状腺癌患者支持向量回归模型预测左甲状腺素钠片剂量与真实剂量分布图Figure 2 The distribution of actual and predicted levothyroxine sodium tablet dose by support vector regression model in different gender group of differentiated thyroid cancer patients
3 讨论
相关研究结果证实,许多因素与甲状腺疾病患者术后所需的L-T4 剂量相关,如年龄、体重、去脂体重、身高、药物的吸收情况、雌激素水平等[9-13]。上述大部分指标反映了机体的代谢水平,影响给予患者的L-T4 剂量。Liwanpo 和Hershman[13]指出,所有影响胃酸分泌的消化功能障碍疾病(如慢性胃炎或肝胆疾病)均会降低机体对L-T4 的吸收率。女性是否绝经即雌激素水平也会影响L-T4 在体内的代谢情况[12]。从以上研究结果可知,患者所需L-T4 剂量与多种因素相关,美国甲状腺协会指南推荐的仅基于体重确定的剂量参考区间在临床实践中的指导意义不足。
近年来,随着医疗大数据的迅猛发展,越来越多的机器学习算法开始被应用于医疗领域中,机器学习在处理较为复杂的问题上有较好的准确率和泛化能力。机器学习是通过一些可以让计算机自动“学习”的算法,从我们提供的数据中分析获得规律,然后利用规律对新样本进行预测。因此,我们可以利用机器学习的方法从回顾性数据中寻找与L-T4 剂量相关的指标,建立并训练回归模型,通过交叉训练验证其准确率。其实,国外已有多篇关于预测TSH 替代治疗的L-T4 初始剂量的公式或模型的报道[14-16]。Zaborek 等[15]曾筛选出7 项相关因素(年龄、性别、体重、BMI、术前TSH 水平、是否服用铁剂、是否服用复合维生素)并运用机器学习方法为甲状腺全切患者构建多种回归模型来预测L-T4 的最佳初始剂量,该研究得出泊松回归模型的准确率最高(64.8%),并证实与既往文献报道的只基于年龄、体重或BMI 计算出的准确率相比,其准确率显著提高;但遗憾的是,该研究的对象是良性甲状腺疾病患者,这些患者甲状腺全切术后仅需要TSH 替代治疗,而替代治疗所需的L-T4剂量明显低于DTC 患者TSH 抑制治疗所需的剂量,并且由于人种差异,此模型并不适用于中国人。而国内目前仅有1 项针对DTC 患者术后初始L-T4 剂量的研究[17],但其主要研究对象是DTC 术后患者,并非131I 治疗后的患者。由于131I治疗进一步清除了DTC 患者术后少量残存甲状腺组织,因此患者对L-T4 的需求量也相应增加,故该研究的模型不适合接受过131I 治疗的DTC 患者;其次,该研究纳入的病例数及筛选出的相关指标较少(只有年龄和BMI),应用的左甲状腺素钠片(雷替斯)在临床中的使用率明显低于本研究使用的左甲状腺素钠片(优甲乐),采用的数据分析方法是单一的Logistic 回归,因此该研究对临床的应用价值也比较局限。
本研究共纳入16 项临床、生化指标,通过计算随机森林特征重要度筛选出6 项较为重要的特征,依次为BSA、体重、HB、身高、BMI、年龄。其中BSA、体重、身高、BMI 及年龄均反映了患者的基础代谢率,这与先前多篇文献报道的内容一致[12-15],但关于HB 这项指标尚未有文献报道。Di 等[14]发现,MCV 与L-T4 剂量呈负相关,其基于Liwanpo 和Hershman[13]的观点(L-T4 的吸收依赖于机体的胃酸水平)猜测铁的吸收同样依赖于胃酸水平,而MCV 间接反映了体内铁的水平,因此两者存在相关性。在本研究中,我们发现HB 的重要度明显高于MCV,这其中的原因并不清楚,仍需进一步探究。本研究构建并训练出8 种回归预测模型,通过交叉训练的方式验证出SVR模型的准确率最高。SVR 模型采用结构风险最小化原则和核函数思想,将低维空间的非线性问题转化成高维空间的线性问题,能够较好地解决小样本、高维数、非线性等问题。本研究在随访过程中发现266 例患者出院后第1 次复查(4~6 周)左甲状腺素钠片剂量达标的仅有40 例,显然经验给药的达标率明显低于SVR 模型的准确率(15.0%对53.4%)。随后,我们根据患者性别进行比较,结果显示女性组的准确率明显高于男性组(60.6%对35.9%),这提示该模型对女性患者更适用。分析原因可能与本研究纳入的女性患者例数明显多于男性,因此构建的模型准确率更偏倚于女性患者有关,这需要我们进一步去研究。
本研究为回顾性研究,纳入的病例数较少,且由于影响左甲状腺素钠片最佳剂量的因素比较庞杂,本研究纳入的临床指标可能不够全面,虽然通过交叉验证初步证实了SVR 模型的准确率明显高于经验给药,但我们目前尚缺乏前瞻性的研究进一步验证,可能有一定的误差或偏倚。下一步我们将对此模型进行前瞻性验证,若首次达标率明显高于经验给药,即可在此基础上开展多中心临床试验进行外部验证,若研究结果理想可将此模型加以推广,甚至形成行业共识,进而使广大的甲状腺癌患者获益。
利益冲突 所有作者声明无利益冲突
作者贡献声明 岳园芳负责研究过程的实施、数据的采集与统计、论文的撰写;刘建井负责命题的完善、数据的分析、论文的修订;尹国涛负责数据的统计分析;戴东负责论文的修订;徐文贵负责命题的提出、论文的审阅
