肝细胞癌射频消融术后疗效的MRI评价
2022-07-27明志强曹金明陈天武吴玉平杨丽芹高丹
明志强,曹金明,陈天武,吴玉平,杨丽芹,高丹
原发性肝癌是全球常见恶性肿瘤,2018 年发病率居全球癌症第6 位,死亡率居第4 位[1]。目前我国原发性肝癌发病率居恶性肿瘤第4 位,死亡率居第2 位,其中原发性肝细胞癌(hepatocellular carcinoma,HCC)占85%~90%[2-3]。
射频消融(radiofrequency ablation,RFA)是一种利用射频热效应使肿瘤组织发生凝固性坏死的治疗方法,在临床上应用广泛,RFA 对小肝癌的治疗与外科手术切除疗效相近[4-6]。但HCC经RFA术后仍然存在肿瘤残余、局部肿瘤进展及新发肿瘤的风险。因此,对HCC经RFA治疗后疗效的及时准确评价非常重要。影像学评价方法以CT、MRI 及其功能成像、超声为主。但超声易受肠道气体、呼吸运动及操作者经验等因素的影响,CT 对术后少许肿瘤残余及早期局部肿瘤进展敏感度并不高,而MRI 凭借其较高的软组织分辨力及多参数成像的优势,被认为是评价HCC 经RFA 术后疗效的有效手段,但未见MRI 对其术后疗效具体评价效果的研究报道,特别是缺乏对HCC 经RFA 术后不同疗效结果的全面评价,针对HCC 经RFA术后最佳影像学评价方法和时机尚无统一标准[7-8]。本研究回顾性分析了HCC 患者接受RFA 术前、术后系列随访MRI 平扫、多期增强和扩散加权成像(diffusion weighted imaging,DWI)图像资料,首次全面评价HCC 经RFA 术后不同疗效结果,为临床判定HCC 经RFA 术后疗效并制订下一步治疗方案提供客观的影像学依据。
1 资料与方法
1.1 临床资料
本回顾性研究获得川北医学院附属医院伦理委员会批准,免除受试者知情同意,批准文号:2021ER(A)021。本研究回顾性分析川北医学院附属医院2018年1月至2021年6月收治的52 例HCC 患者(共60 个病灶) RFA 术前、术后随访的系列MRI 资料。本研究队列中,男42 例、女10 例,年龄30~78 岁,平均年龄54.1岁;病灶最大径1.30~4.95 cm,平均3.57 cm;术前AFP≥400 μg/L者共44例,AFP<400 μg/L者共8例。
1.2 纳入标准及排除标准
纳入标准:(1)符合《原发性肝癌诊疗规范(2019年版)》中的HCC诊断标准[3];(2)符合《影像引导肝脏肿瘤热消融治疗技术临床规范化应用专家共识》中RFA治疗完全消融适应证范围[9],包括单发肿瘤,最大径≤5 cm或多发(数目≤3个)肿瘤,最大径≤3 cm;(3)无RFA治疗禁忌证(如肝功能为Child-Pugh C级、无法纠正的凝血功能障碍)。排除标准:(1)图像质量太差,病灶显示不清楚;(2)未按指南要求进行随访或随访资料不全者;(3) RFA术后随访期间行放化疗治疗者。
1.3 RFA治疗方式
在超声引导下对HCC行RFA治疗,RFA范围,要求超过肿瘤边缘0.5~1.0 cm,以达到充分消融的要求[9]。
1.4 随访方案
所有纳入病例经RFA 术后,均按照《影像引导肝脏肿瘤热消融治疗技术临床规范化应用专家共识》进行规范随访,随访方案如下:(1) HCC 经RFA 术后首次随访在术后7 天内完成;术后前3 个月,每月行肝脏MRI 平扫、多期增强及DWI 扫描,肿瘤标志物检查,若结果阴性,则在术后3 个月后每间隔3 个月重复上述检查;(2)若术后任何一次随访,发现肿瘤残余、局部肿瘤进展及新发肿瘤中的一种或多种情况,有消融指征者再予消融,之后按(1)中的方案重新随访;若无消融指征,则采取其他疗法治疗[9]。
在每一次随访中,若肝脏MRI 检查、肿瘤标志物检查结果均为阴性,即肝脏MRI 检查未发现活性肿瘤[10];血清AFP<400 μg/L,则认为此次检查结果为阴性。若上述两项检查中,任何一项检查出现阳性结果,即肝脏MRI 检查发现活性肿瘤征象或血清AFP≥400 μg/L,由病理学活检和/或综合AFP检查、对系列影像学检查进行对比以综合判断[11]。本组病例按前述随访方案,随访时间6~42个月。
1.5 检查方法
使用GE Discovery MR 750 3.0 T 磁共振扫描仪,上腹部三十二通道相控阵线圈。所有病例每次检查前6 h 禁食,并在检查前行呼吸训练后,再行上腹部MRI 平扫、DWI 及多期增强扫描。常规扫描序列与参数如下:(1)横轴位T1WI (TR 4 ms、TE 2 ms)与脂肪抑制T2WI (TR 6316 ms、TE 73 ms),层厚4 mm,层间距1 mm,视野(field of view,FOV) 32 cm×32 cm;(2) DWI 扫描采用轴位扫描,用单次激发平面自旋回波序列,b值400、600、800、1000 s/mm2,FOV 32 cm×32 cm,矩阵192×192,TR 4600 ms,TE 81 ms,层厚4 mm,层间距1 mm,激励次数(NEX) 3 次;(3)多期增强扫描,使用高压注射器通过肘静脉团注钆喷酸葡胺注射液(马根维显,拜耳医药,德国),注射剂量0.2 mmol/kg 体质量计算,注射速度2~3 mL/s,注射后用10~20 mL 生理盐水冲管,分别于注入对比剂后18 s 采集动脉早期图像,25 s 采集动脉晚期图像,60 s 采集门静脉期图像,180 s采集平衡期图像,扫描参数:TR 4 ms,TE 2 ms,层厚3 mm,FOV 36 cm×36 cm。
1.6 图像分析
由两名具备10 年以上工作经验的放射诊断主治医师分别对MRI图像进行分析,若出现意见分歧,由另一名具备20年以上工作经验的放射诊断主任医师参与分析,三人共同商讨达成一致。
1.6.1 MRI观察指标
本研究以HCC 经RFA 术前、术后系列随访MRI 影像资料为基础,参照《影像引导肝脏肿瘤热消融治疗技术临床规范化应用专家共识》,对HCC 经RFA 术后疗效分以下4 种情况进行观察评价:(1)完全消融:术后首次MRI随访提示肿瘤消融区无活性肿瘤且肿瘤边缘充分消融;不完全消融的情况包括肿瘤残余或消融区无肿瘤残余但肿瘤边缘未充分消融。MRI 评价肿瘤边缘是否充分消融的方法,将RFA术前MRI检查图像与术后第一次MRI 检查图像进行同序列同期相逐层对比,观察病灶大小及边界,判定是否达到充分消融;(2)肿瘤残余:术后首次MRI随访表现为消融范围没有完全覆盖术前肿瘤范围,消融区存在活性肿瘤;(3)局部肿瘤进展:肿瘤消融后首次随访MRI判定为无肿瘤残余的消融区内,在随后任何一次MRI 随访中发现活性肿瘤;(4)新发肿瘤:肿瘤消融后任何一次MRI随访发现消融区以外的肝实质内出现活性肿瘤[9]。
1.6.2 活性肿瘤的MRI判断标准
活性肿瘤的MRI 判断标准参照《2010 年修改后的实体瘤疗效评价标准》[10],当MRI增强扫描动脉期消融区出现偏心、散在、结节状不规则强化,或在消融区外其余肝实质内出现结节状强化灶,门静脉期及平衡期强化消退并低于周围肝实质强化程度,同时结合平扫T1WI呈稍低信号、T2WI呈稍高信号、高b 值DWI 显示水分子扩散受限呈高信号,即认为有活性肿瘤存在。
1.6.3 肿瘤RFA术后疗效真实结果的判断标准
当怀疑消融区存在肿瘤残余、局部肿瘤进展和/或肝内新发肿瘤时,穿刺活检是确诊的唯一金标准,但在临床实际工作中,往往达不到对每一个可疑活性肿瘤病灶均行穿刺活检。对于没有行穿刺活检的病灶,本研究采取综合影像学(RFA 术前与术后系列随访MRI、术中超声)及RFA 术前与术后系列随访AFP 检查指标进行判断[11-13]。若连续影像学随访显示病灶进一步增大,AFP持续升高,则认为有活性肿瘤存在,再结合前述《影像引导肝脏肿瘤热消融治疗技术临床规范化应用专家共识》,判定其为肿瘤残余、局部肿瘤进展还是新发肿瘤。关于完全消融真实结果的判定,不可能采用病理学金标准来研判,而以RFA 术中超声显示肿瘤区域已全部被消融为参考,将RFA术后第一次随访MRI与术前的图像逐层对照,也显示出肿瘤区域已全部消融,且覆盖消融前病灶边缘外0.5~1.0 cm的癌旁组织,并在随后的随访MRI 也呈现相似的征象,以验证RFA术后第一次随访MRI诊断为肿瘤完全消融的准确性。
1.7 统计学分析
本研究中HCC 经RFA 治疗后完全消融、肿瘤残余、局部肿瘤进展、新发肿瘤系计量资料,其中完全消融、肿瘤残余、局部肿瘤进展用病灶数目进行统计,对于新发肿瘤用患者数结合病灶数进行统计。MRI 对完全消融、肿瘤残余、局部肿瘤进展及新发肿瘤检测的敏感度、特异度、阳性预测值(positive predictive value,PPV)、阴性预测值(negative predictive value,NPV)及准确率,用诊断性实验方法进行计算。数据用SPSS 22.0 统计学软件包进行统计分析,并采用Kappa 检验其与真实结果的一致性。P<0.05表示差异有统计学意义。
2 结果
本组52 例HCC 患者60 个病灶,结合病理和RFA 术后系列随访资料,对于完全消融(图1)、肿瘤残余(图2)、局部肿瘤进展(图3)和新发肿瘤(图1)的统计结果见表1。被确认为有肿瘤残余的9例患者11个病灶中,有6例患者8个病灶行二次消融治疗后证实无肿瘤残余,其余3例患者3个病灶行外科手术切除,后者不再纳入后续随访研究,故后续MRI 随访研究纳入共49例患者57个病灶。
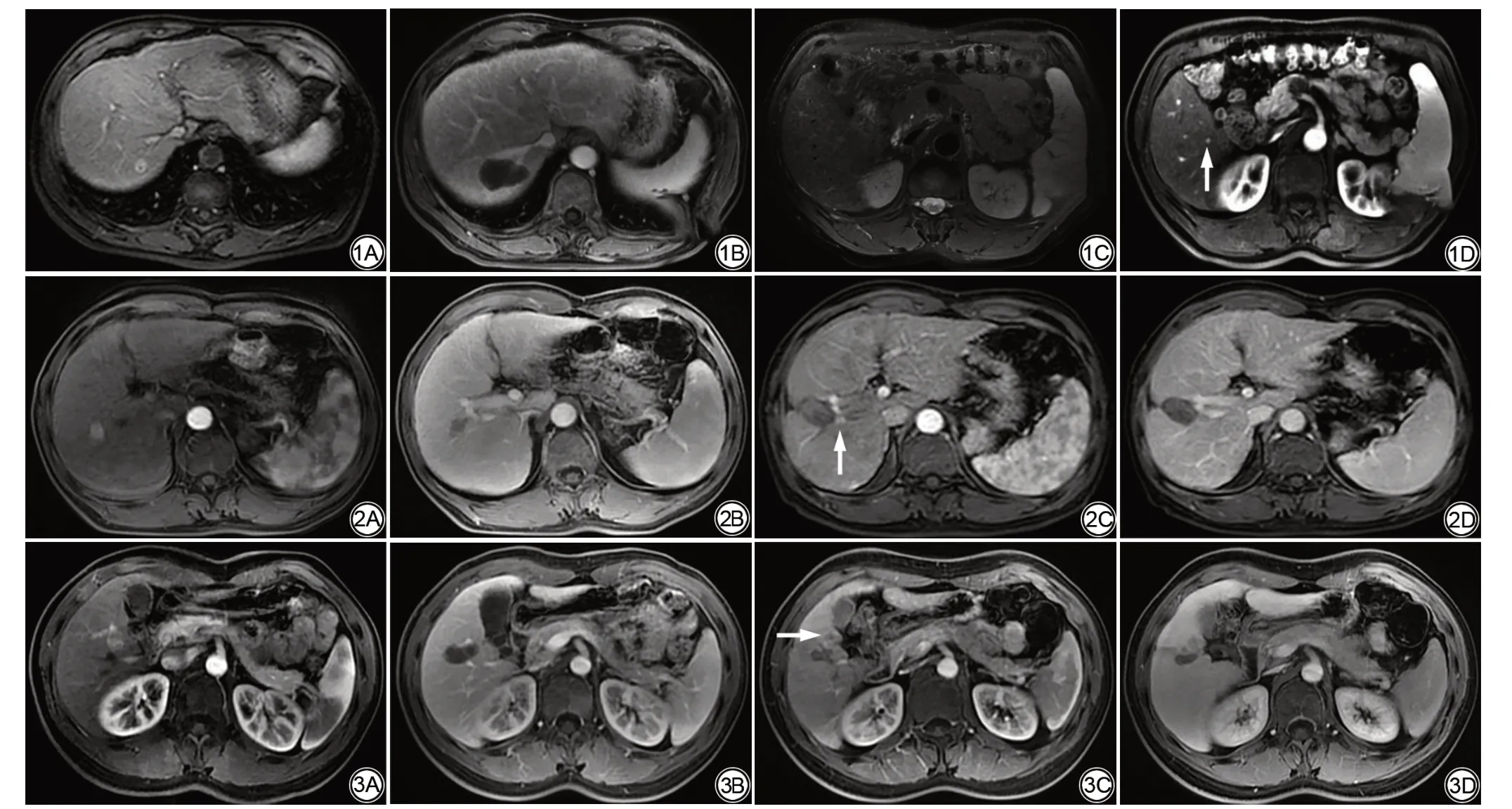
图1 男,59 岁,射频消融术后完全消融及新发肿瘤。肝右叶后上段小肝癌,最大径约1.3 cm,射频消融术前3 d 行MRI 检查,增强扫描动脉晚期明显强化(1A)。术后2个月随访MRI,完全消融区增强扫描平衡期(1B)未见异常强化,消融区完全覆盖术前肿瘤范围且肿瘤边缘充分消融;此时肝右叶后下段另见一小结节,最大径约0.5 cm,压脂T2WI 呈稍高信号(1C),增强扫描动脉晚期明显强化(1D,箭)。 图2 男,55 岁,射频消融术后肿瘤残余。肝右前叶HCC,最大径约2.2 cm,射频消融术前5 d行MRI检查,增强扫描动脉早期明显强化(2A),门静脉期强化消退(2B)。射频消融术后3 d,术后首次MRI随访,增强扫描动脉晚期明显强化(2C,箭),平衡期强化消退(2D),病理证实为HCC 消融后肿瘤残余。 图3 男,32岁,射频消融术后局部肿瘤进展。肝右叶前下段HCC,最大径约1.6 cm,射频消融术前3 d 行MRI检查,增强扫描动脉早期明显强化(3A)。射频消融术后2 d,术后首次MRI随访,增强扫描门静脉期(3B)示消融区完全覆盖术前肿瘤范围,消融区未见肿瘤残余,但肿瘤边缘未达到充分消融。射频消融术后30 个月MRI随访,增强扫描动脉晚期明显强化(3C,箭),平衡期强化消退(3D)。
2.1 完全消融及肿瘤残余
本组52 名患者60 个病灶中,表1 显示术后第1 次随访MRI,表中19 个不完全消融的病灶中包含11 个病灶存在肿瘤残余和8 个病灶无肿瘤残余但消融边界不充分。被确认为肿瘤残余的11 个病灶,均得到病理证实。另有4 个病灶MRI 怀疑存在肿瘤残余,经穿刺活检证实无肿瘤残余,系MRI误诊。
2.2 局部肿瘤进展及新发肿瘤
表1 中被确认为有局部肿瘤进展的13 个病灶均为RFA 术后首次随访确认为无肿瘤残余的病灶,在随后的随访中于消融区再次发现活性肿瘤,其中11 个病灶得到穿刺病理证实,另2 个病灶由综合消融后第二次及之后的系列随访MRI、AFP检查判断,予以确认。有3 个病灶MRI 提示存在局部肿瘤进展,其中2 个行穿刺活检证实为无局部肿瘤进展,另1 个病灶由综合消融后第二次及之后的系列随访MRI、AFP 检查证实为无局部肿瘤进展。
表1 中被确认为有新发肿瘤的11 例患者(共16 个新发病灶)中,有7 例患者(共8 个新发病灶)由病理证实,另有4 例患者(共8 个新发病灶)为综合消融后多次随访MRI、AFP 检查证实。被MRI 误诊为有新发肿瘤患者2 例(2 个病灶),经穿刺活检证实为无新发肿瘤,而系肝硬化不典型增生结节。
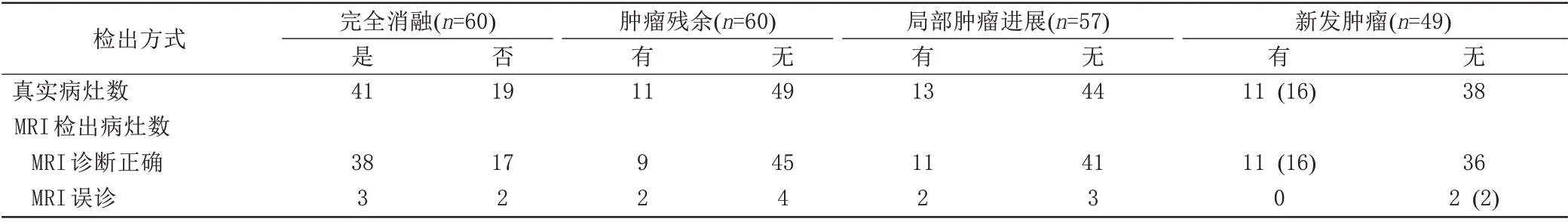
表1 HCC经RFA术后完全消融、肿瘤残余、局部肿瘤进展及新发肿瘤统计结果
本研究中对完全消融及不完全消融,肿瘤残余及局部肿瘤进展的判断,在少数病灶存在误判,且主要发生在RFA 术后3个月以内,这主要是由于RFA术后3个月以内,术区充血水肿等炎性反应明显,这导致消融边界显示不清,进而影响完全消融及不完全消融的判断,同时炎性反应可在消融区边缘呈现类肿瘤样表现,如T2WI 呈稍高信号或增强扫描时出现异常强化等,这就导致部分无肿瘤残余或局部肿瘤进展的病灶被误判;另一方面术后3 个月内部分存在肿瘤残余或局部肿瘤进展的病灶内活性肿瘤较小,在常规MRI 扫描难以显示,加之前述炎性反应干扰,容易导致误判,这表明在对完全消融及不完全消融,肿瘤残余及术后3 个月以内的局部肿瘤进展的评价时,应特别注意炎性反应的干扰,并与术前、术后数次MRI 检查图像仔细对比分析,必要时联合其他评价方法综合考虑,如对病灶区域ADC 值的测定,灌注扫描及波谱分析等也被认为是有助于发现肿瘤残余、局部肿瘤进展的方法[14-16],但其具体评价效果有待进一步研究。
本研究中对新发肿瘤的误判,是由于部分无新发肿瘤的患者肝内存在肝硬化不典型增生结节,被误判为新发肿瘤病灶,这提示对于存在肝硬化的患者,判断其存在新发肿瘤时,应特别注意与肝硬化不典型增生结节鉴别,必要时可行肝脏特异性对比剂造影或穿刺活检,避免误诊导致下一步诊疗方向的错误。
2.3 MRI对HCC经RFA术后疗效的诊断学分析
以HCC 经RFA 术后真实结果为参考,计算MRI 检测RFA 术后完全消融、肿瘤残余、局部肿瘤进展、新发肿瘤的敏感度、特异度、PPV、NPV及准确率,统计结果见表2。
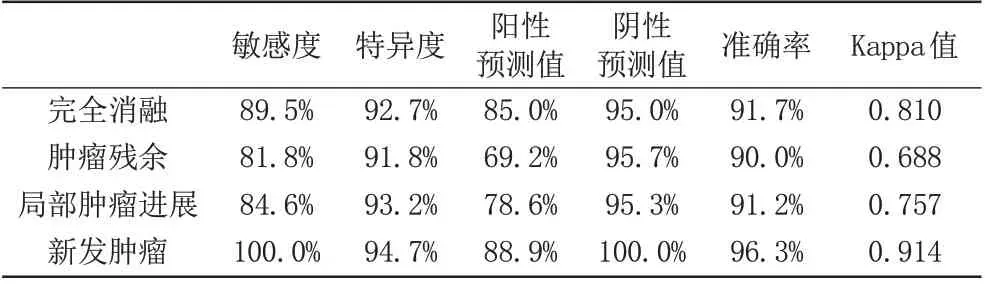
表2 MRI检测HCC经RFA术后完全消融、肿瘤残余、局部肿瘤进展及新发肿瘤诊断性研究
3 讨论
HCC 经RFA 治疗后疗效可呈肿瘤完全消融、肿瘤残余、局部肿瘤进展及新发肿瘤,既往关于HCC行RFA治疗后疗效研究集中在肿瘤残余及局部肿瘤进展,而少有完全消融及新发肿瘤的MRI研究报道[11-13,17]。但HCC未完全消融与局部肿瘤进展的发生密切相关[17],且HCC 经RFA 治疗后还存在新发肿瘤的风险。本研究利用MRI 良好的软组织分辨力与多参数成像的优势[13,18],结合DWI,首次对HCC 经RFA 治疗后完全消融、肿瘤残余、局部肿瘤进展及新发肿瘤进行了全面评价,显示出MRI 可对HCC行RFA术后疗效做出准确评价的优势,为临床判定疗效及制订下一步治疗方案提供重要的影像学参考依据。
3.1 完全消融
本研究显示,绝大多数HCC病灶经RFA治疗后能达到完全消融,少数病灶经RFA治疗后未能达到完全消融,MRI结合DWI能对其做出准确判断。HCC 完全消融的病理学基础为RFA 使肿瘤组织发生凝固性坏死,消融区可伴发出血或蛋白样物质沉积,消融区边缘出现炎性反应及肉芽组织增生,部分消融区周围肝实质可出现异常动脉血流灌注[19-20]。DWI 能帮助判定完全消融的病理学机制在于,在RFA 治疗前,HCC 肿瘤组织较正常肝组织细胞致密,细胞外间隙亦较小,细胞膜限制了水分子的扩散运动,高b 值DWI 呈高信号;在RFA 治疗后,肿瘤组织发生凝固性坏死,细胞膜破损,水分子扩散运动不受限,高b值DWI 呈低信号[14,21]。未完全消融主要原因在于HCC 病灶毗邻较大血管、重要脏器,或病灶较大、形态不规则及浸润性生长,使病灶在RFA治疗中难以达到完全消融[22]。
Koda等[23]发现,HCC经RFA术后2~7 h,在MR平扫T1WI可准确识别肿瘤消融边缘,但未见其对敏感度、特异度、准确率的报道。本研究在平扫T1WI 基础上,结合多期增强扫描图像及DWI,在确认消融区无肿瘤残余的基础上,通过对肿瘤消融边缘的准确判断,以对完全消融和不完全消融做出准确评价,其敏感度、特异度、准确率分别达89.5%、92.7%、91.7%,相对于CT 对完全消融和不完全消融评价的敏感度(66.7%)、特异度(86.4%)、准确率(80.0%)均有所提高[8]。
3.2 肿瘤残余及局部肿瘤进展
本研究发现,MRI 平扫及多期增强,并结合DWI,能准确显示HCC 经RFA 治疗后肿瘤残余及局部肿瘤进展。HCC 经RFA 术后,肿瘤残余及局部肿瘤进展具有与HCC 相似的病理及影像特征[24]。
文献[25-27]报道常规MRI 平扫及增强扫描能判断HCC 经RFA治疗后是否存在肿瘤残余,DWI序列信号改变早于病灶形态学改变,具备早期评价HCC经RFA治疗后是否存在肿瘤残余的能力,但DWI 信号易受微循环影响及各种伪影的干扰,这些研究均未报道MRI 对HCC 经RFA 治疗后肿瘤残余判断的敏感度、特异度和准确率。本研究结合MRI平扫及多期增强、DWI,对HCC经RFA 治疗后肿瘤残余评价的敏感度达81.8%,特异度达91.8%,准确率达90.0%。而本团队前期研究[8]发现,CT 对肿瘤残余评价的敏感度、特异度、准确率分别54.5%、85.2%、80.0%,本研究显示MRI 将其敏感度提高近30%,特异度、准确率提高近10%。
文献[19]报道,MRI平扫及增强是显示局部肿瘤进展的有效检查手段,但未对MRI评价HCC经RFA治疗后局部肿瘤进展的敏感度、特异度和准确率予以报道。本研究表明,MRI平扫及增强扫描结合DWI 能对HCC经RFA治疗后局部肿瘤进展做出准确评价,其敏感度达84.6%,特异度达93.2%,准确率达91.2%。与已发表的CT对HCC经RFA治疗后局部肿瘤进展研究报道[8]对比,在RFA治疗后3个月内,MRI相对于CT对局部肿瘤进展判断的敏感度(84.6% vs. 57.1%)、特异度(93.2% vs. 88.7%)及准确率(91.2% vs. 85.0%)均明显提高;在RFA治疗后3个月后,MRI相对于CT 对局部肿瘤进展判断的敏感度(84.6% vs. 80.0%)、特异度(93.2% vs. 93.8%)及准确率(91.2% vs. 92.5%)相近。
3.3 新发肿瘤
本研究显示,HCC经RFA治疗后,随访MRI平扫及多期增强扫描,并结合DWI,对新发肿瘤能做出非常准确的评估。HCC经RFA 术后,新发肿瘤与原HCC 行RFA 治疗前具有相近的病理及影像特征。本组数据显示,MRI 平扫及多期增强扫描、DWI对新发肿瘤检测的敏感度达100%,特异度及准确率均在95%左右。与已发表的CT 对HCC 经RFA 治疗后新发肿瘤报道[8]对比,在RFA 治疗后3 个月内,MRI 相对于CT 对新发肿瘤判断的敏感度(100.0% vs. 66.7%)、特异度(94.7% vs. 93.0%)及准确率(96.3% vs. 89.8%)均明显提高;在RFA 治疗后3 个月后,MRI相对于CT对新发肿瘤判断的敏感度(100.0% vs. 76.9%)、特异度(94.7% vs. 94.3%)及准确率(96.3% vs. 89.6%)也有明显提高。
综上所述,MRI用于HCC经RFA治疗后的疗效评价时,其对完全消融、肿瘤残余、局部肿瘤进展及新发肿瘤的评价效果很好,尤其是在完全消融及新发肿瘤方面,具有非常高的检测价值,较已报道的CT 对HCC 经RFA 治疗后疗效评价效果有全面提高,表明MRI 可被推荐为HCC 经RFA 治疗后的疗效评价的重要检查手段。
作者利益冲突声明:全部作者均声明无利益冲突。
