磷酸体系中超细氧化镁悬浮液的分散行为研究
2022-07-25沈慧玲刘红宇谢凯欣刘佳乐郑兴农廖家蔚
*沈慧玲 刘红宇 谢凯欣 刘佳乐 郑兴农 廖家蔚
(沈阳工业大学石油化工学院 辽宁 111003)
与传统方法比,氧化镁膨胀剂具有延迟水化后体积膨胀的特点,可抑制混凝土收缩变形,从而解决混凝土裂缝问题,并且已经在一些工程中得以应用[1-2]。但由于碱性环境的水泥浆水化时产生的水化热会限制氧化镁膨胀剂的水化效果,需要与延缓混凝土凝结时间的缓凝剂搭配使用[3]。刘加平[4]等人研究制备一种与氧化镁膨胀剂相适合的缓凝剂,以磷酸铵为主要成分,在与草酸铵和柠檬酸铵的共同作用下起到延迟膨胀的目的。这种方法制备的缓凝剂在与氧化镁膨胀剂一起使用时,会导致部分氧化镁生成磷酸镁而丧失活性。为确保磷酸根离子在不与镁离子反应的情况下吸附在氧化镁表面,延缓氧化镁水化,并在水泥浆中充分发挥作用,本文将采用添加表面活性剂包裹超细氧化镁的方法,并对磷酸体系下的分散性能进行探究,找到最合适的分散剂,考察氧化镁最佳分散条件;并对其分散剂用量、磷酸浓度及其所需搅拌时间等影响因素进行考察,探究超细氧化镁的悬浮稳定性。
1.实验部分
(1)试剂与仪器
试剂:工业电熔氧化镁(MgO)、磷酸(H3PO4)、焦磷酸钠(Na4P2O7)、聚乙二醇(PEG)、柠檬酸(CA)、十二烷基苯磺酸钠(SDBS),以上试剂均为分析纯。
仪器:土壤研磨机(TR400,天津东方天净科技发展有限公司);集热式恒温加热磁力搅拌器(DF-101S,巩义市予华仪器有限责任公司);超声波清洗机(SK3200LH,上海科导超声仪器有限公司);电热恒温鼓风干燥箱(DHG-9076,上海一恒科学仪器有限公司);激光粒度分布仪(BT-9300S,丹东市百特仪器有限公司);紫外可见分光光度计(UV-2600,岛津仪器苏州有限公司);傅里叶红外变换光谱仪(TENSORⅡ,德国布鲁克科技有限公司)。
(2)超细氧化镁悬浮液的制备
工业氧化镁,氧化镁含量为98%,土壤研磨机干磨40min制得中位径为4.159μm的超细氧化镁粉体。将制得的粉体和分散剂在磷酸体系中混合,室温下进行磁力搅拌,并超声分散1h后制成悬浮液。将制好的悬浮液放入30mL的试剂瓶中,静置12h。后续改变分散条件,对比不同条件对其分散性能的影响。
2.结果与讨论
(1)分散剂对超细氧化镁悬浮稳定性的影响
分散剂能修饰氧化镁颗粒悬浮介质界面,在超细氧化镁颗粒的表面形成吸附层,将颗粒包裹在内,增大颗粒间距,减小颗粒间范德华作用[5-6]。图1为不同分散剂对氧化镁粉体粒度的影响。颗粒在磷酸溶液中相互接近,当双电层重叠时会产生电荷排斥现象,颗粒间排斥力大于吸引力,使得悬浮液得以均匀分散[6-7]。选用四种不同分散剂,经过相同时间的机械搅拌和超声分散,静置。取悬浮液的相同部分进行粒径分析。根据超细粉体容易团聚的特点,考察悬浮液中超细氧化镁粉体的粒径大小,判断分散剂吸附效果。由图发现,分散剂作用下,氧化镁粒径发生不同的变化;未添加任何分散剂的悬浮液,粒径分布较宽,团聚作用明显;焦磷酸钠参与后,氧化镁粒径分布区间较小,阻止团聚和沉降行为的能力更优于其他分散剂。
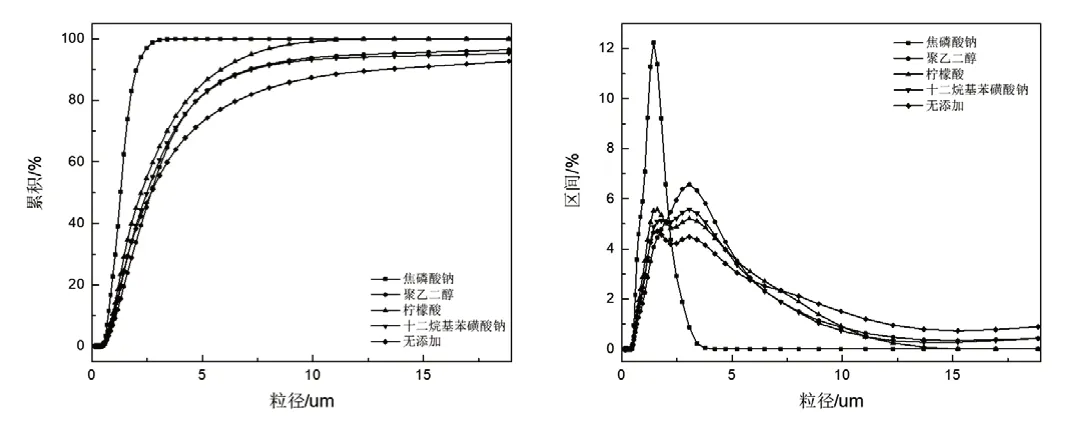
图1 不同分散剂对氧化镁粒度分布的影响
(2)分散剂用量对超细氧化镁悬浮稳定性的影响
颗粒受布朗运动影响相互碰撞聚集成团聚体,沉降过程中,团聚颗粒沉降速度会超过未团聚颗粒,导致悬浮液浓度从上到下依次增大。由朗伯-比尔定律可知,悬浮液浓度变化时,其光吸光度曲线趋势和最大吸收波长不会改变,只有吸光度与悬浮液浓度成正相关[8-9]。且溶液中Na+属于静电吸附的共存电解质,Na+增加使双电层被压缩。图中0.5%~ 2.5%为焦磷酸钠质量分数;1、2、3为超细氧化镁悬浮液的上中下层取样标志。其中下层为悬浮液底层,5支样品瓶中均有沉淀。图2可知,悬浮液受沉降行为影响,上中下层吸光度逐渐增大。随着焦磷酸钠增加,中下层曲线逐渐上升并向上层靠拢,2.5%焦磷酸钠时,吸收曲线开始下降,远离上层吸收曲线。对比发现,悬浮液加入2%焦磷酸钠后自上而下分散均匀。

图2 氧化镁悬浮液吸光度随分散剂用量的变化
(3)固含量对氧化镁悬浮液沉淀量的影响
为研究固含量对悬浮液的影响,分别放入不同含量的氧化镁粉末,静置后,取下层沉淀烘干,测得悬浮液中的氧化镁沉淀量。图3为悬浮液沉淀量随粉体加入量的变化关系。颗粒的范德华力可通过空间稳定来平衡,悬浮液中氧化镁含量较小时,双电层重合几率较低,颗粒团聚可能性较小;逐渐增加氧化镁的量,粉体间作用力增大,促使颗粒与颗粒相互碰撞产生团聚。图中沉降曲线非线性上升。随着氧化镁颗粒的加入,粉体受范德华力影响,沉淀开始增加;继续加入氧化镁会减小颗粒间距,提高粉体间的相互作用,阻碍自由沉降现象[10]。因此10%~18%之间沉淀量趋于稳定;继续加入粉体,加大了颗粒与颗粒的相互碰撞几率,打破空间稳定,悬浮液中氧化镁颗粒开始团聚,提高自由沉降速度,沉淀再次增多。
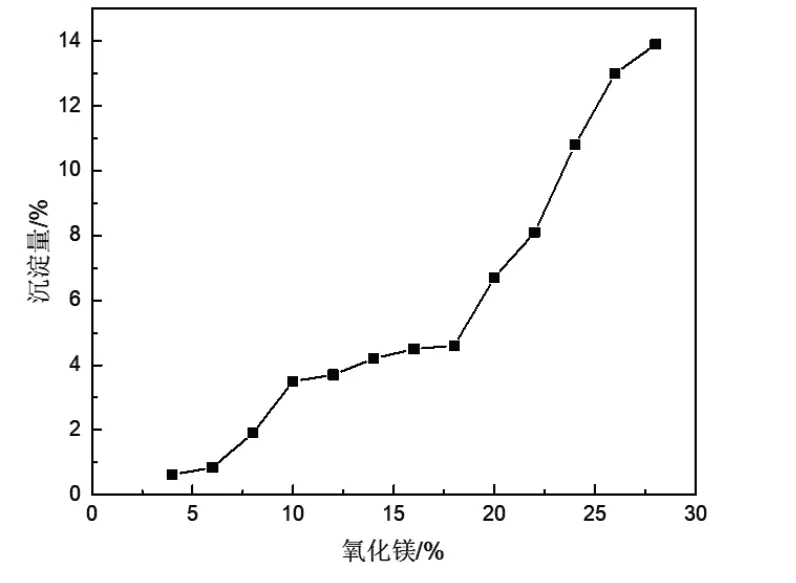
图3 氧化镁含量对悬浮液中沉淀量的影响
(4)搅拌时间对悬浮液稳定性的影响
图4为搅拌时间对氧化镁悬浮液吸光度的影响。磁力搅拌能让颗粒与分散剂在溶液中充分接触,将分散剂有效地吸附在氧化镁颗粒上,同时搅拌过程中可以避免氧化镁团聚成大颗粒,将悬浮液中团聚的颗粒尺寸接近于颗粒初始粒 度[11]。图中可看出,随着搅拌时间的增加,吸光度曲线逐渐升高,10h后趋于稳定并略有降低。这是因为氧化镁颗粒分散到一定效果后,其颗粒间相互作用达到平衡,分散团聚相对稳定,甚至可能出现新的团聚现象,导致吸光度下降。即使延长搅拌时间,氧化镁悬浮液的吸光度也不会有明显变化。

图4 搅拌时间对氧化镁悬浮液吸光度的影响
(5)磷酸的浓度对超细氧化镁悬浮稳定性的影响
图5为磷酸浓度对氧化镁悬浮液中位粒径的影响。由于氧化镁表面的Mg-O键极性较强,极易吸附溶剂中的水分子并使表面被OH-覆盖。随着磷酸不断加入,氧化镁颗粒表面开始吸附磷酸中的H+,且PO43-在表面也有一定吸附,产生双电层,双电层重叠出现双电层排斥力抵消范德华力,致使颗粒分散,避免氧化镁颗粒团聚;3%磷酸时,粒径到达最低点,但继续增加磷酸浓度,新加入的PO43-由于静电排斥力将扩散层内原有的PO43-挤入到吸附层中,双电层排斥力消失,颗粒开始团聚[12]。因此磷酸浓度不断增加,氧化镁的粒径先小后大,直接影响悬浮液分散效果。
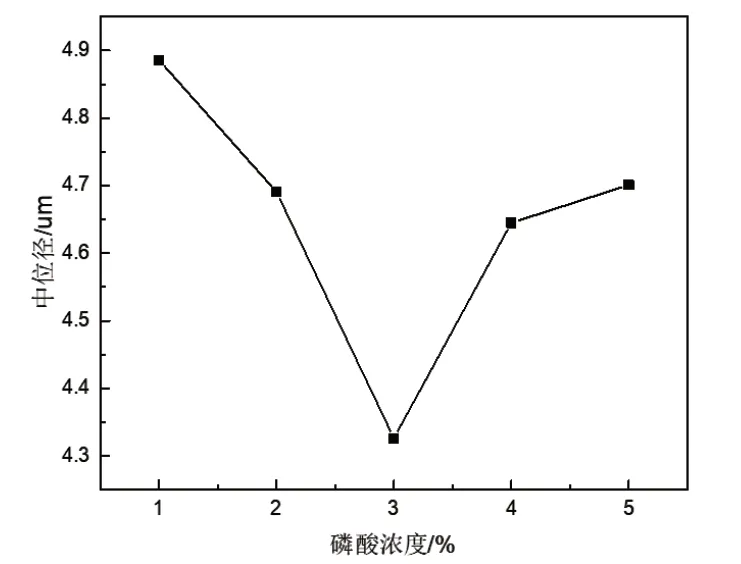
图5 磷酸浓度对悬浮液粒径的影响
将3%磷酸的悬浮液离心烘干,图6为烘干后的氧化镁FTIR光谱对照图。其中Na+并不受吸附的影响存在于极性头的四周,溶液中也包括一部分游离。由图知,水洗离心后,改性的氧化镁粉体较未处理粉体相比,焦磷酸钠与磷酸处对应的峰值均在处理后的氧化镁峰值中体现,且焦磷酸钠吸附明显,说明氧化镁颗粒表面被有效包覆。图7为超细氧化镁悬浮液延缓水化机理,氧化镁表面因静电引力与范德华力会吸附水溶液中的氢氧根离子,在溶液中添加焦磷酸根离子可实现竞争吸附,抑制氢氧根离子吸附在氧化镁表面,形成Stern双电层,其余的离子则扩散分布在双电层外侧,达到防止氧化镁颗粒间的团聚和延缓水化的目的。
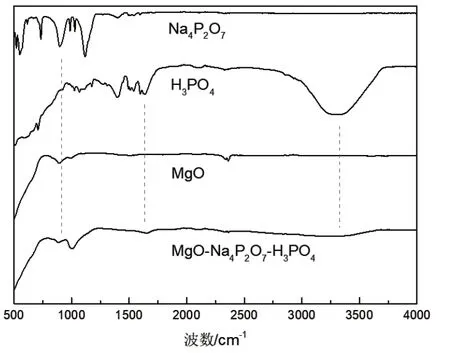
图6 3%磷酸的氧化镁FTIR光谱对照图

图7 超细氧化镁悬浮液延缓水化的机理
3.结论
(1)分散剂的改变对超细氧化镁影响较为显著,选用焦磷酸钠作为分散剂,可得分散稳定的超细氧化镁悬浮液且静置时间越长,分层现象越明显;(2)通过改变磷酸浓度、氧化镁含量以及搅拌时间调节悬浮液中颗粒间力的平衡,使颗粒在悬浮液中分散稳定;(3)经过定量分析,超细氧化镁粉体、磷酸、焦磷酸钠质量分数占比为18:3:2,磁力搅拌10h,可实现超细氧化镁悬浮液分散稳定。
