菌落总数测定结果的不确定度评定
2022-07-25蔡晓霞吴家碧陈叶兰蔡伟江曹艳娟
蔡晓霞,吴家碧,陈叶兰,蔡伟江,曹艳娟,李 露
(汤臣倍健股份有限公司,广东珠海 519040)
随着我国经济的飞速发展,人民的物质生活水平得到了巨大的提升。食品的质量和种类也在不断丰富。但是,近几年来频繁出现了关于食品安全的问题,而这其中又以食品微生物安全问题最为严重。食品微生物导致的安全问题比较严重而且发病速度快,部分致病菌所引起的疾病还具有传染性。正因为微生物的巨大隐患,国家相关部门将微生物检测列为食品检测的强制指标。食品中菌落总数的测定则是强制检测项目,因此对其进行研究十分必要。菌落总数可以反映食品在生产过程中是否符合卫生要求。但是,食品检验的工作复杂繁琐,试验过程中常常会受到诸多不确定因素的影响,因此检测结果与真值之间经常存在一定的误差[1-3]。为了更加准确地表示检测结果,出具可靠准确的检测报告,需要引入测量不确定度。测量不确定度[4]是表征合理赋予被测量的分散性,是目前国际公认的用来评价检测结果质量的参数。近年来,关于食品中菌落总数不确定度评定[5-15]的研究越来越多。依据GB 4789.2—2016《食品安全国家标准食品微生物学检验 菌落总数测定》[16],采用平板计数法测定加标试验样品中的菌落总数,建立菌落总数测定结果不确定度评定的基本方法,分析检测过程中影响结果的主要因素,确立了菌落总数不确定度的评定,提升检测结果的可信度,为今后实验室中菌落总数测定结果的准确性提供有力的保障。
1 材料与方法
1.1 仪器与试剂
培养基:PCA 琼脂培养基,广东环凯微生物有限公司提供;稀释液:0.85%无菌氯化钠溶液,广州化学试剂厂提供;实验室用水为二级纯化水;对照菌:枯草芽孢杆菌ATCC6633,广东省微生物菌种保藏中心提供;供试品:健乐多乳清蛋白营养强化粉固体饮料,汤臣倍健股份有限公司提供。
LT1002 E 型电子天平,常熟市天量仪器有限公司产品;BSC-1600ⅡA2 型生物安全柜,苏州安泰空气技术有限公司产品;QL-866 型振荡器,海门市其林贝尔仪器制造有限公司产品;EZ-FitTM 型通用型实验室过滤系统,德国默克公司产品;SPX 质250BSH-Ⅱ型生化培养箱,上海新苗医疗器械制造有限公司产品;BXM-30R 型立式压力蒸汽灭菌器,上海博讯实业有限公司医疗设备厂产品;HMB-400B 型拍击式均质器,天津市恒奥科技发展有限公司产品。
1.2 试验方法
1.2.1 检测依据
国家标准GB 4789.2—2016《食品安全国家标准食品微生物学检验 菌落总数测定》。
1.2.2 检测过程
菌液:接种枯草芽孢杆菌的新鲜培养物至TSB液体培养基中,35 ℃下培养24 h;用0.85%无菌氯化钠溶液稀释并制成试验所需浓度的菌悬液,待用。工作用菌株为第3 代。
称取25 g 样品至无菌均质袋中, 加入225 mL 无菌氯化钠溶液,然后用拍打器拍打2 min,待样品溶解后加入适量菌液(接种菌悬液的体积不得超过样液体积的1%),再次用拍打器进行拍打,直至菌液均匀分布于样液中,溶液即是1∶10(g∶mL) 的样品匀液。将上述1∶10 的样品匀液用无菌吸头吸取1 mL,注入盛有9 mL 无菌氯化钠溶液的试管后,旋涡混匀,制成1∶100 的样品匀液。吸取2 个稀释度样品匀液1 mL 于无菌平皿内, 每个稀释度做2 个平行。同时,分别取1 mL 样品稀释液加入2 个无菌平皿作空白对照;及时将20~25 mL 冷却至46 ℃的平板计数琼脂(可放置于46 ±1 ℃恒温水浴箱中保温) 倾注平皿,并转动平皿使其混合均匀,置水平台面待琼脂完全凝固后,正置平板,置于36±1 ℃培养箱中培养, 观察并记录培养至第2 天的结果,记录稀释倍数和相应的菌落数量, 计算结果并报告。在同一相对恒定的试验条件下,对该样品重复测20 次,然后对检测结果进行不确定度评定。
2 结果与分析
2.1 识别测量不确定度的来源
根据GB 4789.2—2016 检测加标样品中的菌落总数,分析检测流程,识别该方法的不确定度来源。
菌落总数的不确定度来源见图1。
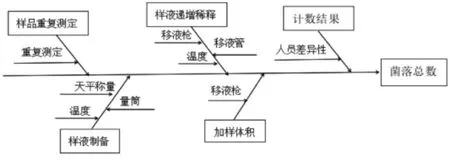
图1 菌落总数的不确定度来源
2.2 建立数学模型
据GB 4789.2—2016 菌落总数的计算公式为:
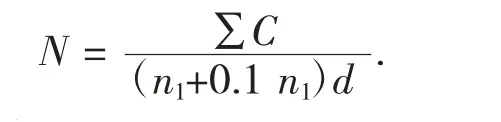
式中:N——样品中菌落数;
∑C——平板(含适宜范围菌落数的平板) 菌落数之和;
n1——第一稀释度(低稀释倍数) 平板个数;
n2——第二稀释度(高稀释倍数) 平板个数;
d——稀释因子(第一稀释度)。
当只有一个稀释倍数的平板菌落数在计数范围内,n2=0。考虑到结果的分散性,将计算得到的菌落数转换为对数值之后再计算其不确定度。
通过分析菌落总数检测过程中不确定度的来源及建立数学模型可知,影响菌落总数测定结果不确定度的因素主要是样品重复测定、样液制备过程、样液递增稀释过程、加样体积和不同人员计数结果差异性等。
2.3 不确定度分量的评定
2.3.1 测量重复性引入的不确定度
重复性检测引起的不确定度,主要是检测过程中各种因素作用下随机性所得各次菌落数值不同引起的。在同一相对恒定的试验条件下,对该加标样品重复测20 次,然后对检测结果进行不确定度评定。
样品重复测定的结果表1。
从表1 可看出,检测结果数值的发散性较大,所以采用统计学方法,以菌落数值的对数值求不确定度。按A 类评定,根据贝塞尔公式计算检测结果对数值的样本标准偏差:

表1 样品重复测定的结果

日常检测工作中,样品只做单次试验,因此标准不确定度U(重复)==0.0255961,相对标准不确定度Urel(重复)=。
2.3.2 样液制备过程引入的不确定度
样液制备过程中,需要用500 mL 量筒量取225 mL生理盐水,以制备成待用的稀释液。根据该量筒的检定证书,允许误差为±0.7mL,属于B 类评定,按均匀分布,标准不确定度为:相对标准不确定度为:
试验样品使用电子分析天平进行称量, 根据天平的检定证书,当20 g≤m≤50 g 时,示值允许误差为±0.05 g,偏载允许误差为±0.15 g,天平的重复性误差引入的不确定度已包括在样品重复测定的不确定度中,因此这里不再做进一步的考虑。示值允许误差和偏载允许误差采用B 类不确定度评定,区间半宽度为a1=0.05 g,a2=0.15 g,按均匀分布计算,,则合成标准不确定度U(m)=,样品的称样量m=25 g,则样品称量引入的相对标准不确定度为=0.0036515。
由于实验室温度在20±5 ℃的范围内波动, 假设温度变化为5 ℃, 该温度引起的不确定度可通过估算温度范围和体积膨胀系数计算,液体的体积膨胀明显大于容量瓶的体积膨胀,故只考虑前者即可。设温度为均匀分布,,水的膨胀系数为2.1×10-4/℃。则:
综合以上,样品制备过程所引入的相对标准不确定度为Urel(制备)=0.0041142。
2.3.3 样液递增稀释引入的不确定度
该不确定度来源于用1 mL 无菌吸头吸取不同稀释级溶液1~9 mL 灭菌生理盐水的稀释过程。所使用的量器分别是1 mL 移液枪和10 mL 的移液管,根据该1 mL 移液枪的检定证书,其容量允许误差为±0.002 mL。根据10 mL 的移液管的检定证书,其允许误差为±0.03 mL,属于B 类评定,按均匀分布计算,,试验选择的稀释度为(10-1和10-2),即稀释过程1 mL 移液枪和10 mL 的移液管各使用了1 次,所以稀释过程的标准Urel(V21)不确定度为:U(V21)=相对标准不确定度为,温度引起的相对标准不确定度。因此,样品递增稀释过程所引入的相对标准不确定度为:
2.3.4 加样体积引入的不确定度
检测结果以稀释因子为10-1平板上的菌落总数进行计数和报告,每次检测各平板上接种的稀释液的体积均为1 mL,做2 个平行,1 mL 移液枪使用2 次,属于B 类评定, 按均匀分布,加样体积引起的不确定度为相对标准不确定度为温度引起的相对标准不确定度0.0006060。因此,加样过程引入相对标准不确定度Urel(加样)=
2.3.5 不同人员计数结果差异性引入的不确定度
检测人员在计数培养基平板上的菌落时,因经验和计数平板上菌落的复杂培养结果等出现随机误差和识别误差,该误差通过对同一个培养基平板的菌落进行重复计数后统计得出,采用10 位检验人员对同一个平板的菌落进行计数的方法进行不确定度的计算。
不同人员计数结果见表2。
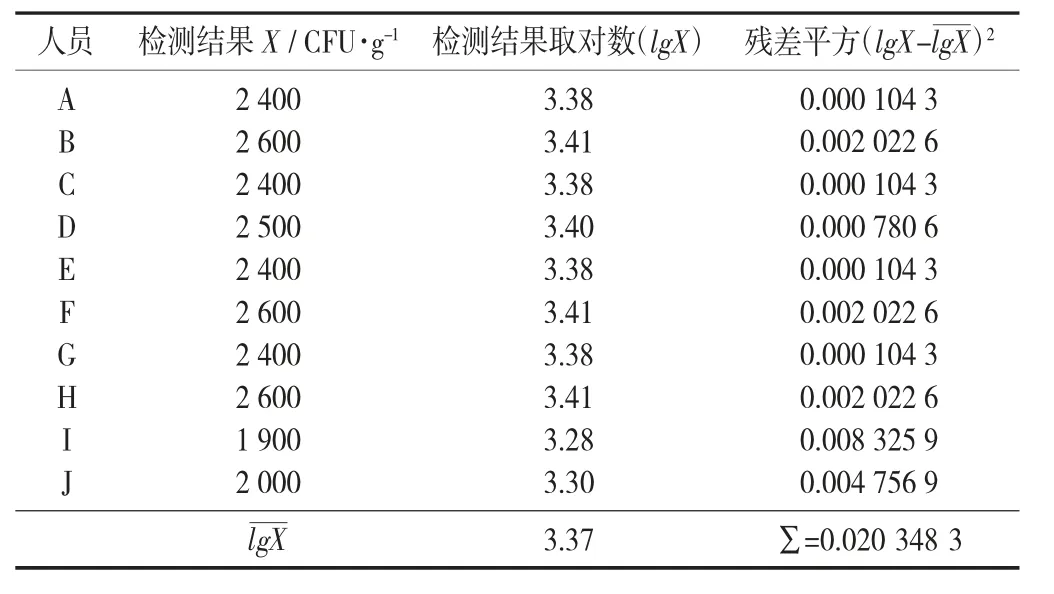
表2 不同人员计数结果
按A 类评定,根据贝塞尔公式计算检测结果对数值的样本标准偏差:=0.0475492,标准不确定度U(计数)=0.0150364。
2.4 合成不确定度和扩展不确定度
此次研究的不确定度主要有以下4 个。
相对标准不确定度一览表见表3。
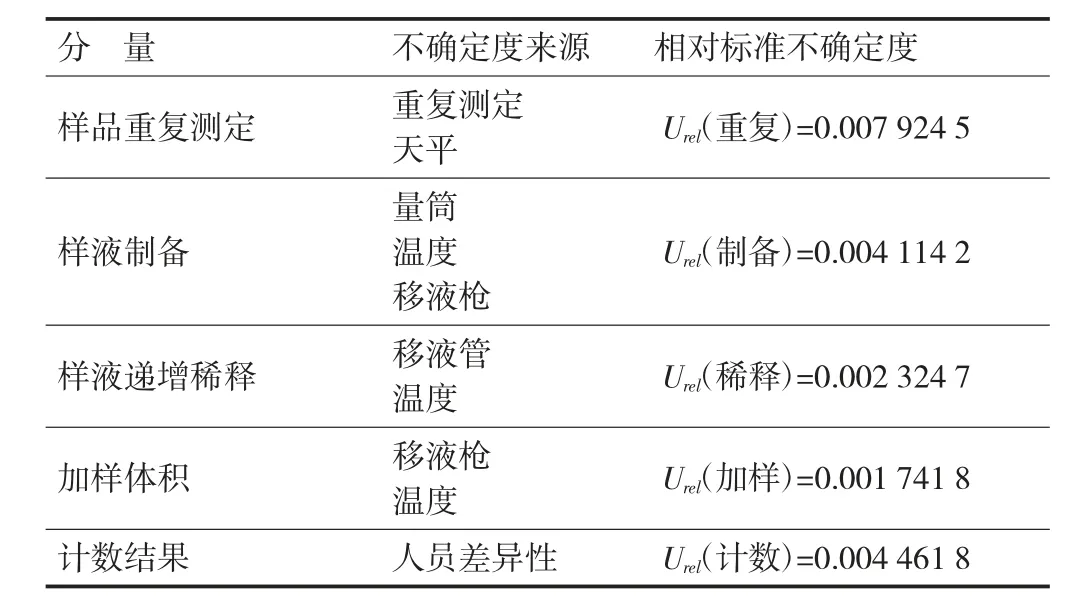
表3 相对标准不确定度一览表
该方法的合成相对标准不确定度为:
试验结果以扩展不确定度来表示,U=k×UCrel,取置信水平为95%,自由度=20,查t 分布表得t95(20)=2.086,因此U=2.086×0.0103957=0.0217。由于lgX与X 之间呈非线性关系,不能直接求扩展不确定度U 的反对数。因此,应首先确定lgX 的取值范围为lgX=3.23±0.0217,即3.2083≤lgX≤3.2517。再取反对数后,得检测结果X 的分布区间为1615≤X≤1785。
2.5 结果报告
此次加标试验样品的菌落总数的估计值为1600~1800 CFU/g,包含因子k=2.086。
3 结论
研究对样品重复检测、样品制备、递增稀释、加样体积和不同人员计数结果差异性引起的不确定度进行评估,从不确定度计算的结果来看,5 种因素对测量结果均有影响。但样品重复测定过程引入的不确定度贡献最大,其次是不同人员计数结果的差异性和样液的制备过程,这与刘荔等人[17]对膨化食品中菌落总数不确定度的研究结果一致。因此,在今后检测过程中要从多方面加强质量控制,要求检验技术人员熟练掌握各个环节的技术要点,另外实验室应对人员进行定期培训和考核,严格按照规范统一的计数标准进行计数,最大限度地减小不确定度引入的分量值。
除了以上列出的几个分量之外,通过查阅文献可知培养条件、不同批次的培养基、培养基的灭菌时间、温度等因素也会影响菌落总数不确定度的结果。但由于这些因素不便计算,且对总不确定度的贡献度比较小,所以此次评估不纳入考虑[18],但是微生物培养环境的稳定性对降低不确定度有着非常重要的作用[19]。因此,日常工作中,实验室进行微生物培养时应该提供相对稳定的环境,这为实验室出具准确可靠的检测结果提供有力的保障。
