沉默中性粒细胞Orai1影响NETs内ROS的表达
2022-07-25麻芯茹赵莹莹吕鑫泉张冰冰
麻芯茹,郭 寒,张 伟,李 铭,赵莹莹,王 爽,吕鑫泉,李 享,徐 闯*,杨 威*,张冰冰*
(1.黑龙江八一农垦大学 动物科技学院,黑龙江 大庆 163319;2.黑龙江八一农垦大学 生命科学技术学院,黑龙江 大庆163319)
奶牛业是畜牧业的重要组成部分,奶牛饲养业是现代国家农业的核心行业,与此同时奶牛相关营养代谢性疾病的发病率也在不断升高[1]。除了牧场的日常管理与预防,奶牛其自身机体的免疫也是极其重要的。其中先天免疫作为动物机体的第一道防线,中性粒细胞(PMN)是先天免疫反应的主要效应细胞,约占白细胞总量的70%[2],细胞显示出强大的抗菌功能,包括迁移、黏附、吞噬、脱粒和中性粒细胞胞外诱捕网(NETs)。NETs形成过程的主要特征是核重排:核小叶丢失,伴有染色质缩合并同时使颗粒解体。在后期阶段核膜解体,随后细胞内容物被弹射到细胞膜上,细胞外空间形成NETs[3]。NETs可以结合微生物,阻止微生物传播,NETs的产生和网状组织被认为是无菌性炎症中非常重要的武器。PMN衍生的微囊泡代表了另一种机制,通过这种机制,PMN可以放大炎症过程,在损伤部位和血液中都能发现高水平的炎症过程[4]。
有研究表明,NETs的形成可以在保留PMN功能的情况下进行,包括吞噬和趋化功能。这种现象被称为生命性NETs;相反则称为自杀性NETs。自杀性NETs与生命性NETs的主要区别在于刺激的性质,其中自杀性NETs多由佛波肉豆蔻酸乙酸酯(PMA)诱导[5]。可通过激活蛋白激酶C活化泛素连接酶-促分裂原活化的蛋白激酶-胞外信号调节激酶信号转导通路,激活还原型烟酰胺腺嘌呤二核苷酸磷酸氧化酶,进而促发NETs释放[6-7]。PMA具有广泛的生物学活性,在动物体内可诱导多种细胞因子的生成、调节心肌细胞、促癌因子作用等[8]。旨在研究不同时间与浓度的PMA刺激PMN对NETs形成的影响。
细胞内Ca2+是最重要的第二信使,对真核细胞的广泛生物学过程至关重要[9],Ca2+释放激活的Ca2+(CRAC)通道是细胞内钙的主要来源,由钙通道蛋白Orai1组成,形成通道的Ca2+渗透孔。Ca2+升高有利于ROS代谢途径的产生进而增加活性氧(ROS)的表达[10],而NETs细胞死亡过程不同于凋亡和坏死,取决于NADPH氧化酶产生的ROS[11]。ROS可以触发细胞内NETs的增加并通过调节内质网、线粒体、质膜上的Ca2+传感器和转运蛋白来调节Ca2+的水平[12]。
1 材料与方法
1.1 实验动物自黑龙江省大庆市某集约化奶牛场选取体况相似的健康奶牛,尾静脉采血,肝素抗凝管抗凝。
1.2 主要试剂牛外周血PMN分离试剂盒、多聚赖氨酸购自北京索莱宝科技有限公司;PBS缓冲液购自Hyclone公司;RPMI-1640培养液、PMA购自Sigma;Hoechst33342核染抗荧光衰减封片剂(含DAPI)购自北京索莱宝试剂公司;Ca2+荧光探针购自碧云天生物技术有限公司;ROS检测试剂盒购自北京普利莱基因技术有限公司;siOrai1 RNA与siRNA-mate转染试剂购自上海吉玛制药技术有限公司。
1.3 奶牛血液PMN的分离在清晨喂料之前,选取体况相近且无任何疾病的奶牛,固定后通过尾静脉采血后收集到肝素抗凝管内,根据牛外周血PMN分离试剂盒分离PMN,在15 mL离心管内按比例先后加入试剂盒中的A液、C液与血液,离心收集细胞,待红细胞裂解液完全后,洗涤3次即为PMN。
1.4 NETs检测将包被好的多聚赖氨酸爬片放入12孔板,调整PMN浓度后将细胞放入板内,添加PMA刺激后于37℃、5% CO2培养箱中培养。弃掉12孔板内的培养基,PBS清洗3次,吸尽PBS后,加入300 μL的4%多聚甲醛固定,重复PBS清洗。去除爬片上的多余液体,载玻片上滴1滴Hoechst33342核染抗荧光衰减封片剂,避光,激光共聚焦显微镜下观察。
1.5 在不同PMA刺激时间的条件下培养PMN将1.3分离的健康组的PMN分成6组,每组分别用加入100 nmol/L的PMA的RPMI-1640培养基培养,经37℃、5% CO2培养箱分别培养1,2,3,4,5,6 h,根据1.4步骤通过激光共聚焦显微镜下观察。
1.6 在不同PMA浓度的条件下培养PMN将1.3分离的健康组的PMN分成4组,每组分别用加入10,50,100,200 nmol/L PMA的RPMI-1640培养基培养,经37℃、5% CO2培养箱培养3 h,根据1.4步骤通过激光共聚焦显微镜下观察。
1.7 沉默Orai1基因将分离出的PMN调整浓度后,为稳定细胞,使用完全培养基培养1 h后,根据吉玛基因转染试剂说明书进行转染,根据siOrai1 RNA引物序列(表1),设计引物沉默Orai1基因。设计对照组,不加入siOrai1 RNA沉默24 h。

表1 siOrai1 RNA引物序列
1.8 流式细胞术检测钙为了分析Orai1基因对NETs内钙的影响,将收集到的PMN调整密度后,按照1.7方法沉默24 h后加入PMA刺激3 h,清洗后经改良台氏液重悬后,经Fluo-3AM试剂盒配比稀释染色,避光37℃孵育30 min,清洗后上机检测。
1.9 流式细胞术检测ROS为了分析Orai1基因对NETs内ROS水平的影响,将收集到的PMN调整密度后,进行1.7步骤沉默24 h后加入PMA刺激3 h,经改良台氏液重悬后,根据普利来ROS检测试剂盒说明书操作,清洗后通过FCM测定荧光强度。

2 结果
2.1 不同PMA刺激时间的条件下PMN NETs检测经激光共聚焦显微镜检测结果显示,奶牛PMN经PMA刺激3 h,NETs的形成效果最好(图1)。
2.2 不同PMA刺激浓度的条件下PMN NETs检测如图2所示,激光共聚焦显微镜观察结果表明,PMA浓度为100 nmol/L时,奶牛血液PMN细胞NETs的形成效果最好。

A.~D.分别为10,50,100,200 nmol/L PMA刺激3 h形成的NETs
2.3 检测PMA刺激下PMN内Ca2+水平如图3可见,沉默PMNOrai1后, NETs内Ca2+极显著降低,表明NETs通过Orai1影响Ca2+水平(P<0.01)。

A.转染siNEG和siOrai1细胞中的Ca2+表达水平;B.转染siNEG和siOrai1细胞中的Ca2+水平相对丰度;“**”表示对照组和沉默PMN Orai1呈现极显著性差异
2.4 检测PMA刺激下PMN内ROS水平由图4可见,沉默Orai1后,NETs内ROS水平明显降低(P<0.05)。
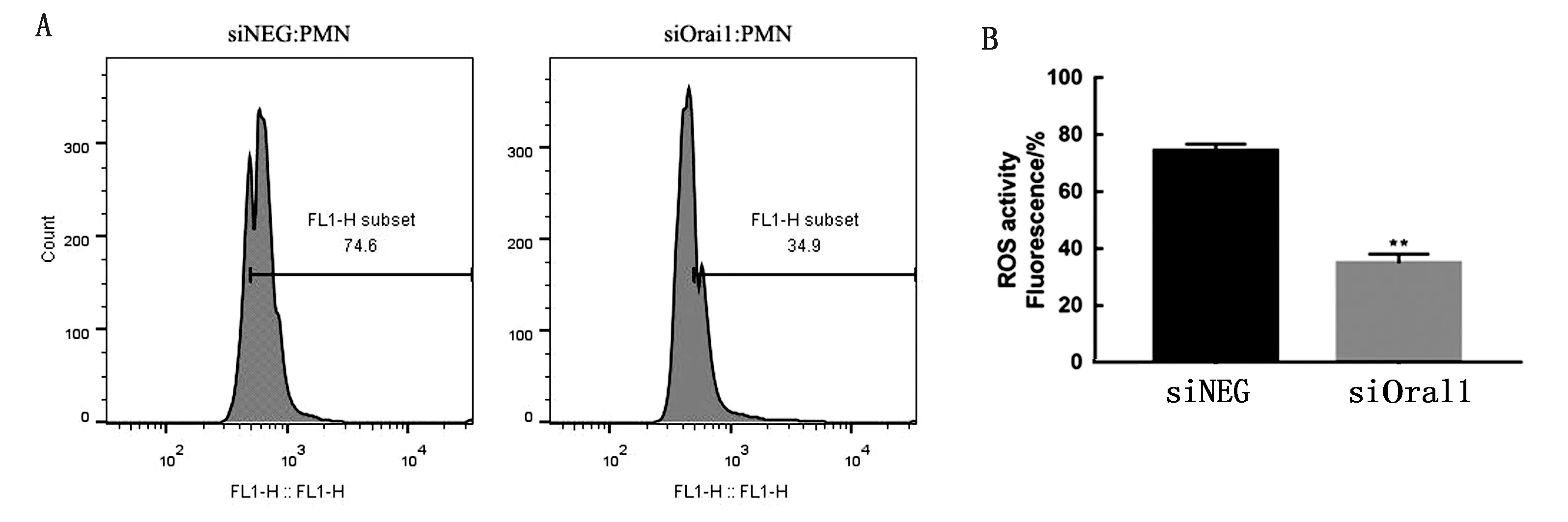
A.转染siNEG和siOrai1细胞中的ROS表达水平;B.转染siNEG和siOrai1细胞中的ROS水平相对丰度;“**”表示对照组和沉默PMN Orai1呈现极显著性差异
3 讨论
PMN是维持机体生理状态稳定的重要细胞,其能对破坏机体屏障的病原体做出快速和多样化的反应,并使组织恢复到无菌状态。PMN能有效地吞噬和杀死微生物,在动物非特异性免疫系统中起关键作用[13]。NETs形成是一种新的PMN程序性死亡方式,是一个多步骤的死亡途径[14],通过髓过氧化物酶(myeloperoxidase,MPO)、弹性蛋白酶(neutrophil elastase,NE)对抗细胞外微生物。而NE缺陷型小鼠不能形成NETs,表现出免疫缺陷[15]。
PMA刺激的PMN释放DNA,形成细胞外网状结构,修饰杀菌蛋白。本研究发现PMA诱导1 h后NETs形成较少,在刺激2~3 h后NETs形态逐渐增加,4~6 h后开始下降。分别用10,50,100,200 nmol/L PMA刺激3 h,结果发现,100 nmol/L的PMA形成NETs效果最好。
Ca2+在细胞的信号传导和执行功能等各方面发挥着重要作用,由于内质网的体积小,内质网的Ca2+储量减少会导致细胞质Ca2+的增加很小。所以当细胞被激活时,储存在内质网中的Ca2+被释放。进而细胞内的主要来源是由Ca2+释放激活Ca2+产生的,Ca2+通过释放激活位于质膜中,由钙通道蛋白Orai组成,这些通道蛋白具有很高的Ca2+选择性,形成通道的Ca2+渗透孔,从而使钙流入细胞,以确保连续的细胞外来源的Ca2+。流式细胞检测结果表明,当PMN沉默Orai1,NETs内Ca2+水平极显著降低,证明PMN成功沉默Orai1,影响奶牛血液PMN Ca2+进入细胞内,进而影响细胞内Ca2+浓度。NETs的形成取决于ROS的产生,ROS使PMN能够通过NADPH氧化酶激活来满足其抗菌功能。沉默Orai1导致NETs内ROS表达极显著下降,由于沉默Orai1影响细胞内Ca2+,从而影响NETs状态下的ROS水平。
奶牛PMN在100 nmol/L的PMA条件下刺激3 h NETs形成的效果最好。沉默PMN膜上Orai1蛋白,导致NETs内Ca2+和ROS水平降低。
