β-环糊精改性多级孔纤维素膜的制备及其吸附性能
2022-07-22孟建强郜慧慧马六甲侄伦豪
孟建强,郜慧慧,潘 赢,马六甲,侄伦豪
(1.天津工业大学 省部共建分离膜与膜过程国家重点实验室,天津 300387;2.天津工业大学 材料科学与工程学院,天津 300387)
膜分离技术具有分离效率高、工艺简单的特点,已在包括废水处理和海水淡化等多种领域得到了广泛应用[1]。通过表面改性,经过吸附或催化作用除去或降解污染物分子是目前除去水体中有机污染物较为常用的一种方式[2-4]。由于超微滤膜孔径较大、传质阻力小,常被用于表面改性制备吸附膜或催化膜。但是,超微滤膜较大的孔径又限制了其吸附容量。为了提高通过表面修饰制得吸附膜的吸附容量,目前最常见的方法是通过增加修饰层的厚度来提高活性官能团的数量,但这样又大大增加了传质阻力,降低了吸附速率,导致trade-off 关系形成。所以,制备兼具高吸附速率和高吸附容量的理想型吸附膜是当前研究人员所面临的重要挑战之一。
多级孔具有不同的孔径分布结构[5-6],在膜表面构建多级孔结构是有效缓解上述难题的一种可行的策略[7]。在吸附膜表面构筑同时含有大孔和小孔的多级孔结构,大孔作为传质流道,提高吸附速率;小孔提供吸附位点,增加吸附容量,这就可以满足同时优化吸附速率和吸附容量的需求。环糊精具有均一的微孔孔径以及外腔亲水内腔疏水的特殊结构,能够有效地与有机分子形成包合物,经常被用于处理水体中的有机污染物[8-12]。本文利用这一特性,尝试将β-环糊精通过简单的硅烷偶联反应修饰到纤维素微滤膜表面,构建大孔加小孔的多级孔结构,将其用于苯酚和异丙甲草胺的吸附研究。
1 实验部分
1.1 原料和试剂
再生纤维素微滤(RC)膜,平均孔径0.45 μm,德国赛多利斯生物技术有限公司产品;β-环糊精(β-CD)、γ-(2,3-环氧丙氧)丙基三甲氧基硅烷(KH560)、氢化钠(NaH)等试剂,分析纯,上海泰坦科技股份有限公司产品;N,N-二甲基甲酰胺(DMF),高效色谱纯,阿拉丁试剂有限公司产品;苯酚、异丙甲草胺(99%),百灵威科技有限公司产品;乙醇、甲醇,分析纯,天津科密欧化学试剂有限公司产品。
1.2 测试与表征
傅里叶变换红外光谱仪(FT-IR,Vector 22):全反射光谱范围为370~7 500 cm-1,仪器分辨率为0.9 cm-1,其波数精度为0.01 cm-1。X 射线光电子能谱(XPS,Thermo Fisher K-Alphα):X 射线源采用K-AlKα(1 486.6 eV),扫描全谱图的测试能量范围是0~1 000 eV,探测深度为2 nm,分析精度为1%~2%。场发射扫描电镜(SEM,Hitachi S-4800):背散射电子分辨率为3.0 nm(15 kV),二次电子分辨率为1.0 nm(15 kV),加速电压为0.5~30 kV,放大倍数为30~800 000 倍。BET(Micromeritics ASAP 2460M):测试前将样品在150 ℃脱气24 h,在77 K 下测试样品对N2的吸附-脱附曲线。热重分析(TGA,STA409PC/PG):在N2气氛下将样品从室温(25 ℃)以10 ℃/min 加热到800 ℃。紫外可见分光光度计(UV-Vis,T6 新世纪):测试吸附前后溶液吸光度的变化。
1.3 β-CD 修饰RC 膜的制备
图1为β-环糊精修饰纤维素膜(RC-g-KHCD)的合成路线。

图1 β-环糊精修饰纤维素膜的合成路线Fig.1 Synthesis route of RC-g-KHCD membrane
(1)RC 膜预处理:将RC 膜(d孔=0.45 μm,d膜=47 mm)浸泡在适量的去离子水中,50 ℃下处理1 h,去除其表面杂质。之后,将处理后的RC 膜在60 ℃下干燥至恒重,并称量。
(2)KH560 修饰β-CD:量取3 g β-CD、0.3 g NaH和100 mL DMF,放入250 mL 烧瓶中,室温下搅拌30 min,对β-CD 进行活化。之后,将反应后的混合液进行抽滤,除去未反应的NaH。将滤液倒入250 mL 三口烧瓶中,用移液管量取1 mL KH560,放入三口烧瓶中,在N2气氛下于90 ℃搅拌5 h,即可得到KH560 修饰β-CD(KH-CD)。
(3)KH560 修饰RC 膜:将干燥的RC 膜浸泡在KH-CD 液体中5 min,然后转移置真空干燥箱中,于110 ℃使KH-CD 上的硅烷与RC 膜表面的羟基进行缩聚反应。
反应结束后,将修饰后的膜用去离子水和乙醇充分洗涤以去除未反应的残留杂质,然后在60 ℃下干燥直到质量不再变化,即可得到KH560 修饰RC 膜(RCg-KHCD),RC-g-KHCD 膜的接枝率Rg可由公式(1)计算:

式中:m0和mt分别为RC 膜修饰前后洗涤干燥后的质量(g);M是KHCD 的摩尔质量(g/mol)。
1.4 RC-g-KHCD 膜的吸附性能评价
(1)吸附性能。苯酚和异丙甲草胺作为污染物模型,来评价RC-g-KHCD 膜的吸附性能。将干燥的0.035 g 的RC-g-KHCD 膜碎片样品浸泡在10 mL 不同浓度的苯酚/异丙甲草胺的水溶液中,于25 ℃室温震荡12 h,用紫外分光光谱测试吸附前后溶液浓度的变化,通过公式(2)计算平衡吸附容量:

式中:C0和Ce分别为溶液的初始质量浓度和平衡质量浓度(g/L);V为溶液的体积(mL);m为RC-g-KHCD 膜的质量(g);Mb为苯酚/异丙甲草胺的摩尔质量(g/mol)。
(2)循环使用性能。将吸附饱和的RC-g-KHCD膜用甲醇洗涤6 h,然后用去离子水洗涤1 h 后,再次测试吸附性能,通过公式(3)计算再生效率:

式中:qn和q1分别为第n次和第1 次循环的平衡吸附容量。
2 结果与讨论
2.1 RC-g-KHCD 膜的化学结构
图2为RC 膜和RC-g-KHCD 膜的性能表征。

图2 RC 膜和RC-g-KHCD 膜性能表征Fig.2 Performance characterization maps of RC membrane and RC-g-KHCD membrane
图2(a)为反应时间对RC 膜表面KHCD 接枝率的影响。由图2(a)可见,在反应2 h 内,接枝率随反应时间的增加而增加;超过2 h 后,接枝率稳定在0.1 mmol/g 不再变化,此时RC 膜表面的活性位点已经达到饱和。图2(b)为RC 膜修饰前后的红外图谱,KHCD修饰后,由于β-CD 和RC 均由吡喃葡萄糖单元构成,所以未有新的吸收峰产生。在3 330 cm-1处—OH 的吸收峰明显减弱,这是由于KHCD 和RC 的反应消耗了RC 膜表面的—OH。图2(c)为RC 膜修饰前后的XPS 全谱图,对于RC 膜和RC-g-KHCD 膜表面,在287.08 eV 和533.08 eV 均出现C 1s 和O 1s 的特征峰。对于RC-g-KHCD 膜,在100.4 eV 和150.5 eV 位置出现了Si 2p 和Si 2s 的特征峰,表明硅烷偶联反应成功发生,并且硅烷偶联剂成功接枝到RC 膜表面。图2(d)为RC 膜和RC-g-KHCD 膜的热重分析结果。由图2(d)可见,RC 膜和RC-g-KHCD 膜均经历了2 个降解阶段:第1 个阶段发生在60 ℃,是由于膜表面羟基通过氢键所结合的水分的蒸发,在此阶段,RC-g-KHCD 膜的降解程度明显低于RC 膜,是反应消耗了膜表面的羟基使得修饰后膜表面结合的水分减少所致;第二阶段发生在260 ℃,是由于葡萄糖单元的降解,当温度增加到500 ℃,质量均逐渐稳定,由于经过硅烷偶联剂得修饰会生成二氧化硅,RC-g-KHCD 膜的残余质量明显高于RC 膜。
2.2 RC-g-KHCD 膜的表面形貌
图3为修饰前后膜表面场发射扫描电镜图。

图3 RC 膜和RC-g-KHCD 膜表面的场发射扫描电镜图Fig.3 FESEM images of RC membrane and RC-g-KHCD membrane
由图3 可以看出,RC 膜的孔径较大,属于微米级。经过KHCD 修饰后,膜表面出现很多小凸起,粗糙度明显增加,这是所接枝的聚硅氧烷聚集体所致。
2.3 RC-g-KHCD 膜的孔径分布
用SEM 观察膜表面孔结构,微孔和介孔结构以及比表面积可由BET 氮气吸附-脱附曲线分析,结果如图4 所示。
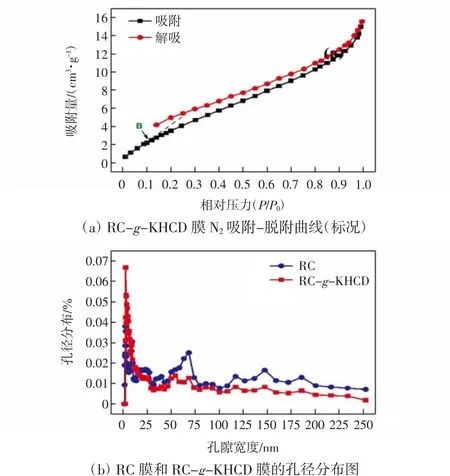
图4 RC 膜和RC-g-KHCD 膜N2 吸附-脱附曲线及孔径分布图Fig.4 N2 adsorption and desorption isotherm and pore size distribution of RC membrane and RC-g-KHCD membrane
由于β-CD 含有孔径均一(0.6 nm)的纳米空腔(微孔),但是根据IPUAC 技术报告的定义[13],图4(a)中RC-g-KHCD 膜对氮气的吸附-脱附曲线不符合微孔型,即在低相对压力范围没有明显的“拐点”,而且吸附量随相对压力的升高没有趋于稳定而是逐渐增加。这是由于β-CD 的微孔比较特殊,两端开口的结构使得用BET 方法很难检测到,在很多文献报道中也出现过类似现象[9,14-15]。除此之外,等温线在脱附阶段出现了由毛细凝结产生的明显的“回滞环”,即根据IUPAC 定义符合的介孔特征[13]。等温线在P/P0=1 时,吸附量持续上升没有达到饱和,又符合大孔结构的特征。所以,修饰后的RC-g-KHCD 膜含有“介孔-大孔”的多级孔结构,交联的聚硅氧烷分子链构成介孔,RC膜本征提供大孔。图4(b)为由DFT 模型计算的RC 膜和RC-g-KHCD 膜的孔径分布,其结果表明,修饰后RC-g-KHCD 膜的介孔范围明显增加。
2.4 RC-g-KHCD 膜的吸附性能
2.4.1 初始浓度的影响
初始浓度对RC 膜和RC-g-KHCD 膜吸附性能的影响如图5 所示。

图5 初始浓度对苯酚和异丙甲草胺平衡吸附量的影响(T=25 ℃,pH=7)Fig.5 Effect of initial concentration on adsorption capacity of phenol and metolachlor(T=25 ℃,pH=7)
由图5 可见,由于KHCD 的修饰,RC-g-KHCD 膜对苯酚和异丙甲草胺的平衡吸附量均高于RC 膜。对于RC-g-KHCD 膜,苯酚的平衡吸附量随初始浓度的增加先增加然后趋于稳定,最大平衡吸附量稳定在0.13 mmol/g。而对于异丙甲草胺,平衡吸附量随初始浓度的增加并没有出现稳定的趋势,是由于异丙甲草胺在水中的溶解度有限,低浓度范围不能使β-CD 对其吸附达到饱和,在异丙甲草胺可溶解的范围内,RC-g-KHCD 膜对其最大平衡吸附量为0.048 mmol/g。
2.4.2 吸附热力学
通过Langmuir 和Freundlich 等温吸附模型对吸附数据进行拟合,探究复合膜的吸附热力学性能,拟合所得数据如表1 所示。注:qmax为达到饱和时最大吸附量;b为Langmuir 吸附常数;Kf为Freundlich 吸附常数;n为非均质系数。

表1 RC-g-KHCD 膜对苯酚和异丙甲草胺的吸附等温线拟合参数(T=25 ℃)Tab.1 Adsorption isotherm parameters for phenol and metolachlor of RC-g-KHCD membrane(T=25 ℃)
由表1 可明显看出,对于苯酚和异丙甲草胺的吸附,Langmuir 模型的相关系数R2均大于Freundlich 模型。根据Langmuir 模型所拟合的理论最大平衡吸附量更接近实验所测得实际数据,所以,苯酚和异丙甲草胺分子在RC-g-KHCD 膜表面的吸附行为更符合Langmuir 吸附,形成单分子层。
图6为RC-g-KHCD 膜对苯酚和异丙甲草胺的吸附等温线。
表1和图6 表明,RC-g-KHCD 膜对异丙甲草胺的吸附有持续增长的趋势。这是由于当苯酸浓度较高时,疏水作用使苯酚发生富集,吸附量再次大幅增加。

图6 RC-g-KHCD 膜对苯酚和异丙甲草胺的吸附等温线(T=25 ℃)Fig.6 Adsorption isotherms of phenol and metolachlor of RC-g-KHCD membrane(T=25 ℃)
2.4.3 吸附动力学
RC-g-KHCD 膜对苯酚和异丙甲草胺在不同浓度下的吸附动力学曲线如图7 所示。
由图7 可知,在不同浓度下,平衡吸附量随吸附时间的变化呈现相同的趋势,在起始阶段,吸附量随吸附时间的增加快速增加,然后逐渐趋于稳定。当起始质量浓度比较低时,对于苯酚的吸附在20 min 内可达到平衡状态,而对于异丙甲草胺,吸附平衡时间需要120 min 以上,吸附平衡时间随起始浓度的增加而呈增加趋势。很明显,对于异丙甲草胺达到吸附平衡的时间要高于苯酚,原因是由于其较大的分子体积增加了传质阻力。为了进一步分析吸附动力学行为,采用伪一级动力学模型和伪二级动力学模型对该数据进行拟合,拟合参数如表2 所示。

表2 RC-g-KHCD 膜对苯酚和异丙甲草胺的吸附动力学拟合参数Tab.2 Kinetic parameters for phenol and metolachlor adsorption of RC-g-KHCD membranes

图7 RC-g-KHCD 膜对苯酚和异丙甲草胺在不同浓度下的吸附动力学曲线(T=25 ℃,pH=7)Fig.7 Adsorption kinetics of RC-g-KHCD membrane for phenol and metolachlor at different initial concentrations(T=25 ℃,pH=7)
伪一级动力学模型:
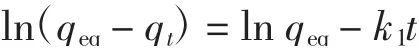
伪二级动力学模型:

式中:qt和qeq分别对应t时刻和吸附平衡时的吸附量(mmol/g);k1(min-1)和k2(g·mmol-1·min-1)分别是伪一级和伪二级动力学模型的吸附速率常数。
由表2 可知,无论对于苯酚还是异丙甲草胺,伪二级动力学模型的相关系数R2均略微高于伪一级动力学。然而,由伪一级动力学拟合的平衡吸附量更接近实际实验测得的数据。所以,很难通过当前的拟合结果判断该吸附行为的属性。为了进一步描述吸附动力学模型,可将β-CD 吸附苯酚(异丙甲草胺)分为3 个过程:一是膜扩散,即苯酚或异丙甲草胺分子通过边界层从本体溶液迁移到RC-g-KHCD 膜表面;二是孔内扩散,即苯酚或异丙甲草胺分子从膜表面转移到膜孔内;三是化学反应,即苯酚或异丙甲草胺分子与RC-g-KHCD 膜孔内活性吸附位点KH-CD 发生相互作用(氢键、疏水作用和π-π 相互作用)[16],其相互作用机理如图8 所示。每一个过程用一个具体模型进行描述,即膜扩散模型、孔内扩散模型和化学反应模型,将吸附动力学曲线再次用以上3 个模型拟合,来确定具体的决速步,拟合结果如表3 所示。

表3 RC-g-KHCD 膜对苯酚和异丙甲草胺吸附的决速步拟合参数Tab.3 Fitting parameters of rate-limiting step for phenol and metolachlor adsorption of RC-g-KHCD membranes

图8 氢键、π-π 相互作用和疏水相互作用的作用机理Fig.8 Interaction mechanism of hydrogen bond and π-π interaction and hydrophobic interaction
对于苯酚和异丙甲草胺的吸附,膜扩散模型的相关系数R2均明显高于其他2 个模型,而且膜扩散模型所拟合的吸附量与实际数据最接近。所以,膜扩散是RC-g-KHCD 膜吸附苯酚和异丙甲草胺的决速步,伪一级动力学模型更适合描述该吸附行为,故可判断为物理吸附在吸附过程中是主要限速步骤。孔内模型呈现最低的相关性,表明孔内扩散的阻力最小,源于RC 膜大孔促进传质的优势。吸附过程中,RC-g-KHCD 膜中因β-环糊精的存在而含有大量的—OH 基团,—OH基团参与了RC-g-KHCD 吸附苯酚和异丙甲草胺。同时,通过R2值的对比发现Langmuir 模型更适合模拟苯酚和异丙甲草胺在RC-g-KHCD 上的吸附,表明RC-g-KHCD 对苯酚和异丙甲草胺的吸附为单层吸附[21]。
2.4.4 循环使用性能
为了对RC-g-KHCD 膜实际应用的经济性进行评价,分析其循环使用性能如图9 所示。

图9 RC-g-KHCD 膜对苯酚和异丙甲草胺的循环使用性能(T=25 ℃,C0=0.15 g/L)Fig.9 Regeneration performance of RC-g-KHCD membrane for phenol and metolachlor adsorption(T=25 ℃,C0=0.15 g/L)
由图9 可知,经过温和的甲醇洗涤再生后,RC-g-KHCD 膜对苯酚和异丙甲草胺重复吸附10 次后,再生效率均可达到90%以上,具有巨大的工业应用潜力。
2.4.5 与同类吸附剂的比较
表4为几项有代表性且与本工作可比较的结果。

表4 RC-g-KHCD 膜与其他β-CD 功能化的吸附剂对苯酚吸附的比较Tab.4 Comparisons of phenol adsorption property with different cyclodextrin-based adsorbents and RC-g-KHCD
由表4 可以看出,多级孔RC-g-KHCD 膜具有较高的吸附速率与相当的平衡吸附容量。值得一提的是,得益于其介孔-大孔的多级孔结构,使得其吸附平衡时间明显低于其他环糊精修饰的吸附剂。虽然,其吸附容量很大程度上受到RC 大孔膜低比表面积的本征局限,但是,通过优化表面交联聚硅氧烷的微观结构仍有改进的潜力。
3 结 论
(1)通过简单的硅烷偶联反应,将β-CD 修饰RC膜制备出具有介孔-大孔多级孔结构的RC-g-KHCD膜。
(2)RC-g-KHCD 膜对苯酚和异丙甲草胺具有良好的吸附性能,分别达到0.130 mmol/g 和0.048 mmol/g,其对苯酚的吸附平衡时间明显低于其他环糊精修饰的吸附剂,同时具有较高的再生效率,重复使用10 次后,再生效率仍均达到90%以上。
