Fe3O4-nZVI类Fenton法降解水中磺胺甲恶唑
2022-07-19谢欣卓钟金魁郑博文
谢欣卓,钟金魁,2*,李 静,郑博文
Fe3O4-nZVI类Fenton法降解水中磺胺甲恶唑
谢欣卓1,钟金魁1,2*,李 静1,郑博文1
(1.兰州交通大学环境与市政工程学院,甘肃 兰州 730070;2.甘肃省黄河水环境重点实验室,甘肃 兰州 730070)
采用共沉淀和液相还原两步法制得四氧化三铁负载纳米零价铁(Fe3O4-nZVI),将其作为类Fenton反应的催化剂用于水中磺胺甲恶唑(SMX)的降解.通过批实验法研究了H2O2浓度、Fe3O4-nZVI投加量、pH值、SMX初始浓度、反应温度等因素对SMX降解的影响.SEM、EDS、XRD和XPS表征结果表明,制备的Fe3O4-nZVI为纳米级磁性复合材料.批实验结果表明,在一定实验条件范围内,提高H2O2浓度、Fe3O4-nZVI投加量和反应温度,以及降低体系pH值,均可提高SMX的降解率.动力学拟合参数表明,SMX的类Fenton催化降解符合拟一级动力学模型.在25℃时,当H2O2浓度为10mmol/L、Fe3O4-nZVI投加量为0.8g/L、pH=3、SMX初始浓度为10mg/L,SMX在180min时的降解率为99.61%.用VSM测得Fe3O4-nZVI的饱和磁化强度为105.52emu/g,表明其易于磁回收.重复利用实验表明,Fe3O4-nZVI具有较好的反应活性和稳定性.自由基淬灭实验表明,·OH的氧化作用是SMX降解的主要机理.
Fe3O4-nZVI;高级氧化;类Fenton;磺胺甲恶唑
磺胺类抗生素(SAs)因其抗菌谱广、性质稳定成为使用较多的抗生素,世界上许多河流沉积物、地下水和土壤中可检出的SAs多达10几种[1].磺胺甲恶唑(SMX)作为SAs的典型代表,在我国长江、黄河、珠江等水域均有检出[2-3].低剂量时SMX仍具有生物活性,在相当低的浓度范围内,也可能对水生生物构成生态毒理风险,进而对人类健康带来潜在危害.因此,有效消除环境中的SMX成为当前研究的热点.
Fenton法作为高级氧化技术(AOPs),广泛用于有机污染物的处理[4].Fenton体系中的金属催化剂与H2O2反应生成的高活性·OH自由基可攻击有机化合物,将其降解直至矿化.传统均相Fenton催化反应存在pH值适用范围窄、铁泥量大等缺点.为此,相关研究提出用非均相催化剂取代均相催化剂,活化H2O2产生·OH[5].
纳米零价铁(nZVI)具有较强的吸附、还原及抗菌能力,是目前研究较多的环境纳米材料[6].但由于nZVI粒径小且具有磁性,极易团聚,大大降低了nZVI的电子转移能力和反应活性.同时,其在空气中稳定性差,表面易氧化[7-9],因此,对nZVI改性十分必要.其改性方法有金属修饰、表面改性和固体负载等.研究表明负载法可以提高nZVI的稳定性,抑制颗粒之间的团聚,使其在水中的迁移能力显著增强,对污染物的处理效果大大提高[10].
近年来,邓俊敏[11]以生物炭、Gopal等[12]以膨润土为载体制备了nZVI复合材料与H2O2构建非均相类Fenton体系,可分别去除74.04%的磺胺二甲基嘧啶和95%的四环素.陈苗等[13]用磁性纳米Fe3O4活化H2O2,短时间内几乎可以完全降解20mg/L的SMX.由此可见,负载型nZVI和Fe3O4常作为类Fenton体系的非均相催化剂.以上研究虽然对污染物有较好的去除效果,也能实现部分催化剂的回收利用,但无法实现Fe0-Fe2+-Fe3+的动态循环.将nZVI负载到Fe3O4上,可促进Fe在Fenton体系中的内循环,减少铁泥量,缓解nZVI的团聚和氧化,提高污染物的降解效率,实现催化剂的高效磁回收利用,但这方面的研究还鲜见报道.
本文通过共沉淀和液相还原两步法制得Fe3O4-nZVI纳米复合材料,与H2O2结合,构建类Fenton体系对SMX进行降解研究.重点考察了H2O2浓度、Fe3O4-nZVI投加量、pH值、SMX初始浓度、反应温度、Fe3O4-nZVI回收利用次数对SMX降解效果的影响.初步探究了Fe3O4-nZVI类Fenton体系中SMX的降解机理.
1 材料与方法
1.1 实验试剂
试剂:磺胺甲恶唑(SMX)购自上海麦克林生化科技有限公司(生物技术级);FeSO4∙7H2O和FeCl3∙6H2O购自上海阿拉丁生化科技股份有限公司;NaBH4和NH3·H2O购自天津大茂化学试剂有限公司;H2O2、NaOH购自国药集团化学试剂公司;CH3COOH购自利安隆博华(天津)医药化学有限公司;HCl购自北京化工厂.以上试剂均为分析纯.CH3OH购自山东禹王和天下新材料有限公司(色谱纯).高纯氮气购自咸阳伟丽气体制造有限公司.
1.2 实验材料
Fe3O4-nZVI的制备:首先通过共沉淀法制备纳米Fe3O4,再通过自下而上制备法中的液相还原法制备nZVI,完成负载过程[14-16].
准确称取2.8082g的FeSO4∙7H2O和5.4606g的FeCl3∙6H2O至四口烧瓶,加入去离子水,在高纯氮气保护下,持续搅拌溶解,缓慢滴入1mol/L的NH3·H2O (为使充分反应,氨水应过量),反应见式(1).
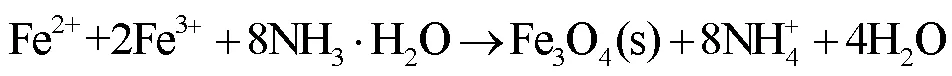
利用强磁铁将制得的Fe3O4从悬浊液中分离,用去离子水清洗5遍后,将所得Fe3O4再次分散至含有FeSO4溶液的四口烧瓶中.在氮气氛围中,通过恒压漏斗缓慢滴加过量的NaBH4溶液,并不断搅拌,当NaBH4滴加完毕后继续搅拌30min,即得Fe3O4- nZVI,反应见式(2).
(2)
1.3 实验方法
准确称取0.01g的SMX,先用少量色谱级甲醇助溶,再用去离子水定容于100mL棕色容量瓶,得100mg/L的SMX储备液,4℃恒温避光保存.SMX降解实验在50mL棕色具塞三角瓶中进行,准确量取一定量的SMX、H2O2、Fe3O4-nZVI、去氧水,控制反应总体积为40mL.用0.1mol/L的HCl和NaOH调节反应体系的初始pH值,将三角瓶密封置于恒温振荡器中.设定转速为150r/min,调节反应温度,分别于10,30,60,90,120,150,180min时取样2mL,过0.22μm膜,用高效液相色谱仪(HPLC)测定滤液中SMX的含量.取样时,在进样瓶中加入0.15mL甲醇对体系内的自由基进行淬灭.每组实验设2个平行样.
1.4 分析方法
SMX浓度用液质联用仪(Thermo LCQ Advantage-40000)中的HPLC进行测定,色谱柱为C18反相柱(4.6×150mm,5μm Thermo).流动相为甲醇和0.2%乙酸溶液(:=40:60),流速0.2mL/min,柱温35℃,进样10μL,检测波长270nm.
SMX降解率()计算见式(3),降解动力学数据用拟一级动力学方程拟合,见式(4).
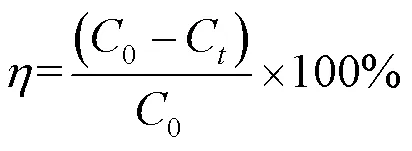
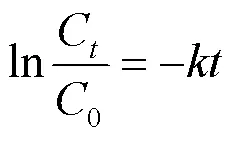
式中:0和C分别为SMX的初始浓度和反应时刻的浓度,mg/L;为反应时间,min;为拟一级反应速率常数,min-1.
2 结果与讨论
2.1 Fe3O4-nZVI的表征
由Fe3O4-nZVI放大20.00´103倍的扫描电镜图(SEM,图1)可以看出,Fe3O4-nZVI纳米颗粒呈球形,排列成链状.但也发现Fe3O4-nZVI之间的团聚现象严重,可能是磁偶极子和纳米尺寸效应所致[17],也可能是Fe3O4-nZVI分离回收时氧化团聚所致.

由Fe3O4-nZVI的X射线能谱图(EDS,见图1)可知,制备的样品中含有Fe、O、C、B、S元素,其中Fe、O元素质量分数较大.Fe出现3个特征峰,是由于Fe元素原子核外层的电子向其他层跃迁时,释放出的能量不同,在能谱图中显示出不同峰值.Tan等[17]对制备的Fe0@Fe3O4的核和外层进行EDS分析,证明了该复合材料的内核为Fe3O4,由此推测Fe3O4-nZVI以Fe3O4为核,外层被nZVI球形粒子包覆.
图2为nZVI、Fe3O4和Fe3O4-nZVI的X射线衍射图(XRD),可用于分析物质的晶相组成.将Fe3O4-nZVI的XRD图与Fe3O4标准图谱(JCPDS PDF#65-3107)进行对比,在2=30.10°、35.46°、43.10°、53.47°、57.01°、62.60°处均有衍射峰,分别对应Fe3O4晶体的(220)、(311)、(400)、(422)、(333)和(440)晶面,说明该材料中含有Fe3O4.在典型的nZVI衍射区,Fe3O4-nZVI的XRD图中仅有宽峰,说明nZVI在复合材料中呈无定形态[17].Fe3O4-nZVI衍射峰尖锐且窄,说明制得的复合材料结晶度较好.
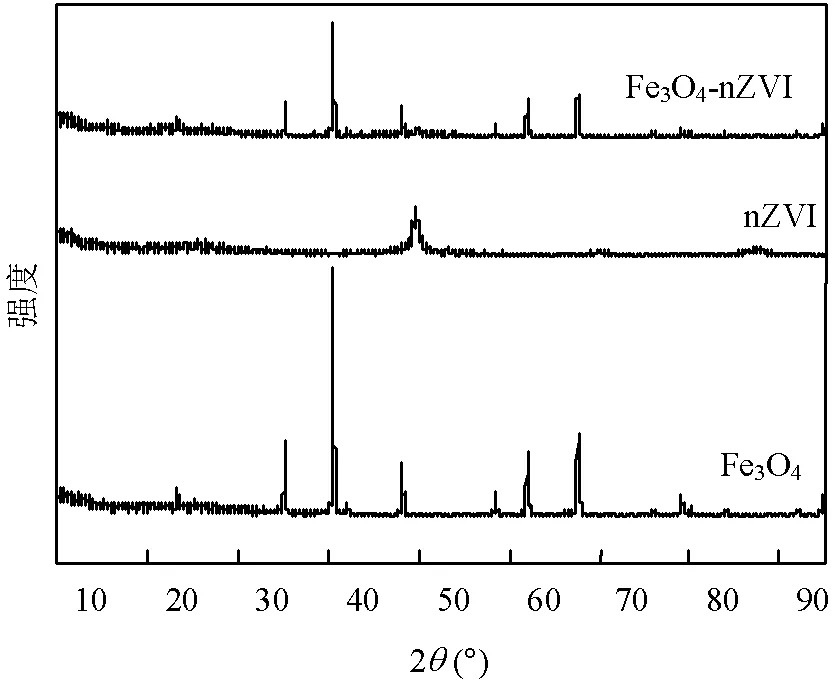
图2 nZVI、Fe3O4和Fe3O4-nZVI的XRD图
室温下3种物质的磁化曲线如图3所示,可以看出,nZVI、Fe3O4和Fe3O4-nZVI的饱和磁化强度(Ms)值分别为173.14,81.511和105.52emu/g.在外加磁场下,Ms值反映了磁分离性能,表明Fe3O4-nZVI易于实现固液分离[18],可磁回收利用,是该材料在水处理中使用的显著优势.
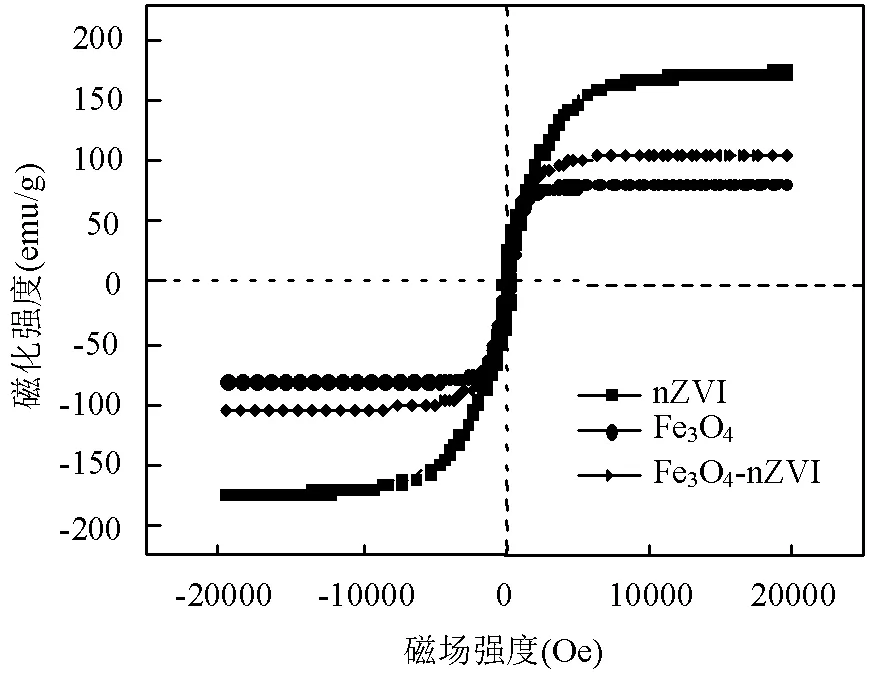
图3 nZVI、Fe3O4和Fe3O4-nZVI的磁化曲线
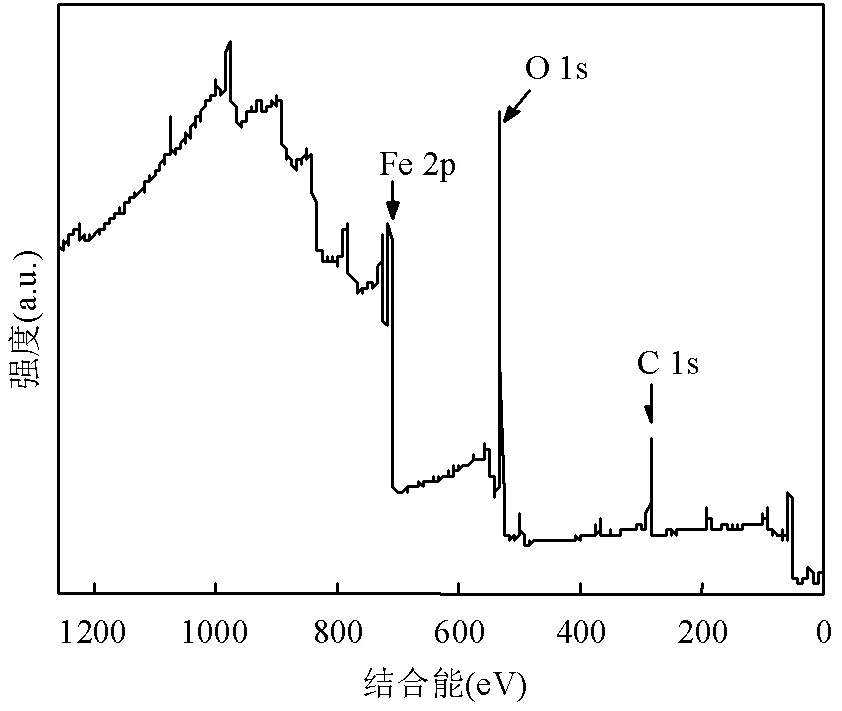
图4为Fe3O4-nZVI的X射线光电子能谱(XPS)分析,全谱扫描分析表明在710.31, 530.57, 284.80eV分别对应于Fe3O4-nZVI中的Fe 2p,O 1s和C 1s,表明制备的复合材料中有Fe、O、C 3种元素.Fe 2p中结合能为723.98和710.48eV时出现特征峰,分别为Fe 2p1/2和Fe 2p3/2.拟合后Fe02p3/2和Fe02p1/2的特征峰在结合能分别为706.74,719.67ev处出现,两处Fe0特征峰的出现说明复合材料中成功引入nZVI,Fe0含量较低可能是由于制备过程nZVI的氧化所致[19].
2.2 不同反应体系对SMX降解的影响
图5为25℃,pH=3,SMX初始浓度为10mg/L条件下,在H2O2、Fe3O4、nZVI单一体系及Fe3O4+H2O2、Fe3O4-nZVI、nZVI+H2O2、Fe3O4-nZVI +H2O2复合体系中SMX降解效果.
从图中看出,在单独的H2O2体系中,SMX经过180min反应后,去除率为13.63%,体系内无活性自由基产生,SMX难以去除.在Fe3O4、Fe3O4+H2O2体系中SMX去除率分别为35.74%和38.32%,这是因为Fe3O4具有一定的吸附能力,对SMX产生了吸附作用.在nZVI体系中,SMX的去除率为54.54%,这可能是由于酸性条件下,nZVI发生腐蚀,产生Fe2+和电子,nZVI的还原作用对SMX进行了一定程度的降解[20-21],另外,nZVI比表面积大,对SMX也有一定的吸附作用.相较于nZVI,在Fe3O4-nZVI体系中,去除率又增加了9.27%,可能是吸附和还原降解共同作用的结果.在nZVI+H2O2体系中,nZVI活化H2O2产生·OH,SMX降解率达到76.37%.Fe3O4-nZVI结合H2O2体系中,SMX降解率为94.09%,体系中的复合材料的核Fe3O4可以为体系提供更多的Fe2+,增加·OH的产生量.
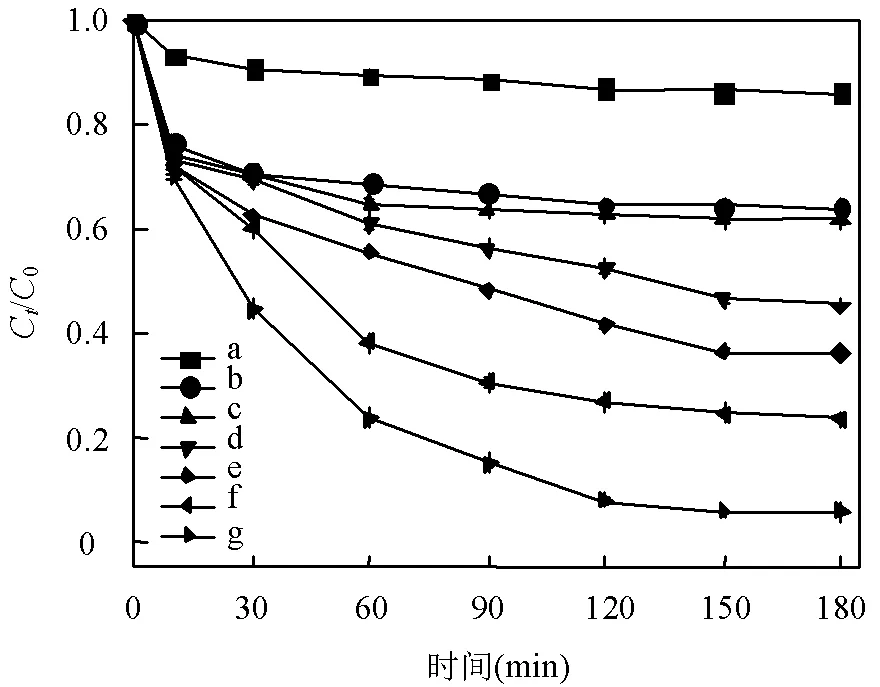
图5 不同反应体系对SMX降解的影响
a、H2O2;b、Fe3O4;c、Fe3O4+H2O2;d、nZVI;e、Fe3O4-nZVI;f、nZVI+H2O2;g、Fe3O4-nZVI +H2O2
铁基氧化物催化类Fenton降解SMX机理主要有(1)铁氧化物在酸性条件下产生的Fe2+与H2O2反应产生·OH;(2)H2O2吸附在铁基氧化物表面,实现Fe3+和Fe2+的相互转换,再与H2O2反应产生·OH[22].因此·OH对氧化降解有机污染物起到了重要作用.
2.3 H2O2浓度对SMX降解的影响
图6为25℃,SMX初始浓度为10mg/L,Fe3O4- nZVI投加量为0.6g/L,pH=3条件下,H2O2浓度对SMX降解的影响.
从图中看出反应150min后趋于稳定.当H2O2浓度在5~10mmol/L范围内,增加H2O2浓度,180min时SMX的降解率由87.15%增加至94.33%;当H2O2浓度继续增加至15mmol/L时,SMX降解率反而降低了11.48%.当H2O2浓度为20mmol/L时,SMX最大降解率为39.43%,降解效果较差.原因是H2O2作为类Fenton反应体系中的关键因素,·OH产生速率和数量受到其浓度的限制,增加H2O2浓度,·OH产生量增多,SMX降解速率加快.但当H2O2浓度过高时,会发生·OH的消除反应[23],见式(5)和式(6).反应过程中虽有HO2·生成,但其氧化能力弱于·OH[24],导致SMX降解率降低.因此H2O2有拐点浓度,并不是越大越好,这与裴欢等[25]研究结果一致,后续实验中H2O2浓度选用10mmol/L.
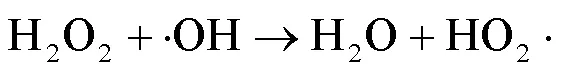
(6)
2.4 Fe3O4-nZVI投加量对SMX降解的影响
图7为25℃,SMX初始浓度为10mg/L,H2O2浓度为10mmol/L, pH=3条件下,Fe3O4-nZVI投加量对SMX降解的影响.
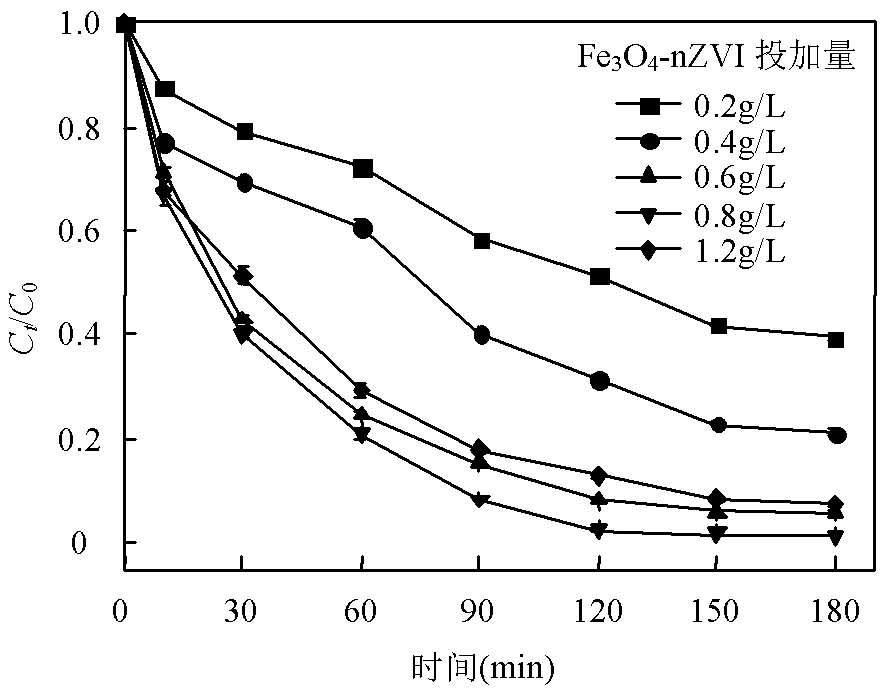
图7 Fe3O4-nZVI投加量对SMX降解的影响
当Fe3O4-nZVI投加量在0.2~0.8g/L范围时,随着Fe3O4-nZVI量的增加,SMX的降解率逐渐增大, 180min时SMX降解率由60.60%增至98.48%.原因是Fe3O4-nZVI越多,与H2O2结合的反应活性位点越多,产生的·OH也就越多,SMX的降解也就越彻底[11].但当Fe3O4-nZVI的量增至1.2g/L时,SMX降解率反而下降至92.69%,这可能是Fe3O4-nZVI表面反应活性位点增加,体系中·OH量增加,但·OH寿命极短,在液相中仅10-9s,还未与SMX发生反应,就被体系中的H2O2、HO2·、Fe2+消耗,分别见式(5)~式(7),·OH数量减少,SMX降解率就会下降[26].因此,后续实验中Fe3O4-nZVI投加量取0.8g/L.
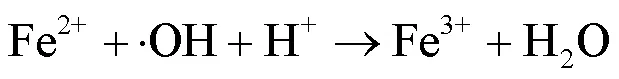
2.5 pH值对SMX降解的影响
图8为25℃,SMX初始浓度为10mg/L,H2O2浓度为10mmol/L,Fe3O4-nZVI投加量为0.8g/L条件下下,溶液初始pH值对SMX降解率的影响.
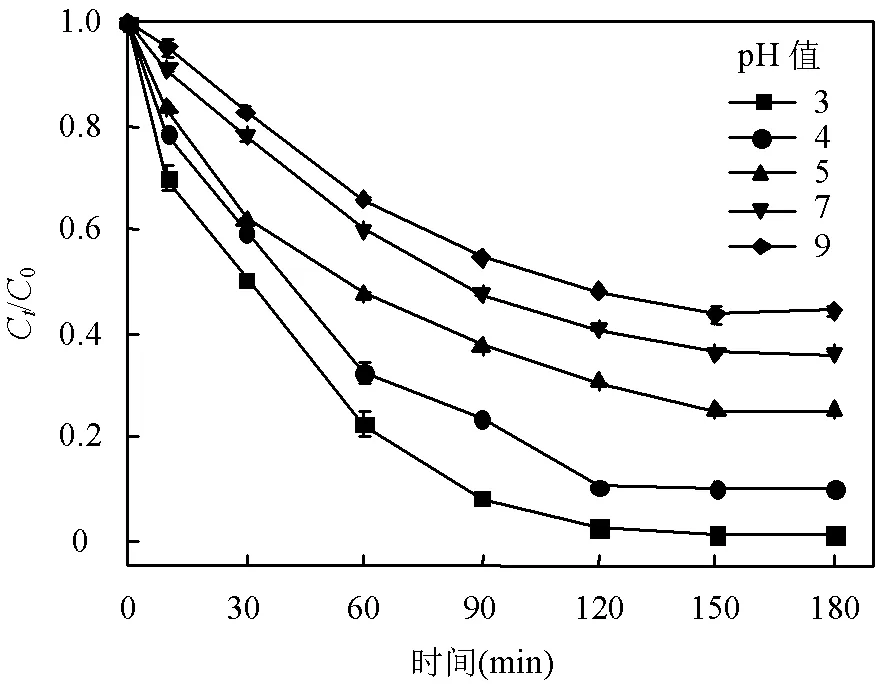
图8 初始pH值对SMX降解的影响
从图中可知,随着pH值的增大,SMX的降解率下降.当pH=3时,180min时SMX降解率为98.97%,体系中大多数SMX被降解.当pH值由4升高至5时,降解率仍保持在75%以上.当初始溶液呈中性时,SMX降解率降至63.93%,随着pH值继续增大至9时,SMX降解率降至55.63%.说明SMX的降解在酸性体系下效果更好.这是因为酸性条件下,有利于Fe2+的形成和维持,Fe2+对·OH的形成起关键作用,从而产生更多的·OH,同时nZVI的析氢腐蚀也发生在酸性条件,见式(8),nZVI被腐蚀导致表面积增大,从而增加Fe2+的释放速率[27-28].当反应体系中pH值较高时,体系中的H+减少,OH-增多,Fe2+容易发生沉淀,见式(9),高pH值加速了nZVI表面钝化,阻止了nZVI进一步释放Fe2+[29].
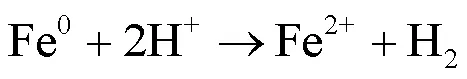
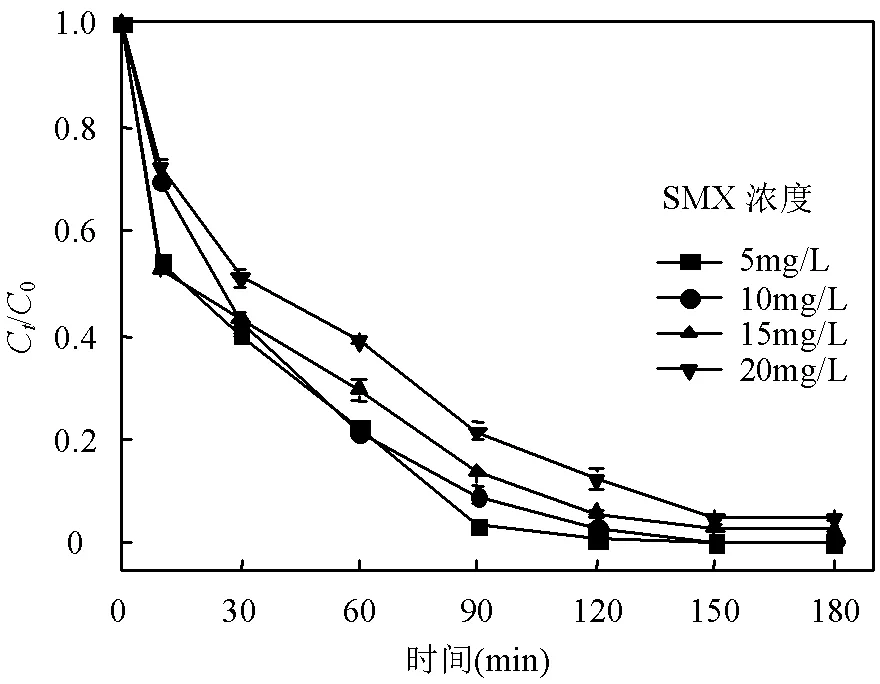
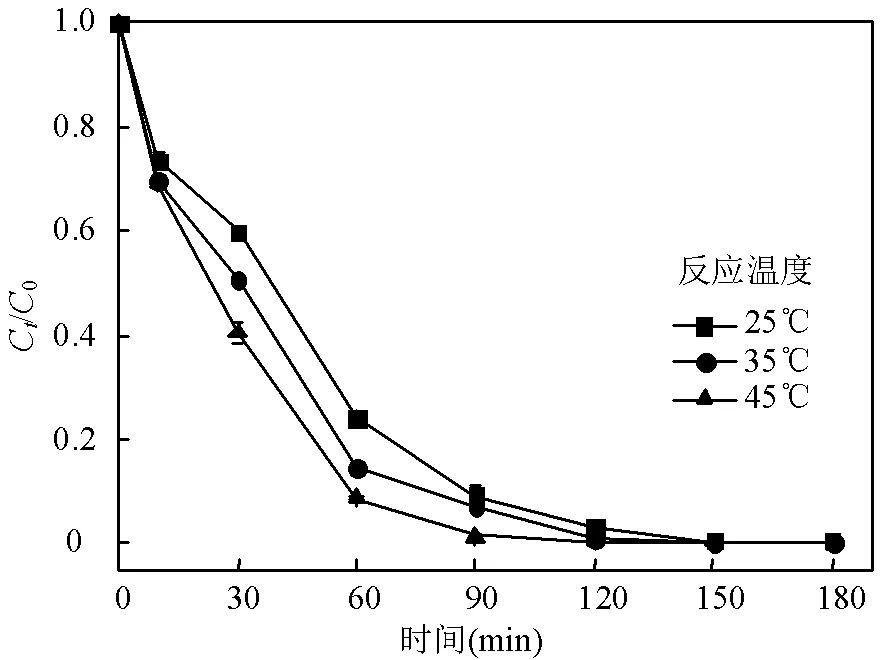
Sun等[30]研究表明可离子化有机物在不同pH值下,由于pa的不同,会表现出不同的存在形态(分子态或离子态),影响有机物与氧化体系中的活性物质的结合和反应.另一方面,不同pH值下,氧化体系中的自由基的类型和氧化能力也有所不同.SMX有1个碱性氨基(-NH2)和1个酸性亚氨基(-NH-),2个基团的解离常数pa1= (1.85±0.30)和pa2= (5.60± 0.04)分别对应苯胺的质子化和磺酰胺的去质子化.在特定的pH值下,氨基能够获得一个质子,而亚氨基能够释放一个质子[31].在3£pH£5时,中性的SMX0占主导;pH³6时,阴离子形式的SMX-占主导;当pH 图9可得,在25℃,H2O2浓度为10mmol/L, Fe3O4-nZVI投加量为0.8g/L, pH=3的条件下,反应180min,SMX初始浓度为5,10,15,20mg/L,SMX的降解率分别为99.78%、99.52%、97.27%和95.24%. SMX降解率均在95%以上,说明Fe3O4-nZVI类Fenton法对SMX有较好的降解效果.随着SMX初始浓度的增加,SMX的降解率略有降低.可能是当体系内Fe3O4-nZVI的量一定时,产生的·OH数量就一定,当SMX浓度增加时,·OH相对不足,SMX与·OH接触的机率相对减少,同时体系内产生的中间产物也会消耗一定的·OH[33]. 图9 SMX初始浓度对SMX降解的影响 图10为SMX初始浓度为10mg/L,H2O2浓度为10mmol/L,Fe3O4-nZVI投加量为0.8g/L, pH=3时,反应温度对SMX降解效果的影响,当温度由25℃升至45℃,反应180min后,SMX降解率由99.61%增至99.92%,反应温度对SMX降解的影响并不明显.在90min内, 45℃的反应速率高于35℃和25℃,但随着反应时间的增加,SMX的降解率逐渐趋于稳定. 图10 反应温度对SMX降解的影响 在0~90min时,随着温度升高,反应体系获得了能量,加剧了分子的热运动,SMX与体系中·OH的接触更加充分,从而提高了反应速率和降解率.升高温度促进了体系中复合材料表面nZVI转变为Fe2+[28],继而产生·OH降解SMX.反应120min后,升高温度对SMX最终降解率无明显提升,而且高温需要消耗大量能量,从节能角度出发,最佳反应温度选25℃. 根据图3磁化曲线分析可知,Fe3O4-nZVI在强磁场下易于回收分离,材料具有循环利用的优势.因此,本文对反应后的Fe3O4-nZVI材料进行磁回收.具体说,将反应后的Fe3O4-nZVI材料利用强磁场分离后,先用甲醇清洗2~3遍,再用去离子水清洗2遍,洗去材料表面附着的污染物及可能存在的降解副产物,置于60℃真空干燥箱干燥.干燥后的样品在单因素最佳实验条件下,即25℃, pH=3,SMX浓度为10mg/L,H2O2浓度为10mmol/L,Fe3O4-nZVI投加量为0.8g/L,进行了Fe3O4-nZVI重复利用性能研究. 图11为Fe3O4-nZVI循环使用次数对SMX降解率的影响.由图看出,Fe3O4-nZVI使用4次,其对SMX的降解率仍保持在90%以上,表现出较好的反应活性,说明该复合材料具有良好的循环利用性能. 图11 Fe3O4-nZVI循环利用次数对SMX降解的影响 表1 Fe3O4-nZVI类Fenton体系降解SMX的拟一级动力学拟合参数 由表1看出,Fe3O4-nZVI投加量、pH值、SMX初始浓度、反应温度、使用次数拟合结果中,相关系数2值均大于0.93,说明Fe3O4-nZVI对SMX的降解过程符合拟一级动力学方程. H2O2浓度、Fe3O4-nZVI投加量、pH值拟合参数中的最大反应速率常数()约为最小反应速率常数的5倍多.当SMX浓度从5mg/L增大到20mg/L时,反应速率常数约为原来的1/2,反应活性降低.当温度由25℃升至45℃时,由0.0361min-1增至0.0466min-1,根据阿伦尼乌斯公式(见式(10)),用ln对1/作图,通过拟合后的斜率计算表观活化能a.计算得该反应需要的反应活化能为10.12kJ/mol,活化能很低,表明催化活性很高[28,34].使用次数为1、2、3和4次分别对应的为0.0361、0.0217、0.0191和0.0159min-1,材料使用1次的值与循环4次后相差约1.27倍,说明该材料重复使用后仍有较好的反应活性和催化性能. 式中:为拟一级反应速率常数,min-1;为指前因子, min-1;是理想气体常数,8.314J/(mol·K);a为反应活化能,kJ/mol,是绝对温度,K. 据报道[35],在·OH氧化体系下,亚硝酸钠(NaNO2)、甲醇(MeOH)、乙醇(EtOH)和叔丁醇(TBA)作为淬灭剂的淬灭效果更佳. 图12 自由基淬灭实验 本文选取甲醇作为·OH的淬灭剂进行淬灭实验.实验在25℃,H2O2浓度为10mmol/L、Fe3O4-nZVI投加量为0.8g/L、pH=3.0、SMX初始浓度为10mg/L的条件下进行,空白为不加淬灭剂,淬灭组加入一定体积的甲醇.结果如图12所示.反应180min后SMX降解率由无淬灭剂的99.58%降低至有淬灭剂的27.54%,降解率下降了72.04%,表明类Fenton体系内产生的·OH是SMX降解的主要机理. Zhang等[36]、Huang等[37]在类Fenton体系中对SMX的降解实验研究表明,SMX降解的主要路径有(1)·OH攻击S-N键和C-N键,是SMX氧化降解的典型途径;(2)苯环上的氨基作为富电子基团易受到·OH攻击,形成氧化产物,是经典的氧化过程;(3)苯环上引入·OH后形成羟基化的SMX;(4)异恶唑环被打开或者是发生双环加成反应.上述路径生成的中间产物可在·OH进一步氧化作用下,打开芳香环生成短链酸,短链酸氧化后可形成CO2和H2O,实现SMX的矿化. 3.1 通过共沉淀和液相还原法制得Fe3O4-nZVI纳米材料,并将其用于类Fenton反应降解水中的SMX,在25℃,H2O2浓度为10mmol/L、Fe3O4-nZVI投加量为0.8g/L、pH=3、SMX初始浓度为10mg/L的条件下,反应180min后,SMX降解率为99.61%. 3.2 Fe3O4-nZVI类Fenton法降解水中SMX的过程符合拟一级动力学模型. 3.3 Fe3O4-nZVI纳米复合材料具有良好的重复利用性能,循环使用4次后, Fe3O4-nZVI类Fenton体系对SMX降解率仍保持在90%以上. 3.4 ·OH氧化SMX是Fe3O4-nZVI类Fenton技术降解SMX的主要机理. [1] Dmitrienko S G, Kochuk E V, Apyari V V, et al. Recent advances in sample preparation techniques and methods of sulfonamides detection – A review [J]. Analytica Chimica Acta, 2014,850:6-25. [2] 赵富强,高 会,张克玉,等.中国典型河流水域抗生素的赋存状况及风险评估研究 [J]. 环境污染与防治, 2021,43(1):94-102. Zhao F Q, Gao H, Zhang K Y, et al. Occurrence and risk assessment of antibiotics in typical river basins in China [J]. Environmental Pollution & Control, 2021,43(1):94-102. [3] 张晶晶,陈 娟,王沛芳,等.中国典型湖泊四大类抗生素污染特征[J]. 中国环境科学, 2021,41(9):4271-4283. Zhang J J, Chen J, Wang P F, et al. Pollution characteristics of four-type antibiotics in typical lakes in China [J]. China Environmental Science, 2021,41(9):4271-4283. [4] Yang B, Tian Z, Zhang L, et al. Enhanced heterogeneous Fenton degradation of Methylene Blue by nanoscale zero valent iron (nZVI) assembled on magnetic Fe3O4/reduced graphene oxide [J]. Journal of Water Process Engineering, 2015,5:101-111. [5] 陈 勇,胡 鹭,谭 旎,等.Al0-Gr-Fe0活化O2类Fenton氧化降解土霉素的研究[J]. 中国环境科学, 2021,41(10):4645-4653. Chen Y, Hu L, Tan N, et al. Oxidative degradation of oxytetracycline by a Fenton-like process with Al0-Gr-Fe0activated of O2[J]. China Environmental Science, 2021,41(10):4645-4653. [6] Lv D, Zhou X, Zhou J, et al. Design and characterization of sulfide-modified nanoscale zero valent iron for cadmium(II) removal from aqueous solutions [J]. Applied Surface Science, 2018,442: 114-123. [7] Zou Y, Wang X, Khan A, et al. Environmental remediation and application of nanoscale zero-valent iron and its composites for the removal of heavy metal ions: a review [J]. Environmental Science & Technology, 2016,50(14):7290-7304. [8] Wu Y, Zhang J, Tong Y, et al. Chromium (VI) reduction in aqueous solutions by Fe3O4-stabilized Fe0nanoparticles [J]. Journal of Hazardous Materials, 2009,172(2/3):1640-1645. [9] 徐海玉,张明青,陈翌昱.有机凹凸棒石负载纳米零价铁去除水中六价铬[J]. 中国环境科学, 2019,39(12):5079-5084. Xu H Y, Zhang M Q, Chen Y Y. Removal of Cr(VI) from aqueous solution using organically modified attapulgite-supported nanoscale zero-valent iron [J]. China Environmental Science, 2019,39(12):5079- 5084. [10] Lyu H, Tang J, Huang Y, et al. Removal of hexavalent chromium from aqueous solutions by a novel biochar supported nanoscale iron sulfide composite [J]. Chemical Engineering Journal, 2017,322:516-524. [11] 邓俊敏.生物炭负载纳米零价铁在还原及氧化体系下对污染物的去除研究 [D]. 长沙:湖南大学, 2018. Deng J M. A study on the application of nanoscale zero-valent iron/biochar composite on remediation of contaminated water in both reducing and oxidizing system [D]. Changsha: Hunan University, 2018. [12] Gopal G, Sankar H, Natarajan C, et al. Tetracycline removal using green synthesized bimetallic nZVI-Cu and bentonite supported green nZVI-Cu nanocomposite: A comparative study [J]. Journal of Environmental Management, 2020,254:109812. [13] 陈 苗,胡春华,郭昌胜,等.磁性Fe3O4纳米颗粒的制备及其催化降解水中磺胺甲恶唑研究 [J]. 水资源与水工程学报, 2018,29(5):46- 52. Chen M, Hu C H, Guo C S, et al. Synthesis of Fe3O4magnetic nanoparticles and its application in catalytic degradation of sulfamethoxazole in water [J]. Journal of Water Resources and Water Engineering, 2018,29(5):46-52. [14] Huang R, Fang Z, Yan X, et al. Heterogeneous sono-Fenton catalytic degradation of bisphenol A by Fe3O4magnetic nanoparticles under neutral condition [J]. Chemical Engineering Journal, 2012,197:242- 249. [15] Xu J, Tan L, Baig S A, et al. Dechlorination of 2,4-dichlorophenol by nanoscale magnetic Pd/Fe particles: Effects of pH, temperature, common dissolved ions and humic acid [J]. Chemical Engineering Journal, 2013,231:26-35. [16] 黄雪征,张永祥,田振军,等.纳米零价铁的制备、改性及场地应用研究进展 [J]. 水处理技术, 2021,47(1):12-18,26. Huang X Z, Zhang Y X, Tian Z J, et al. Research progress in synthesis, modification and field application of nano zero-valent iron [J]. Technology of Water Treatment, 2021,47(1):12-18,26. [17] Tan L, Lu S, Fang Z, et al. Enhanced reductive debromination and subsequent oxidative ring-opening of decabromodiphenyl ether by integrated catalyst of nZVI supported on magnetic Fe3O4nanoparticles [J]. Applied Catalysis B: Environmental, 2017,200:200-210. [18] 刘焕联,李贤英,魏贝贝,等.超顺磁性纳米Fe3O4的制备及其类Fenton反应性能[J]. 环境工程学报, 2017,11(6):3525-3531. Liu H L, Li X Y, Wei B B, et al. Synthesis of super-paramagnetic Fe3O4nanoparticles and its Fenton-like properties [J]. Chinese Journal of Environmental Engineering, 2017,11(6):3525-3531. [19] Lv X, Xu J, Jiang G, et al. Highly active nanoscale zero-valent iron (nZVI)–Fe3O4nanocomposites for the removal of chromium(VI) from aqueous solutions [J]. Journal of Colloid and Interface Science, 2012, 369(1):460-469. [20] Fu F, Dionysiou D D, Liu H. The use of zero-valent iron for groundwater remediation and wastewater treatment: A review [J]. Journal of Hazardous Materials, 2014,267:194-205. [21] Sun X, Kurokawa T, Suzuki M, et al. Removal of cationic dye methylene blue by zero-valent iron: Effects of pH and dissolved oxygen on removal mechanisms [J]. Journal of Environmental Science and Health, Part A, 2015,50(10):1057-1071. [22] Kwan W P, Voelker B M. Rates of hydroxyl radical generation and organic compound oxidation in mineral-catalyzed Fenton-like systems [J]. Environmental Science & Technology, 2003,37(6):1150- 1158. [23] Kitajima N, Fukuzumi S, Ono Y, et al. Formation of superoxide ion during the decomposition of hydrogen peroxide on supported metals [J]. The Journal of Physical Chemistry, 1978,82(13):1505-1509. [24] Wu H, Dou X, Deng D, et al. Decolourization of the azo dye Orange G in aqueous solution via a heterogeneous Fenton-like reaction catalysed by goethite [J]. Environmental Technology, 2012,33(14):1545-1552. [25] 裴 欢,毛 飞,司友斌.纳米铁氧化物催化类Fenton反应降解抗生素磺胺[J]. 农业环境科学学报, 2015,34(7):1356-1362. Pei H, Mao F, Si Y B. Degradation of antibiotic sulfanilamide in aqueous solution via a heterogeneous fenton-like reaction catalyzed by nano-iron oxides [J]. Journal of Agro-Environment Science, 2015, 34(7):1356-1362. [26] 邓景衡,文湘华,李佳喜.碳纳米管负载纳米四氧化三铁多相类芬顿降解亚甲基蓝[J]. 环境科学学报, 2014,34(6):1436-1442. Deng J H, Wen X H, Li J X. Degradation of methylene blue by heterogeneous Fenton-like reaction using Fe3O4/carbon nanotube composites [J]. Acta Scientiae Circumstantiae, 2014,34(6):1436-1442. [27] 关英红,孙维敬,王盼盼.PMS/Fe0体系中自由基产率比及莠去津降解动力学[J]. 哈尔滨工业大学学报, 2022,54(2):50-58. Guan Y H, Sun W J, Wang P P. Radical production ratio and atrazine degradation kinetics in PMS/Fe0system [J]. Journal of Harbin Institute of Technology, 2022,54(2):50-58. [28] Wei X, Gao N, Li C, et al. Zero-valent iron (ZVI) activation of persulfate (PS) for oxidation of bentazon in water [J]. Chemical Engineering Journal, 2016,285:660-670. [29] 林爱秋,程和发.芬顿及光芬顿法降解氟喹诺酮类抗生素研究进展[J]. 环境化学, 2021,40(5):1305-1318. Lin A Q, Cheng H F. Recent development in the degradation of fluoroquinolones by Fenton and photo-Fenton processes [J]. Environmental Chemistry, 2021,40(5):1305-1318. [30] Sun X, Qin Y, Zhou W. Degradation of amoxicillin from water by ultrasound-zero-valent iron activated sodium persulfate [J]. Separation and Purification Technology, 2021,275:119080. [31] Xekoukoulotakis N P, Drosou C, Brebou C, et al. Kinetics of UV- A/TiO2photocatalytic degradation and mineralization of the antibiotic sulfamethoxazole in aqueous matrices [J]. Catalysis Today, 2011, 161(1):163-168. [32] Kobayashi M, Kurosu S, Yamaguchi R, et al. Removal of antibiotic sulfamethoxazole by zero-valent iron under oxic and anoxic conditions: Removal mechanisms in acidic, neutral and alkaline solutions [J]. Journal of Environmental Management, 2017,200:88-96. [33] 王 磊,王海霞,吕效平.Fenton法处理水中4,4’-二溴联苯及动力学研究[J]. 环境科学与技术, 2007,(12):69-72,121. Wang L, Wang H X, Lv X P. Treatment of 4,4’-dibromobiphenyl aqueous solution by Fenton's reagent and its kinetics study [J]. Environmental Science & Technology, 2007,(12):69-72,121. [34] 杨 博.金属氧化物/石墨烯复合材料催化降解亚甲基蓝研究[D]. 兰州:兰州大学, 2015. Yang B. Study on the Degradation of methylene blue catalyzed by metal oxide/graphene composites [D]. Lanzhou: Lanzhou University, 2015. [35] 白孟琦,李敏睿,丁欣欣,等.不同猝灭剂对SO4·-和·OH高级氧化体系的猝灭效果[J]. 工业水处理, 2021,41(8):75-80. Bai M Q, Li M R, Ding X X, et al. Quenching effect of different quenchers on SO4·-and ·OH based advanced oxidation processes [J]. Industrial Water Treatment, 2021,41(8):75-80. [36] Zhang X, Wang J, Duan B, et al. Degradation of sulfamethoxazole in water by a combined system of ultrasound/PW12/KI/H2O2[J]. Separation and Purification Technology, 2021,270:118790. [37] Huang Y, Yang J. Degradation of sulfamethoxazole by the heterogeneous Fenton-like reaction between gallic acid and ferrihydrite [J]. Ecotoxicology and Environmental Safety, 2021,226: 112847. Degradation of sulfamethoxazole in water by Fenton-like method using Fe3O4-nZVI. XIE Xin-zhuo1, ZHONG Jin-kui1,2*, LI Jing1, ZHENG Bo-Wen1 (1.School of Environmental and Municipal Engineering, Lanzhou Jiaotong University, Lanzhou 730070, China;2.Key Laboratory of Yellow River Water Environment of Gansu Province, Lanzhou 730070, China)., 2022,42(7):3103~3111 Fe3O4-nZVI was prepared by co-precipitation and liquid phase reduction method. The obtained Fe3O4-nZVI was used as catalyst of Fenton-like reaction to degrade sulfamethoxazole (SMX) in water. The effects of H2O2concentration, Fe3O4-nZVI dosage, pH of solution, SMX concentration and temperature on SMX degradation were investigated. The charactering results of SEM, EDS, XRD and XPS showed that the magnetic composite material with nanometer size was successfully prepared. The batch experimental results showed that the degradation rate of SMX in Fenton-like system increased as the increase of H2O2concentration, Fe3O4-nZVI dosage and temperature, and decrease of pH in studied experimental ranges. The fitting parameters of kinetic showed that SMX degradation fitted the pseudo-first-order kinetic model. Under the given conditions, which were H2O210mmol/L, Fe3O4-nZVI 0.8g/L, pH=3, SMX 10mg/L, and reaction temperature 25℃, the degradation rate of SMX was 99.61% at 180min. The magnetization of Fe3O4-nZVI was 105.52emu/g, indicating it was easy for magnetic recycle. Reused experiments showed that Fe3O4-nZVI had excellent reactivity and stability. Free radical quenching experiments showed that the oxidation of ·OH played a key role on degrading SMX in water. Fe3O4-nZVI;advanced oxidation;Fenton-like;sulfamethoxazole X703.1 A 1000-6923(2022)07-3103-09 谢欣卓(1997-),女,山西运城人,兰州交通大学硕士研究生,主要从事水污染控制研究.发表论文2篇. 2021-12-09 国家自然科学基金资助项目(22166022);甘肃省科技计划项目(20JR2RA002);兰州交通大学大学生科技创新项目(DXS2022-035) * 责任作者, 教授, zhongjk@mail.lzjtu.cn2.6 SMX初始浓度对SMX降解的影响
2.7 反应温度对SMX降解的影响
2.8 Fe3O4-nZVI重复利用性能
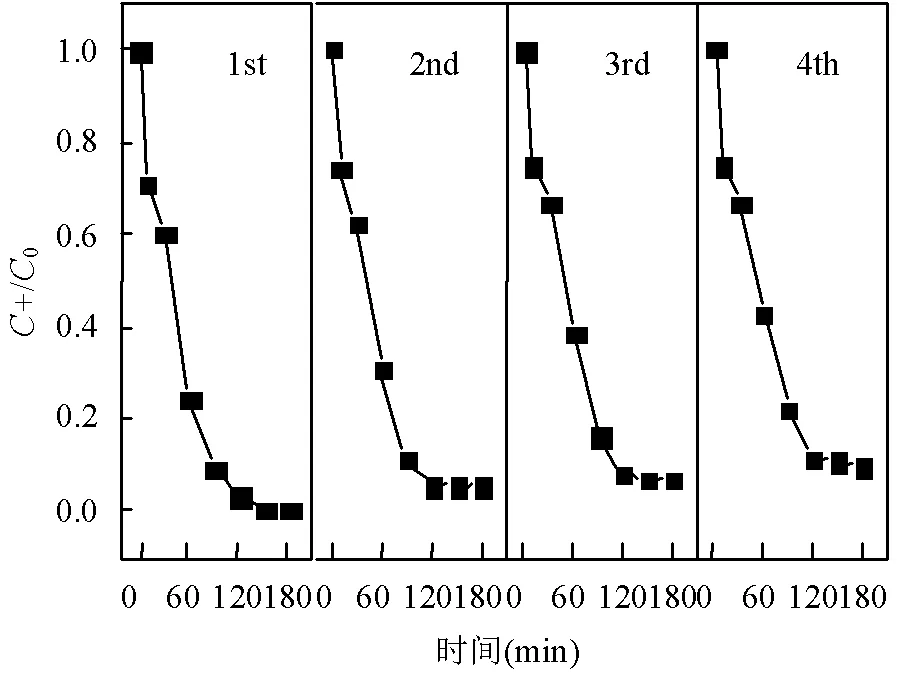
2.9 SMX降解动力学
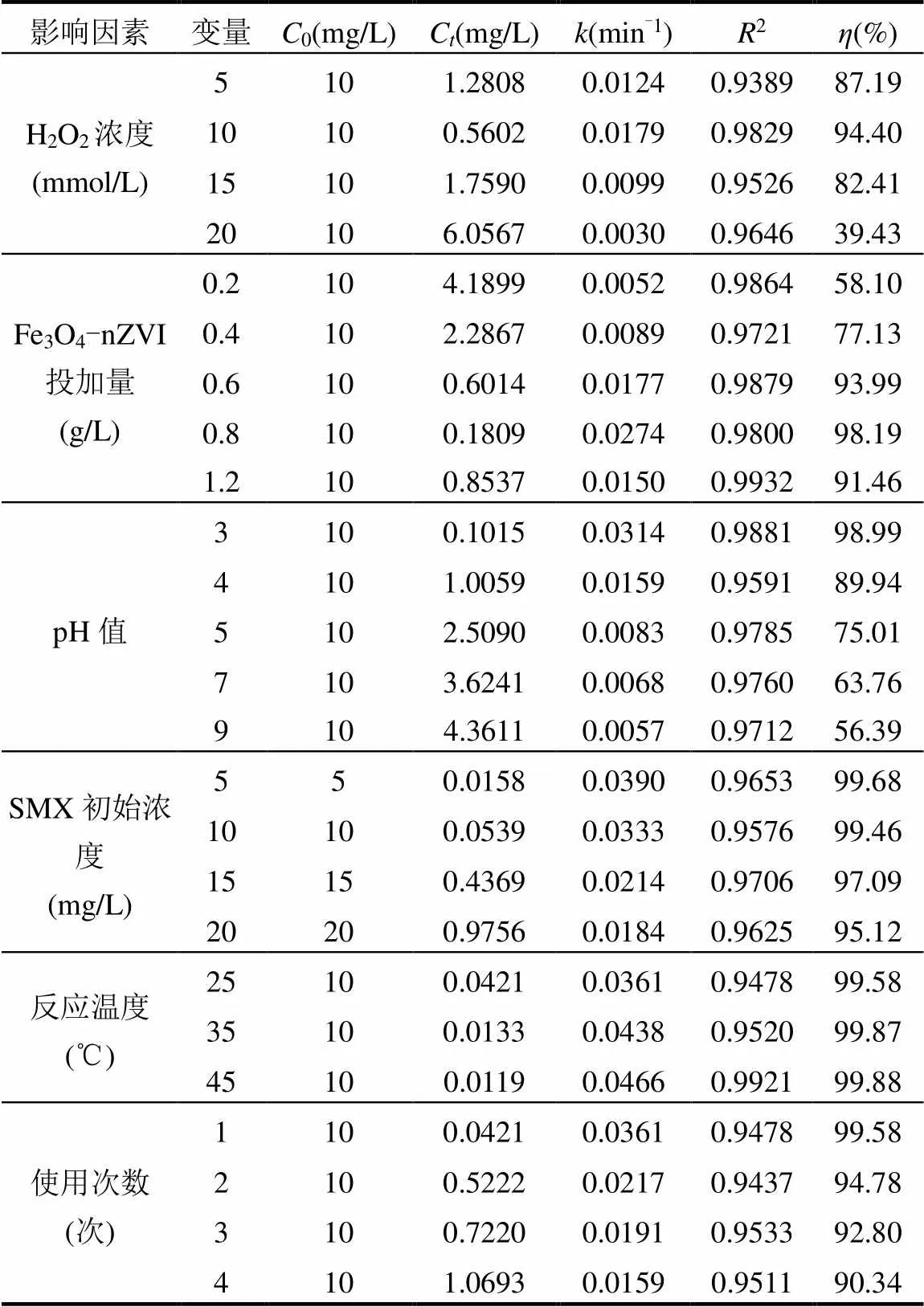
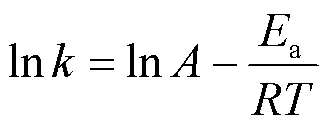
2.10 自由基淬灭实验
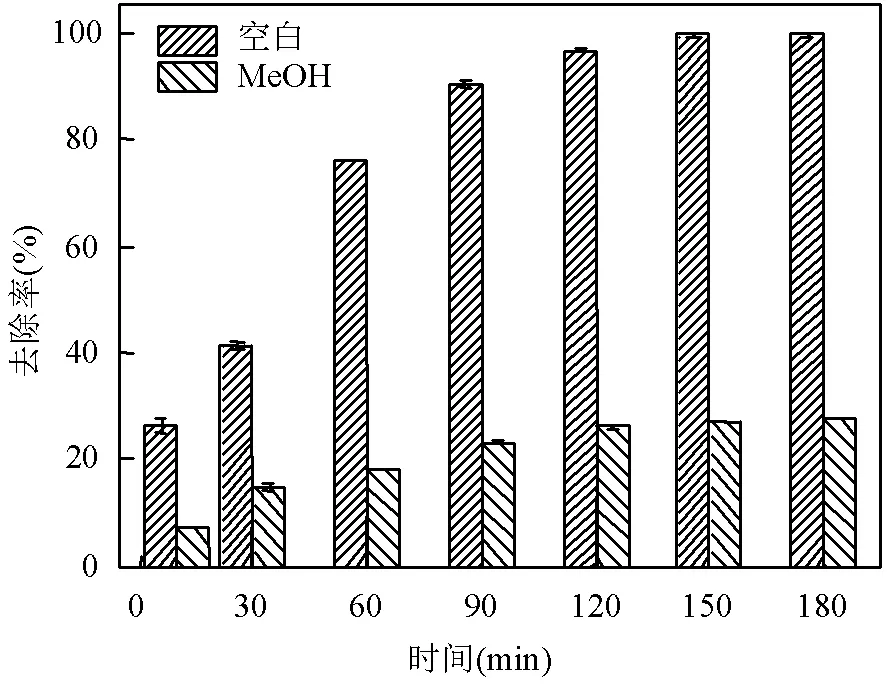
3 结论
