不同剂量利伐沙班对高龄非瓣膜性心房颤动患者卒中预防效果及安全性评价*
2022-07-19彭琛沈相福卫静茹李波
彭琛,沈相福,卫静茹,李波
(萍乡矿业集团有限责任公司总医院心血管内科,江西萍乡 337000)
非瓣膜性心房颤动是常见的心律失常疾病之一,多发于老年人群,60 岁以上高龄人群中发病率甚至可达到45%以上,发病率随年龄增加而升高[1-2]。非瓣膜性心房颤动最主要的并发症为各种血栓栓塞,非瓣膜性心房颤动患者栓塞风险是非心房颤动患者的2~7 倍,血栓脱落增大了缺血性脑卒中的风险,极易导致死亡[3-4]。预防非瓣膜性心房颤动患者发生血栓栓塞是临床治疗该病的重要基础,而抗凝治疗是预防非瓣膜性心房颤动发生血栓的关键。利伐沙班是我国首个获准用于预防非瓣膜性心房颤动患者脑卒中的新一代口服抗凝药,可通过内源性及外源性途径选择性阻断Xa因子活性位点,发挥抗凝效果,可有效预防血栓栓塞形成[5-6]。
抗凝治疗为改善非瓣膜性心房颤动患者预后的关键治疗措施,抗凝药物的应用成为临床医师关注的焦点。与传统华法林比较,利伐沙班的药效及药代动力学可预测,受食物影响较小,主要不良反应为肝肾功能损害及出血。目前我国利伐沙班使用剂量是根据国外指南[7]推荐的20 mg/d,由于亚洲人群与欧洲、美洲人群的种族差异可能出现不同药代动力学效果、肝肾功能损害及出血风险,目前尚缺乏利伐沙班在亚洲人群中的临床研究数据。日本一项研究[8]表明,非瓣膜性心房颤动患者利伐沙班的最佳使用剂量为15 mg/d,不仅具有满意的抗栓效果,还可有效降低颅内出血、胃肠道出血等风险。我国台湾地区利伐沙班的常用剂量为15 mg/d 和10 mg/d[9]。高龄非瓣膜性心房颤动患者多伴有基础疾病,各组织器官功能降低,房颤卒中风险高,同时脑出血风险增加,因此临床医师对高龄非瓣膜性心房颤动患者利伐沙班抗凝治疗存在剂量的顾虑。目前国内尚缺乏针对高龄非瓣膜性心房颤动患者利伐沙班最佳使用剂量的研究。鉴于此,本研究探讨不同剂量(20 mg/d、15 mg/d、10 mg/d)利伐沙班应用于高龄非瓣膜性心房颤动患者,分析其脑卒中的预防效果及安全性,为临床利伐沙班的应用提供参考。
1 资料与方法
1.1 一般资料
本研究按照前瞻性、随机、对照、单盲、单中心临床研究方法设计。选取2018年3月—2021年1月萍乡矿业集团有限责任公司总医院收治的174 例高龄非瓣膜性心房颤动患者为研究对象。纳入标准:①符合《心房颤动:目前的认识和治疗的建议(2018)》[10]的非瓣膜性心房颤动的诊断标准;②生命体征稳定;③年龄>80 岁;④符合利伐沙班应用指征。排除标准:①伴有恶性肿瘤、呼吸衰竭、风湿性心脏病、左束支传导阻滞、心肌梗死恢复早期及中重度主动脉瓣、二尖瓣狭窄或关闭不全等疾病;②有吸毒史、药物滥用史、颅内出血史、循环衰竭、中枢神经系统抑制;③有明显活动性出血倾向、凝血功能异常及有出血风险的肝脏疾病者;④肝肾等重要脏器功能严重障碍、免疫功能缺陷者;⑤需行双联抗血小板、非甾体抗炎药或溶栓药合用者;⑥合并急性冠脉综合征者;⑦对利伐沙班过敏者;⑧失访或无法配合治疗者;⑨发生不能耐受等不良事件致治疗中断者。采用随机数字表法将患者分为3 组,每组58 例;3 组采用不同剂量的利伐沙班治疗,分别为高剂量组(20 mg/d)、中剂量组(15 mg/d)、低剂量组(10 mg/d)。3 组患者的性别构成、年龄、体质量指数、肾小球滤过率、房颤血栓危险度评分、房颤出血风险评分、既往病史、心房颤动类型比较,差异均无统计学意义(P>0.05),见表1。本研究经医院医学伦理委员会审批通过,患者及家属自愿签署知情同意书。
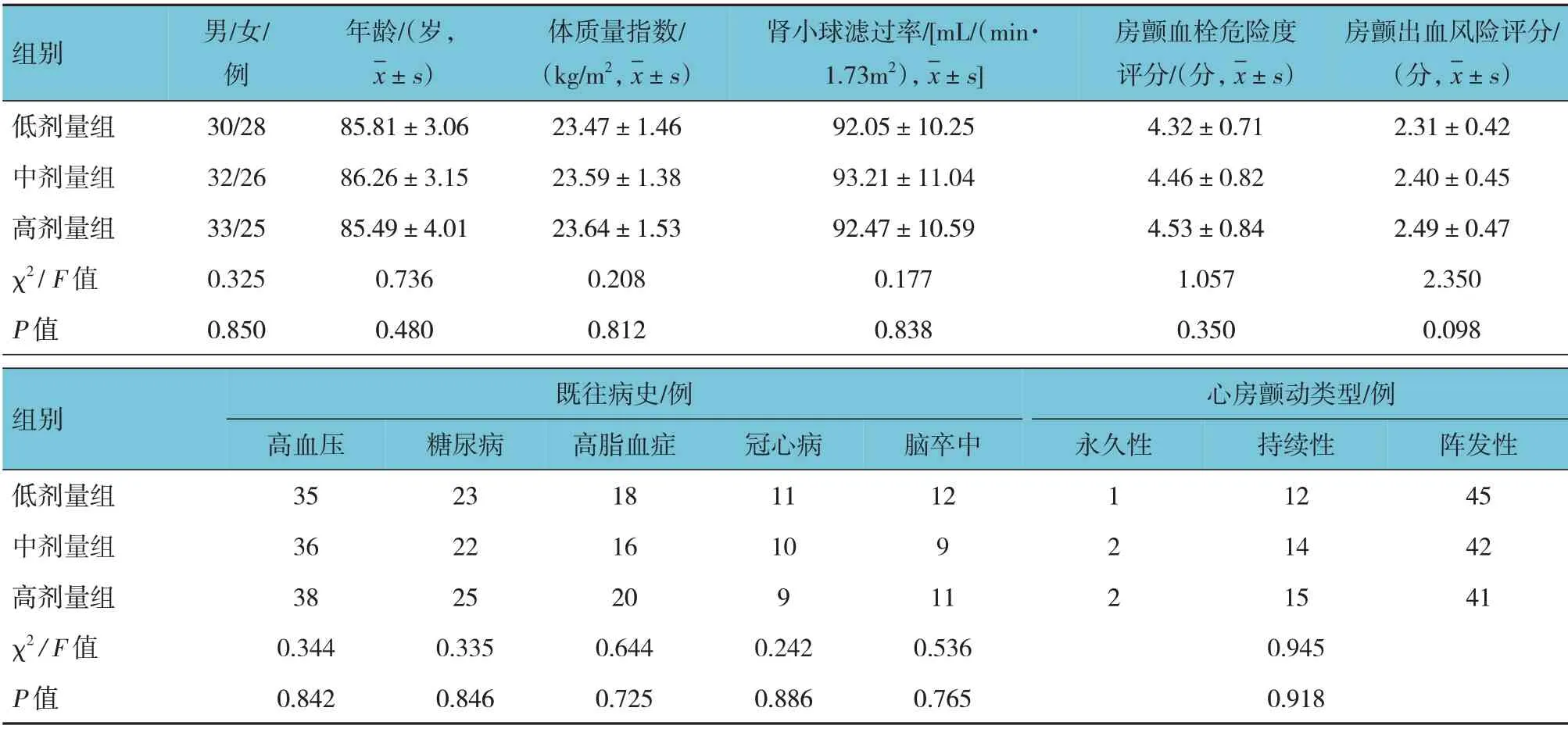
表1 3组患者临床资料比较 (n=58)
1.2 方法
所有患者均根据个体情况给予健康教育、降压、控糖、降脂等基础治疗措施。利伐沙班购自石家庄石药集团欧意药业有限公司,国药准字H20203077,规格:10 mg/片。高剂量组口服20 mg/d,1 次/d;中剂量组口服15 mg/d,1 次/d;低剂量组口服10 mg/d,1 次/d。3 组患者自开始治疗起接受随访,每个月以电话或门诊方式随访1 次,共随访12 个月,出现不良事件后给予对症治疗措施。
1.3 观察指标
1.3.1 栓塞发生情况统计随访期间脑卒中、心肌梗死、其他体循环栓塞、死亡事件发生情况。
1.3.2 出血发生情况统计随访期间轻微出血(如齿龈渗血、皮肤出血点、痰中带血等一般出血)、中度出血(肠道、泌尿系统等组织器官出血,但血流动力学未受损伤)和严重出血(颅内出血或血流动力学受损需干预的出血)的发生情况。
1.3.3 凝血功能变化患者分别于治疗前、治疗3 个月、治疗后(治疗结束后第1 天)分别抽取静脉血2.7 mL,枸橼酸钠抗凝,3 500 r/min 离心10 min,离心半径8 cm,收集血浆,采用ACL7000 型全自动血凝分析仪(美国贝克曼公司)检测凝血酶原时间(PT)、活化部分凝血活酶时间(APTT)、凝血酶时间(TT)、国际标准化比值(INR)。
1.3.4 肝肾功能变化患者分别于治疗前、治疗3 个月、治疗后(治疗结束后第1 天)使用URIT-8401 型全自动生化分析仪(济南泽凯医疗器械有限公司)检测血清丙氨酸氨基转移酶(ALT)、天门冬氨酸氨基转移酶(AST)及肌酐、尿素氮、尿酸。
1.3.5 药物不良反应记录治疗期间患者恶心呕吐、消化不良、眩晕、失眠、皮疹等不良反应发生情况。
1.4 统计学方法
数据分析采用SPSS 18.0 统计软件。计量资料以均数±标准差(±s)表示,组间比较用t检验或重复测量设计的方差分析;计数资料以构成比或率(%)表示,比较做χ2检验。P<0.05 为差异有统计学意义。
2 结果
2.1 3组栓塞情况比较
3 组患者均有脑卒中、心肌梗死及其他体循环栓塞发生,无死亡。3 组总栓塞发生率比较,经χ2检验,差异无统计学意义(χ2=3.467,P=0.177)。见表2。

表2 3组栓塞情况比较 [n=58,例(%)]
2.2 3组出血情况比较
3 组患者均有不同程度出血发生,3 组总出血发生率比较,经χ2检验,差异无统计学意义(χ2=3.064,P=0.216)。见表3。
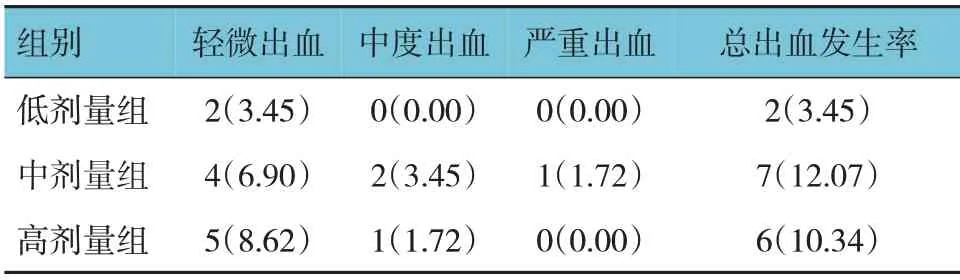
表3 3组出血情况比较 [n=58,例(%)]
2.3 3组治疗前后凝血功能比较
低剂量组、中剂量组、高剂量组治疗前、治疗3 个月、治疗后的PT、APTT、TT、INR 比较,采用重复测量设计的方差分析,结果:①不同时间点的PT、APTT、TT、INR 有差异(F=14.987、13.362、11.265 及13.045,均P=0.000);②3 组的PT、APTT、TT、INR 无差异(F=2.645、0.308、0.183 及0.569,P=0.074、0.735、0.833 及0.567);③3 组的PT、APTT、TT、INR 变化趋势有差异(F=12.225、10.065、10.989 及10.047,均P=0.000)。见表4。
表4 3组治疗前后凝血功能比较 (n=58,±s)

表4 3组治疗前后凝血功能比较 (n=58,±s)
注:①与本组治疗前比较,P<0.05;②与本组治疗3个月比较,P<0.05。
组别PT/s APTT/s低剂量组中剂量组高剂量组治疗前12.99±2.01 13.59±2.03 13.82±1.98治疗3个月14.21±1.89①14.81±1.95①14.85±2.01①治疗后16.98±1.97①②17.12±2.01①②17.31±2.03①②治疗前30.98±4.21 31.34±3.98 31.57±4.05治疗3个月33.86±4.05 34.01±4.22 34.25±4.16治疗后36.12±4.27 36.83±4.03 37.05±3.89组别TT/s INR低剂量组中剂量组高剂量组治疗3个月1.41±0.22 1.45±0.24①1.47±0.26①治疗前10.29±1.25 10.31±1.21 10.42±1.28治疗3个月12.21±1.49①12.42±1.55①12.75±1.61①治疗后14.98±1.92①②15.03±2.13①②15.21±2.13①②治疗前1.29±0.20 1.33±0.22 1.32±0.21治疗后1.75±0.24 1.78±0.23①②1.81±0.25①②
2.4 3组治疗前后肝肾功能比较
低剂量组、中剂量组、高剂量组治疗前、治疗3 个月、治疗后的ALT、AST、肌酐、尿素氮、尿酸比较,采用重复测量设计的方差分析,结果:①不同时间点的ALT、AST、肌酐、尿素氮、尿酸无差异(F=0.719、1.727、1.884、2.581 及2.144,P=0.489、0.181、0.155、0.079 及0.120);②3 组ALT、AST、肌酐、尿素氮、尿酸无差异(F=0.789、0.196、2.042、1.240 及1.473,P=0.456、0.822、0.133、0.292 及0.232);③3 组ALT、AST、肌酐、尿素氮、尿酸变化趋势无差异(F=0.688、0.760、2.005、2.224 及2.278,P=0.504、0.469、0.138、0.111 及0.106)。见表5。
表5 3组治疗前后肝肾功能比较 (n=58,±s)
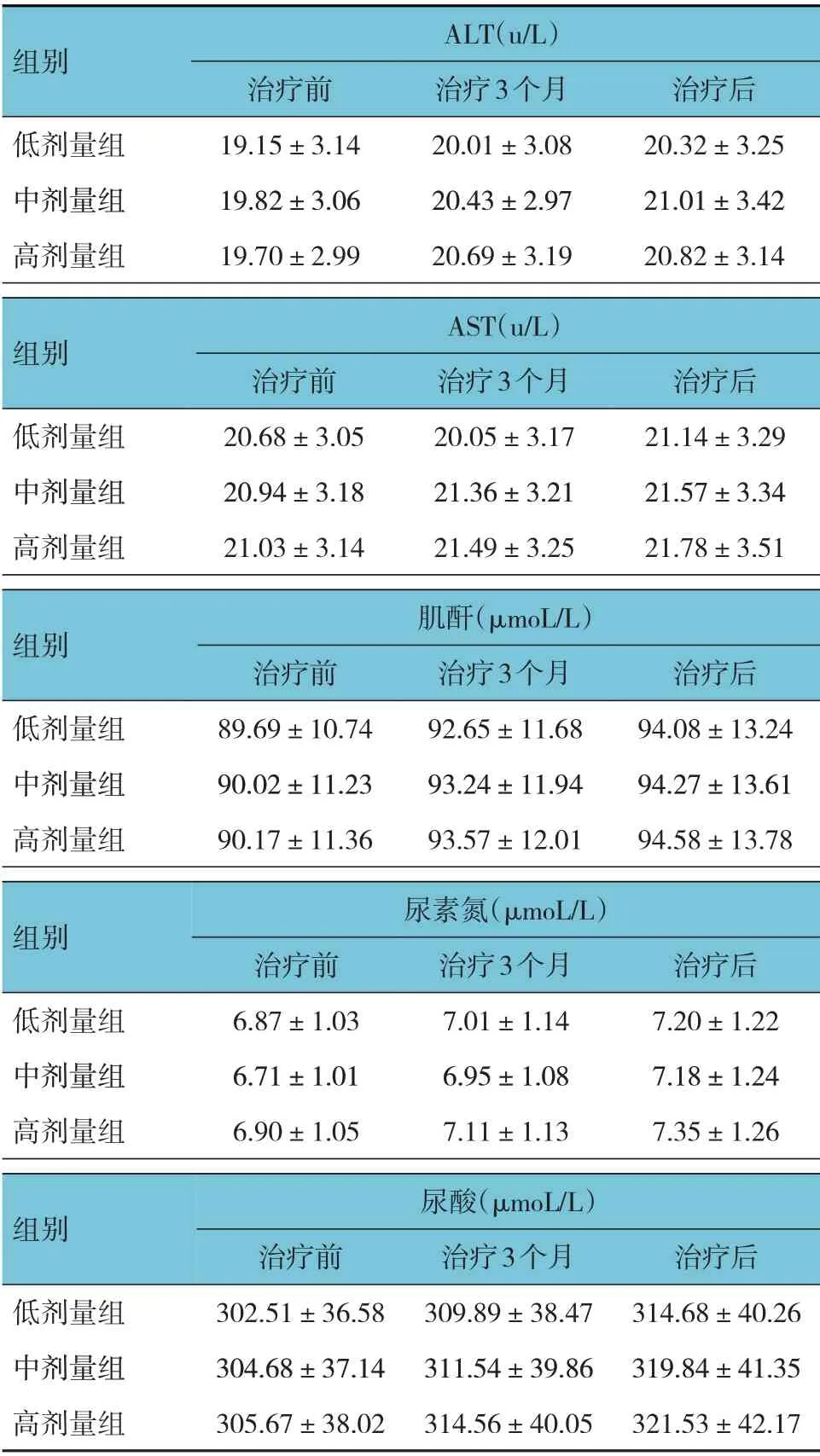
表5 3组治疗前后肝肾功能比较 (n=58,±s)
组别ALT(u/L)低剂量组中剂量组高剂量组治疗前19.15±3.14 19.82±3.06 19.70±2.99治疗3个月20.01±3.08 20.43±2.97 20.69±3.19治疗后20.32±3.25 21.01±3.42 20.82±3.14组别AST(u/L)治疗前20.68±3.05 20.94±3.18 21.03±3.14低剂量组中剂量组高剂量组治疗3个月20.05±3.17 21.36±3.21 21.49±3.25治疗后21.14±3.29 21.57±3.34 21.78±3.51组别肌酐(μmoL/L)低剂量组中剂量组高剂量组治疗前89.69±10.74 90.02±11.23 90.17±11.36治疗3个月92.65±11.68 93.24±11.94 93.57±12.01治疗后94.08±13.24 94.27±13.61 94.58±13.78组别尿素氮(μmoL/L)低剂量组中剂量组高剂量组治疗前6.87±1.03 6.71±1.01 6.90±1.05治疗3个月7.01±1.14 6.95±1.08 7.11±1.13治疗后7.20±1.22 7.18±1.24 7.35±1.26组别尿酸(μmoL/L)低剂量组中剂量组高剂量组治疗前302.51±36.58 304.68±37.14 305.67±38.02治疗3个月309.89±38.47 311.54±39.86 314.56±40.05治疗后314.68±40.26 319.84±41.35 321.53±42.17
2.5 3组治疗期间不良反应发生情况比较
低剂量组发生恶心呕吐1 例、眩晕1 例,中剂量组发生恶心呕吐1 例、眩晕1 例、皮疹1 例,高剂量组发生恶心呕吐2 例、皮疹2 例。3 组患者总不良反应发生率比较,经χ2检验,差异无统计学意义(χ2=0.703,P=0.704)。见表6。
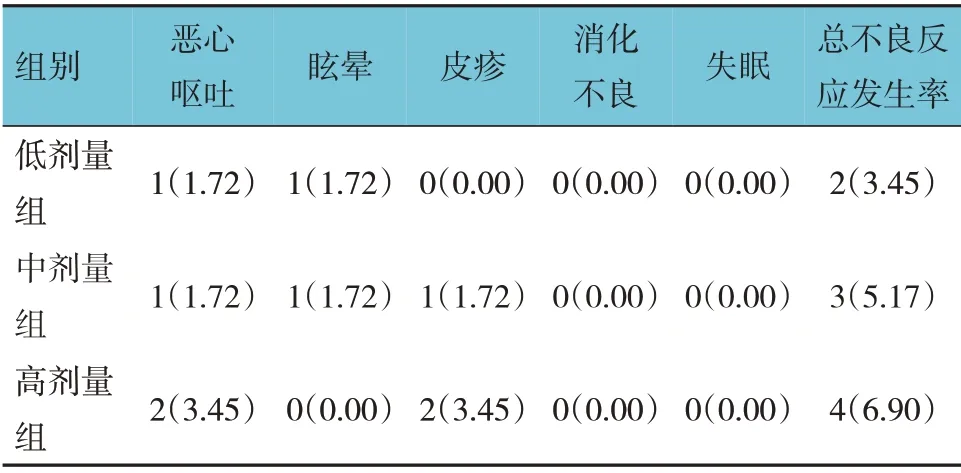
表6 3组不良反应发生情况比较 [n=58,例(%)]
3 讨论
利伐沙班属于新型抗凝药,可以选择性抑制凝血酶产生。目前国内外研究[11-12]已证实利伐沙班预防血栓形成的效果良好,但临床上仍存在过度抗凝或抗凝不足的情况。本研究结果显示,3 组患者总栓塞发生率和总出血发生率的差异无统计学意义,提示20 mg/d、15 mg/d 和10 mg/d 3 种剂量的利伐沙班对于高龄非瓣膜性心房颤动患者血栓栓塞及出血的发生风险相当,低、中剂量利伐沙班用于高龄非瓣膜性心房颤动患者的治疗方案在临床实践中可行。笔者认为可能与以下原因有关:①高龄非瓣膜性心房颤动患者年龄偏大,代谢功能减退,因基础疾病服药物种类多,出血风险较高,对于此类患者可以降低利伐沙班剂量。②利伐沙班在年轻患者中的半衰期为5~9 h,在老年患者中的半衰期为11~13 h[13];有研究发现老年受试者的利伐沙班浓度-时间曲线下面积比青年受试者高41%左右[14];高龄非瓣膜性心房颤动患者随年龄增加,肾功能出现生理性减弱,利伐沙班肾清除率也随之降低,高龄非瓣膜性心房颤动患者体内利伐沙班的血药浓度仍维持在相对较高水平。因此15 mg/d 和10 mg/d 剂量利伐沙班用于高龄非瓣膜性心房颤动患者血栓栓塞及出血的发生率与20 mg/d 剂量利伐沙班患者无差异。一项关于亚洲人群的研究[15]指出,相同剂量利伐沙班在黄种人群中的暴露浓度比白种人群高。LIN 等[16]研究指出,10 mg/d 利伐沙班用于非瓣膜性房颤患者可获取满意的脑卒中预防效果。李茜等[17]研究也指出年龄较大患者服用较15 mg/d 和10 mg/d 利伐沙班可行。笔者认为对于高龄非瓣膜性心房颤动患者脑卒中防治前需综合考量缺血/出血风险,抗凝治疗优先推荐低剂量利伐沙班。
本研究结果显示,3 组患者治疗3 个月、治疗后的PT、APTT、TT、INR 均高于治疗前,治疗后的PT、APTT、TT、INR 均高于治疗3 个月,治疗前、治疗3 个月、治疗后的PT、APTT、TT、INR 差异均无统计学意义,说明20 mg/d、15 mg/d 和10 mg/d 3 种剂量利伐沙班用于高龄非瓣膜性心房颤动患者均可改善其凝血功能,均具有良好的抗凝效果,推测可能与高龄非瓣膜性心房颤动患者体内利伐沙班血药浓度保持相对较高水平有关。肝肾功能损害及出血是利伐沙班的主要不良反应,本研究结果显示3 组患者治疗前、治疗3 个月、治疗后的ALT、AST、肌酐、尿素氮、尿酸差异均无统计学意义,提示20 mg/d、15 mg/d 和10 mg/d 3 种剂量利伐沙班用于高龄非瓣膜性心房颤动患者对其肝肾功能影响较小,安全可靠,这也可能与本研究未纳入肝肾等重要脏器功能严重障碍患者有关,所有患者的肝肾代谢功能良好。王海明等[18]研究指出15 mg/d 和10 mg/d 利伐沙班用于非瓣膜性房颤患者,治疗前后两组患者肝肾功能无显著性变化。本研究结果显示3 组总不良反应发生率比较差异无统计学意义,再次印证利伐沙班用于高龄非瓣膜性心房颤动患者的安全性良好。
综上所述,利伐沙班20 mg/d、15 mg/d、10 mg/d在高龄非瓣膜性心房颤动患者的治疗中,血栓栓塞及出血发生相当,均具有良好的抗凝疗效,对肝肾功能影响小,安全性良好,推荐低剂量利伐沙班用于高龄非瓣膜性心房颤动患者。本研究为单中心研究,纳入样本量有限,随访时间相对较短,后期将进一步开展多中心研究,并延长随访时间进一步研究。
