LncRNA调控病原微生物致病作用的研究进展
2022-07-07周媛媛贾永超王临喜尹荣兰郭忠博尹荣焕
严 平 , 周媛媛 , 贾永超 , 郭 营 , 王临喜 , 尹荣兰 , 郭忠博 , 王 欣 , 尹荣焕
(1.沈阳农业大学动物科学与医学学院 重要家畜疫病研究教育部重点实验室 , 辽宁 沈阳 110866 ;2.吉林省畜牧兽医科学研究院 , 吉林 长春 130062 ; 3.辽宁农业职业技术学院 , 辽宁 营口115009)
长链非编码RNA(Long non-coding RNA,lncRNA)是一类长度超过200个核苷酸的RNA。由于它不具有开放阅读框因而缺乏蛋白编码能力,或者仅能编码短的多肽[1]。LncRNA广泛存在于动植物、酵母、原核生物与病毒等多种生物中,并在生物学过程中发挥关键的作用。目前,基因表达调控是病原微生物与宿主关系中的热门研究问题。研究发现,lncRNA在病原微生物感染过程中起着重要的调控作用,与疾病的发生、发展息息相关。
1 LncRNA的分类及功能
在哺乳动物基因组中仅少量转录成编码RNA,大部分转录为非编码RNA。而非编码RNA中大多数是lncRNA,其余包括microRNA、circRNA和snoRNA等。LncRNA主要位于细胞核中,其次存在于细胞质中,由RNA聚合酶转录形成,经过剪接、加帽和多聚腺苷酸化等加工过程可成为含有5′帽子和3′poly(A)尾结构的成熟RNA分子。其与编码RNA的区别在于具有更少的外显子、较低保守性和更高的组织特异性[2]。
1.1 LncRNA分类 依据lncRNA相对于相邻编码基因的位置关系,其可分为5种类型[3]:正义lncRNA、反义lncRNA、双向lncRNA、内含子lncRNA和基因间lncRNA,其中基因间lncRNA研究较为透彻。LncRNA的数量庞大,作用方式多,其繁琐的调控机制是紧密联系而非彼此孤立的,充当着信号分子、诱饵分子、引导分子、骨架分子等角色,作用于多种基因形成互作网络在宿主的生理过程中扮演着重要的角色。
1.2 LncRNA功能 LncRNA参与了协调宿主状态,代谢与发育,影响细胞的迁移、分化、周期与凋亡等各种不同的生物过程[4-5]。位于细胞核内的lncRNA参与调控染色质重塑、组蛋白修饰、基因转录、编码基因的剪接和修饰等过程;而位于细胞质中的lncRNA则调控编码基因的稳定性、翻译和细胞信号传导通路[6]。LncRNA可以与DNA、RNA和蛋白质相互作用,且在表观遗传水平、转录水平和转录后水平等多个水平调控基因的表达,发挥生物学功能。
1.2.1 LncRNA在表观遗传水平的基因调控 表观遗传现象包括DNA甲基化、组蛋白修饰、基因组印迹、基因沉默等,均与lncRNA的调控密切相关。LncRNA作为向导将染色质修饰复合物招募到特定的基因组位点并赋予其催化活性来影响表观遗传效应。LncRNA NeST通过与WD重复序列蛋白5(WD-repeat protein,WDR5)形成复合物来促进组蛋白第三亚基四号赖氨酸三甲基化(Histone H3 lysine 4 methyl-transferase,H3K4 me3)的形成,激活CD8+T细胞中IFN-γ转录水平的增加[7]。LncRNA也参与印迹结构域内基因的调控,Zhang等(2014年)发现lncRNA Kcnq1ot1在Kcnq1等位基因的启动子上积累而介导等位基因的抑制,从而在Kcnq1基因印迹中发挥重要的作用[8]。
1.2.2 LncRNA在转录水平的基因调控 在真核生物中,lncRNA与转录因子结合形成复合物,调节转录因子的活性从而调控转录过程。例如,lncRNA DHFR与二氢叶酸还原酶(Dihydrofolate reductase,DHFR)基因的上游启动子互补配对形成稳定的螺旋结构复合物阻碍转录因子(Transcription factor IID,TFIID),与DHFR基因的启动子区域相结合,导致DHFR基因的转录受抑制[9]。LncRNA不仅可以招募转录因子到启动子,还可以招募增强子来启动基因的转录。Wang等(2014年)研究发现,在树突状细胞中lncRNA DC受到病原体刺激时可以调节多种转录因子的活性,激活的信号转导子与转录激活子3(Signal transducer and activator of transcription 3,STAT3)与lncRNA DC形成复合物,阻碍STAT3与蛋白酪氨酸磷酸酶1(SH2-containing protein tyrosine phosphatase,SHP1)结合使其去磷酸化,促进酪氨酸705上的STAT3磷酸化[10]。此外,lncRNA作为诱饵分子或分子支架与转录因子结合形成复合物,影响基因的转录过程。LncRNA NRON与鸟苷三磷酸酶激活蛋白及T细胞胞浆中活化细胞的核因子(Nuclear factor of activated T cells,NFAT)激酶的复合物作为激活核因子NFAT的分子支架,使NFAT从复合物中释放出来并促进核转运,进而启动基因转录[11]。
1.2.3 LncRNA在转录后水平的基因调控 LncRNA在转录后水平的调控包含mRNA的剪接和编辑、蛋白翻译及转运等。其与蛋白编码基因形成RNA双链,成为mRNA的重叠基因中的顺式调控元件,导致基因的可变剪切。细胞核中lncRNA MALAT1与细胞核斑点结构域中的丝氨酸、精氨酸剪接因子相互作用,影响其分布并调节mRNA的可变剪接,可能通过调节细胞核区域中精氨酸蛋白的浓度,实现最佳的选择性剪接[12]。LncRNA还参与调控mRNA的降解,是影响mRNA稳定性的重要因素。Faghihi等(2008年)研究表明,贝塔分泌脢(Beta-secretase-1,BACE1)是在阿尔茨海默病中起关键作用的一种酶,发现体外引入BACE1的反义转录本(BACE1-antisense transcript,BACE1-AS)可保护BACE1的mRNA不被核糖核酸酶降解,并且沉默BACE1-AS后可促进培养细胞BACE1的mRNA的降解,证明BACE1-AS与保护BACE1的mRNA不被降解密切相关[13]。由于lncRNA与microRNA的结构相似,所以它可与microRNA竞争性结合靶向mRNA或作为microRNA的海绵。有研究发现,H19可作为microRNA的海绵,间接调控microRNA下游靶基因的表达,从而介导多种类型疾病的发生和发展[14]。
2 LncRNA在细菌感染致病过程中的调控作用
LncRNA是宿主免疫系统发育及病原菌感染宿主的免疫应答过程中新的调控分子,具有重要的功能。LncRNA XLOC-09813充当竞争性内源RNA来稳定原癌基因(FOS)的mRNA表达,作为调节Toll样受体信号通路和相关的免疫功能中的关键调控分子[15]。LncRNA M2存在于M2巨噬细胞的胞核和胞浆内,在转录因子STAT3作用下可以促进lncRNA M2转录,并通过PKA/CREB途径调控M2巨噬细胞的分化[16]。总之,lncRNA可通过调控染色质甲基化状态、NF-κB等信号通路和microRNA相互作用等模式介导病原菌感染过程。近年来,lncRNA在病原菌感染过程中发挥调控作用的研究情况见表1。

表1 LncRNA在病原菌感染过程中的调控机制研究
3 LncRNA在病毒感染致病过程中的调控作用
病毒可以通过诱导细胞的lncRNA的特异性表达,逃避抗病毒免疫系统监视,降低抗病毒免疫力,提高病毒复制效率。同样,细胞也可以特异性表达多种lncRNA来抵抗病毒感染。随着高通量测序的发展,鉴定出多种lncRNA在病毒感染过程中的表达变化。在宿主的抗病毒反应中lncRNA发挥着不可或缺的作用,lncRNA是病毒感染期间宿主免疫反应的关键调控因子。近年来,lncRNA在病毒感染过程中发挥调控作用的研究情况见表2。
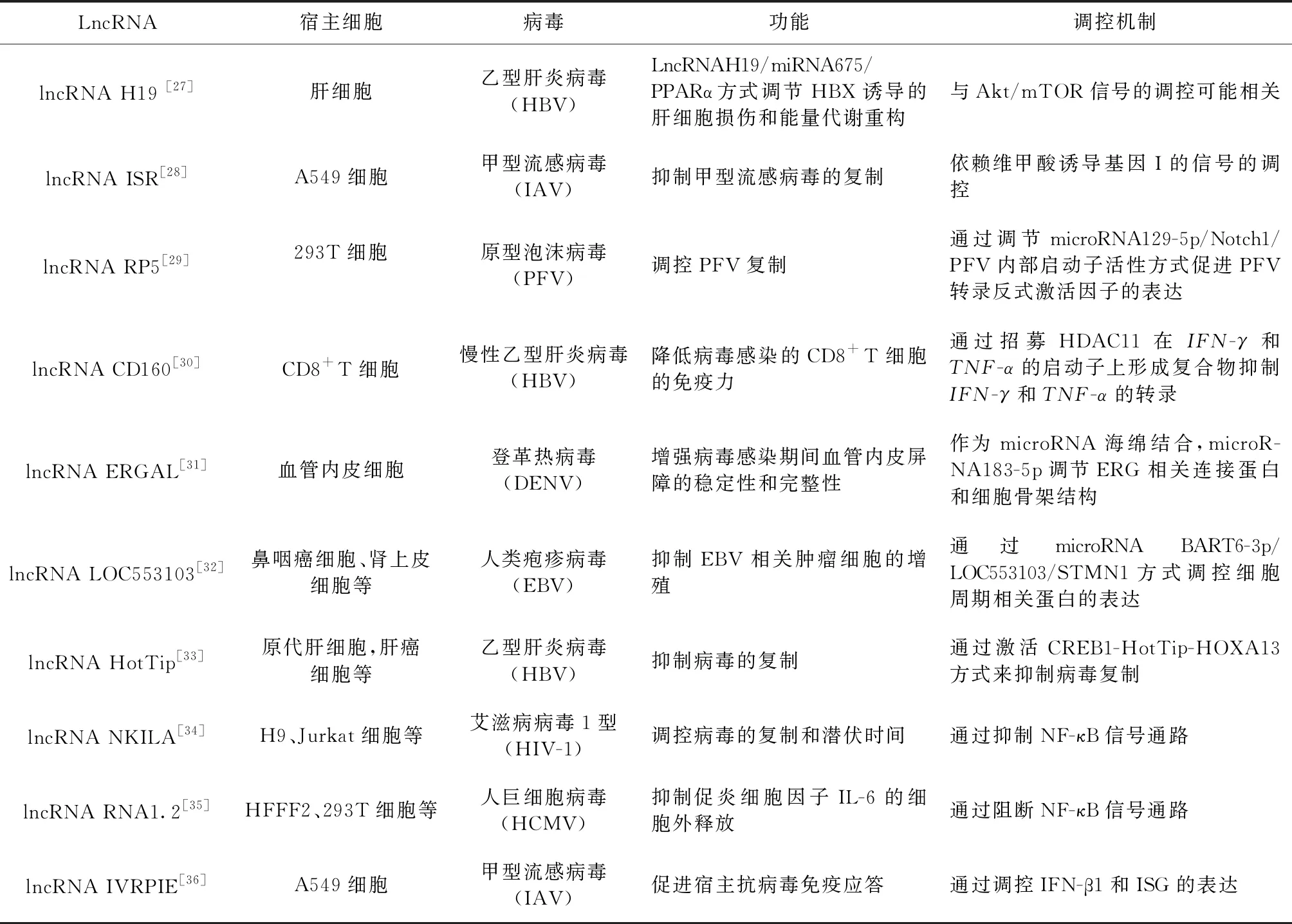
表2 LncRNA在病毒感染致病过程中的调控机制
根据lncRNA的来源可将病毒感染中发挥作用的lncRNA分为三类:病毒感染的细胞内lncRNA、病毒编码的lncRNA和由病毒与细胞共同形成的嵌合lncRNA。
3.1 病毒感染细胞内lncRNA 病毒已被发现利用细胞内的lncRNA来调节宿主和病毒基因的表达和功能。然而,宿主在病毒感染过程中也可通过胞内的lncRNA表达来启动抗病毒反应。在IAV感染过程中,lncRNA ISR依赖于维甲酸诱导基因I(Retinoic acid-inducible gene I,RIG I)的信号调控,IFN-β能诱导lncRNA ISR的表达,具有抑制病毒复制的能力[28]。在宿主的抗病毒反应中,lncRNA能够调节宿主的先天免疫系统参与病毒感染,不仅参与调节T细胞的生长和分化,还调控干扰素刺激基因(Interferon-stimulated genes,ISGs)的表达。IAV感染A549细胞后,lncRNA IVRPIE表达上调显著抑制了A549细胞中IAV的复制。此外,lncRNA IVRPIE通过影响组蛋白修饰,正向调节IFN-β1和几个关键的ISGs的转录是宿主抗病毒反应的关键调节因子[36]。
研究表明,大多数lncRNA通过几种机制来调节炎症或抗病毒基因的表达。有些是诱导剂,lncRNA NEAT1通过抑制IL8的抑制因子即富含脯氨酸/谷氨酰胺的剪接因子(Splicing factor proline/glutamine-rich,SFPQ)而增加IL8的表达量[37]。有些是负调节因子,呼吸道合胞体病毒(Respiratory syncytial virus,RSV)感染时宿主抗病毒应答负性调节因子lncRNA NRAV的表达减少,lncRNA NRAV与囊泡蛋白竞争胞浆中的microRNA509-3p,促进RSV囊泡运输从而加强RSV的增殖[38]。
3.2 病毒编码的lncRNA LncRNA可以调控转录因子和蛋白质的表达,对病毒复制和病毒潜伏期的激活至关重要。除细胞内lncRNA的表达受病毒感染的调控,还发现病毒编码的lncRNA同样如此。黄病毒基因组RNA的3′UTR含有许多茎环结构保护它们不被宿主核酸酶XRN1降解,并产生功能性的lncRNA。LncRNA sfRNA与microRNA结合并诱导microRNA的降解以保护病毒基因组RNA,从而允许病毒在宿主中复制[39]。
3.3 病毒与细胞嵌合lncRNA 嵌合lncRNA指的是通过将病毒基因组整合到宿主基因组中而产生的lncRNA。HBV诱发肝细胞癌主要是通过位于8号染色体短臂的HBV的DNA插入位点产生了重复序列,其被转录形成嵌合的lncRNA HBx-LINE1。LncRNA HBx-LINE1的表达促进了细胞由上皮表型向间质表型的转化,从而增加了细胞的恶性程度并且激活Wnt/β-catenin的信号通路,促进β-catenin转位到细胞核,从而促进细胞迁移[40]。
4 其他病原微生物
LncRNA在其他病原微生物如螺旋体、支原体等致病过程中也起着一定的调控作用。在梅毒螺旋体感染的患者中检测发现有2 258个差异表达的lncRNA,通过lncRNA-mRNA共表达网络分析显示,59个lncRNA存在显著差异,其中部分lncRNA参与了CD4+T细胞对梅毒螺旋体应答的关键生物学过程[41]。全基因组分析感染和未感染牛支原体的牛乳腺组织中,有1 310个差异表达的mRNA和57个差异表达的lncRNA。基因本体论分析表明,差异表达的mRNA和lncRNA在T细胞受体信号通路、TGF-β信号通路、PI3K-Akt信号通路、NF-κB信号通路、mTOR信号通路和细胞凋亡等重要生物学通路中发挥重要作用[42]。
5 展望
LncRNA不再是转录上的“噪音”,而是在基因表达调控中扮演着重要的角色,代表一个新的基因表达调控网络。比如,现今研究的热点ceRNA调控机制,lncRNA与mRNA竞争性结合microRNA,从而调控mRNA的表达量。在病原微生物致病过程中,lncRNA通过与DNA、RNA和蛋白质相互作用来调控自身与宿主基因的表达,涉及到转录、转录后和表观遗传水平等多方面。研究发现,许多lncRNA差异表达与疾病的发生、发展息息相关。与microRNA相比,lncRNA似乎更具有组织特异性和靶向性。这使lncRNA能够成为具有特异性的生物标志物[43],为理解疾病的机制扩展了新的视角、提供了新的治疗策略,成为多种疾病的诊断标志。
尽管lncRNA的调控机制错综复杂,其如何调控病原微生物感染和致病过程还要继续深入研究。而且随着lncRNA与病原微生物感染致病关系的深入探索,必将为病原微生物致病机制的研究开辟新的道路。
