分化型甲状腺癌131I治疗患者唾液及汗液131I污染的监测
2022-07-07巴建涛罗亚平
郭 宁,巴建涛,罗亚平,王 瞳,李 方
中国医学科学院 北京协和医学院 北京协和医院核医学科,北京 100730
131I治疗是分化型甲状腺癌术后重要的辅助治疗方法,可清除术后残余甲状腺,治疗转移灶,有效降低术后的复发和转移率,便于治疗后利用甲状腺球蛋白水平监测病情。131I治疗通过口服给药,从肠道吸收的碘除被甲状腺组织吸收外,主要分布在细胞外液、唾液腺、胃液和乳汁中[1]。大部分碘从肾脏排出,其中,尿碘占排出碘的85%,粪便碘占10%,从汗液中排出的碘不到5%[1]。随着高活度131I在分化型甲状腺癌患者治疗中的广泛应用,患者住院期间的起居活动有可能通过体液增加病房放射性污染,给工作人员及工作场所周围公众带来潜在的辐射风险。本研究通过监测分化型甲状腺癌患者131I治疗后唾液和汗液放射性活度,评估了131I在唾液和汗液中的排泌情况,以期为核医学治疗病房放射性污染水平的控制提供参考。
对象和方法
对象2015年10月至2016年3月在北京协和医院核医学科行131I治疗的分化型甲状腺癌患者15例,其中,男9例,女6例,平均年龄(45.0±12.1)岁(27~68岁)。所有患者均行甲状腺全切术,病理诊断为分化型甲状腺癌。本研究经北京协和医院伦理委员会批准,所有患者均签署知情同意书(S-K2108)。
131I治疗患者入住核医学治疗病房,治疗方式为口服给药,131I治疗活度为3.70~5.55 GBq。15例患者中,9例口服3.70 GBq胶囊,6例口服5.55 GBq胶囊。所有患者131I治疗后即刻含服维生素C 100 mg/片,每日3次,以促进131I从唾液腺排出,保护唾液腺。
唾液收集试验开始前将每根待用的医用棉棒装入密封塑料袋内,用天平称取质量并编号记录;分别于131I治疗后2、4、8、24、48 h通过手持医用棉棒刺激唾液腺排泌唾液的方法收集唾液。棉棒吸附唾液后,装入密封塑料袋等待称重和活度测量。
汗液收集采取擦拭取样法,分别于131I治疗后2、4、18、24、28、48 h采集汗液,共收集以下5个部位:额头、左颈、前胸、左腋窝、左手掌。具体为:将3 cm×4 cm中空硬纸框架放置于做好位置标记的计划采样部位,每次按照取样标记的位置擦拭收集汗液。持棉球在框架内顺时针、逆时针各擦1圈,然后将样本棉球放入标记的密封袋内封口,重复上述过程直到所有部位、时间点汗液样本收集完毕。
质量控制样本采集前培训患者正确的采集方法,包括采集部位、皮肤的擦拭力度,唾液收集的部位和停留时间等。为避免棉球被患者手上的汗液污染,每位患者每个时间点均戴一次性手套取样。唾液和汗液采集期间保持病房温度的恒定。
计算方法采用BH1324型一体化多道分析器,能峰值选择364 keV,所有测量均使用20%窗宽。仪器经北京市计量检测院检定合格,测定数据前先进行60 s的本底测试。取131I放射性活度333 kBq胶囊(标准品胶囊由原子高科股份有限公司提供)作为标准源,半衰期8.02 h。

结 果
唾液放射性活度监测情况15例患者排泌唾液的平均重量为0.14 g。131I治疗后,唾液放射性活度于2~4 h达到高峰,之后唾液内放射性活度随时间推移逐渐减少,治疗后2、4、8、24、48 h测得的放射性比活度分别为(553.58±478.94)×104、(484.72±431.76)×104、(389.78±254.63)×104、(141.15±104.83)×104、(53.23±49.8)×104(图1)。
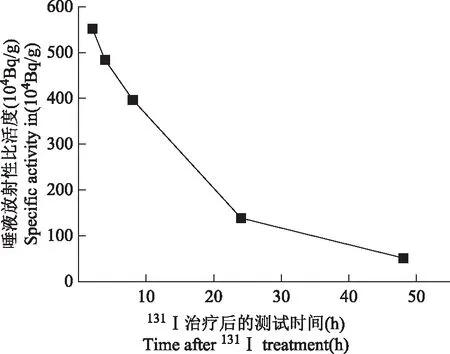
图1 15例患者131I治疗后唾液放射性平均比活度-时间曲线
汗液放射性活度监测情况131I治疗后,手掌汗液排泌的131I放射性活度高于额头、左颈、前胸和左腋窝,随着时间推移,患者体内131I经汗液排出量呈现逐渐减少的趋势。服用5.55 GBq131I胶囊患者汗液的放射性活度高于服用3.70 GBq131I胶囊患者(表1、2)。
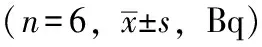
表1 5.55 GBq131I治疗后患者汗液的体表面污染(Bq/12 cm2)平均值
讨 论
本研究测量了15例分化型甲状腺癌术后接受131I治疗患者的唾液排泌放射性比活度及体表面污染水平,结果显示,最大的唾液比活度出现在治疗后2 h。因个体差异及可能采集方法不同,也有采集样本在4 h或6 h唾液的比活度最高,其中唾液的最大比活度平均值达到了5.53 MBq/g。131I给药后,由于唾液腺有钠/碘同向转运体表达,唾液腺可从循环中摄取131I,唾液腺的摄131I高峰多在给药后的2 h内,此后唾液腺中的131I逐步下降[2],在给药后24 h即降到较低水平。实际测得唾液中的放射性比活度也支持这一代谢特点。
对汗液的检测结果发现,汗液对手掌、额头、颈部、前胸、腋窝最高表面污染集中在24 h内,范围在645~7043 Bq/12 cm2间。在131I给药后48 h测得的汗液表面污染为较低水平,体表面污染的变化与治疗131I活度关系不大。汗液排泄是人体内碘的代谢途径之一,有报道显示,131I全身扫描时发现因汗液污染造成的异常显影[3],证实131I会经过汗液排泄。本研究通过测量131I治疗后患者汗液中的表面污染获得实际测量值也证实了这一代谢过程,与Ibis等[4]研究结果相似,提示汗液中的放射性可能造成病房环境潜在的污染。
邢海群等[5]检测了治疗病房内各采样点外照射辐射剂量率及表面污染水平,其治疗病房内外照射本底剂量率平均为0.24 μSv/h,结果发现,门把手、电器把手外照射剂量率接近病房本底剂量率水平,分别为0.92、0.39 μSv/h;汗液对病床用品造成的外照射污染水平较低,平均为6.86 μSv/h,表面污染280 Bq/cm2;受唾液里131I影响,面盆表面的外照射剂量率明显高于病床用品造成的外照射污染水平,外照射剂量率为33.13 μSv/h,表面污染1370 Bq/cm2。该结果与本研究中唾液排泌的放射性比活度及汗液表面污染水平的结果相吻合。

表2 3.70 GBq 131I治疗后患者汗液的体表面污染(Bq/12 cm2)平均值
综上,本研究结果证实,131I治疗后的前几天,131I治疗患者唾液和汗液除了产生外照射外,还会因其造成的放射性污染可能导致病房人员受到内照射。测量唾液和汗液中的放射性活度可作为预防病房环境放射性污染估算的参考,有利于细化131I治疗病房的防护措施。为了减少住院期间的放射性污染,在管理131I治疗患者的病房时,应采取以下措施:(1)加强给药后24 h内的患者饮食起居的宣教,提醒患者将使用后的一次性水杯、餐巾纸、卫生纸及剩余食品妥善收集于塑料袋内密封,待出院后作放射性废物处理;(2)在核医学住院区内的病房、专用卫生间、病房走廊、高活性实验室设置空气过滤区[6],病房内安装专用进、排风系统用于过滤污染空气和补充新鲜空气;(3)医务人员宜通过视频及对讲系统进行查房等医疗活动[7],以降低住院期间痰液、汗液中131I气溶胶放射性污染对环境的影响。
