Sn掺杂NaNi1/3Fe1/3Mn1/3-xSnxO2正极材料制备及其电化学性能
2022-07-07张浩然车海英郭凯强张云龙陈航达廖建平刘海梅马紫峰
张浩然,车海英,郭凯强,申 展,张云龙,陈航达,周 煌,廖建平,刘海梅,马紫峰,
(1上海电力大学环境与化学工程学院,上海200090;2浙江钠创新能源有限公司,浙江绍兴312000;3上海交通大学化学工程系,上海200240)
锂离子电池因具有高能量密度、高比容量、对环境友好等优点,已被广泛应用在便携式电子设备、新能源汽车中。近年来,以磷酸铁锂电池为代表的锂离子电池被广泛应用于储能领域,使锂资源的需求量急剧上升。然而,自然界中的锂储量仅占地壳中元素总含量的0.01%且分布不均,导致与锂资源相关材料价格大幅度上涨[1-2]。钠离子电池与锂离子电池工作原理相近,而钠资源丰富、成本低廉、工作环境适应性强,已经成为重要的电化学储能器件[3]。Che等[4-5]通过电解质体系优化与工程化,已经开发出循环寿命长、安全性良好的钠离子电池。基于NASICON电解质为安全性更佳的固态钠离子电池设计提供新的选择[6]。层状结构过渡金属氧化物因其理论比容量高、导电性好、制备过程简便,已成为钠离子电池正极材料工程化的首选。层状结构的O3 型NaNi1/3Fe1/3Mn1/3O2正极材料因具有低成本、高比容量等特点,自Kim 等[7]报道以来得到广泛关注。Wang 等[8-9]开发出NaNi1/3Fe1/3Mn1/3O2正极材料规模化的湿法合成工艺,以硬碳为负极制备了软包电池,研制出全球首套钠离子电池储能系统原型样机,证明了NaNi1/3Fe1/3Mn1/3O2是一种具有商业化开发价值的钠离子电池正极材料。然而,NaNi1/3Fe1/3Mn1/3O2的空气稳定性较差,长期暴露在空气中会与CO2反应生成碳酸钠,导致性能急剧下降,只有通过复烧才能恢复其性能[10]。为改善层状结构氧化物正极材料的循环稳定性、倍率性能,掺杂不同的元素改性或表面包覆被认为是改善层状氧化物正极材料空气稳定性和循环性能的有效手段[11-14]。Sun 等[15]率 先 提 出 在NaNi1/3Fe1/3Mn1/3O2材料的Na位,以少量Ca取代Na,有效扩展了Na层间距,掺Ca样品O3-P3-P3-O3相变可逆性得到提升。Yu 等[16]通过在Na(Ni0.6Co0.2Mn0.2)1-xTixO2材料中掺杂部分Ti,有效地稳定了材料结构,使材料的循环性能得到增强。Mao等[17]通过在NaNi0.2Fe0.35Mn0.45O2材料中掺杂较Mn离子半径更大的Zn,有效地降低了Na+脱嵌过程中晶格单元的变化,并促进了O3-P3可 逆 相 变 的 能 力。 此 外, Zhang 等[18]在 对NaNi0.2Fe0.3Mn0.5O2材料研究中也发现,通过掺杂离子半径较大的Mg2+,可使材料的层间距得到提高,增强Na+在固相中的扩散能力。我们通过对镍、铁、锰元素离子半径对照分析[Ni2+(0.69 Å)、Fe3+(0.645 Å)、Mn4+(0.53 Å)],选择离子半径更大的Sn4+(0.71 Å)部分取代Mn,合成出不同Sn 掺杂比例的NaNi1/3Fe1/3Mn1/3-xSnxO2正极材料,对其结构变化规律与电化学性能进行研究,并分析了掺杂改性机理。
1 实验
1.1 材料制备
采用固相法制备Sn 掺杂NaNi1/3Fe1/3Mn1/3O2三元正极材料,方法如下:选用碳酸钠、氧化镍、氧化铁、氧化锰和二氧化锡作为前驱体原料(其中碳酸钠过量3%以弥补烧结过程中的钠源损失),按照相应的化学计量比与一定质量的氧化锆球共同添加至球磨罐中,随后在行星式球磨机中以600 r/min球磨10 h得到正极前驱体。在马弗炉中,900 ℃烧结15 h得到一系列Sn离子掺杂的NaNi1/3Fe1/3Mn1/3-xSnxO2正极材料。本实验制备出的不同量Sn(1%、2%、3%、10%)掺杂样品的化学式分别为NaNi1/3Fe1/3Mn1/3-0.01Sn0.01O2(NFMS1)、NaNi1/3Fe1/3Mn1/3-0.02Sn0.02O2(NFMS2)、NaNi1/3Fe1/3Mn1/3-0.03Sn0.03O2(NFMS3) 及 NaNi1/3Fe1/3Mn1/3-0.1Sn0.1O2(NFMS10)。
1.2 材料结构表征
采用日本理学Rigaku smartlab9型X射线衍射仪分析材料物相,测试条件为:Cu 靶,40 kV,150 mA,XRD 扫描速度2°/min,扫描范围5°~80°。材料的微观形貌由SEM(型号Quanta 400FEG)和TEM(型号Jem 2100f 200KV)观察,元素分布由美国EDAX 公司生产的APPLO xl能谱仪分析。
1.3 电池极片制作及组装电池
按活性物质、导电剂(碳黑Super P)和黏结剂聚偏氟乙烯(PVDF)8:1:1的质量比,搅浆后涂覆在铝箔集流体,80 ℃鼓风干燥30 min,120 ℃真空干燥10 h,烘干后裁剪得到直径为12 mm 的圆形极片并冲压。在水氧含量均低于0.1 ppm(1 ppm=0.0001%)的手套箱中以金属钠片为对电极,聚丙烯隔膜,并选用1.0 mol/L 的NaPF6/PC:EMC=1:1和2%FEC 添加剂为电解液装配成2016 型扣式电池。在LAND CT2001A 电池测试系统中进行恒流充放电测试,电压测试区间为2~4 V。循环伏安及交流阻抗使用荷兰Ivium-n-Start 电化学测试仪,CV 扫描速度为1 mV/s,EIS 测试频率为1 MHz~0.01 Hz,振幅10 mV,所有电池测试均在室温下(25 ℃)进行。
2 结果与讨论
2.1 材料结构表征
2.1.1 XRD分析
不同掺杂比例NaNi1/3Fe1/3Mn1/3-xSnxO2样品的XRD 谱如图1(a)所示,NFM、NFMS1、NFMS2及NFMS3 四种材料的特征衍射峰均与R3m空间群、α-NaFeO2构型相匹配,而NFMS10 样品部分O3材料典型的衍射峰已经消失,表明过量的Sn掺杂会破坏材料的晶体结构。对此,本工作后续不再对已经造成材料晶体结构破坏的NFMS10样品做进一步的电化学性能分析。由于Ni在O3正极材料中溶解度有限,少量杂质属于NiO。NiO 具有电化学惰性,不参与电化学反应[19-20]。特别地,Sn掺杂后代表层间距的(003)峰随着掺杂量的增加逐步向低角度偏移,根据Bragg 方程2dsinθ=nλ,表明正极材料的层间距随着Sn掺入量的增加而逐渐扩大,印证了Sn4+成功掺杂到体相结构中[21]。这是由于Sn4+(0.71 Å)的半径大于Mn4+(0.53 Å)、Fe3+(0.645 Å)、Ni2+(0.69 Å),从而扩展了层间间距,这将有利于提升Na+的扩散速率及材料的动力学性能。然而,层间距的增加虽然与Sn 掺杂量的提升呈正比关系,但如上文介绍可知,过量的Sn 掺杂会破坏材料的晶体结构,从而削弱这种由层间距增大带来的材料性能提升的优势。Sn 掺杂量为3%的NFMS3 样品,虽然没有出现NFMS10样品中衍射峰消失及峰强度大幅降低的现象,但其XRD 强度相比NFM、NFMS1及NFMS2明显减弱,表明Sn掺杂量为3%时同样会对晶体结构产生影响,降低材料的结晶性。但由于3%掺杂量相对10%仍要低很多,对晶体结构产生的有害影响较为轻微。而对于NFMS2样品,其XRD强度并没有出现相较NFM及NFMS1随着Sn 掺杂量的增加强度变低的现象,反而在五个样品中强度保持最大,表明少量的Sn 掺杂对材料的晶体结构成型是具有促进作用的,有利于材料发挥更优异的电化学性能。为了更深入地研究适量的Sn 掺杂对晶体结构的影响,借助GSAS 软件对NFM 和结晶性最好的NFMS2 材料的XRD 图谱Rietveld 精修。由于NiO 杂质的存在,采用两相细化方法,以R3m空间群α-NaFeO2和Fm3m空间群NiO作为精修的标准图谱。精修结果如图1(b),(c)所示,NFM 和NFMS2 的精修参数Rwp分别为10.9%与11.94%,均高度符合材料结构。通过Rietveld 细化获得的晶格参数比较如表1 所示。显然,晶胞参数a、c轴的长度已经延长(由a=2.933 Å、c=16.15 Å 提升至a=3.010 Å 和c=16.298 Å),Na—O 键的长度增加,TM—O键的长度缩短。这可能是因为Sn4+的半径大于Mn4+的半径,并且Sn—O键(548 kJ/mol)具有比Mn—O键(391.6 kJ/mol)、Ni—O键(402 kJ/mol)更强的结合能[22]。强大的Sn—O键增强了过渡金属离子和氧离子之间的静电吸引,增大了TMO2层中TM 对O 的引力,并降低了Na 层中Na对O的引力[23]。此外,氧原子作为维持层状结构中钠层与过渡金属层的桥梁,TM—O 键长度越短,TM—O 键能越强,对应的过渡金属对氧的束缚能力就越强,一定程度上抑制了TM—O 键的断裂防止氧的析出,维持了TMO2层的结构稳定[24]。同时,Na+嵌/脱过程中受到的剪切应力也会相应减小,避免了晶体结构的损坏。而Na—O 键长的增加会提高Na层的高度,降低钠离子的扩散势垒[25]。
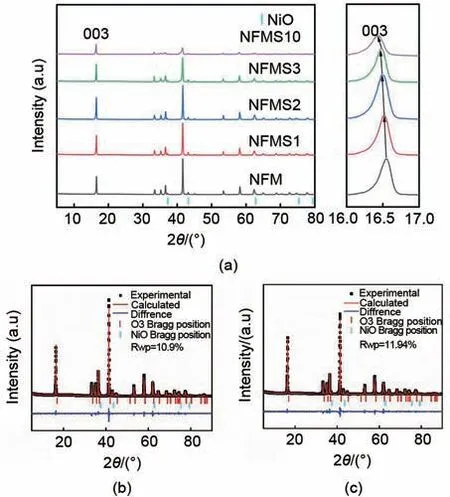
图1 (a)不同比例Sn掺杂的NaNi1/3Fe1/3Mn1/3-xSnxO2材料的XRD图谱及其(003)特征峰;(b)NFM和(c)NFMS2材料的XRD精修结构表征Fig.1 (a)XRD patterns of Sn-doped NaNi1/3Fe1/3Mn1/3-xSnxO2 materials and the corresponding(003)peaks;Rietveld refinements of the XRD data of NFM(b)and NFMS2(c)

表1 样品NFM和NFMS2 Rietveld细化得到的晶格参数Table 1 The lattice parameters of NFM and NFMS2 obtained by the Rietveld method
2.1.2 材料形貌分析
为探究Sn4+的掺入对材料形貌的影响,对不同量Sn掺杂的正极材料进行FESEM测试。图2(a)~(d)为四种不同掺杂量(x=0、0.01、0.02、0.03)的FESEM 图。四种材料均由众多不规则纳米块状颗粒堆积成的大颗粒,棱角清晰,表面光滑。这表明Sn掺杂并不会改变材料的微观形貌。NFMS2样品的能谱分析结果图(e)证明了钠、镍、铁、锰、锡元素在样品中均匀分布,验证了Sn4+的成功掺入。

图2 四种材料(a)NFM(b)NFMS1(c)NFMS2(d)NFMS3的FESEM图;(e)NFMS2的能谱;(f)NFM与(g)NFMS2高分辨TEM图Fig.2 FESEM images of NaNi1/3Fe1/3Mn1/3O2 materials with different Sn doping contents,(a)NFM(b)NFMS1(c)NFMS2(d)NFMS3;EDS spectrum of(e)NFMS2;TEM images of(f)NFM and(g)NFMS2
采用HRTEM 进一步研究材料的晶体结构。如图2(f)~(g)所示,两种材料均可以看到清晰的晶格条纹。值得说明的是,NFM 中发现了部分区域的晶格条纹严重变形或缺失[图2(f)红框],这可能导致Na+固相迁移时受到的阻力更大,以及材料丢失部分储钠位点。然而,得益于Sn4+的成功掺入,以上问题得到缓解,在NFMS2 中只发现了轻微变形[图2(g)绿框]的区域。这表明Sn掺杂构造了更完善的层状晶体结构,一定程度上抑制了晶格畸变。5.343 Å 对应于傅里叶变换测量出的(003)晶面间距。与预期一致,掺Sn 后的NFMS2(003)晶面间距为5.407 Å,相较NFM 的晶面间距也有所增加,有利于Na+更快速地扩散。
2.2 电化学性能分析
对四种材料组装成的扣式电池在0.2 C 倍率,2~4 V电压区间内进行首圈充放电测试。如图3(a)所示,四种样品具有相似的充放电曲线,放电平台在3 V左右,NFM正极材料具有131.9 mAh/g的首圈放电比容量。NFMS1、NFMS2、NFMS3 放电比容量分别为136.7 mAh/g、139.1 mAh/g、133.9 mAh/g,掺杂后材料的首次放电比容量有所提升。随后对四种样品活化完成后的电池分别在1 C、2 C、5 C、8 C、1 C 倍率下连续充放电,每个倍率循环5 圈。如图3(b)所示,四种样品随着电流增大其放电比容量出现不同程度的衰退,其中NFMS2样品在每个倍率下都能保持最佳,NFMS1、NFMS3稍差,但都优于NFM样品。尤其在8 C倍率下,NFM样品由1 C的127.2 mAh/g放电比容量已衰减至91.7 mAh/g(放电比容量保持率72.1 %),而NFMS2 样品由1 C 的134.3 mAh/g 仅下降到110.5 mAh/g(放电比容量保持率82.3%),对比差异显著。当电流密度回至1 C倍率时,NFM样品放电比容量为120.2 mAh/g,容量恢复率为94.49%;NFMS2 样品放电比容量为131.5 mAh/g,容量恢复率为97.92%。这表明Sn掺杂后材料的可逆性得到增强。对于倍率性能的巨大改善,原因可能是Sn掺杂扩大了材料的层间距,提高了Na+扩散速率,降低了Na+脱/嵌过程中受到的阻力。图3(d)为四种样品的充放电循环曲线,1 C倍率下循环200 圈后,NFM、NFMS1、NFMS2、NFMS3放电比容量分别衰减至91.8、103.1、107.2和98.9 mAh/g,放电比容量保持率相较初始(126.5、131.3、133.9 和128.4 mAh/g)为72.5%、78.5%、80.1%、77%,由此可见,材料的循环性能得益于Sn4+的引入也有所提升。这可能是因为Sn掺杂后,强大的Sn—O 键增强了TM 对O 原子的结合能力。更强的TM—O键使得材料在循环过程中,TMO2层能够更好地保持结构稳定。同时,更大的Na 层间距减少了长循环过程中Na+的不断脱/嵌对晶体结构的破坏。但如上文分析,Sn掺杂量不是越大越好,过量的Sn 掺杂会降低材料的结晶性,并引起晶体结构的微改变,这可能是NFMS3 样品循环性能相较NFMS1、NFMS2下降的重要原因。因此,综合结构表征分析和电化学测试,2%的Sn掺杂量最有利于提升正极材料的综合电化学性能。进一步对四种不同Sn 掺杂量的样品在充电段与放电段分别进行了恒电流间歇滴定技术(GITT)测试。如图3(d)所示,四种样品均表现出钠离子扩散系数DNa+与荷电状态SOC 相关联的电化学性质。无论是充电段或是放电段,掺Sn 材料的扩散系数都明显大于NFM。尤其是在2.9 V 附近的区域,这部分的DNa+值主要来自材料固相内部的钠离子扩散[21],NFMS1样品GITT曲线稍高于NFM,而NFMS2及NFMS3明显更高,这与倍率性能相吻合。由此可见,Sn掺杂确实可以有效改善材料内部的扩散动力学性能。

图3 NaNi1/3Fe1/3Mn1/3-xSnxO2样品(a)0.2 C倍率下首次充放电曲线;(b)倍率性能曲线;(c)2~4 V下的1 C循环曲线以及(d)NFM和NFMS2的GITT曲线Fig.3 (a)First charge-discharge curves at 0.2C;(b)Rate performance;(c)Cycling properties under 2-4 V at 1 C;(d)GITT curves of NaNi1/3Fe1/3Mn1/3-xSnxO2samples
从前文的叙述可知,四种样品在1 C以及更大电流密度下的电化学性能差异明显,因此对活化完成后1 C倍率循环首圈及第200圈的四种样品,采用1 mV/s扫速,扫描区间2~4 V,进行了电池CV测试以观察其循环前后的结构演化。
如图4(a)~(d)所示,NFM、NFMS1、NFMS2、NFMS3 样品在循环第一圈时的氧化还原峰电位分别为3.350/2.530 V、3.304/2.514 V、3.328/2.548 V、3.332/2.552 V,所对应的是Ni2+/Ni4+氧化还原对,即O3-P3 的相变[26]。对比循环前后的CV 曲线,四种材料都有不同程度氧化还原峰的位置偏移以及峰型变化。200 圈循环后的NFM、NFMS1、NFMS2、NFMS3 样品氧化还原峰电位分别为3.566/2.416 V、3.418/2.518 V、3.376/2.546 V、3.520/2.510 V。NFMS2 样品的氧化还原峰保持效果最佳,仍能看到较清晰的峰型,氧化还原峰电位差值由首圈的0.78 V略微增加至0.83 V。NFMS1(首圈0.79 V)与NFMS3(首圈0.78 V)的峰电位差值分别增加至0.9 V和1.01 V。对比NFM 样品由首圈的峰电位差值0.82 V 已大幅度增加至1.15 V。这表明Sn 掺杂可以有效降低电池极化,提高材料的氧化还原反应可逆性。其次,NFM 首圈尖锐的氧化还原峰随着电池不断循环后逐渐宽化,至第200圈时峰型基本变平,这与Wu等人[27]对LiNi0.8Co0.1Mn0.1O2材料CV测试所观察到的现象一致,它可能代表着相的损失。对于NaNi1/3Fe1/3Mn1/3O2材料,其在首圈活化完成后会得到一个O相和P相的混合相产物,P相的存在可减小纯O 相中钠离子在层间迁移带来的应力[28]。相比之下,图3(c)NFMS2 样品的氧化还原峰虽有一定的衰减,但相对峰型仍保持较好,表明Sn 掺杂后可能减少了有利相P相的损失,这有助于容量的保持以及循环稳定性的提升[27]。

图4 (a)NFM(b)NFMS1(c)NFMS2(d)NFMS3样品200循环前后的循环伏安曲线及(e)NFM和(f)NFMS2样品的等效电路及EIS图Fig.4 The cyclic voltammograms of(a)NFM,(b)NFMS1,(c)NFMS2,(d)NFMS3 after 1 cycle and 200 cycles witin 2-4 V at 1 mV/s;EIS diagrams of(e)NFM,(f)NFMS2 and the equivalent circuit in inset
对最佳样NFMS2和NFM样品分别在活化完成后的首圈及循环至第200圈的电池进行了交流阻抗(EIS)测试,测试频率区间为1 MHz~0.01 Hz,振幅10 mV。由于SOC 对于电池的阻抗会产生较大的影响,在测试前将NFMS2和NFM样品统一恒流充电至满电态(SOC=100%)并静置30 min,以保证相同的测试状态及数据的准确性。图3(e)、(f)分别为首圈和第200圈NFMS2和NFM样品测试得到的奈奎斯特图,由中高频区的两段圆弧与低频区的斜线组成。其中,中高频区的第一段圆弧代表着Rf界面电阻、第二段代表着Rct电荷转移电阻,低频区斜线代表着扩散电阻Zw。使用Zsimpwin 软件对测量数据拟合结果见表2,两种材料在循环后总阻抗增加,界面电阻Rf增加、电荷转移电阻Rct变小。Rf的增大是因为电池随着不断循环,界面的副反应会不可避免地增多。Rct减小是由于电池在初始的循环阶段,内部仍处于不断调整,对电池的充放电过程会一定程度提高其动力学性能,这将导致Rct的变小[29-30]。对比两种样品,NFMS2 相较NFM 样品在循环前后各类阻抗数值都保持最小,这有利于Na+在充放电过程中的迁移与脱嵌[31]。较小的Rct阻值表明Sn 掺杂增强了材料的导电性。阻抗作为电池内部动力学及电化学过程中的一种反应,印证了Sn掺杂有效地改善了材料的电化学性能。

表2 NFM和NFMS2样品的阻抗拟合值Table 2 Impedance fitting values of NFM and NFMS2 samples
3 结 论
本工作采用固相法制备了不同比例Sn4+掺杂的NaNi1/3Fe1/3Mn1/3-xSnxO2材料,相较NFM 材料具有更优异的循环稳定性以及倍率性能。Sn 掺杂没有破坏原始材料R3m空间群的O3层状结构,并增大了材料的晶面间距。XRD 结果表明:适量的Sn 掺杂有利于提高材料的结晶性,Sn 掺杂氧化物优异的电化学性能可归因于层间距的增加、TM—O 键的缩短。层间距的增加提升了Na 层的宽度,增大了Na+扩散系数,降低Na+嵌入/脱出过程中所受到的阻力,为其提供更好的传输通道,有效提升了材料的倍率性能。TM—O 键的缩短,减少了Na+嵌入/脱出过程中受到TMO2层剪切应力的影响,并稳定了TMO2层结构,维持了循环中晶体结构的稳定性进而提高材料的循环性能。HRTEM 显示得益于Sn4+的引入,材料的晶格更趋于完整,为钠离子提供了更多储钠位点。CV 与EIS 测试结果表明,Sn掺杂降低了电池极化,增强了电极材料在充放电循环中的氧化还原反应可逆性。本研究验证了Sn掺杂在层状三元材料中的可行性,为设计高倍率、高循环稳定性的正极材料提供一定的理论依据与指导。
