解读中考综合计算题
2022-07-05刘甲明
刘甲明


化学计算是重要的化学基本技能,是从量的角度反映了物质之间的相互关系及其转化规律。它必须在理解、掌握有关化学概念、原理和元素化合物知识的基础上进行应用。无论计算题型怎样变化,化学的概念、原理不变。无论计算的方法如何变化,化学的原理、知识不变。所以,中考综合计算题的解题关键是准确理解题意,找到已知和求解之间的思路和线索,把概念、公式和求解条件等紧密结合起来考虑,形成完整的解题思路,选择科学简洁的解题方法进行解题运算。
一、有关综合计算的题型
(1)文字叙述型计算(2)表格数据型计算
(3)坐标图像型计算(4)图解实验型计算
二、题型探究
1.文字叙述
典型例题1(2021·内蒙古中考)钙是人体中的常量元素,缺钙时可服用补钙剂来增加摄入量。为测定某种钙片中碳酸钙的含量,某同学取钙片10片(每片2g)研碎后放于烧杯中,向其中加入一定浓度的稀盐酸至不再产生气泡,过滤后得到不溶物的质量为10g,再向滤液中加入55.4g水,此时溶液中溶质的质量分数为10%(钙片中主要成分为碳酸钙,假设其他成分不溶于水,也不与盐酸反应)。计算:
(1)该种钙片中碳酸钙的质量分数。
(2)加入稀盐酸的质量。
(3)若配制200g上述浓度的稀盐酸,需用36.5%的浓盐酸的质量。
解题思路(1)依据反应前后相关数据的变化,计算出钙片中碳酸钙的质量(10片钙片的质量—不溶物的质量);(2)先写出发生反应的化学方程式,然后找出已知量和未知量,最后列式进行计算;(3)溶液稀釋前后,溶质的质量不变。
解(1)该种钙片中碳酸钙的质量分数:
(2)该反应所消耗的氯化氢的质量为x,生成氯化钙的质量为y,生成二氧化碳的质量为z。
设加入稀盐酸质量为m。
(3)设需用36.5%浓盐酸的质量为n200
答:略。
2.表格数据
典型例题2(2021·铜仁中考)小红同学在网店花了200元买了一个10g重的手镯(银锌合金),他想探究此手镯中银的含量,于是请化学老师和她一起探究:在实验室用足量的稀硫酸分多次与手镯充分反应,实验结果如表1:
依据表1中的数据分析,完成下列问题:
(1)如果小红用所得的银制作一枚戒指,其质量不超过多少克?
(2)计算所用稀硫酸的溶质质量分数。
解题思路做此类题目时,首先明确表格中各栏表示的含义,然后比较分析数据的变化,在变化规律中找出实际参加反应的纯量,通常用差量法计算相关的量(一般能计算出生成气体或沉淀的质量)。
解(1)比较第四次和第五次的数据可以知道,剩余固体的质量都为4.8g,可以说明该固体中银的质量4.8g,小红用所得的银制作一枚戒指,其质量不超过4.8g;
(2)设稀硫酸中溶质质量为x,固体中锌的质量为:
所用稀硫酸的溶质质量分数是:7.84g
答:略。 3.坐标图像
典型例题3(2021·自贡中考)在82.8g碳酸钠溶液中,逐滴加入盐酸,所加盐酸的质量与产生气体的质量关系如图1所示,滴加过程中先发生化学反应:
Na2CO3+HCl=NaHCO3+NaCl
试计算(不考虑气体的溶解和盐酸的挥发):
(1)m的值为g;
(2)刚好不再产生气体时,溶液中溶质的质量分数(写出化学方程式及计算过程)。
解题思路对坐标图像式的综合计算题,解题时需先分析坐标曲线图中横、纵坐标表示的含义,再结合题中所涉及的化学反应分析图像的起点、转折点和终点的含义。找已知量的方法一般有三种:转折点对应的横坐标(某些情况下需要进行换算才能代入,如乘以溶质的质量分数等);转折点对应的纵坐标(多为生成的气体或沉淀的质量,可直接代入);起点和转折点对应的坐标差。
解(1)由图中数据可知,20g稀盐酸完全反应生成2.2g二氧化碳,加入盐酸至160g时仍然产生二氧化碳,说明加入140g盐酸时,盐酸完全反应,m的值为:2.2x3=6.6。故填:6.6。
(2)设反应生成氯化钠质量为x,Na2CO3+2HCl2NaCl+H2O+CO2↑
刚好不再产生气体时,溶液中溶质的质量分数是:
答:略。
4.图解实验
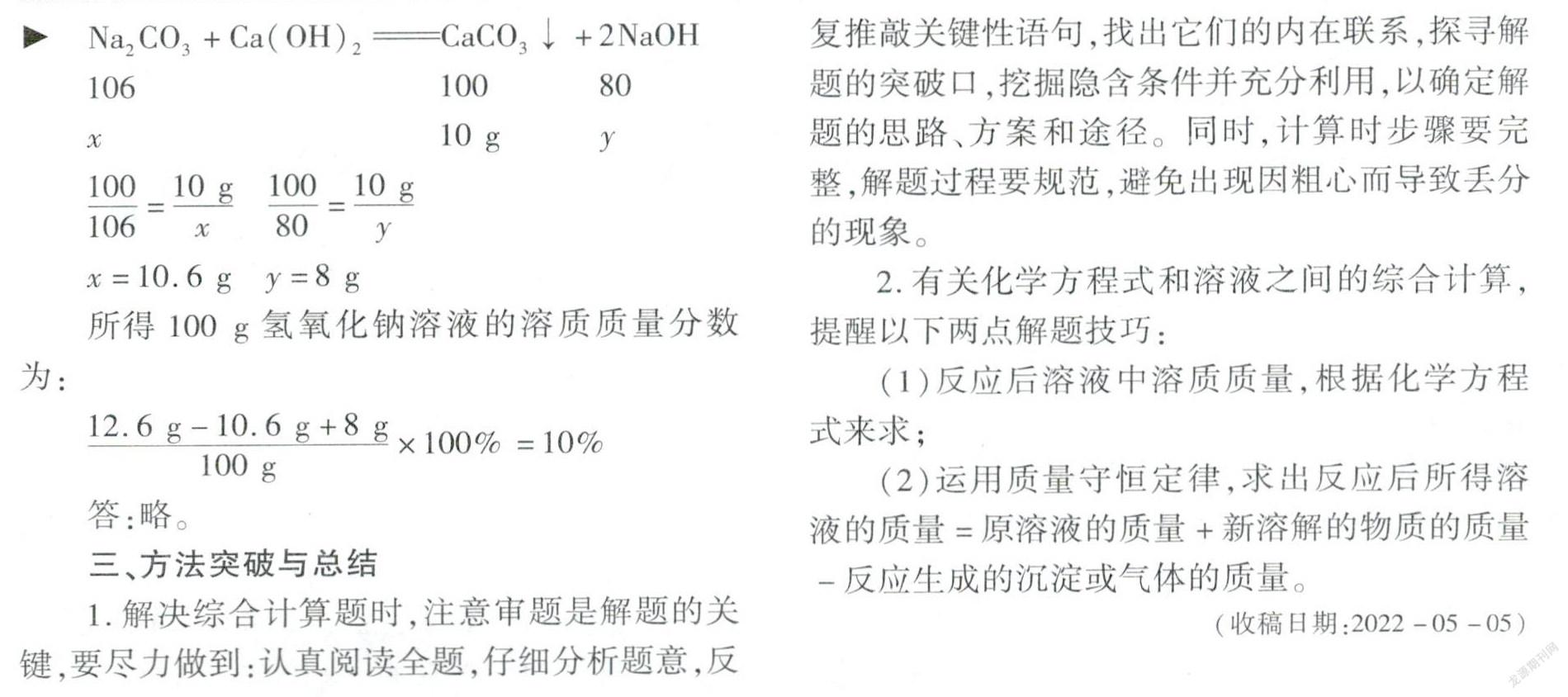
典型例题4(2021·聊城中考)某化学兴趣小组将一瓶已变质的氢氧化钠固体进行如图2所示操作,最后获得100g氢氧化钠溶液。请解答下列问题:
(1)请写出氢氧化钠在空气中变质的化学方程式。
(2)求最后所得100g氢氧化钠溶液的溶质质量分数(写出计算过程)。
解题思路解此类题目时,要分析题中反应前后有关数据的变化,一般可利用差量法计算出生成的某种气体的质量或沉淀的质量,或混合物中参加反应的某物质的质量。
该题考查化学方程式与溶质质量分数的综合计算题。由碳酸钠和氢氧化钙溶液恰好完全反应,得出反应生成的碳酸钙的质量(依据反应前后有关数据关系)为10g,进而根据反应的化学方程式,求出参加反应的碳酸钠的质量和反应生成的氢氧化钠的质量。
解(1)CO2+2NaOH=Na2CO3+H2O
(2)设原固体中碳酸钠的质量为x,生成氢氧化钠的质量为y
Na2CO3+Ca(OH)2CaCO3↓+2NaOH 106
所得100g氢氧化钠溶液的溶质质量分数为:
答:略。
三、方法突破与总结
1.解决综合计算题时,注意审题是解题的关键,要尽力做到:认真阅读全题,仔细分析题意,反复推敲关键性语句,找出它们的内在联系,探寻解题的突破口,挖掘隐含条件并充分利用,以确定解题的思路、方案和途径。同时,计算时步骤要完整,解题过程要规范,避免出现因粗心而导致丢分的现象。
2.有关化学方程式和溶液之间的综合计算,提醒以下两点解题技巧:
(1)反应后溶液中溶质质量,根据化学方程式来求;
(2)运用质量守恒定律,求出反应后所得溶液的质量=原溶液的质量+新溶解的物质的质量—反应生成的沉淀或气体的质量。
(收稿日期:2022—05—05)C7190285-9A30-42A9-AEF5-9D2FAB1B5BA1
