丹皮酚醇质体凝胶的成型工艺优化及经皮渗透性研究
2022-07-04王睿郭东艳翟秉涛程江雪张小飞杨荣平陕西中医药大学秦药特色资源研究与开发国家重点实验室培育陕西省中药基础与新药研究重点实验室西安72046西南大学药学院重庆40075
王睿,郭东艳,翟秉涛,程江雪,张小飞,杨荣平,2*(.陕西中医药大学,秦药特色资源研究与开发国家重点实验室(培育)/陕西省中药基础与新药研究重点实验室,西安 72046;2.西南大学药学院,重庆 40075)
丹皮酚(paeonol)是从毛茛科植物牡丹皮的干燥根皮和萝藦科植物徐长卿的干燥根及根茎中提取的主要有效成分,具有抗过敏、抗炎、抗肿瘤、心血管保护及神经保护作用[1],丹皮酚对多种急慢性炎症反应都有抑制作用,对于湿疹、过敏性皮炎等皮肤炎症有一定抑制作用。目前市场上的丹皮酚外用制剂仅丹皮酚软膏一种,其主要成分为丹皮酚和丁香油,利用中药挥发油来促进丹皮酚的透皮效果,但这种促渗技术效果有限,药物经皮渗透率较低,且部分患者依从性不高,因此,对现有制剂进行技术改良,提高丹皮酚的经皮渗透能力具有重要意义。
醇质体(ethosomes)具有生物膜类囊泡结构[2],能够包裹药物透过角质层进入皮肤及血液,达到病变部位,在结构上与脂质体相似,不同的是醇质体处方中含有相对较高浓度的乙醇,乙醇是一种促渗剂,乙醇的加入提高了传统脂质体的柔韧性,帮助药物通过角质层进入皮肤深层直至血液循环,发挥药物潜在的治疗效果。醇质体作为中间体,没有固定的剂型,存在流动性太强的问题[3-4],因此本研究拟在前期课题组研究结果[5]的基础上,将丹皮酚醇质体混悬液(paeonol ethosomal suspensions,PES)进一步制备成凝胶剂,优化丹皮酚醇质体凝胶(paeonol ethosomal gels,PEG)的成型工艺,并对比丹皮酚溶液凝胶(paeonol solution gels,PSG)及市售丹皮酚软膏(paeonol otintmemt,PO)的经皮渗透性能,以期为丹皮酚经皮给药制剂的开发提供实验依据。
1 材料
Agilent 1260 高效液相色谱仪(美国安捷伦科技公司),纳米粒径电位分析仪(ZS90,英国马尔文仪器有限公司),X1高速冷冻离心机(美国贝克曼库尔特有限公司),HJ-3型恒温磁力搅拌器(常州国华电器有限公司),pHS-3C型雷磁pH计(上海精密科学仪器有限公司),AR1140电子天平(梅特勒-托利多仪器上海有限公司),Brookfield旋转黏度计(江苏胜祥电子科技有限公司)。
大豆卵磷脂(纯度≥98%,批号:J27M8R 32632)、胆固醇(纯度≥98%,批号:C10090003(上海麦克林生化科技有限公司);丹皮酚原料药(纯度>99%,西安德生元生物科技有限公司);丹皮酚软膏(批号:Z34020837,合肥立方制药股份有限公司);卡波姆 Carbomer 934(廊坊聚通化工);超滤管(密理博中国有限公司);甲醇(色谱级,美国飞世尔科学世界公司);水(杭州娃哈哈集团有限公司);其他化学试剂均为分析纯(天津市天力化学试剂有限公司)。
2 方法及结果
2.1 PES的制备
依据课题组前期实验结果[5]得出,制备PES的方法为乙醇注入法,处方为25%(V/V)乙醇、1.5%(W/V)胆固醇和2.5%(W/V)卵磷脂。在此结果下,称取处方量的丹皮酚样品、胆固醇和卵磷脂,加入处方量的无水乙醇进行溶解,置于30℃恒温磁力搅拌器中进行搅拌,充分溶解后缓慢注入PBS(pH=6.8),700 r·min-1持续搅拌1 h,细胞超声粉碎仪冰浴超声10 min,过0.45 μm滤膜,得到乳白色PES,4℃下保存。
2.2 PEG及PSG的制备
分别取处方量的PES和丹皮酚溶液,称取适量卡波姆,均匀撒于混悬液和溶液液面,放置24 h溶胀后,加入保湿剂甘油,搅匀后,再加入三乙醇胺调节pH至弱酸性以接近皮肤pH,搅拌均匀即得PEG和PSG。
2.3 丹皮酚分析方法的建立
2.3.1 色谱条件 色谱柱:Thermo Scientific C18色谱柱(250 mm×4.0 mm,5 μm);流动相:甲醇-水(80∶20);流速:0.8 mL·min-1;柱温:30℃;紫外检测波长:274 nm;进样量:10 µL。
2.3.2 专属性 按照“2.1”项下方法,分别制备PES及不加药物的空白醇质体混悬液,取适量丹皮酚对照品配制成100 g·mL-1的对照品溶液,分别取10 μL进样测定,进行专属性考察,结果显示丹皮酚峰形良好,空白醇质体混悬液无干扰,色谱图见图1。
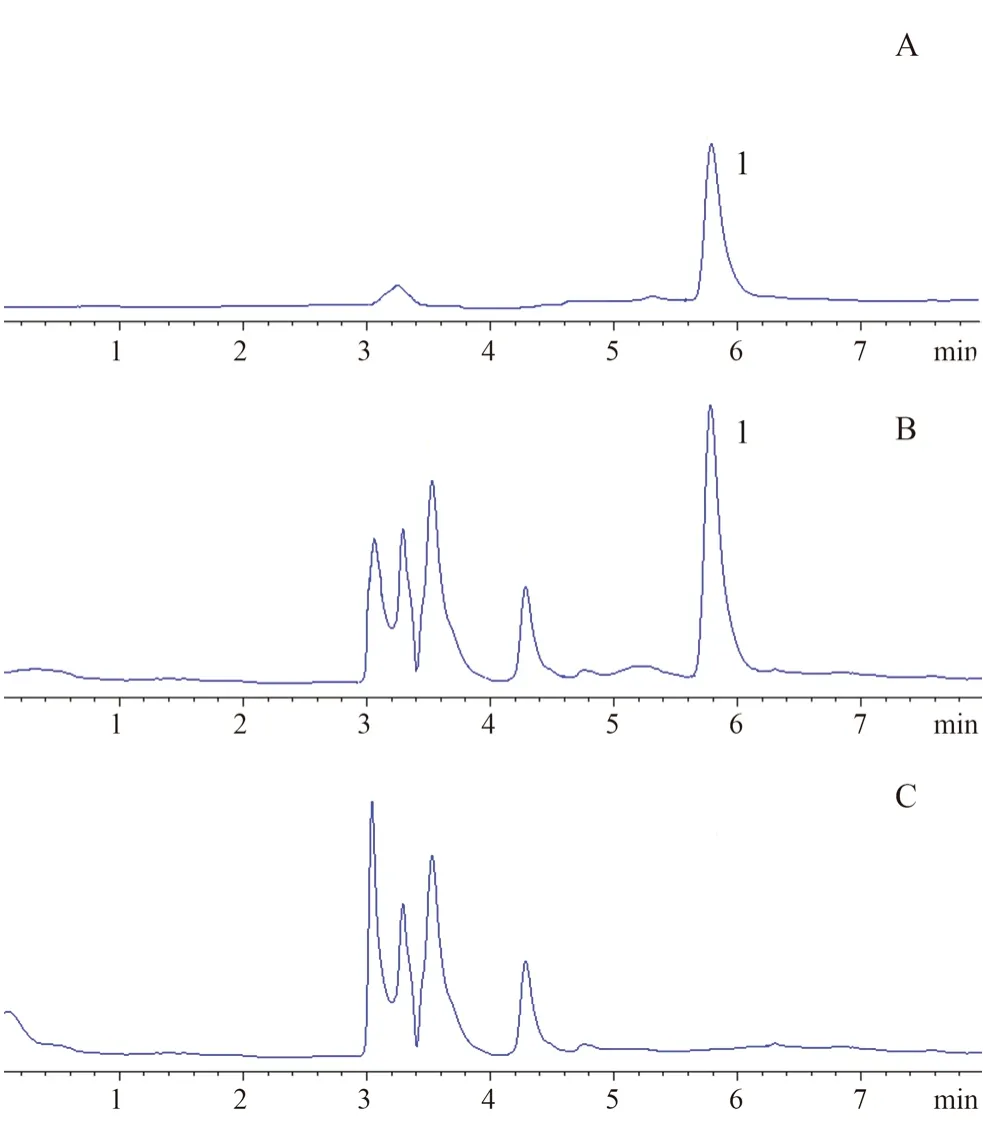
图1 丹皮酚的HPLC色谱图Fig 1 HPLC chromatogram of paeonol
2.3.3 线性关系 吸取丹皮酚对照品溶液,加入色谱甲醇逐级稀释为10、20、40、60、80、100、120、200 μg·mL-1,进样测定,以峰面积(Y)对质量浓度(X,μg·mL-1)进行线性回归,得到线性方程Y=33.14X+14.87(r=0.9997),结果表明丹皮酚在10~200 μg·mL-1内与峰面积线性关系良好。
2.3.4 精密度考察 精密吸取丹皮酚对照品溶液,在“2.3.1”项色谱条件下重复进样6次,计算峰面积RSD为0.41%,表明仪器精密度良好。
2.3.5 稳定性考察 取丹皮酚供试品溶液分别在0、2、4、6、8、10 h取样测定,记录峰面积,计算其RSD为0.24%,表明该方法稳定性良好。
2.3.6 加样回收率考察 制备3组样品,每组3份,加入已知含量的80%、100%、120%丹皮酚对照品,制备供试品溶液,分别进样,计算得低、中、高浓度平均加样回收率分别为97.95%、98.02%、99.07%,RSD值均为1.2%,表明该方法准确度良好。
2.4 PEG成型工艺的优化
2.4.1 PEG评分标准的建立 2020年版《中国药典》四部[6]规定凝胶剂应均匀、细腻,在常温时保持胶状、不干涸或液化。因此以凝胶剂的外观、均匀度、黏稠度、pH、涂展性、稳定性(离心、高温、低温)为综合指标[7-10],考察凝胶剂的成型情况。综合评分满分为8.0分,评分标准如表1所示。

表1 凝胶剂综合评分标准 Tab 1 Comprehensive scoring criteria for gels
2.4.2 Box-Behnken响应面法优化PEG成型工艺 采用Box-Behnken 法,选择卡波姆用量(A)、甘油用量(B)、三乙醇胺用量(C)为影响凝胶剂的主要因素,综合评分为响应值,设计因素水平表进行实验(见表2),利用Design Expert软件进行响应面分析,确定PEG的最佳成型工艺。实验结果见表3。

表2 因素水平(%) Tab 2 Factor and level (%)

表3 实验设计及结果 Tab 3 Experimental design and result
采用Design Expert进行数据分析,对各因素进行回归分析后,得到二项式拟合方程为Y=7.99-0.225A-0.0724B-0.1566C-0.0592AB-0.2654AC+0.025BC-1.69A2-0.7025B2-0.3525C2(R2=0.9691,P<0.001),对二次回归进行方差分析,如表4所示。模型的A、B、C、AC、A2、B2、C2均具有显著性,失拟项检验不具有显著性,说明该模型的拟合度和可信度高,可用于对凝胶成型工艺的分析和预测。

表4 方差分析结果 Tab 4 Analysis of variance
综合评分的等高线图及三维效应曲面图见图2,可得出最大预测值,A为1.14,B为17.26,C为0.43,Y为7.95,即PES的成型工艺理论条件为:卡波姆用量1.14%,保湿剂用量为17.26%,三乙醇胺用量为0.43%。改进最佳条件,最终确定凝胶成型工艺为1%卡波姆、17%甘油、0.5%三乙醇胺,按照此工艺平行三次实验,综合评分平均值7.89与理论值7.95较为接近,说明该回归方程与实际情况拟合较好,该工艺切实可靠。

图2 卡波姆用量(A)、保湿剂用量(B)和三乙醇胺用量(C)在综合评分上拟合方程的响应面和等高线图Fig 2 Response surface and contour plots of the fitted equations for carbomer dosage(A),humectant dosage(B)and triethanolamine dosage(C)on the composite score
2.5 PEG的显微观察
取PEG 1 g,加入纯水稀释后,取适量样品于铜网格上,用1%磷钨酸负染并在室温下干燥,然后在透射电镜下观察囊泡形态。结果如图3所示,丹皮酚醇质体囊泡呈圆形或椭圆形,大小适宜,表明醇质体在凝胶基质中结构完整、分散良好。

图3 PEG形态图Fig 3 TEM of paeonol ethosomes
2.6 经皮渗透性研究
取健康大鼠,脱颈处死,剥取腹部皮肤,剃去毛发,除去脂肪、结缔组织,用生理盐水冲洗数遍;将大鼠皮肤水平放置于Franz扩散池[11],角质层面向供给池,皮下组织面向接收池。接收液为25%乙醇,排尽气泡,平衡30 min,水浴加热,使其保持在(37±0.5)℃,接收液用小磁粒持续磁搅拌24 h以确保药物均匀分散。将制剂(等量的PSG、PEG及PO)涂抹在皮肤表面,并用封口膜覆盖,以避免蒸发。在 0.5、1、2、4、6、8、12 和 24 h取出 0.5 mL 的接收液,同时补充等量的新鲜接收液。通过高效液相色谱法分析 0.5 mL 接收液中的药物含量,并根据下式计算单位面积内药物的累积渗透量(Qn):
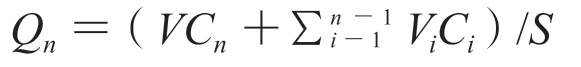
Cn为n小时接收池内的药物浓度,Ci代表样品的药物浓度,S为有效扩散面积(0.785 cm2),V和Vi分别代表接收池体积(15 mL)和取样体积(0.5 mL)。以Qn对取样时间(t)作渗透曲线,并对渗透曲线的前12 h进行线性回归,所得斜率即为渗透速率Js(μg·cm-2·h-1)。
对各制剂的累积渗透曲线的前12 h进行数据拟合包括零级动力学、一级动力学、Higuchi方程以及Hixcon-Crowell方程,如表5所示,根据r值可得出PEG和PO对于Higuchi模型拟合度最高,说明两者的释药过程符合Higuchi方程,具有缓释效果。不同丹皮酚制剂的累积渗透曲线如图4所示,24 h内丹皮酚的含量均在稳定增加,24 h累积渗透量最高的是PEG,其次是PO,累积渗透量最低的是PSG(见表6)。与PSG组相比,PEG和PO提高了药物的渗透性(P<0.05)。以上结果表明醇质体能够增加皮肤对丹皮酚的吸收,原因可能是醇质体外层的脂质层能够与细胞膜融合,携带药物高度变形进入深层皮肤细胞间隙,增强其渗透能力[12]。

图4 不同丹皮酚制剂24 h体外累积渗透曲线(*P<0.05,n=3,±s)Fig 4 24 h in vitro cumulative permeation curves of different paeonol formulations(*P<0.05,n=3,±s)

表5 体外透皮量-时间模型拟合方程 Tab 5 Fitting equation for the in vitro transdermal volume-time model

表6 丹皮酚在各制剂中的渗透动力学参数 Tab 6 Osmotic kinetic parameters of paeonol in each formulation
2.7 体外皮肤沉积性研究
在皮肤渗透性研究结束后取下皮肤,用滤纸轻轻擦拭皮肤表面多余的丹皮酚制剂,用甲醇和生理盐水冲洗皮肤表面并用滤纸吸干。将皮肤切成小块,加入1 mL 甲醇,匀浆10 min,然后超声提取3次,每次15 min,以7000 r·min-1离心 10 min,收集上清液,用 0.45 µm 的微孔滤膜过滤后进行HPLC分析,计算药物在皮肤中的沉积量。如图5所示,24 h后,PEG组的皮肤沉积量大于PO组皮肤沉积量,两者差异无统计学意义,而与PSG组相比,PEG组与PO组的皮肤沉积量显著增加(P<0.01),说明醇质体能够使药物缓慢渗透进入皮肤,而凝胶是充水性三维网状交联体结构,具有贮库效应,延长了药物在皮肤的滞留时间。
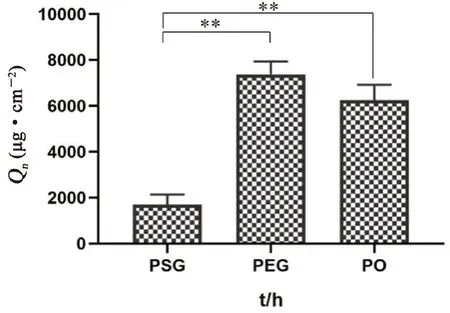
图5 24 h内丹皮酚制剂的大鼠皮肤滞留量(**P<0.01,n=3,±s)Fig 5 Dermal retention of paeonol preparation in rats within 24 h(**P<0.01,n=3,±s)
2.8 皮肤刺激性实验
将6只健康SD大鼠随机分成3组,每组2只,剔除大鼠背部鼠毛,去毛范围为 3 cm×3 cm。给药前仔细检查大鼠剔毛区域有无破损。A组作为对照,不做任何处理;B 组应用PEG;C 组应用PO。将制剂均匀涂抹于大鼠背部皮肤,用纱布覆盖,并用医用胶带固定。24 h后将大鼠断头处死并取下处理过的皮肤,生理盐水清洗除去残留的制剂,然后将皮肤样本置于10%福尔马林中,组织固定。24 h后,垂直切割成3~4 μm厚的切片。对石蜡组织切片进行苏木精-伊红染色(HE染色)[13]。目视观察发现应用PEG和PO的大鼠皮肤无红肿现象,HE染色结果表明PEG组(B)、PO组(C)与空白组(A)无明显差异,显示PEG和PO应用于皮肤安全无刺激性(见图6)。

图6 HE染色后的皮肤(×100)Fig 6 Skin after HE staining(×100)
3 讨论
经皮给药系统作为新型给药方式,其最大的优势在于能够有效避免口服给药存在的肝脏首过效应以及胃肠道对药物的降解的问题,在一定时间内维持恒定的血药浓度,延长了药物的作用时间,从而达到缓释效果[13]。但经皮给药制剂起效首先要透过皮肤角质层,因此如何克服皮肤角质层障碍正是经皮给药技术的核心。当前应用较广的促渗技术有物理技术、化学技术和纳米载体,离子导入技术和微针技术促透效率有限且对皮肤会造成一定的创伤,部分患者依从性不好。化学技术主要是加入化学促渗剂,如中药挥发油、氮酮、二甲基亚砜等,其促渗效果有限,且氮酮、二甲基亚砜等化学试剂用量不当或对皮肤有一定的刺激性[14],纳米载体常见的有脂质体、醇质体、传递体等,其原理是类脂(磷脂、胆固醇等)自由分散于水相中时,头部亲水端插入水中,尾部疏水端伸向空气,在搅拌作用下形成的具有双分子层结构的封闭囊泡,囊泡与皮肤角质层的脂质双层融合,起到促进皮肤渗透的作用。
醇质体是一种中间体,常以混悬液的形式存在,流动性太强,容易发生药物的渗透、聚集等,不利于药物吸收。凝胶剂制备工艺简单,生物相容性好,常用于皮肤、腔道及黏膜给药,因此,将两者结合,制备成醇质体凝胶,不仅能够促进药物的透皮吸收,提高药物的生物利用度,还增加了药物的稳定性,使得药物平稳释放进入皮肤,具有一定的缓释效果[15]。
从渗透曲线来看,给药2 h,PEG和PO的累积渗透量均大于PSG,说明醇质体和中药挥发油提高了药物的渗透性;给药6 h后,PEG的累积渗透量逐渐大于PO,说明醇质体使得药物持续稳定渗透,而中药挥发油的促渗效果则较为有限。结合沉积结果来看,制备成凝胶剂后药物在皮肤的滞留时间延长,具有一定的缓释效果。通过透射电镜显微观察发现醇质体囊泡在凝胶中结构完整,未受到破坏。刺激性实验结果表明显示PEG对皮肤无刺激,说明制备的PEG缓慢渗透,持续稳定释放,安全可靠。
本研究为丹皮酚经皮给药新剂型的开发提供了实验依据,但对于PEG的药效学评价还有待于进一步研究。
