窄带成像技术联合放大内镜JES分型对早期食管癌的诊断价值
2022-06-29吕富靖张澍田
李 雪 邢 洁 张 倩 李 鹏 吕富靖 张澍田
(首都医科大学附属北京友谊医院消化内科 国家消化系统疾病临床医学研究中心 北京市消化疾病中心 消化疾病癌前病变北京市重点实验室,北京 100050)
内镜下黏膜切除术(endoscopic mucosal resection,EMR)及内镜黏膜下剥离术(endoscopic submucosal dissection,ESD)现已成为早期食管癌治愈性微创治疗方法[1]。早期食管癌淋巴结转移率与肿瘤浸润深度成正比。根据日本食管癌诊疗指南[2],黏膜上皮层(mucosal epithelium,EP)癌或黏膜固有层(lamina propria mucosae,LPM)癌被认为是内镜治疗的绝对指征;黏膜肌层(muscularis mucosa,MM)癌或黏膜下层浅层(submucosal superficial layer,SM1)癌,是内镜治疗的相对指征;黏膜下层中层(submucosal middle layer,SM2)癌为内镜治疗禁忌证。提高早期食管癌的诊断率及早期预判早期食管癌浸润深度,准确评估早期食管癌的内镜治疗适应证,能够减少不必要的手术或放射治疗及化学药物治疗,也减少非治愈性内镜切除后的二次追加治疗。
日本食道学会(Japan Esophageal Society,JES)通过放大内镜窄带成像(narrow-band imaging magnifying endoscopy,NBI-ME)观察病灶组织部位上皮乳头内毛细血管袢(intrapapillary capillary loops,IPCL)提出JES分型以预测早期管道鳞癌的浸润深度[3]。本研究对本院消化内镜中心早期食管癌病例进行分析,旨在评价NBI-ME下JES分型预测肿瘤浸润深度的准确性。
1 对象与方法
1.1 研究对象
将2014年1月至2020年10月于首都医科大学附属北京友谊医院内镜中心就诊的疑似早期食管癌患者为研究对象。纳入标准:(1)白光内镜下高度疑似或病理活检证实为早期食管癌的病变;(2)术前完善放大内镜检查并由2名内镜医师评估JES分型,经内镜或外科手术切除病变;(3)2名病理医生判定内镜治疗标本的水平及垂直切缘是否干净、病理类型及病灶浸润深度。排除标准:(1)未成功切除病变者;(2)NBI-ME检查资料、术后病理资料或其他相关资料不全者。
本研究通过首都医科大学附属北京友谊医院机构审查委员会的伦理审查(编号:2020-P2-290-01),作为历史性研究可免除研究对象知情同意。
1.2 内镜检查
普通胃镜检查留取白光下疑似病变图像,详细记录病变或疑似病变组织位置、形态及大小等信息,并转换为NBI模式,对患者展开NBI-ME检查,并对其病灶组织部位上皮乳头内毛细血管袢血管区大小、形态等详细记录,留取图像。对于有切除指征的病变,取得患者及家属同意后,根据病变实际情况行内镜或外科手术治疗,术后标本送病理科交予病理医师判断。
1.3 放大内镜JES分型标准[3]
A型为IPCL变化很小甚至未改变,存在于正常黏膜内;B1型为IPCL呈现形状不一、粗细不同、迂曲、血管扩张等袢样血管,且出现异常形态,此时浸润深度达EP-LPM;B2型为未见成袢的IPCL,此时浸润深度为MM-SM1;B3型为IPCL发生明显扩张并呈不规则形态,其直径超过B2型血管至少2倍,此时浸润深度在SM2及以下(图1)。另外,对由B型血管组成的乏血管区域(avascular area,AVA)展开判断:小AVA直径≤0.5 mm;0.5 mm<中AVA直径<3 mm;大AVA直径≥3 mm(图2)。任何AVA包绕B1型血管预示肿瘤浸润深度至EP-LPM,中AVA包绕B2或B3型血管预示肿瘤浸润深度至MM-SM1;大AVA包绕B2或B3型血管预示肿瘤浸润深度至SM2及以下。由1名普通内镜医师和1名有经验的主任医师共同对食道病变进行JES分型评估,若存在分歧,请第3位有经验的放大内镜医师参与共同协商结果。
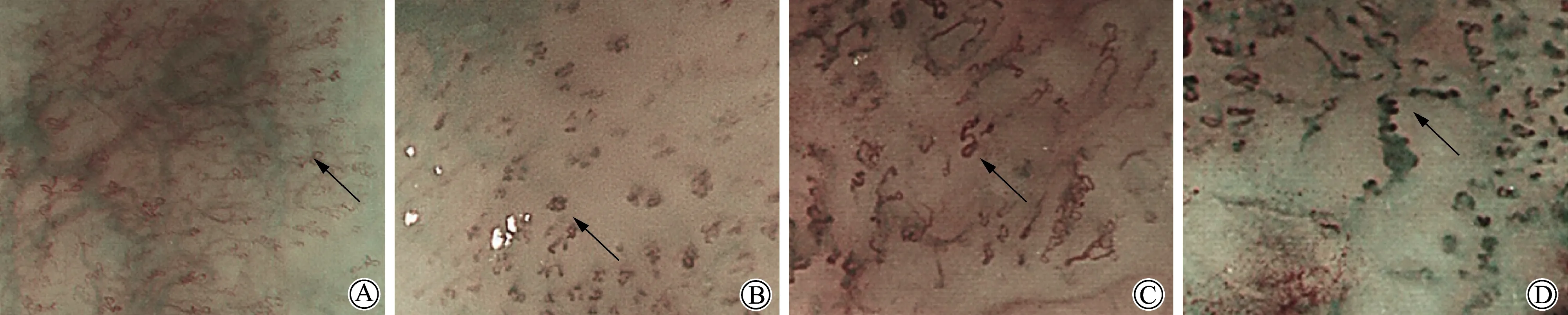
图1 JES分型血管在NBI-ME下表现
1.4 标本处理及病理分类、组织学评价标准
ESD/EMR切除标本经10%(质量分数)甲醛溶液固定,病变组织切片行苏木精-伊红(Hematoxylin-eosin,HE)染色及免疫组化染色。病理分类标准参照2014年中国消化内镜活组织检查与病理学检查规范专家共识[4],分为非早期食管癌病变、高级别上皮内瘤变(high-grade intraepithelial neoplasia, HGIN)、鳞状细胞癌(squamous cell carcinoma,SCC),本研究中将正常食道黏膜组织、炎性组织、中低级别上皮内瘤变定义为非早期食管癌性病变,高级别上皮内瘤变及鳞状细胞癌定义为癌性病变。由本院2名病理医师对术后病理进行检阅,若病理专家意见不一致,可经过商讨得出最终结论。以术后病理作为金标准,判断JES分型对早期食管癌浸润深度的诊断价值。
1.5 统计学方法
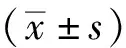
2 结果
2.1 早期食管癌的临床病理特征
共190例早期食管癌患者纳入本次研究,其中男性142例,女性48例,平均年龄(66.2±7.25)岁。共203处局灶性病变纳入研究,4处位于食管颈段,17处位于胸上段,胸中段和胸下段分别为75和107处。136处病变≤1/2食道环周,43处病变≤3/4食道环周,24处病变≥3/4食道环周。4处病灶行EMR治疗,4处病灶行多环黏膜套扎术(multi-band mucosectomy,MBM)治疗,194处病灶行ESD治疗,1处病灶行外科手术治疗。术后病理证实,25处病灶为非早期食管癌病变,109处病灶为高级别上皮内瘤变,69处病灶为鳞状细胞癌。178处癌性病变中,143处病灶浸润至黏膜内层及黏膜固有层,32处病灶浸润至黏膜肌层及黏膜下层浅层,3处病灶浸润至黏膜下层中层及以下,详见表1。

表1 早期食管癌的临床病理特征
2.2 早期食管癌的JES分型
203处局灶性病变JES分型结果显示,IPCL扩张A型病灶9处,B1型119处,B2型70处,B3型5处。联合AVA分型分析,1处早期食管癌由大AVA包绕B2型血管,调整预测浸润深度为SM2及以下;1处由小AVA包绕B3型血管,3处由中AVA包绕B3型血管,均调整浸润深度为MM-SM1(表2)。调整后的JES分型B2、B3型分别有73处、2处。
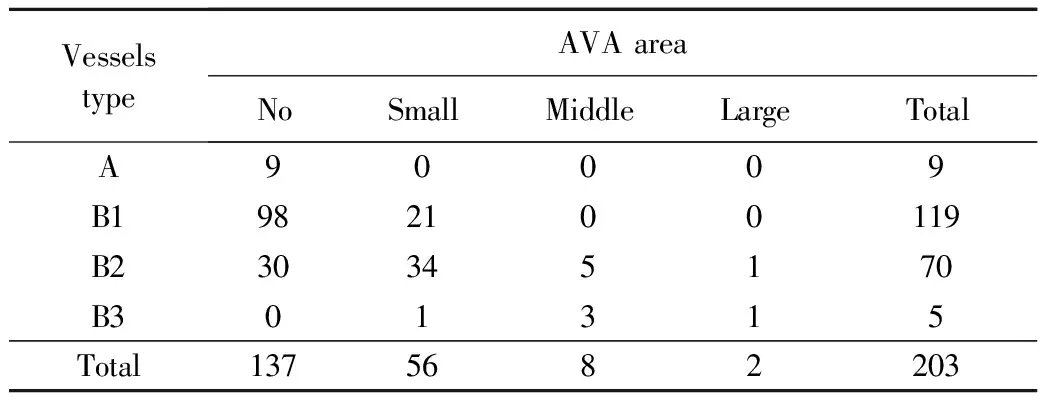
表2 早期食管癌的JES分型
2.3 放大内镜下JES分型对早期食管癌浸润深度的判断
以术后病理诊断为金标准,放大内镜JES分型正确判断5处病变为非早期食管癌(A型9处),94处病变浸润至EP及LPM(B1型119处),24处病变浸润至MM及SM1(B2型73处),2例B3型病变均为过度预测(表3)。NBI-ME下JES分型B1型、B2型判断早期食管癌准确度分别为63.5%(95%CI:63.3%~63.8%)和71.9%(95%CI:71.7%~72.1%),灵敏度分别为65.7%(95%CI:58.0%~73.5%)和75.0%(95%CI:60.0%~90.0%),特异度分别为58.3%(95%CI45.9%~70.8%)和71.3%(95%CI:64.6%~78.1%)。比较放大内镜JES分型及术后病理判断病变浸润至黏膜固有层及以上与黏膜肌层及以下的一致性,Kappa值为0.25,差异有统计学意义(P<0.01)。

表3 JES分型判断早期食管癌浸润深度的准确性
3 讨论
随着计算机和图像处理技术的不断进步,多种光学增强内镜技术应运而生,主要包括窄带成像技术、智能比色分光技术、高清智能电子染色及蓝激光成像四大类,均能清晰显示消化道黏膜细微结构[5]。放大内镜利用镜头变焦的原理,通过对消化道黏膜进行几十甚至上百倍的放大,从而能观察消化道黏膜细微变化,如表面微观结构、浅表毛细血管网等。NBI技术的基本原理是基于消化道黏膜对光的吸收和反射,将窄带滤波器置于传统疝灯光源及红、绿、蓝旋转滤光片之间,过滤掉宽带红光,仅保留(415±30)nm、(540±30)nm范围内的窄带蓝绿光作为照明光。由于光波对消化道黏膜的穿透能力与其波长成正比,光波波长越长,穿透深度越深,因此以415 nm为中心的蓝光可穿透黏膜浅层至0.16 mm深度,且恰好对应血红蛋白的主吸收峰谱,可突出显示黏膜表面腺体及微血管结构,而以540 nm为中心的绿光穿透较深,深度可达0.24 mm,可见黏膜深层和黏膜下层的血管结构,故黏膜表面腺体、绒毛等结构及浅层毛细血管以吸收415 nm蓝光为重点,镜下呈褐色,而较深的黏膜下血管在540 nm绿光下可见,镜下呈青色,不需要使用化学染色剂即可清晰地显示黏膜表面腺体结构及微血管形态,极大地提高了黏膜表面对比度,利于黏膜细节的可视化[6-7]。日本食道学会利用放大内镜联合窄带成像对食道上皮乳头内毛细血管袢进行分析,制定出JES分型以诊断早期食管癌并以此评估肿瘤浸润深度[3]。
本研究共纳入203处病变,收集NBI-ME下IPCL形态迂曲、延长、形态不规则、增粗等,以术后病理结果为金标准,参照JES分型进行分类,B1型准确度为63.4%,灵敏度为65.7%,特异度为58.3%。这是首个基于国内内镜中心数据讨论早期食管癌JES分型诊断意义的研究,既往研究多源于日本。Oyama等[3]报道JES分型B1、B2型血管的灵敏度和特异度分别为97.5%/72.9%及75.0%/96.2%。Katada等[8]报道JES分型B1型血管的诊断准确度为91%,特异度为87%,未提及B2型血管诊断准确度及特异度。本研究较前两项研究[3,8]加入了ESD术后病理证实非早期食管癌的病变(18处),因此降低了B1型对于早期食管癌病变浸润至EP/LPM的诊断准确度和特异度。本研究早期食管癌病变中共有101处B1型病变,其中有94处(93.1%)浸润至EP/LPM,因此B1型血管联合AVA能够有效预测浸润至EP/LPM的早期食管癌病变。
本研究中B2型有73处病变,其中24处病变浸润至MM及SM1,45处浸润至EP及LPM,B2型诊断准确度为71.9%,灵敏度为75.0%,特异度为71.3%。B2型对早期食管癌浸润至MM/SM1的判断有待商榷。Tanaka等[9]报道了关于B2亚型的研究,78处B2型病变中,47处浸润至EP/LPM,26处浸润至MM/SM1,5处浸润至SM2,通过ROC曲线将EP/LPM与MM或更深的浸润深度分开来,Cut-off值显示B2型血管区域的最佳截断值为4 mm,当B2型血管区域大于4 mm时,病变被认为浸润至MM及以下。而食管的炎症性病变在内镜下也可表现为非袢样血管,常被归于B2型。这些可能是导致B2型对病变浸润过高预测的原因。近年,日本食道学会又相继提出从三方面修正JES分型下的B2型以提高诊断准确度:(1)进行B2型血管亚型分类;(2)B2型血管结合肿瘤面积评估;(3)结合B2型血管区域面积[9-11]。本研究中比较放大内镜JES分型及术后病理判断病变浸润至黏膜固有层及以上与黏膜肌层及以下的一致性,Kappa值为0.25。目前尚无研究报道JES分型的所有类型病变整体与早期食管鳞癌病理浸润深度的Kappa一致性检验结果。另外,JES分型中提到结合B型血管和乏血管区域进行判断,而AVA只在一部分早期食管癌患者有表现,对于JES分型的修正作用有限。因此,需要高质量的大样本多中心实验去修正JES分型血管分类。
本研究存在以下不足:首先,JES分型中的A型病变被认为是大致正常的食道上皮乳头内毛细血管袢,但该研究中纳入的A型病灶多为经病理活检证实为食道高级别上皮内瘤变的病灶,导致存在明显的选择差异,因此本研究没有探讨A型病灶的诊断价值。另外,因为本研究中通过B型血管联合AVA区域纳入的B3(SM2及以上)仅有2例,故本研究也未探讨B3型诊断的准确性。这2例行内镜治疗后分别为侧切缘、基地切缘阳性,再次行外科手术治疗。最后,本研究为单中心历史性研究,收集的资料有限,尚需多中心、大样本的随机对照试验进一步验证。
综上,本研究收集了近203处高度疑似早期食管癌的病灶,通过对术前JES分型及术后病理评价,证实了JES分型诊断早期食管癌浸润深度的有效性及实用性,国内目前无类似研究报道,仍需多中心、大样本的随机对照试验进一步研究,寻找基于中国人早期食管癌特征的有效分型。
