磺酰基桥联杯[4]芳烃多孔配位笼对海水中U(Ⅵ)的快速吸附
2022-06-23陈梦伟谢祖姬张若倩刘胤江
陈梦伟,刘 涛,汤 帅,谢祖姬,张若倩,刘胤江,王 宁
海南大学 南海海洋资源利用国家重点实验室,海南 海口 570228
核能的开发和利用对于缓解能源危机及解决环境污染等问题都具有非常深远的意义[1]。铀作为核能开发的核心战略资源,主要通过矿石开采得到。然而,陆地矿石中铀的储量有限,随着能源需求的增加,势必会引起资源短缺的问题[2]。海水中铀的总量约为45亿吨,是陆地上铀储量的1 000倍[3-4]。因此,对海洋中铀资源的提取和开发吸引了越来越多研究者的关注。目前,对铀酰离子提取方法的研究中,吸附法由于操作简单、成本低、易大规模生产而被广泛应用[5]。
杯芳烃是由苯酚单元和相同数目的桥联原子连接而成的一类“碗状”大环化合物[6]。由于其具有空腔大小可调和上下沿易于功能化修饰等优点,被应用于分子识别、膜传输、金属离子的回收与利用等方面[7]。近年来,不少杯芳烃衍生物被报道用于溶液中铀的吸附[8-9]。然而,这些杯芳烃衍生物较小的比表面积,在溶液中易团聚等缺点限制了其对铀酰离子的进一步吸附。多孔配位笼具有较大的比表面积和丰富的孔隙结构[10],因此设计合成杯芳烃基多孔配位笼不仅能够解决杯芳烃衍生物的团聚问题还能改善其吸附性能。
本工作拟利用对叔丁基磺酰基桥联杯[4]芳烃(H4TC4A-SO2)、六水氯化钴和1,3-二(2H-四氮唑-5-基)苯(H2L)构筑一例长方体状的多孔配位笼(Co16),利用晶体学、红外光谱(FTIR)、X射线衍射(XRD)和扫描电子显微镜(SEM)等技术对该材料的理化性质进行表征,并通过批量实验研究该材料在海水中的铀吸附能力及不同因素(pH值、温度)对材料吸附性能的影响,进一步对Co16吸附剂在真实海水中的铀吸附性能进行测试。
1 实验部分
1.1 材料和仪器
对叔丁基磺酰基桥联杯[4]芳烃(H4TC4A-SO2)和1,3-二(2H-四氮唑-5-基)苯(H2L)分别根据文献[11-12]方法合成。其它所用试剂均为市售分析纯,其中六水氯化钴(CoCl2·6H2O)购于麦克林,硝酸铀酰(UO2(NO3)2·6H2O)和偶氮胂(Ⅲ)购买自国药集团。模拟海水根据橡树岭国家实验室报告[13]配制,1 L的模拟海水中包含193 mg碳酸氢钠和25 600 mg氯化钠。
亚津CL-J120电子天平,精度0.000 1 g,赛多利斯科学仪器(北京)有限公司;场发射扫描电子显微镜、电感耦合等离子体-原子发射光谱仪(ICP-OES)、电感耦合等离子体-质谱仪(ICP-MS),赛默飞世尔科技有限公司;Bruker D8 QUEST X射线单晶衍射仪、X射线粉末衍射仪(XRD)、傅里叶红外光谱仪,德国Bruker公司;ASAP 2460全自动比表面积及孔隙度分析仪,美国麦克;X射线光电子能谱仪,岛津KRATOS;紫外分光光度计,上海精密仪器有限公司。
1.2 Co16吸附剂的制备
称取H4TC4A-SO2(0.072 0 g,0.10 mmol)、CoCl2·6H2O(0.100 0 g,0.40 mmol)、1,3-二(2H-四氮唑-5-基)苯(H2L)(0.021 4 g,0.01 mmol)于20 mL的聚四氟乙烯内衬的不锈钢反应釜中,然后加入5 mL的乙醇(CH3CH2OH)和5 mL的N,N-二甲基甲酰胺(DMF),在鼓风干燥箱中先升温至140 ℃并恒温3 d,然后以4 ℃/h降温至室温,得到深红色块状晶体。晶体经过滤洗涤后,于真空干燥箱中干燥,最后获得Co16吸附剂。产率为70%。
1.3 吸附实验
1.3.1吸附动力学测试 称取5 mg的Co16吸附剂依次放入2、4、8、16 mg/L 1 L的铀加标模拟海水中,并调节溶液的pH≈7,室温下(298 K)进行吸附,平行做三组实验。在转速为120 r/min的摇床中进行振荡,每间隔一段时间,取一定量的溶液,用偶氮胂(Ⅲ)法测试溶液中的铀浓度,计算Co16吸附剂的铀吸附容量。吸附剂的铀吸附量(qt)用式(1)计算。
(1)
其中:ρ0和ρt分别为溶液中U(Ⅵ)的初始和t时刻的质量浓度,mg/L;V代表溶液的总体积,L;m为吸附剂的质量,g。当吸附达到平衡状态时,ρt即为ρe。
1.3.2其它吸附实验 除非特殊说明,批量实验所用模拟海水的体积为1 L,吸附剂的质量为5 mg。在不同初始质量浓度(2、4、8、16、32、64、128 mg/L)的铀加标模拟海水中进行吸附等温线实验。在8 mg/L的铀加标模拟海水中用盐酸和氢氧化钠分别调节溶液的pH值为3~9,研究溶液pH值对材料吸附铀性能的影响。为了研究Co16的吸附热力学行为,把8 mg/L的铀加标模拟海水置于不同温度(293、298、303、308、313 K)的摇床内进行吸附测试。
2 结果与讨论
2.1 Co16吸附剂结构描述及表征
如图1(a)所示,对叔丁基磺酰基桥联杯[4]芳烃结构下缘的酚羟基氧和桥联磺酰基氧与四个钴离子结合形成羽毛球状结构的Co4-TC4A-SO2次级结构单元,次级结构单元的底部则被一个来自水分子的μ4-O封装。进一步的,Co4-TC4A-SO2次级结构单元与1,3-二(2H-四氮唑-5-基)苯(H2L)(图1(b))连接形成Co16长方体配位笼。
Co16配位笼由四个Co4-TC4A-SO2次级结构单元和八个桥联配体构筑而成(图1(c))。配位笼中的每个钴离子通过与来自H2L的两个氮原子、磺酰基桥联杯[4]芳烃的三个氧原子和一个μ4-O配位,形成了六配位扭曲八面体结构。沿b轴方向对Co16进行堆积,可以发现堆积图中呈现出大量的方形孔穴(图1(d))。
通过X射线粉末衍射(PXRD)分析(图1(e))可知,Co16的粉末衍射数据与拟合数据高度吻合,表明了Co16配合物为纯相。对Co16吸附剂的N2吸附脱附等温线(图1(f))分析得到Co16吸附剂的比表面积为471.07 m2/g。
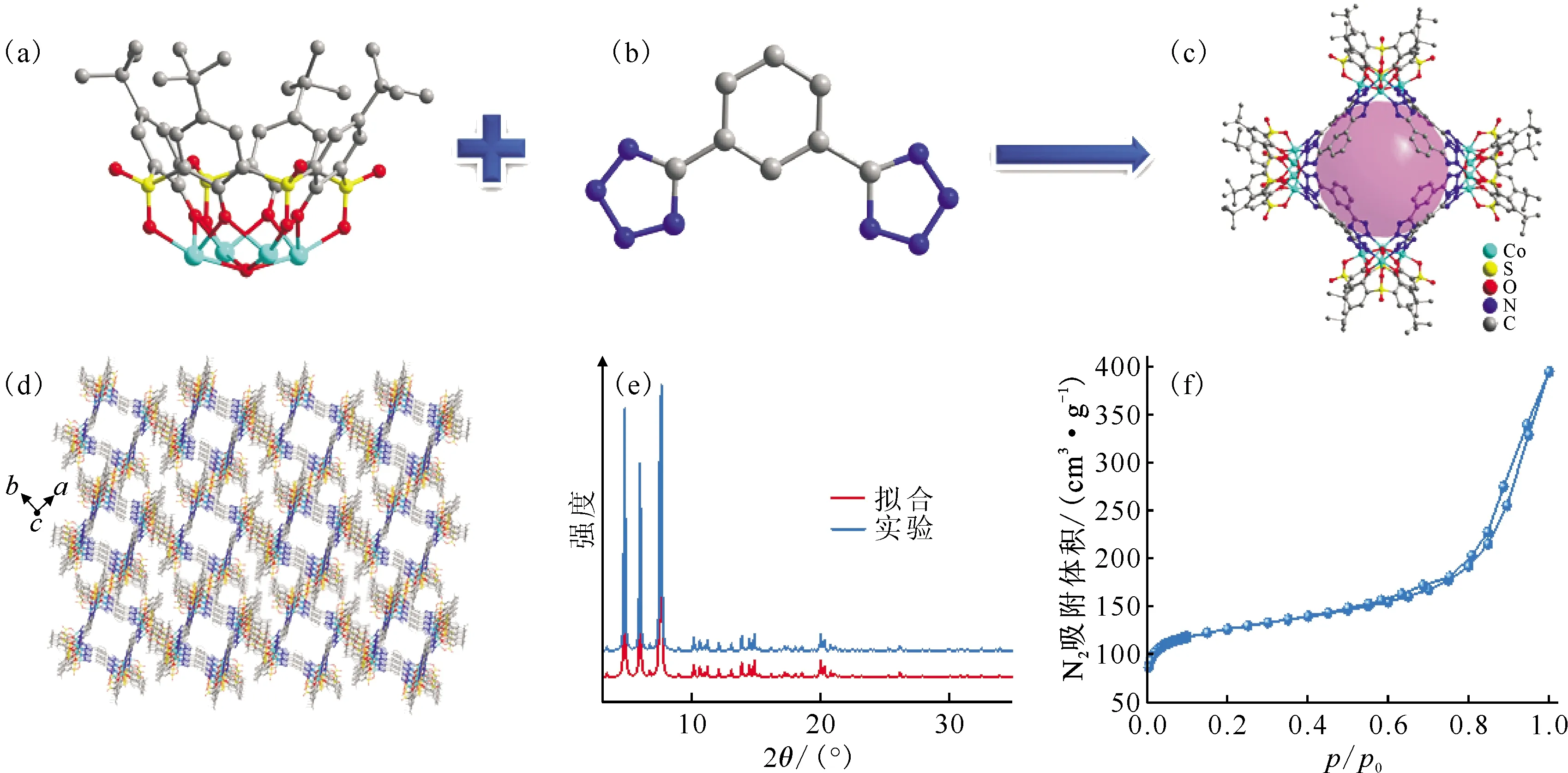
(a)——Co4-TC4A-SO2次级结构单元,(b)——1,3-二(2H-四氮唑-5-基)苯(H2L)分子式,(c)——Co16晶体结构,(d)——Co16晶体结构堆积图,(e)——Co16的X射线粉末衍射,(f)——Co16的N2吸附脱附等温线图1 Co16配位笼合成示意图Fig.1 Illustration of assembly of Co16 coordination cage


(a)、(b)分图中的照片分别为吸附铀前后的晶体粉末图2 Co16在吸附铀前(a)、后(b)的扫描电镜图,Co16吸附铀前后的红外光谱图(c)及X射线光电子能谱图(d)Fig.2 SEM images of Co16 adsorbents before(a) and after(b) uranium sorption, FTIR spectra(c) and XPS spectra(d) of Co16 adsorbents before and after uranium extraction
的两个新峰[16](图2(d))。以上结果均表明,Co16吸附剂成功吸附了铀酰离子。
2.2 吸附动力学和吸附等温线
将5 mg的Co16吸附剂分别放入不同质量浓度(2、4、8、16 mg/L)的铀加标模拟海水中进行吸附测试,结果示于图3(a)。由图3(a)可知:Co16吸附剂能够在90 min内达到吸附平衡,说明该材料具有较快的吸附动力学。此外,Co16在不同铀浓度下(2、4、8、16 mg/L)的平衡吸附容量分别为164.17、205.62、273.51、383.42 mg/g,说明Co16对U(Ⅵ)具有较好的吸附能力。为了更好地研究该材料的动力学吸附行为,对上述数据分别进行了准二级动力学(式(2))和准一级动力学拟合(式(3))[17]。
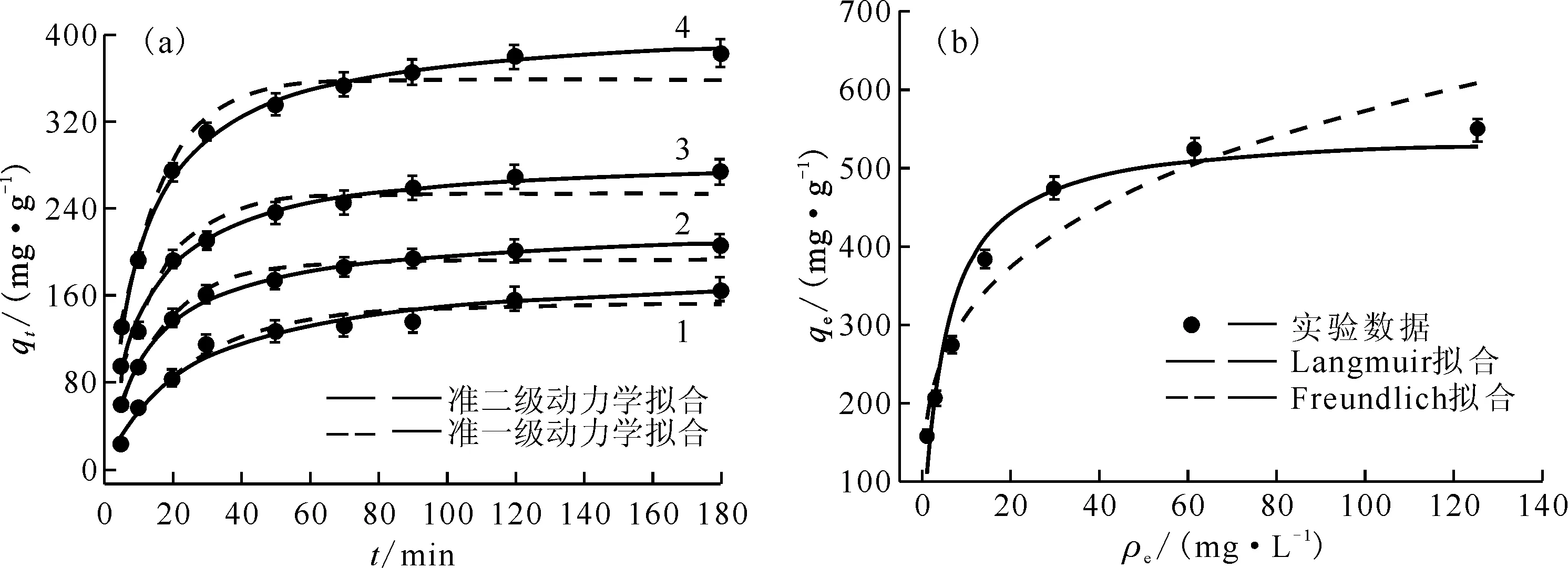
pH=7, 298 K, m=5 mg(a):ρ0,mg/L:1——2,2——4,3——8,4——16;(b): t=180 min图3 Co16在不同铀浓度下的吸附及准一级动力学、准二级动力学拟合(a),Co16的吸附等温线以及Langmuir模型和Freundlich模型拟合(b)Fig.3 Adsorption kinetics data and corresponding fitting curves based on pseudo-first-order and pseudo-second-order kinetic model(a), equilibrium adsorption isotherms of Co16 adsorbents and corresponding fitting curves with Langmuir model and Freundlich model, respectively(b)
(2)
ln(qe-qt)=lnqe-k1t
(3)
式中:qt和qe分别为t时刻和平衡时的吸附容量,mg/g;k2为准二级动力学速率常数,g/(mg·min);k1为准一级动力学速率常数,min-1。由图3(a)可知,拟合后的数据更符合准二级动力学模型,相应的动力学参数列入表1。由表1可知,准二级动力学模型的相关系数高于准一级动力学模型的,说明Co16吸附剂对U(Ⅵ)的吸附属于化学吸附过程[18-19]。

表1 Co16吸附剂对U(Ⅵ)吸附的动力学模型参数Table 1 Fitting parameters for adsorption kinetic of Co16 adsorbents for U(Ⅵ)
此外,还研究了Co16吸附剂对U(Ⅵ)的吸附等温行为,结果示于图3(b)。分别用Langmuir(式(4))和Freundlich(式(5))吸附模型对吸附等温数据进行拟合[20]。
(4)
(5)
式中:ρe,吸附平衡时U的质量浓度,mg/L;qm,饱和吸附容量,mg/g;k3,Langmuir模型的平衡吸附常数,L/mg;k4,Freundlich模型常数,mg/g;1/n,吸附强度相关常数。对U(Ⅵ)的吸附数据进行拟合后常数列于表2。由图3(b)和表2可以看出Co16吸附剂对U(Ⅵ)的饱和吸附容量高达547.31 mg/g,更符合Langmuir吸附等温线模型,因此Co16吸附剂对U(Ⅵ)的吸附属于典型的单层吸附过程[21-22]。

表2 Co16吸附剂对U(Ⅵ)的Langmuir和Freundlich等温拟合参数Table 2 Fitting parameters of Langmuir and Freundlich isotherm model for U(Ⅵ) adsorption on Co16
2.3 pH值对U(Ⅵ) 吸附性能的影响


ρ0=8 mg/L, 298 K, t=180 min, m=5 mg图4 不同pH下Co16吸附剂在模拟海水中的吸附Fig.4 Dependence of uranium adsorption capacityof Co16 adsorbents on pH of simulated seawater
2.4 吸附热力学研究
对吸附热力学的研究有助于进一步地探索吸附过程中的能量变化。因此,研究了Co16吸附剂在不同温度下的热力学吸附行为。Co16吸附剂在不同温度下的U(Ⅵ)吸附容量及lnKd对1/T的线性关系示于图5。由图5(a)可知,随着温度的升高,Co16吸附剂对U(Ⅵ)的吸附表现出较强的温度正响应。为了进一步研究吸附剂对铀酰离子吸附的热力学机制,相关热力学参数包括吉布斯自由能变化(ΔG,kJ/mol)、焓变(ΔH,kJ/mol)和熵变(ΔS,J/(mol·K))可由式(6)—(8)计算得出[24]。
(6)
(7)
ΔG=ΔH-TΔS
(8)
式中:Kd,反应达到平衡时铀在两相的吸附分配系数,mL/g;R,理想气体常数,8.314 J/(mol·K);T,液相温度,K。根据图5(b),计算得出ΔH和ΔS,相关的热力学参数列于表3。吉布斯自由能变化(ΔG)为负值,说明Co16吸附剂对U(Ⅵ)的吸附为自发过程。焓变(ΔH)为正值表示吸附过程为吸热,同时ΔH大于20.9 kJ/mol,进一步说明Co16吸附剂对U(Ⅵ)的吸附主要为化学吸附。熵变(ΔS)为正值反映了Co16吸附剂对铀酰离子具有较好的亲和力[25]。综上,Co16对U(Ⅵ)的吸附属于自发吸热过程。

m=5 mg, ρ0=8 mg/L, pH=7(a):T,K:1——293,2——298,3——303,4——308,5——313图5 Co16吸附剂在不同温度下的U(Ⅵ)吸附容量(a)及ln Kd对1/T的线性关系(b)Fig.5 U(Ⅵ) adsorption capacity of Co16 adsorbents under different temperatures(a) and linear plots of ln Kd of U(Ⅵ) versus 1/T(b)

表3 Co16吸附剂对U(Ⅵ)吸附的热力学参数Table 3 Calculated thermodynamic parameters for U(Ⅵ) adsorption of Co16 adsorbents
2.5 Co16吸附剂的循环使用性能
循环使用性能对评估材料在真实环境中的应用非常重要,因此,研究了Co16吸附剂的可重复使用性。吸附剂每次吸附后,将再循环吸附剂浸入0.08 mol/L的盐酸中振荡6 h,然后用去离子水反复冲洗,并在80 ℃真空干燥箱中干燥以此实现吸附剂的再生。Co16吸附剂对U(Ⅵ)的循环吸附-解吸结果示于图6。由图6可知:经过4次的吸附-解吸实验后,Co16吸附剂对U(Ⅵ)的吸附容量仍高达219.28 mg/g,相比于初始吸附容量只降低了17.8%,且洗脱率仍高达78.3%,以上实验结果表明Co16吸附剂具有良好的可重复使用性。

——吸附容量,□——洗脱率ρ0=8 mg/L, pH=7, 298 K, t=180 min, m=5 mg图6 Co16吸附剂的循环使用性能Fig.6 Cycling performance of Co16 adsorbents
2.6 Co16吸附剂在真实海水中的性能
利用单通道过流实验装置对吸附剂在真实海水中的吸附性能进行了测试。分别取20 mg样品放入透析袋中,并置入装有100 L过滤真实海水的单通道中进行铀吸附测试[26],结果示于图7(a)。由图7(a)可知:经过20 d的吸附测试后,Co16对U(Ⅵ)的吸附容量可达4.88 mg/g,超过了多数多孔框架材料在真实海水中的铀吸附性能(表4)。为了评估真实海水中存在的其它竞争离子对Co16吸附剂吸附铀性能的影响,对吸附剂吸附其它竞争离子进行测试,结果示于图7(b)。由图7(b)可知:Co16吸附剂对U(Ⅵ)的吸附容量远高于其它干扰离子,说明Co16吸附剂对铀酰离子具有较好的离子选择性。以上结果表明,Co16吸附剂对于真实海水中的铀吸附具有很大的应用潜力。

表4 不同多孔框架材料对真实海水中U(Ⅵ)的吸附性能对比Table 4 Comparison of adsorption capacity of different porous frame materials in real seawater for U(Ⅵ)
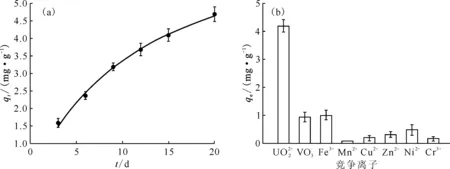
ρ0≈3.3 μg/L, pH≈8.3, 298 K; (b):t=25 d图7 Co16吸附剂在真实海水中的U(Ⅵ)吸附曲线(a)及与竞争离子的吸附图(b)Fig.7 U(Ⅵ) adsorption curve(a) and binding selectivity of competing ions(b) for Co16 adsorbents in real seawater
3 结 论
利用溶剂热法合成了一例新的杯芳烃基金属有机多孔配位笼(Co16),并用于真实海水中的铀吸附,结果表明:
(1) Co16吸附剂具有快速及较高的U(Ⅵ)吸附能力;
(2) Co16吸附剂对U(Ⅵ)的吸附受pH值的影响且具有较好的可重复使用性,经过4次吸附-解吸实验后,对U(Ⅵ)的吸附容量仍高达219.28 mg/g;
(3) Co16吸附剂对U(Ⅵ)的吸附随温度升高而增强,是一个自发吸热的过程;
(4) Co16吸附剂在真实海水中仍具有很好的铀吸附能力和较高的离子选择性。
综上,Co16吸附剂在海水铀吸附方面具有非常好的应用前景。
