铬酸钡液相氧化2-甲基萘制备2-甲基-1,4-萘醌的工艺研究
2022-06-22曾奎姜启彬封承飞全学军邱发成
曾奎,姜启彬,封承飞,全学军,邱发成
(重庆理工大学 化学化工学院,重庆 400045)
2-甲基-1,4-萘醌(2-MNQ)是一种重要的中间体,在医学、饲料等方面有着广泛的用途[1-4]。随着医药业、养殖业的快速发展,对VK类化合物的需求急剧增加[5-8]。因此,2-MNQ合成技术研究具有十分重要的现实意义。
当前,制备2-MNQ的方法有气相氧化法[9]、间接电氧化工艺[10-11]和液相氧化法[12]方法。其中液相氧化法以原料易得,工序简单,是当前制备2-MNQ的主要工艺。当前的研究极大的促进了合成2-MNQ 的工业化,但依然存在产率低、条件苛刻、环境污染严重等问题。因此,如何在当前液相氧化工艺上进一步提高产品收率以及处理好废液问题将是2-MNQ绿色制备工艺的关键。
本工艺以2-MN、 铬酸钡为原料,以盐酸和水为反应介质,采用液相氧化工艺,对2-MN溶液采取超声预处理,使其能与铬酸钡溶液充分混合,进而提高2-MNQ的收率。并对含铬废液进行回收处理。工艺流程见图1。本文研究了铬酸钡液相氧化2-MN的各项工艺参数。
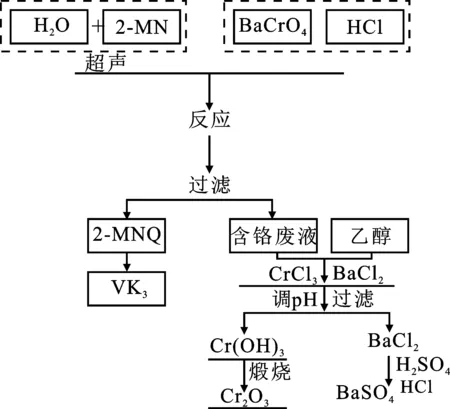
图1 工艺流程Fig.1 Process flow
1 实验部分
1.1 材料与仪器
2-甲基萘,含量 92.6%(上海阿拉丁试剂有限公司);盐酸(质量分数约为37%)、铬酸钡均为化学纯。
SPD-20A型高效液相色谱仪(Akzonobel Cl8150rnIn×4.6 mm(id)色谱柱);XRD-7000 X射线衍射仪;FTIR-650傅里叶红外吸收光谱仪。
1.2 实验方法
1.2.1 实验原理 在酸性条件下,铬酸钡溶解为重铬酸钡,重铬酸钡的重铬酸根离子具有较强的氧化性[13],能将2-MN氧化为2-MNQ,自身则被还原为三价铬离子。
制备中间体2-MNQ发生的主要反应如下式:


2-MNQ+CrCl3+BaCl2+4H2O
1.2.2 实验步骤 将一定量的铬酸钡溶于浓盐酸中,配成重铬酸钡溶液。将2-MN和水加入到三颈烧瓶中,置于超声反应槽中超声一定时间,使2-MN与水充分混合均匀,待超声完毕将三颈烧瓶转移到恒温水浴锅中,升温至一定温度,缓慢滴加重铬酸钡溶液,滴加完毕后反应一定时间。反应结束后取少量反应液进行高效液相色谱分析(HPLC)。余液用冰水冷却后,可得大量沉淀生成,过滤,经乙醇重结晶,最后真空干燥。
1.3 分析方法
用液相色谱法对所得产品中的2-MNQ进行定量分析[14]。Akzonobel Cl8150rnm×4.6 mm(id)色谱柱;流动相为V(乙腈 )∶V(水)=6∶4;流速为1.0 mL/min;柱温为室温;检测波长265 nm;进样量为20 μL。产品溶解于乙腈中用液相色谱仪进行分析,通过HPLC面积归一化法计算产品的收率。产品采用红外光谱进行定性分析。
2 结果与讨论
2.1 超声时间的影响
为考察超声预处理对铬酸钡液相氧化2-MN制备2-MNQ的影响,将超声预处理后的2-MN溶液在反应温度70 ℃,盐酸用量为理论用量1倍,nBaCrO4∶n2-MN为2,液固比为4 mL/g条件下反应3 h。超声预处理时间对产品收率的影响见图2。

图2 超声时间对2-MNQ收率的影响Fig.2 The effect of ultrasonication time on the yield of 2-MNQ
由图2可知,超声预处理时间从0增加到20 min,2-MNQ的收率从10.23%急剧增加到45.90%。进一步增加超声预处理时间,2-MNQ的收率维持在稳定水平。最重要的是没有经过超声预处理的2-MNQ收率仅仅有10%左右,当超声5 min后收率可快速提高到25%左右,收率在短时间超声后便可快速提升。在反应前对2-MN溶液进行超声预处理,由于超声波的空化和活化效应[15-16],极大促进了2-MN在水中的溶解度,使其两相混合更加均匀,在后续的氧化反应提供更多的接触位点,有利于2-MN氧化为2-MNQ,从而提高了收率。然而当超声时间增加到20 min时,2-MN在水中的溶解度达到最大,此时进一步增加超声时间,不能使其收率进一步增加,且造成能源的浪费因此超声预处理的时间20 min为最佳的时间。
2.2 反应时间的影响
为考察反应时间对铬酸钡液相氧化2-MN制备2-MNQ的影响,将超声预处理20 min的2-MN溶液在反应温度70 ℃,盐酸理论用量1倍,nBaCrO4∶n2-MN为2,液固比为4 mL/g的条件下反应一定时间。反应时间对产品收率的影响见图3。
由图3可知,当反应时间从1.5 h增加到3.5 h,2-MN的收率从26.54%上升到46.8%,上升趋势明显,同时可以知道反应时间从1.5 h到3.5 h的过程中2-MN的收率有着明显的上升趋势。当反应时间超过3.5 h,2-MNQ的收率有一定的下降。这是因为反应时间过长,随着反应的进行,虽然原料2-MN的消耗量有所增加,但存在部分产品被过度氧化为2-MNQ的异构体,副产物增加,从而导致2-MNQ的收率降低。所以最佳反应时间为3.5 h。

图3 反应时间对2-MNQ收率的影响Fig.3 The effect of reaction time on the yield of 2-MNQ
2.3 盐酸用量的影响
为考察盐酸用量对铬酸钡液相氧化2-MN制备2-MNQ的影响,将超声预处理20 min的2-MN溶液在反应温度70 ℃、nBaCrO4∶n2-MN为2、液固比为4 mL/g的条件下反应3.5 h。盐酸用量对产品收率的影响见图4。
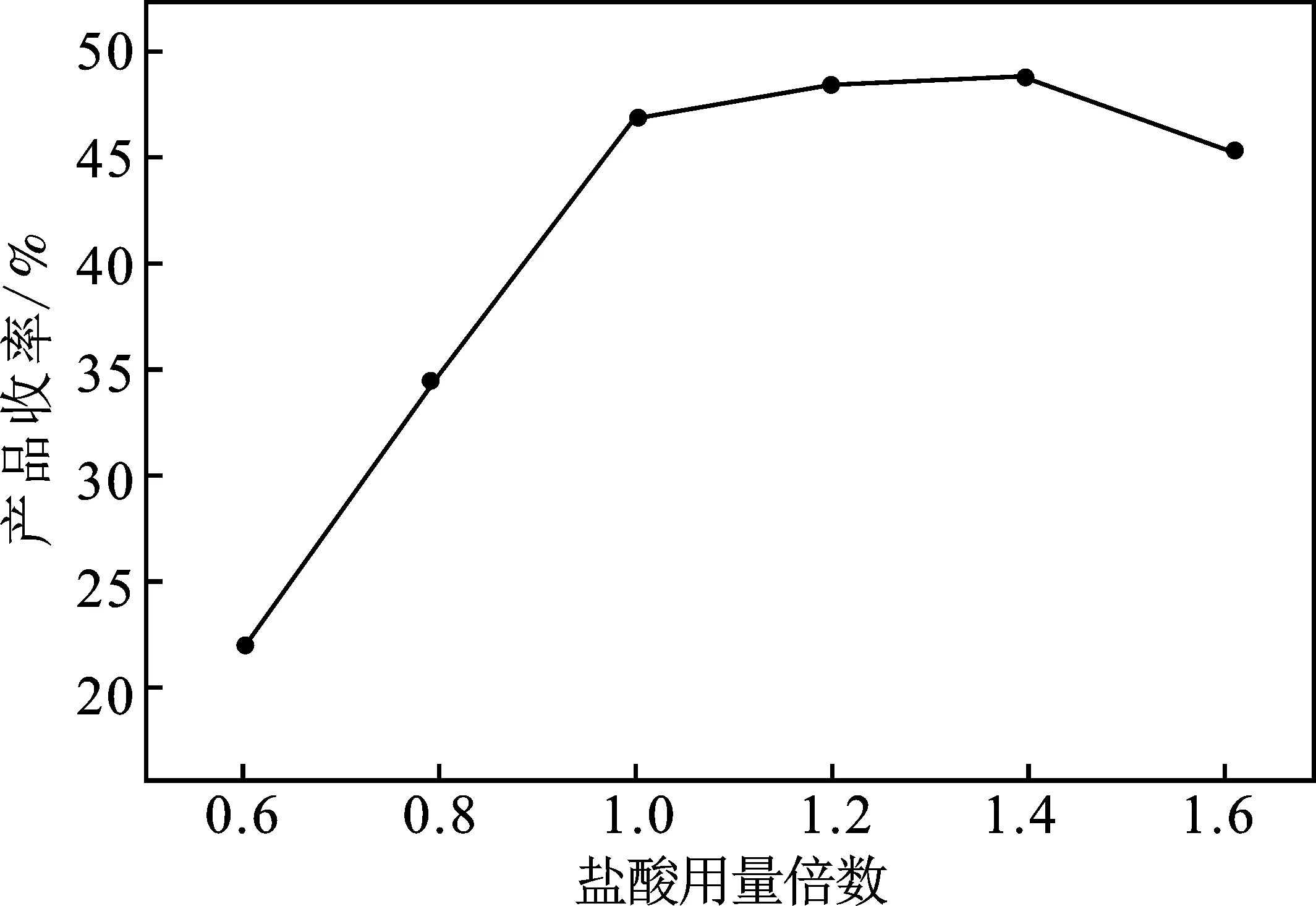
图4 盐酸用量对2-MNQ的影响Fig.4 The effect of hydrochloric acid dosage on 2-MNQ
由图4可知,盐酸用量从理论用量的0.6倍到1.2倍,2-MNQ的收率从22.56%增加到48.57%,进一步增加酸的用量到1.4倍,2-MNQ的收率几乎维持稳定,当进一步提升酸的用量到1.6倍2-MNQ的收率有着明显的下降趋势,收率下降到45.43%。适当增加酸的用量有利于铬酸钡的溶解,提升了重铬酸根的含量,在酸性环境中,六价铬的重铬酸根离子能将芳烃氧化为相应的醌类,也能将芳烃化合物的侧链氧化为羧基。溶液的酸性越强,六价铬的重铬酸根离子的浓度越高,氧化能力就越强,2-MN 被深度氧化的可能性就越大,收率降低,反之,六价铬的重铬酸根离子的浓度越低,氧化能力就越弱,也不能达到理想收率。因此存在着一个最佳的酸性条件,通过比较,盐酸的最佳用量为理论用量的1.2倍为最佳条件。
2.4 氧化剂用量的影响
为考察氧化剂用量对铬酸钡液相氧化2-MN制备2-MNQ的影响,将超声预处理20 min的2-MN溶液,在反应温度70 ℃、盐酸用量为理论用量的1.2倍、液固比为4 mL/g的条件下反应3.5 h。氧化剂用量对产品收率的影响见图5。
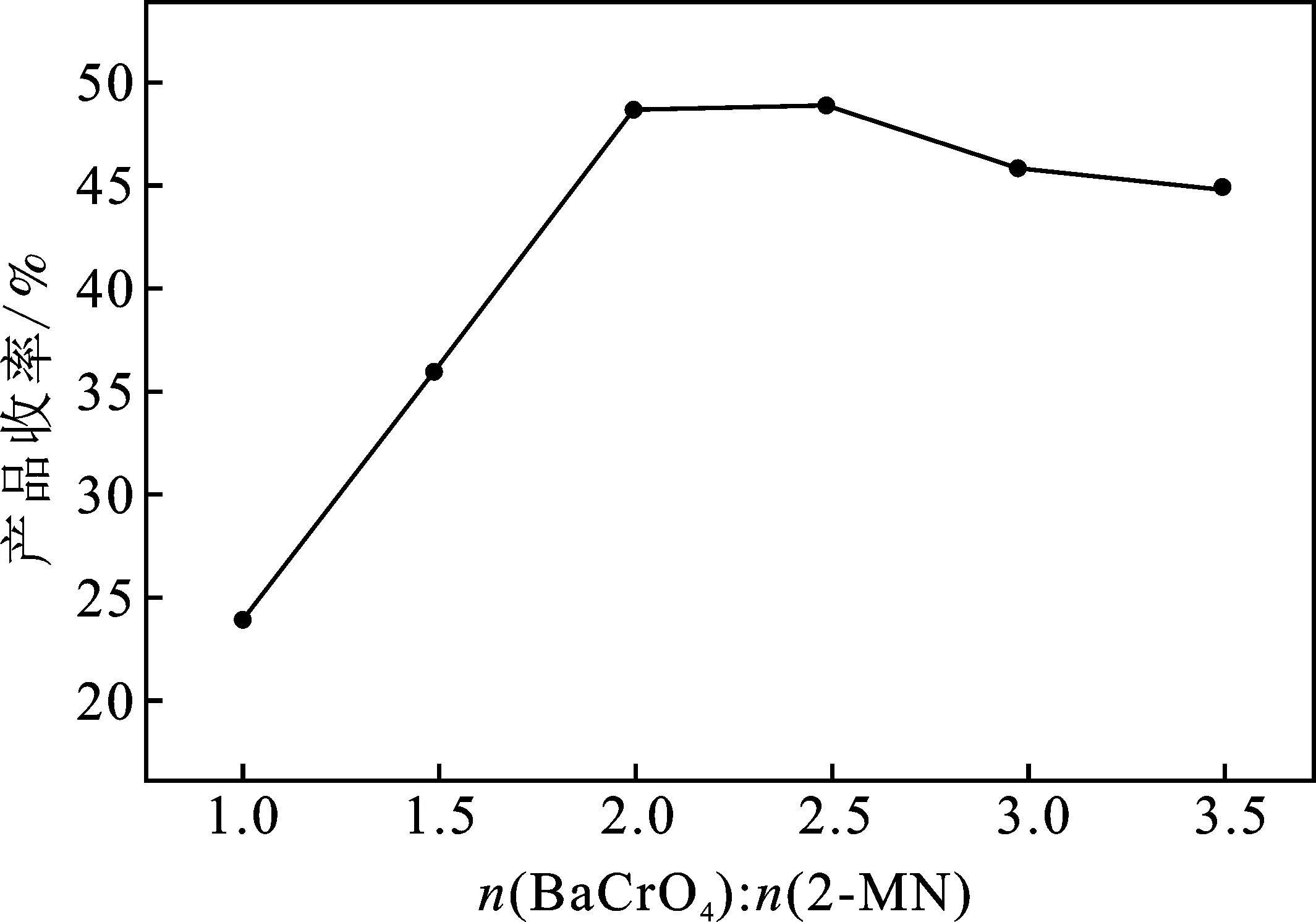
图5 氧化剂用量对2-MNQ收率的影响Fig.5 The influence of oxidant dosage on the yield of 2-MNQ
由图5可知,当n(BaCrO4)∶n(2-MN)从1.0增加到2.0,2-MNQ的收率从24%增加到48.57%。进一步增加到n(BaCrO4)∶n(2-MN)为2.5,2-MNQ的收率涨幅较小,再进一步增加到3.5时2-MNQ的收率下降到44.87%,原因可能是过量的铬酸钡导致对2-MNQ的过度氧化,从而2-MNQ的收率降低。氧化剂铬酸钡的最佳用量为理论用量的2.0倍。
2.5 液固比的影响
为考察液固比对铬酸钡液相氧化2-MN制备2-MNQ的影响,将超声预处理20 min的2-MN溶液,在反应温度70 ℃、盐酸用量为理论用量1.2倍、n(BaCrO4)∶n(2-MN)为2.0条件下反应3.5 h。液固比对产品收率的影响见图6。
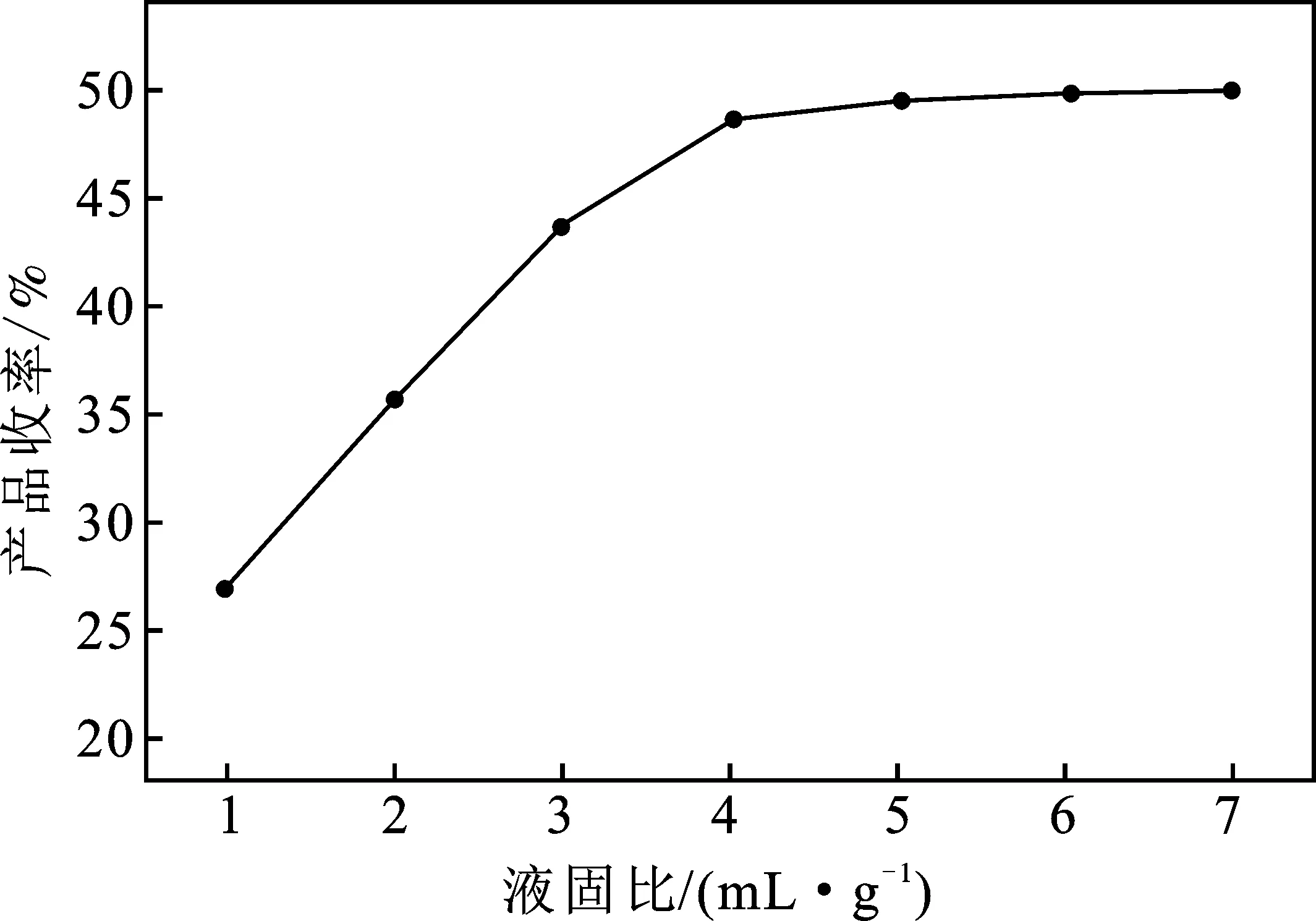
图6 液固比对2-MNQ收率的影响Fig.6 The effect of liquid-solid ratio on the yield of 2-MNQ
由图6可知,液固比从1 mL/g增加到5 mL/g,2-MNQ的收率从26.76%增加到49.43%;进一步增加液固比到8 mL/g,2-MNQ的收率增加不到1%。增加液固比相当于增加了相界面与液相主体的浓度差,使得生成物由相界面转移到液相主体的速率加快,有利于铬酸钡氧化2-MN。随着液固比进一步提升,产品收率无明显增加。因此最佳液固比为 5 mL/g。
2.6 反应温度的影响
为考察温度对铬酸钡液相氧化2-MN制备2-MNQ的影响,将超声预处理20 min的2-MN溶液,在盐酸用量为理论用量1.2倍、n(BaCrO4)∶n(2-MN)为2.0、液固比为5 mL/g的条件下反应3.5 h。反应温度对产品收率的影响见图7。
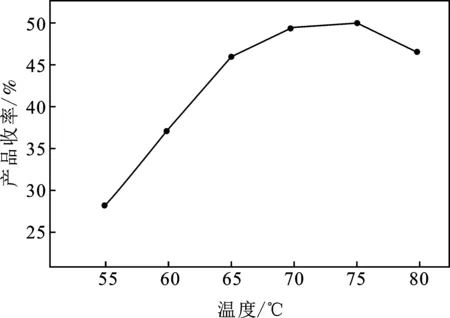
图7 反应温度对2-MNQ收率的影响Fig.7 The effect of reaction temperature on the yield of 2-MNQ
由图7可知,反应温度从55 ℃增加到75 ℃时,2-MNQ的收率从28.21%迅速增加到49.86%;反应温度继续增加,2-MNQ的收率急剧下降,到80 ℃时仅为46.65%,可见温度对2-MNQ收率的影响十分明显。提高反应温度,可显著提高反应的速率,使得2-MNQ的收率迅速上涨,但是副反应的反应速率同样被提升,所以当反应温度超过75 ℃后,铬酸钡2-MNQ的过度氧化速度超过了铬酸钡2-MN的氧化速度,导致2-MNQ的收率降低。因此反应的最佳温度为75 ℃。
2.7 产品的定性分析
将实验产物用乙醇重结晶,利用XRD对产物样品进行分析,结果见图8。
由图8可知,所制备的2-MNQ晶体与2-MNQ标准品晶体具有相同的主要衍射峰。
为了确切证明有目标产物2-MNQ的生成,最后对样品进行红外光谱分析,并把其与2-MNQ红外标准谱图进行对比分析,结果见图9。

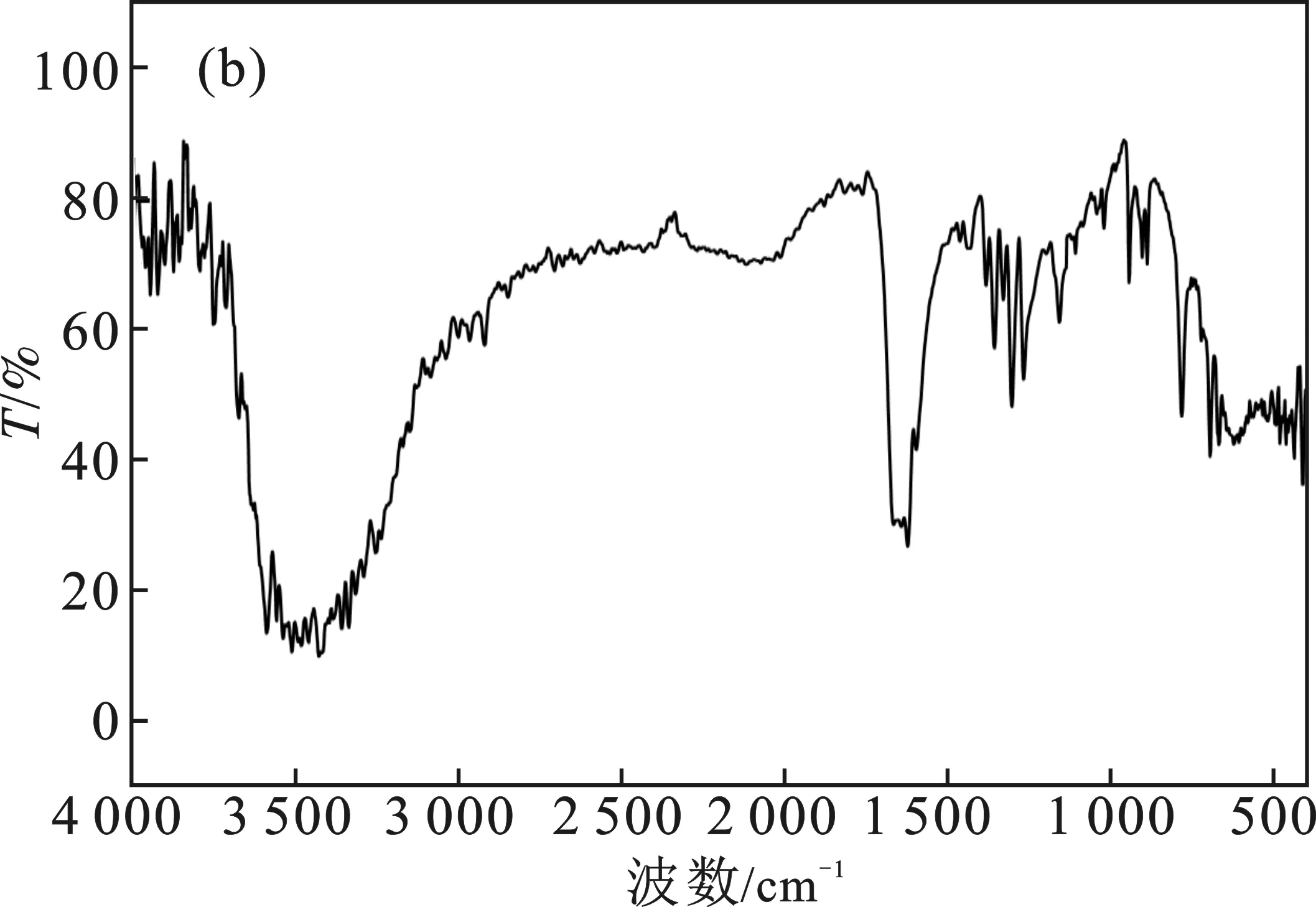
图9 2-MNQ的红外标准谱图(a)和产物(b)的红外光谱图Fig.9 The infrared standard spectrum of 2-MNQ(a) and the infrared spectrum of the product(b)

3 结论
本实验研究了一种高效合成2-MNQ的方法,并且使铬盐中间产品铬酸钡得以有效利用。基于对各种因素的考察,确定了铬酸钡液相氧化2-MN得到2-MNQ的最佳反应条件:超声预处理时间为20 min,反应时间3.5 h,盐酸用量为理论盐酸用量的1.2倍,铬酸钡与2-甲基萘的摩尔比为2.0,液固比5 mL/g 和反应温度75 ℃。在该条件下2-MNQ的最佳收率为49.86%。通过XRD和红外光谱对产品进行分析,证实了所得产品为2-MNQ。相对于生产2-MNQ的传统工艺,该方法的反应条件温和,能耗低,并且使得高毒性的六价铬转化为三价铬,有效降低了含铬废水处理的难度,可获得更大的经济收益,具有重要的现实意义。本研究可为当前液相氧化制备维生素K3以及铬盐产品的应用提供潜在的可行方案和指导思路。
