改性单宁酸铁吸附催化脱氮性能研究
2022-06-22刘莉张瑞娜李溪清王一冰卜培彦陈帅张雅楠
刘莉,张瑞娜,李溪清,王一冰,卜培彦,陈帅,张雅楠
(河北科技大学 环境科学与工程学院,河北省污染防治生物技术重点实验室,河北 石家庄 050018)
本实验通过氧化还原改性和改变制备过程条件,制备了改性TA-Fe吸附催化剂,选用相关设备对材料进行表征。通过摇瓶实验,确定底物浓度、温度、pH值的最佳作用条件,分析TA-Fe以及改性TA-Fe的脱氮性能,以期为含氮废水的实际处理和应用提供理论参考。
1 实验部分
1.1 材料与仪器
TA(C76H52O46),ACS试剂;盐酸(HCl),优级纯;三氯化铁(FeCl3·6H2O)、氯化铵(NH4Cl)、亚硝酸钠(NaNO2)、过氧化氢(H2O2)、碳酸氢钠(NaHCO3)、亚硫酸钠(Na2SO3)、硫酸亚铁(FeSO4·7H2O)、氢氧化钠(NaOH)均为分析纯;用蒸馏水制备所有溶液。
BTP-3XL00X型冷冻干燥机;D-37520型高速离心机;TU-1810 PC型紫外可见分光光度仪;Hitachi S-4800场发射扫描电子显微镜;Mutilab 2000 X射线光电子能谱仪;Tensor27 傅里叶变换红外光谱仪。
1.2 材料制备方法
氧化改性利用强氧化剂氧化表面官能团,提高材料表面含氧酸性官能团(如酚羟基、羧基)含量,增强表面亲水性和极性[5-7]。以双氧水作为氧化剂主要用于烯键的氧化、芳香烃的氧化和羟基化、胺类的氧化等[8]。还原改性是还原剂与材料表面官能团反应,增加材料表面含氧碱性基团含量,增强材料表面非极性[9]。H2O2,Na2SO3作为常见的低成本氧化剂和还原剂用于材料改性,引入杂质离子少并且氧化还原效率高[10-11]。基于H2O2,Na2SO3的绿色氧化还原能力和TA-Fe的高效吸附催化特性,可通过氧化还原改性和改变制备过程条件,制备改性TA-Fe吸附催化剂。
1.2.1 TA-Fe 将TA和FeCl3·6H2O按1∶20的物质的量之比进行反应,NaHCO3调节溶液pH至中性,静置后沉积的黑色物质用去离子水反复洗涤5次后,离心机离心(8 000 r/min,2 min),然后将沉积物放入冷冻干燥机(-72 ℃)冷冻干燥,形成的黑色粉末即为TA-Fe。
1.2.2 TA-Fe/H2O2将制备好的TA-Fe溶于盐酸中,体系中加入H2O2,H2O2氧化TA-Fe,搅拌使之充分反应,NaHCO3调节溶液pH至中性,黑色沉淀物使用去离子水洗涤,离心机离心(8 000 r/min,2 min),沉积物放入冷冻干燥机(-72 ℃),形成的黑色粉末即为TA-Fe/H2O2。
1.2.3 TA-Fe/Na2SO3TA-Fe先溶于盐酸中,后加入Na2SO3充分反应,Na2SO3还原TA-Fe得到的黑色沉淀物按照上述的实验方法用去离子水洗涤,离心,冷冻干燥。
1.2.4 TA-Fe/FeSO4TA和FeSO4·7H2O按照1∶20物质的量之比充分反应,调节pH至中性,静置后黑色沉积物用去离子水洗涤,离心并冷冻干燥。
1.3 实验方法
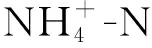
1.3.2 脱氮性能影响因素优化实验
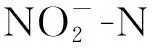

表和不同底物浓度分组Table 1 Grouping of different substrate concentrations
1.3.2.2 不同温度条件下的脱氮实验
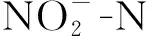
1.3.2.3 不同pH条件下的脱氮实验
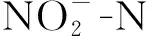
1.4 分析表征方法
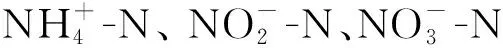
2 结果与讨论
2.1 催化剂的表征
2.1.1 表面形貌与孔隙结构 通过FE-SEM扫描电镜检查微区形态特征,见图1。




图1 TA-Fe/H2O2(a)、TA-Fe/Na2SO3(b)、 TA-Fe/FeSO4(c)、TA-Fe(d) FE-SEM图Fig.1 FE-SEM images of TA-Fe/H2O2(a),TA-Fe/Na2SO3 (b),TA-Fe/FeSO4(c),TA-Fe(d)
由图1可知,TA-Fe 图1(d)呈颗粒聚集状态,表面较粗糙,孔隙较多。TA-Fe/H2O2图1(a)和TA-Fe/Na2SO3图1(b)相对于TA-Fe图1(d)来说,表面更加粗糙,颗粒聚集状态和孔隙结构更为明显,裂纹和孔道数量显著增加[13]。这样的表面结构有助于TA-Fe/H2O2和TA-Fe/Na2SO3表面吸附反应的发生。图1(c)的FE-SEM图显示制备的 TA-Fe/FeSO4形貌特征呈现出纳米球形颗粒 ,相比于其他三种材料,表面形貌发生了改变。由图1可以看出,氧化还原改性以及制备过程条件的不同对TA-Fe表面形态的不同影响。
2.1.2 二价铁和三价铁含量 XPS用于进一步研究制备的改性TA-Fe的表面电子结构和表面性质,结果见图2。TA-Fe/H2O2的Fe 2p光谱在711 eV和724 eV处存在两个主峰。Fe 2p 3/2的峰对应于710.6 eV和712.2 eV的结合能,Fe 2p 1/2的峰对应于724.1 eV和725.8 eV的结合能,卫星吸收峰位于719.2 eV的位置,表2为Fe 2p光谱峰值位置和半峰宽。710.6 eV和724.1 eV处的结合能峰归因于Fe(II),而712.2 eV和725.8 eV的结合能则归因于Fe(III)。故可用峰面积代表材料表面Fe(II)和Fe(III)的相对含量,进而求出Fe(II)和Fe(III)的比例。
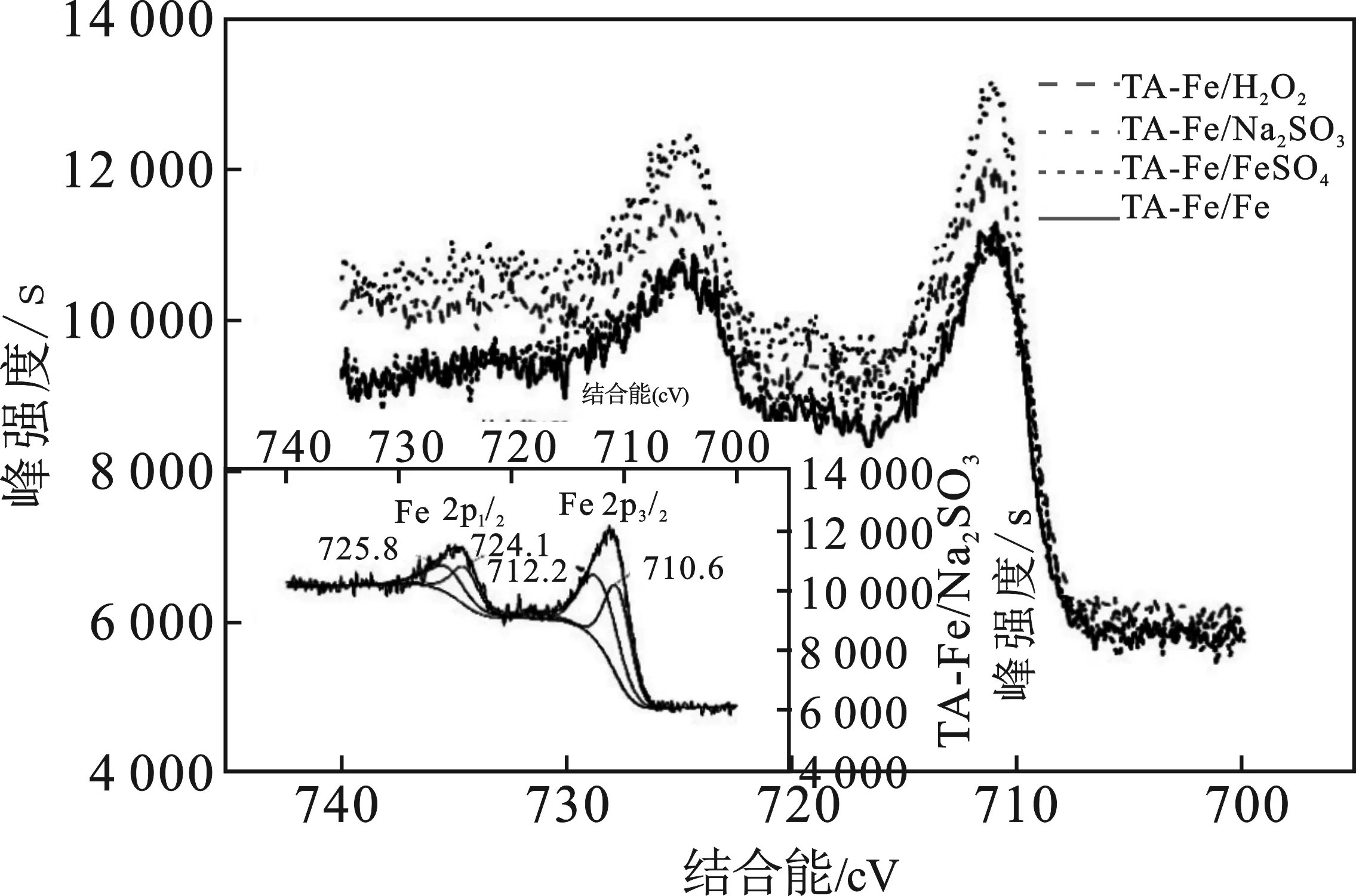
图2 Fe 2p的XPS光谱Fig.2 XPS spectrum of Fe 2p
XPS可用峰面积代表元素价态的相对含量,根据表3列出的铁含量和比例,比较3种改性材料与TA-Fe的差异。TA-Fe/H2O2、TA-Fe/Na2SO3、TA-Fe 3种材料的总铁含量几乎相等,这是因为前两种材料是对TA-Fe进行氧化还原反应所得到的,改性未改变材料的总铁含量。然而TA-Fe/FeSO4的总铁含量相对于前3种材料略低。这是因为TA-Fe/FeSO4的制备不同于TA-Fe的制备方法,采用FeSO4·7H2O与TA反应,而不是TA与FeCl3·6H2O反应。采用TA与FeSO4制备的TA-Fe/FeSO4大部分应呈现Fe(II)的络合状态,然而利用XPS得到的铁相对含量显示其Fe(II)含量低于其他3种材料,仅高于TA-Fe/H2O2,说明制备过程中大部分的Fe(II)被氧化成Fe(III)。TA-Fe/H2O2的Fe(II)的相对含量略低于未改性材料TA-Fe的Fe(II)含量。TA-Fe/H2O2的Fe(III)含量略高于Fe(II)含量,而TA-Fe的Fe(III)含量略低于Fe(II)含量。TA-Fe/H2O2的Fe(III)/Fe(II)是1.0,在4个材料中的比例最高,Fe(III)含量最高。由表3可知,成功制备了不同铁价态比的TA-Fe改性材料。

表2 Fe 2p光谱峰值位置和半峰宽(FWHM )Table 2 Fe 2p spectral peak positions and half-peak widths(FWHM )
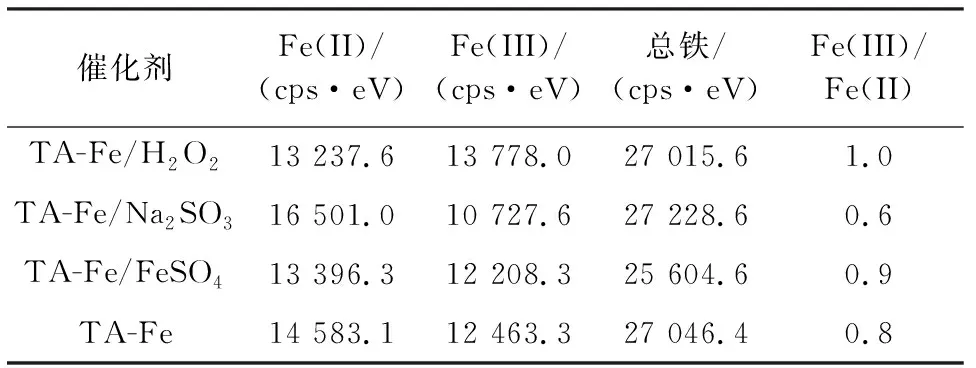
表3 铁含量和比例Table 3 Iron content and ratio
2.1.3 表面官能团 根据材料的FE-SEM和XPS结果分析氧化还原改性以及制备过程中调整Fe(II)和Fe(III)的比例对材料表面物理形貌与表面电子结合能的影响。为了研究制备完成的改性单宁酸铁官能团的变化情况,室温下采用KBr压片法,测定冷冻干燥制备的4种材料的主要官能团,分析改性单宁酸铁的羟基官能团和化学键的变化特征。图3为4种材料的FTIR光谱图。

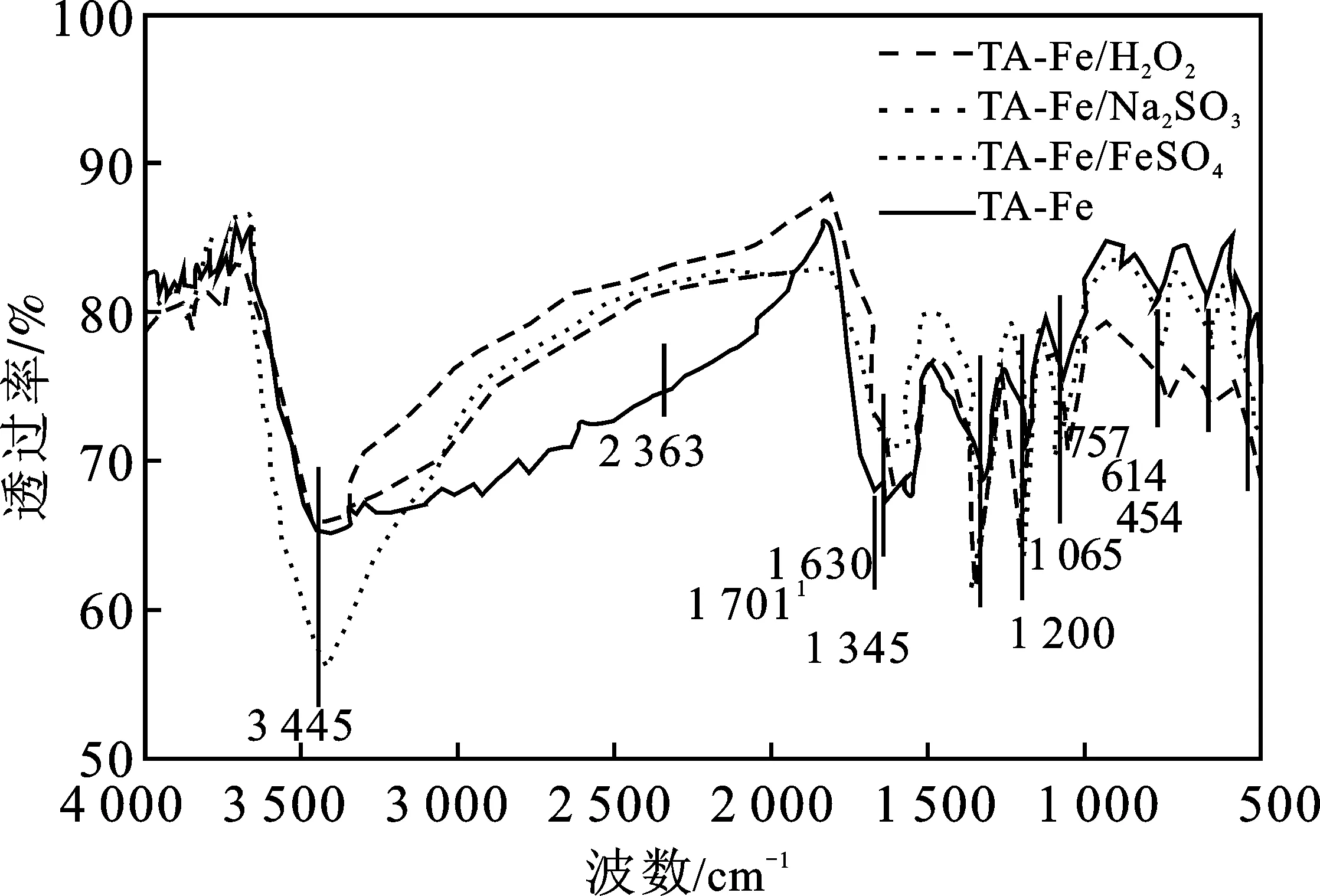
图3 FTIR光谱图Fig.3 FTIR spectrogram
TA-Fe/H2O2不同于其他3种材料的地方在于TA-Fe/H2O2在2 363 cm-1产生了一个新的较小的吸收峰。推测H2O2与TA-Fe表面羟基形成氢键,H2O2与TA-Fe发生了化学反应,产生了一种新的化学键,并不只是简单的物理吸附改性作用。氧化物材料表面改性的作用原理是材料与改性剂发生了物理和化学作用。化学作用是改性剂作用于材料表面的氢键,或者是改性剂与材料表面的羟基形成共价键,改性剂与材料之间形成比较稳固的结构[16]。因此推测2 363 cm-1的吸收峰是氧化剂H2O2与TA-Fe表面的羟基作用形成的氢键。
2.2 吸附催化脱氮性能研究
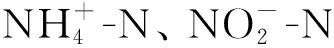
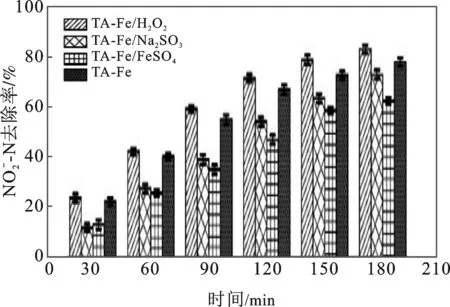

图4 4种材料的和TN去除率 and TN removal rate of the four materials
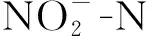
2.3 TA-Fe/H2O2脱氮性能影响因素研究
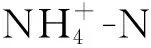
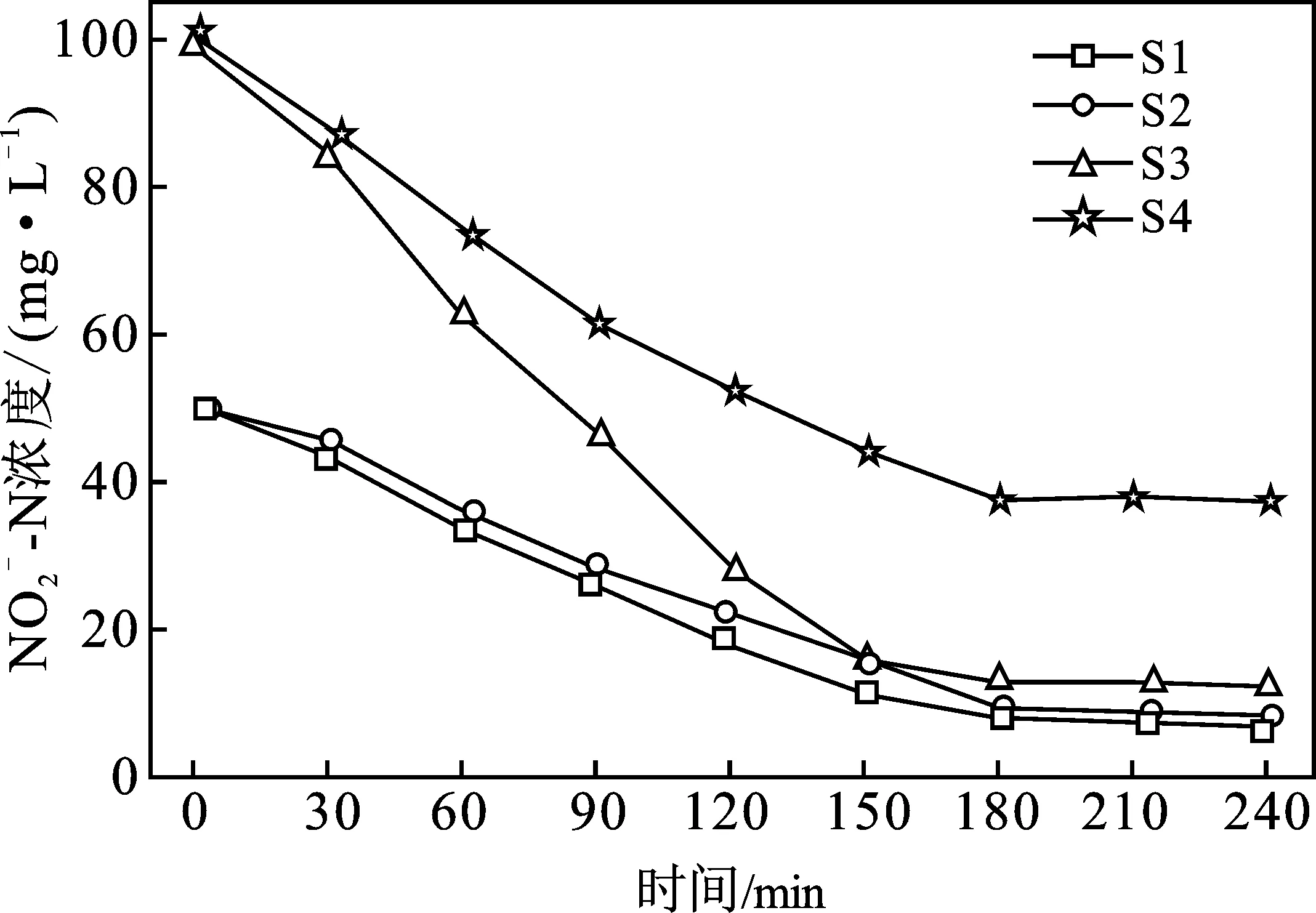
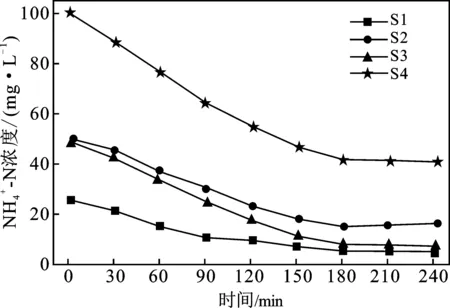
图5 TA-Fe/H2O2在不同底物浓度条件下 吸附催化和浓度的变化Fig.5 Variation of adsorption-catalyzed and concentrations under different substrate concentrations by TA-Fe/H2O2
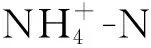
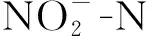
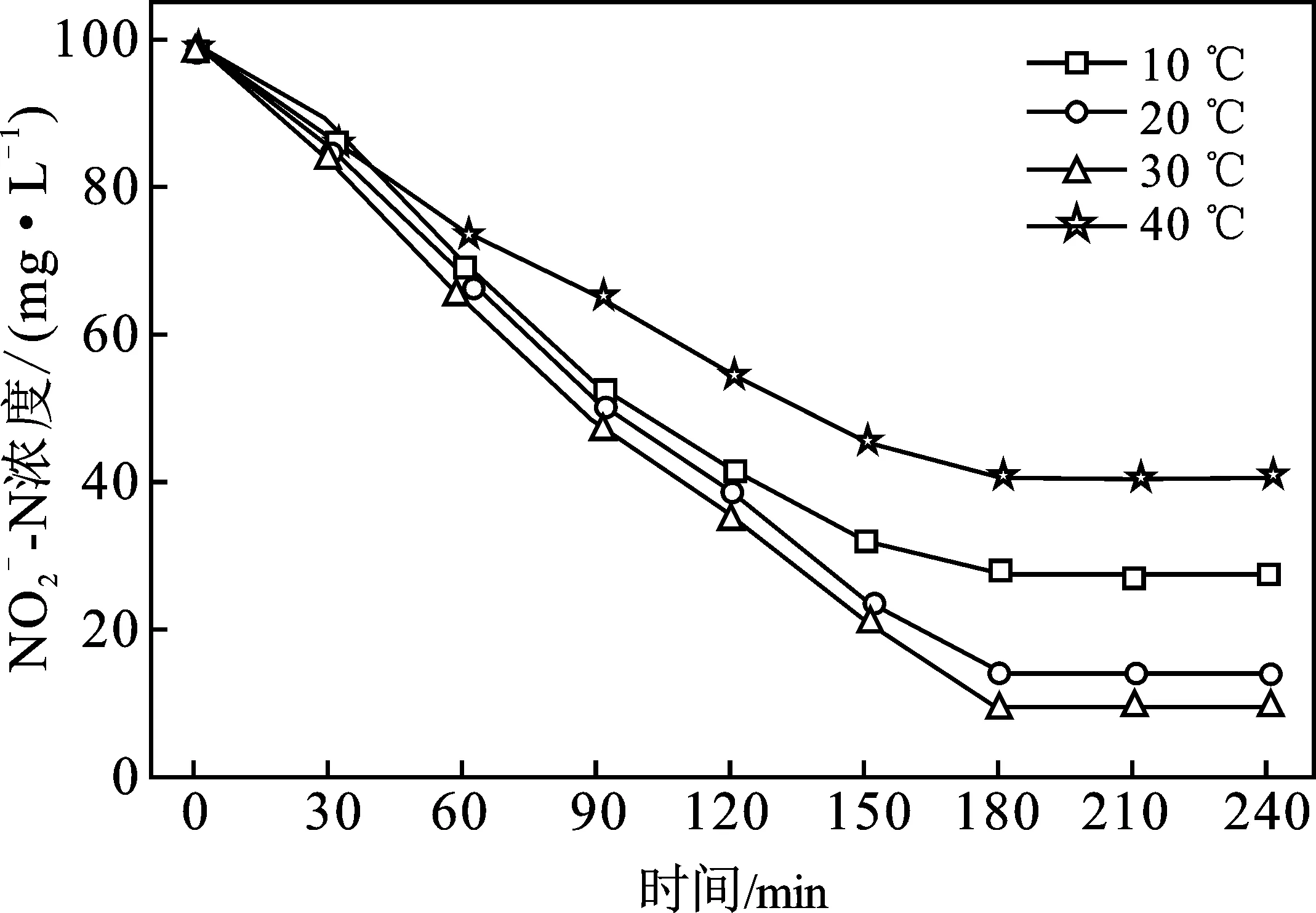

图6 TA-Fe/H2O2 在不同温度条件下吸附 催化和浓度的变化Fig.6 Variation of adsorption-catalyzed and concentrations under different temperature conditions for TA-Fe/H2O2
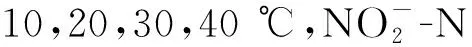
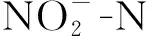
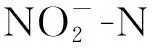
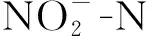
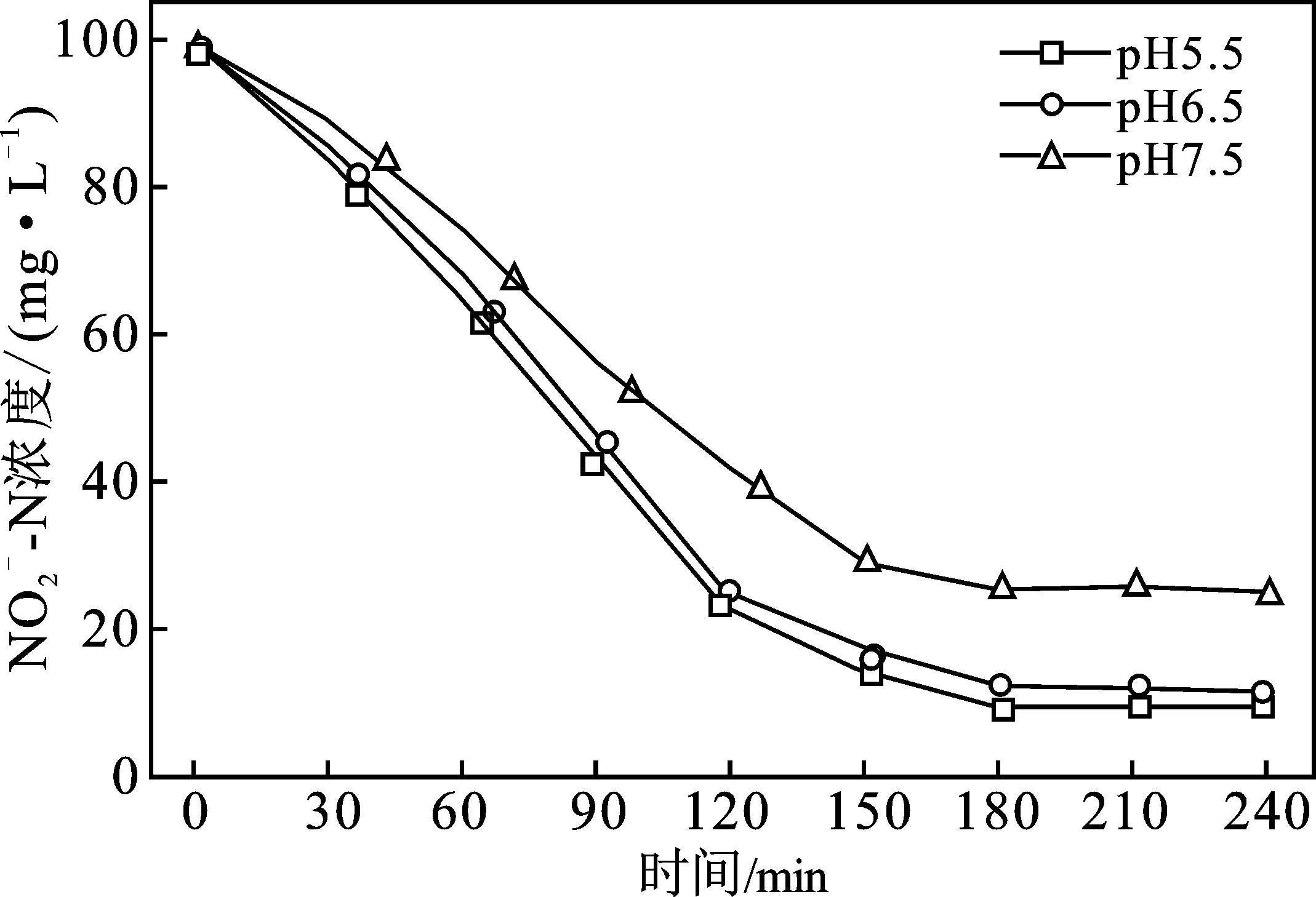
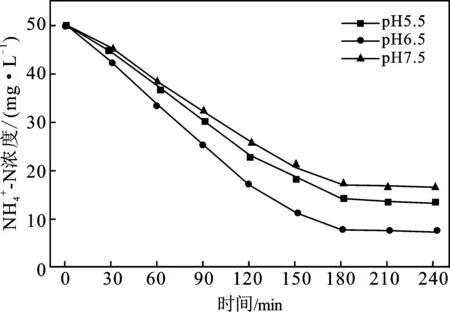
图7 TA-Fe/H2O2 在不同pH条件下吸附催 化和浓度的变化Fig.7 Variation of adsorption-catalyzed concentrations under different pH conditions by TA-Fe/H2O2
综上所述,溶液pH在6~7之间TA-Fe/H2O2脱氮效果最好。溶液的pH值对TA-Fe/H2O2脱氮效果影响明显,故在实际废水脱氮过程中可适当调整废水pH值,提高TA-Fe/H2O2脱氮效果。
3 结论