人参黄精膏质量标准研究
2022-06-22贺清辉罗进杜军罗艳萍王红刚周静仪杨嘉文
贺清辉,罗进,杜军,罗艳萍,王红刚,周静仪,杨嘉文
[1.安利(中国)研发中心有限公司,广东 广州 510730;2.广东一方制药有限公司,广东 佛山 528244;3.广东药科大学中药学院,广东 广州 510006]
随着社会的发展和生活节奏的加快,女性健康越来越受到社会的关注。中医学认为气、血均为人体生命活动的基本物质,为人之本源[1]。《黄帝内经》载有“人之所有者,血与气耳”,充分说明了气、血对于人体的重要性[2]。中医学上对女性病理的研究均统一认为“女子以气为用,以血为本”的观点[3]。由于肾气渐衰,天癸将绝,冲任亏虚,气血暗耗,故导致了阴阳气血失衡[4],从而引发女性疾病。
人参黄精膏由人参、玉竹、黄精、枸杞、玫瑰花等5 种药食同源原料及新食品原料丹凤牡丹花组成。处方中的人参具有大补元气、补脾益肺、生津养血等功效;黄精补气养阴,健脾,润肺,益肾;枸杞滋补肝肾,益精明目;玉竹养阴润燥,生津止渴;玫瑰花行气解郁[5];丹凤牡丹花是2013 年国家卫计委批准的新食品原料,富含多酚、氨基酸、维生素、矿物质等功能营养成分[6];全方滋阴补气,补而不腻。人参黄精膏作为一款功能食品,质量标准主要参考国家标准GB/T 31326《植物饮料》,包括感官、理化、污染物限量及微生物限量等指标。但本品中的人参、玉竹、黄精、枸杞、玫瑰花、丹凤牡丹花等富含皂苷、黄酮和多糖等活性成分,现有质量标准无法体现配方中化学成分的多样性和复杂性。本研究旨在建立人参、枸杞、玫瑰花、丹凤牡丹花的薄层鉴别方法,并建立粗多糖的质量分数测定方法,为提升人参黄精膏的质量标准提供参考。
1 仪器与试药
1.1 仪器
KQ-500DE 超声波处理器(昆明市超声仪器有限公司);ATS4薄层点样机(瑞士卡玛公司);Visual‐izer 薄层呈像仪(瑞士卡玛公司);ME-203 型电子天平(梅特勒-托利多仪器有限公司);TC-15 电热套(海宁市新华医疗器械厂);RE-300 旋转蒸发仪(上海亚荣生化仪器厂);UV-2450 紫外-可见分光光度计(岛津仪器有限公司)。
1.2 试药
人参黄精膏(批号S2202003、S2202004、S2202005、S2202006、S2202007,广东一方制药有限公司生产);人参皂苷Rg1(110703-201832)、人参皂苷Re(110754-202028)、人参对照药材(120917-201401B)、枸杞对照药材(121072-201412B)、玫瑰花对照药材(121508-201607B)均由中国药品生物制品检定所提供;人参皂苷Rb1(S299-D25,成都曼斯特生物科技有限公司);丹凤牡丹花对照药材(DZ12012051,经广东一方制药有限公司魏梅主任药师鉴定为丹凤牡丹Paeonia ostiiT.Hong et J.X.Zhang的干燥花朵);无水葡萄糖(天津市天新精细化工开发中心)、苯酚(广州化学试剂厂)、浓硫酸(广州化学试剂厂)。
2 方法与结果
2.1 TLC鉴别
2.1.1 人参薄层鉴别 参考《中国药典》人参药材鉴别方法,取本品约5.0 g,加三氯甲烷30 mL,加热回流1 h,弃去三氯甲烷,残渣挥干溶剂,加水1.0 mL搅拌溶解,加水饱和的正丁醇20 mL,超声处理30 min,吸取上清液,加3 倍量氨试液,摇匀,放置分层。取上层溶液蒸干,残渣加甲醇1 mL 使溶解,作为人参黄精膏供试品溶液。另取人参对照药材0.5 g,同法制成人参对照药材溶液。分别取人参皂苷Rb1、人参皂苷Re、人参皂苷Rg1 对照品,加甲醇制成每1 mL各含2 mg的溶液,作为对照品溶液。按人参黄精膏处方比例,去掉人参后,依法制成人参黄精膏缺人参的阴性供试品溶液。照薄层色谱法(《中国药典》2020年版四部通则0502)试验,吸取上述溶液各5µL,分别点于同一默克高效板上,以三氯甲烷-乙酸乙酯-甲醇-水(体积比15∶40∶22∶10)10 ℃以下放置的下层溶液为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,在105 ℃加热至斑点显色清晰,置紫外光灯(365 nm)和日光下检视,在供试品、对照药材和对照品薄层色谱相应的位置上,显相同颜色斑点,缺人参阴性样品则无相应的斑点。结果见图1。
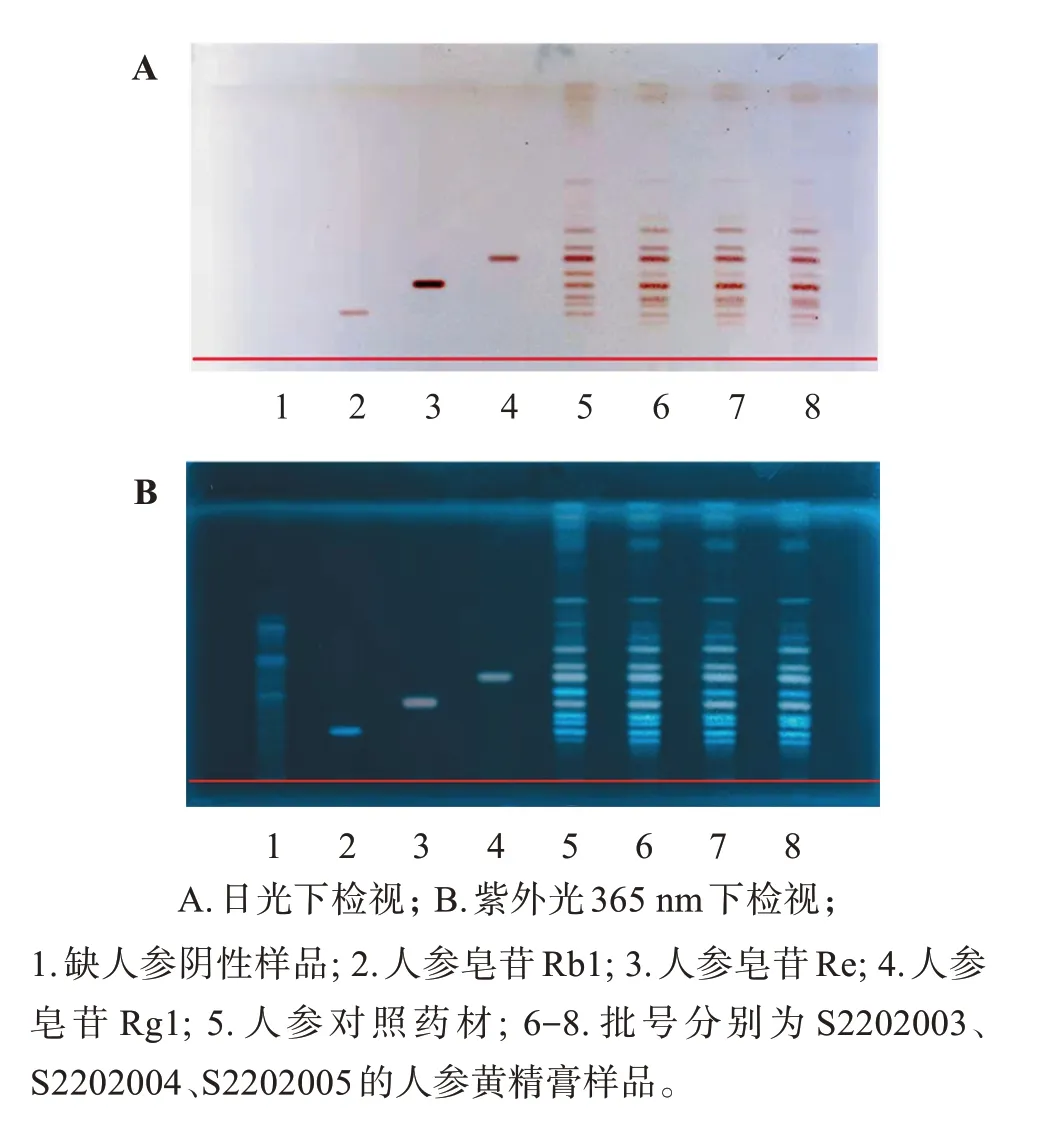
图1 人参对照品、人参对照药材及人参黄精膏样品薄层色谱图Figure 1 TLC identification of Ginseng Radix et Rhizome in Renshen Huangjing ointment samples
2.1.2 枸杞薄层鉴别[7]取本品约5.0 g,加乙酸乙酯20 mL 振摇提取,分取乙酸乙酯液,浓缩至约1 mL,作为人参黄精膏供试品溶液。另取枸杞对照药材1.0 g,加水50 mL,煮沸15 min,滤过,滤液用乙酸乙酯20 mL 振摇提取,同法制成对照药材溶液。按人参黄精膏处方比例,去掉枸杞,依法制成人参黄精膏缺枸杞阴性供试品溶液。照薄层色谱法(《中国药典》2020年版四部通则0502)试验,吸取供试品溶液和对照药材溶液各5µL,分别点于同一硅胶G 薄层板上,以三氯甲烷-乙酸乙酯-甲酸(体积比6∶3∶1)为展开剂,展开,取出,晾干,置紫外光灯(365 nm)下检视。在供试品与对照药材薄层色谱相应的位置上,显相同亮蓝色荧光斑点,缺枸杞阴性样品无相应的斑点,结果见图2。

图2 枸杞对照药材与人参黄金膏样品薄层色谱图Figure 2 TLC identification of Lycii Fructus in Renshen Huangjing ointment samples
2.1.3 丹凤牡丹花薄层鉴别[8]取本品约5.0 g,加水50 mL,溶解离心,取上清液蒸干,残渣加甲醇5 mL,溶解,滤过,取续滤液作为供试品溶液。取丹凤牡丹花对照药材1.0 g,加水50 mL,煮沸30 min,离心,取上清液蒸干,残渣加甲醇5 mL使溶解,滤过,取续滤液作为对照药材溶液。按人参黄精膏处方比例,去掉丹凤牡丹花后,依法制成人参黄精膏缺丹凤牡丹花阴性样品溶液。照薄层色谱法(《中国药典》2020年版四部通则0502)试验,吸取供试品溶液、阴性对照溶液、对照药材溶液各2µL分别点于同一硅胶G薄层板上,以甲苯-乙酸乙酯-甲酸(体积比5∶3∶1)溶液为展开剂,展开,取出,晾干,置紫外光灯(365 nm)下检视。供试品色谱中,供试品与对照药材色谱相同位置上,显相同颜色的斑点,缺丹凤牡丹花阴性样品则无相应斑点,结果见图3。
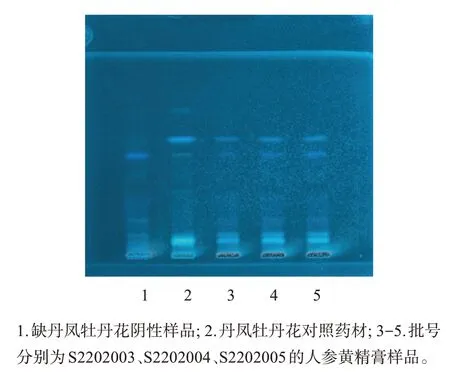
图3 丹凤牡丹花对照药材和人参黄精膏样品薄层色谱图Figure 3 TLC identification of Paeonia ostii Flos in Renshen Huangjing ointment samples
2.1.4 玫瑰花的薄层鉴别[8]取本品约2.0 g,加甲醇20 mL,超声过滤,滤液蒸干,残渣加甲醇2 mL 溶解,滤过,取续滤液作为供试品溶液。取玫瑰花对照药材0.5 g,加甲醇20 mL,超声过滤,滤液蒸干,残渣加甲醇2 mL 溶解,滤过,取续滤液作为对照药材溶液。按人参黄精膏处方比例,去掉玫瑰花后,依法制成人参黄精膏缺玫瑰花阴性样品溶液。照薄层色谱法(《中国药典》2020年版四部通则0502)试验,吸取阴性样品溶液、对照药材溶液、供试品溶液各5µL分别点于同一GF254薄层板上,以甲苯-乙酸乙酯-甲酸(体积比5∶5∶1)为展开剂,展开,取出,晾干,置紫外光灯(254 nm)下检视。供试品与对照药材色谱相同的位置上,显相同颜色的主斑点,缺玫瑰花阴性样品则无相应的斑点,结果见图4。

图4 玫瑰花对照药材与人参黄金膏样品薄层色谱图Figure 4 TLC identification of Rosae Rugosae Flos in Renshen Huangjing ointment samples
2.2 紫外-可见分光光度法测定粗多糖的质量分数[9-10]
2.2.1 葡萄糖对照品溶液的制备 称取0.100 g 葡萄糖于量瓶中,加水溶解,定容至1000 mL,即得。
2.2.2 供试品溶液的制备 精密称取样品0.500 g,置于50 mL具塞离心管内。用5 mL水浸润样品,缓慢加入20 mL无水乙醇,摇匀,超声提取30 min。提取液于4000 r/min 离心10 min,弃去上清液。不溶物用10 mL 80%乙醇溶液洗涤、离心。用水将上述不溶物转移入圆底烧瓶,加入50 mL 水,超声提取30 min。冷却,过滤,重复提取2 次。将滤液转移至200 mL 容量瓶中,残渣洗涤2~3 次,洗涤液转移至量瓶,加水定容,即得。
2.2.3 检测波长的确定 取葡萄糖对照品溶液、样品溶液各1 mL 于具塞试管中,加入5%苯酚溶液1 mL,然后迅速加入浓硫酸5.0 mL,摇匀。静置10 min,充分混匀并于30 ℃水浴中反应20 min,于400~600 nm 波长进行紫外-可见光谱扫描,结果见图5。

图5 葡萄糖对照品溶液与供试品溶液紫外可见光谱图Figure 5 UV-Vis spectra of glucose solution and sample solution
可见,葡萄糖对照品溶液的最大吸收波长为490 nm,人参黄精膏供试品溶液的最大吸收波长为487 nm,两组最大吸收波长接近。结合参考文献,选择490 nm波长作为检测波长。
2.2.4 标准曲线与线性范围 精密量取对照品溶液0.2、0.4、0.6、0.8、1.0 mL,用蒸馏水补至1.0 mL,加入5%苯酚溶液1 mL,再迅速加入浓硫酸5.0 mL。静置10 min,充分混匀并于30 ℃水浴中反应20 min,在490 nm 波长处测定吸光度,以吸光度为纵坐标、质量浓度为横坐标,绘制标准曲线,得线性回归方程y=0.0088x+0.0283,R2=0.9995,表明葡萄糖质量浓度在19.62~98.1 μg/mL 范围内与吸光度线性关系良好。
2.2.5 重复性试验 取同一批号人参黄精膏样品(批号S2201012),按“2.2.2”项下方法平行制备6 份供试品溶液,分别取1 mL 于具塞试管中,加入5%苯酚溶液1 mL,然后迅速加入浓硫酸5.0 mL,静置10 min,充分混匀并于30 ℃水浴中反应20 min,在490 nm 波长处测定吸光度,计算粗多糖质量分数及其RSD 值。结果显示,该批次人参黄精膏样品的粗多糖质量分数在1.74%~1.81%范围内,6 次的测定平均值为1.77%,RSD 值为1.24%,表明方法重复性较好。
2.2.6 精密度试验 取同一批号人参黄精膏样品(批号S2202003),按“2.2.5”项方法进行粗多糖质量分数测定,每天测定1 次,连续测定3 d,结果计算得日间精密度RSD值为2.65%。由两名操作员独立对同一批号人参黄精膏样品(批号S2202003)按“2.2.5”项方法进行粗多糖质量分数测定,结果计算得RSD值为0.8%。
2.2.7 回收率试验 取同一批号人参黄精膏样品(批号S2202003),按“2.2.2”项方法平行制备9 份供试品溶液,分别取供试品溶液各0.5 mL 于具塞试管中,分别加入0.5 mL 相当于样品含量25%、50%、100%的葡萄糖对照品溶液各3 份,按“2.2.5”项方法进行粗多糖质量分数测定,计算加样回收率,结果见表1。可见,加样回收率在96.19%~98.29%之间,平均回收率为97.45%,RSD 值为0.74%,表明方法回收率较好。
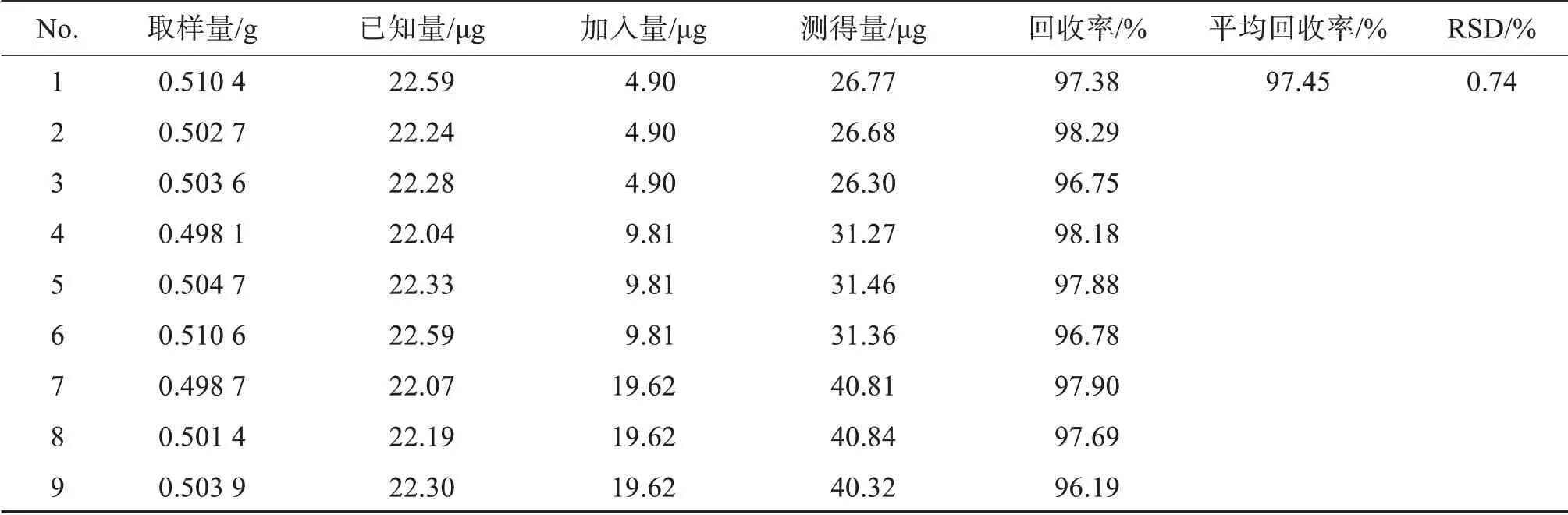
表1 人参黄精膏中葡萄糖的回收率试验结果Table 1 Results of recovery test of glucose in Renshen Huangjing ointment
2.2.8 耐用性试验 取同一批号人参黄精膏样品(批号S2202003),按“2.2.2”项下方法制备供试品溶液,考察超声时间分别为25、30、35 min 时粗多糖的质量分数,并计算其RSD值。结果显示,超声25、30、35 min 时粗多糖的质量分数分别为1.71%、1.76%、1.72%,RSD值为1.53%,表明方法耐用性良好。
2.2.9 粗多糖质量分数的测定 取5批人参黄精膏,按“2.2.2”项方法制备成供试品溶液,再按“2.2.5”项方法进行粗多糖质量分数测定。结果显示,批号S2202003、S2202004、S2202005、S2202006、S2202007的人参黄精膏中粗多糖质量分数分别为1.71%、1.74%、1.63%、1.54%、1.63%。表明采用该方法测定人参黄精膏中的粗多糖质量分数,结果稳定、重复性好,可有效控制人参黄精膏的质量。
3 讨论
本研究以对照药材及特征成分为对照进行人参黄精膏中人参、枸杞等药材的薄层色谱鉴别研究,通过对供试品溶液的制备方法、展开溶剂的种类与比例、点样量等因素进行优化,确定了人参、枸杞、丹凤牡丹花、玫瑰花4种药材的薄层色谱鉴别条件,结果显示薄层色谱斑点清晰、分离明显,阴性对照无干扰,专属性好,可用于人参黄精膏的质量控制。人参的薄层鉴别中,由于供试品溶液的萃取步骤较多,人参皂苷等特征成分提取不完全,导致斑点不清晰,因此溶剂萃取时需充分振摇,确保提取完全。枸杞薄层鉴别中的展开剂比例会影响鉴别结果,因此需要充分优化,以达到更好的分离效果。丹凤牡丹花的供试品溶液制备方法简单,但需控制好溶液浓度和点样量,浓度过高或点样量大,均会导致斑点分离效果差。
另外,在对黄精、玉竹进行薄层鉴别的研究中发现,黄精、玉竹富含多糖成分易与配方中人参、枸杞中的多糖产生干扰。本研究多次分别对多糖、黄酮类等成分进行薄层鉴别试验,均发现阴性样品干扰较大,且无专属性,薄层的斑点不清晰,故认为薄层法不适用黄精和玉竹的薄层鉴别。后期考虑采用HPLC 法对其质量控制进行研究,以完善人参黄精膏的质量控制体系。
人参黄精膏中含有人参、玉竹、黄精、枸杞等富含多糖的中药,而多糖类成分具有良好的免疫调节作用,因此,本研究采用紫外-可见分光光度法建立了人参黄精膏中的粗多糖质量分数测定方法,方法学考察结果表明该方法重复性好、检测结果准确,可用于控制人参黄精膏质量。《中国药典》中黄精多糖含量采用蒽酮-硫酸法,而玉竹和枸杞的多糖采用苯酚-硫酸法。本研究对比2 个多糖检测方法,发现采用苯酚-硫酸法测定人参黄精膏中的多糖,干扰较少,方法简单易操作,重现性好,可用于大规模的连续生产检测。
