腐殖酸催化醛高效快速合成腈
2022-06-17柳聪慧鲁逸文王宏社
柳聪慧, 徐 颖, 鲁逸文, 王宏社
(宝鸡文理学院 化学化工学院,陕西宝鸡 721013)
腈类化合物是重要的香料、化工原料和中间体。氰基是有机合成中通用性较高的官能团之一,它可以非常容易地被转化成其他基团。此外,氰基也是重要的药效基团,具有较好的代谢稳定性和生物相容性[1-3]。近年来,研究人员对腈类化合物的合成研究非常活跃。张绪穆等采用不对称氢甲酰化反应、缩合反应以及aza-Cope消除反应串联的方法,获得了非常有价值的手性腈类化合物[4]。刘文博等发展了高效合成氰基季碳的方法,氰基季碳中心在药物化学和有机合成方面都具有重要的意义[5]。脂肪腈类化合物通常具有独特的化学结构和物理性质,在合成树脂、杀虫剂、胶黏剂和特种溶剂等化工领域中具有广泛应用。张锁江等系统研究了脂肪腈合成方法学[6]。
腈类化合物的合成方法较多[7],以醛[8-14]、羧酸[15-17]、肟[18]、醇[19]和胺[20]等为原料都可以顺利合成腈类化合物。其中以醛和盐酸羟胺为原料一锅法合成腈的方法较为简单。文献已经报道了HCl·DMPU[21]、Fe3O4纳米粒子[22]、FeCl3[23]、ZnO[24]、KF/Al2O3[25]、W-Sn氢氧化物[26]、SnCl2·2H2O[27]、TiCl4[28]、Na2CO3/SO2F2[29]、Salen Ru(Cl)配合物[30]和微波[31]等催化醛和盐酸羟胺反应合成腈的方法。但以上方法普遍存在反应时间长、催化剂获取困难等缺点。
N-甲基吡咯烷酮(NMP)具有良好的化学稳定性和热稳定性,无腐蚀、毒性小、生物降解能力强、挥发度低,是一种环境友好的溶剂[32]。腐殖酸是一种无毒、非金属、价格低廉和商业易得的大分子有机物质,能回收并重复使用。魏振中等[33]报道了腐殖酸催化醛、1,3-二羰基化合物和乙酸铵合成1,4-二氢吡啶类化合物,该法后处理方便、催化剂能回收再利用,为1,4-二氢吡啶类化合物的合成提供了一种简捷绿色的方法。
为拓展腐殖酸的应用范围,本文以其为催化剂,NMP为溶剂,由醛和盐酸羟胺在110 ℃下反应5~8 min合成了一系列腈类化合物(2a~2p, Scheme 1)。该方法具有操作简单、反应条件温和、反应时间短和产率高等优点。

Scheme 1
1 实验部分
1.1 仪器与试剂
X-4型精密显微熔点仪;MA-400 MHz型核磁共振仪(CDCl3为溶剂,TMS为内标);Agilent 1200型质谱仪。
腐殖酸(阿拉丁),NMP(国药上海化学试剂公司),醛类化合物(天津市科密欧化学试剂有限公司);其余所用试剂均为分析纯。
1.2 合成
在装有搅拌器、温度计和冷凝管的三口烧瓶中加入醛(1 mmol)、盐酸羟胺(1.2 mmol)、腐殖酸催化剂(0.1 g)和NMP(2 mL),于110 ℃反应至终点(TCL跟踪)。反应液趁热过滤回收腐殖酸,催化剂用95%乙醇洗涤后,重复使用;在滤液中加入100 mL水,用乙酸乙酯(2 × 25 mL)萃取,合并有机相,依次用饱和食盐水(2 × 10 mL)洗涤,无水硫酸镁干燥,减压蒸除有机溶剂得粗产品,经硅胶柱层析[洗脱剂:V(石油醚)/V(乙酸乙酯)=10/1]得化合物2。
2a:无色液体,产率92%;1H NMR(400 MHz, CDCl3)δ: 7.65~7.59(m, 3 H), 7.51~7.47(m, 2H);13C NMR(100 MHz, CDCl3)δ: 132.87, 132.26, 129.23, 118.94, 112.58; HR-MS(ESI)m/z: Calcd for C7H5N{[M+H]+}104.0495, found 104.0492。
2b:白色固体,产率96%;1H NMR(400 MHz, CDCl3)δ: 7.54(d,J=8.0 Hz, 2H), 7.27(d,J=8.5 Hz, 2H), 2.42(s, 3H);13C NMR(100 MHz, CDCl3)δ: 143.81, 132.20, 129.97, 119.28, 109.50, 21.97; HR-MS(ESI)m/z: Calcd for C8H7N{[M+H]+}118.0651, found 118.0655。
2c:黄色液体,产率95%;1H NMR(400 MHz, CDCl3)δ: 7.49~7.44(m, 2H), 7.41(d,J=7.6, 2.0 Hz, 1H), 7.38~7.31(m, 1H), 2.39(s, 3H);13C NMR(100 MHz, CDCl3)δ: 139.32, 133.75, 132.59, 129.38, 129.09, 119.16, 112.31, 21.25; HR-MS(ESI)m/z: Calcd for C8H7N{[M+H]+}118.0651, found 118.0656。
2d:黄色液体,产率93%;1H NMR(400 MHz, CDCl3)δ: 7.64~7.55(m, 2H), 7.53~7.44(m, 2H), 1.33(s, 9H);13C NMR(100 MHz, CDCl3)δ: 156.79, 132.11, 126.31, 119.29, 109.48, 35.41, 31.09; HR-MS(ESI)m/z: Calcd for C11H13N{[M+H]+}160.1121, found 160.1115。
2e:黄色固体,产率97%;1H NMR(400 MHz, CDCl3)δ: 7.63~7.55(m, 2H), 6.99~6.91(m, 2H), 3.86(s, 3H);13C NMR(100 MHz, CDCl3)δ: 162.99, 134.14, 119.36, 114.89, 104.14, 77.48, 77.16, 76.84, 55.68; HR-MS(ESI)m/z: Calcd for C8H7NO{[M+H]+}134.0604, found 134.0609。
2f:黄色液体,产率94%;1H NMR(400 MHz, CDCl3)δ: 7.57~6.97(m, 4H), 3.03(s, 3H);13C NMR(100 MHz, CDCl3)δ: 161.11, 134.43, 133.75, 120.74, 116.56, 111.24, 101.73, 55.91; HR-MS(ESI)m/z: Calcd for C8H7NO{[M+H]+}134.0604, found 134.0608。
2g:白色固体,产率84%;1H NMR(400 MHz, CDCl3)δ: 8.41~8.31(m, 2H), 7.94~7.85(m, 2H);13C NMR(100 MHz, CDCl3)δ: 150.11, 133.59, 124.37, 118.40, 116.90; HR-MS(ESI)m/z: Calcd for C7H4N2O2{[M+H]+}149.0346, found 149.0341。
2h:白色固体,产率89%;1H NMR(400 MHz, CDCl3)δ: 8.54(t,J=1.9 Hz, 1H), 8.48~8.44(m, 1H), 8.00~7.96(m, 1H), 7.74(t,J=8.0 Hz, 1H);13C NMR(100 MHz, CDCl3)δ: 161.12, 134.42, 133.73, 120.71, 116.57, 111.24, 101.73, 55.91; HR-MS(ESI)m/z: Calcd for C7H4N2O2{[M+H]+}149.0346, found 149.0342。
2i:白色固体,产率90%;1H NMR(400 MHz, CDCl3)δ: 7.60(d,J=8.0 Hz, 2H), 7.46(d,J=8.0 Hz, 2H);13C NMR(100 MHz, CDCl3)δ: 139.57, 133.34, 129.66, 117.92, 110.73; HR-MS(ESI)m/z: Calcd for C7H4ClN{[M+H]+}138.0105, found 138.0109。
2j:白色固体,产率94%;1H NMR(400 MHz, CDCl3)δ: 7.64(d,J=7.8 Hz, 2H,), 7.52(d,J=7.8 Hz, 2H);13C NMR(100 MHz, CDCl3)δ: 133.39, 132.63, 128.02, 118.07, 111.18; HR-MS(ESI)m/z: Calcd for C7H4BrN{[M+H]+}181.9600, found 181.9605。
2k:白色固体,产率88%;1H NMR(400 MHz, CDCl3)δ: 7.72~7.64(m, 2H), 7.49~7.43(m, 2H);13C NMR(100 MHz, CDCl3)δ: 134.39, 133.87, 133.19, 127.64, 125.28, 117.09, 115.89; HR-MS(ESI)m/z: Calcd for C7H4BrN{[M+H]+}181.9600, found 181.9606。
2l:白色固体,产率83%;1H NMR(400 MHz, CDCl3)δ: 7.73~7.64(m, 2H), 7.23~7.12(m, 2H);13C NMR(100 MHz, CDCl3)δ: 165.20, 134.83, 118.16, 117.01, 108.73; HR-MS(ESI)m/z: Calcd for C7H4FN{[M+H]+}122.0401, found 122.0408。
2m:黄色液体,产率87%;1H NMR(400 MHz, CDCl3)δ: 8.25(dd,J=8.1, 1.3 Hz, 1H), 8.09(dt,J=8.4, 1.1 Hz, 1H), 8.03~7.88(m, 2H), 7.67(dddd,J=23.6, 8.1, 6.9, 1.3 Hz, 2H), 7.53(dd,J=8.3, 7.2 Hz, 1H);13C NMR(100 MHz, CDCl3)δ: 133.42, 133.09, 132.78, 132.53, 128.80, 128.75, 127.70, 125.32, 125.07, 117.95, 110.37; HR-MS(ESI)m/z: Calcd for C11H7N{[M+H]+}154.0651, found 154.0657。
2n:黄色液体,产率95%;1H NMR(400 MHz, CDCl3)δ: 7.64~7.59(m, 5H), 7.46(s, 1H), 6.08(d,J=16.7 Hz, 1H);13C NMR(100 MHz, CDCl3)δ: 150.71, 133.75, 131.43, 129.34, 127.56, 118.37, 96.52; HR-MS(ESI)m/z: Calcd for C9H7N{[M+H]+}130.0651, found 130.0644。
2o:无色液体,产率86%;1H NMR(400 MHz, CDCl3)δ: 2.31(t,J=7.0 Hz, 2H), 1.66~1.59(m, 2H), 1.46~1.39(m, 2H), 1.33~1.26(m, 4H), 0.87(t,J=6.8 Hz, 3H);13C NMR(100 MHz, CDCl3)δ: 121.03, 30.80, 28.16, 25.16, 22.29, 16.54, 14.22; HR-MS(ESI)m/z: Calcd for C7H13N{[M+H]+}112.1121, found 112.1115。
2p:黄色液体,产率83%;1H NMR(400 MHz, CDCl3)δ: 2.80~2.78(m, 1H), 1.74~1.71(m, 2H), 1.54~1.46(m, 4H), 1.45~1.35(m, 4H);13C NMR(100 MHz, CDCl3)δ: 123.21, 29.20, 27.32, 25.14, 23.96; HR-MS(ESI)m/z: Calcd for C7H11N{[M+H]+}109.1680, found 109.1686。
2 结果与讨论
2.1 反应条件优化
选择苯甲醛(1a)与盐酸羟胺的反应为模板反应,研究了催化剂用、量反应温度和溶剂等因素对反应的影响,结果见表1~表3。
首先考察了不同溶剂DMF、DMSO、PEG-400、NMP、甲苯以及无溶剂条件对反应的影响。由表1可以看出,以甲苯为溶剂时,产率最低为13%(表1, entry 5),说明反应几乎不发生;在无溶剂条件下,产率适中(71%,表1, entry 6);以NMP为溶剂时,产率最高为92%(表1, entry 3),所以选择NMP为反应溶剂。然后,研究了催化剂用量对反应的影响。由表2可以看出,无催化剂时,反应不进行(表2, entry 1),当催化剂用量增加到0.10 g以上,产率没有发生变化(表2, entries 4~6)。最后,研究了温度对反应的影响。由表3可以看出,室温时,反应不发生(表3, entry 1),当温度升高到110 ℃时,产率最高(表3, entry 5),继续升高温度到120 ℃时,产率开始降低(表3, entry 6)。因此选择反应温度为110 ℃较适宜。
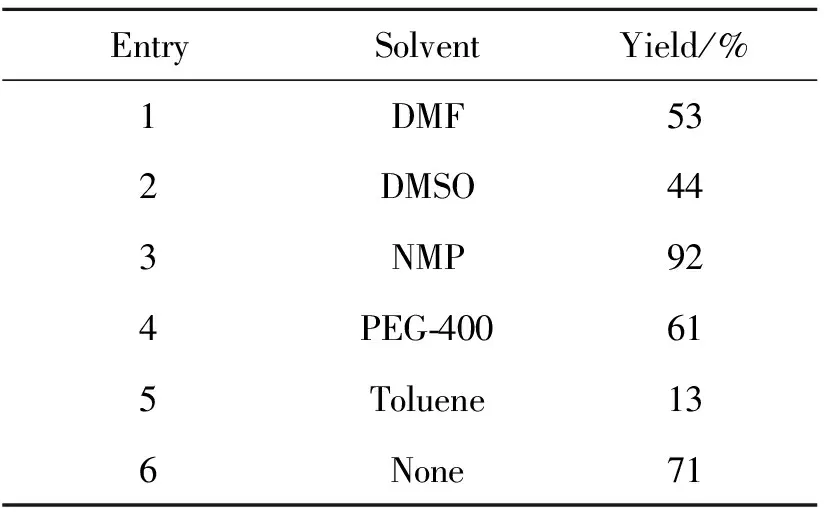
表1 溶剂对产率的影响*

表2 催化剂用量对产率的影响*
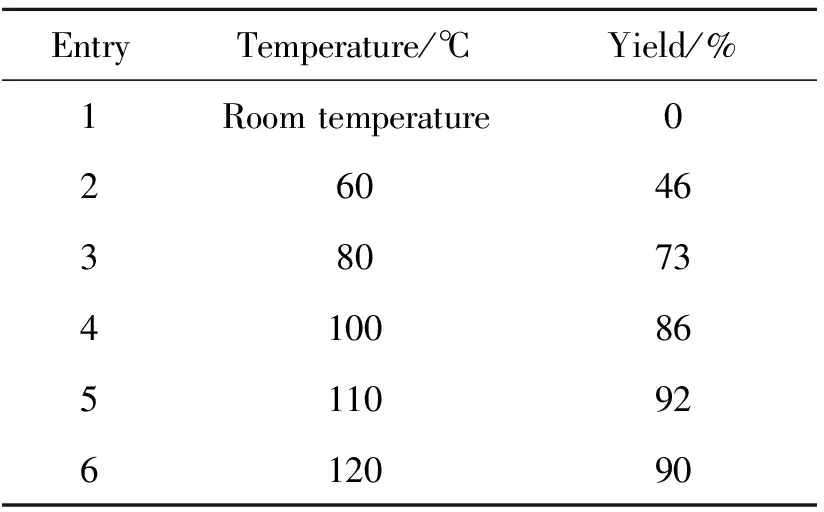
表3 温度对产率的影响*
腐殖酸作为催化剂,既环境友好又具有很好的热稳定性,反应结束后易于再利用,通过过滤便可以回收重复再使用。在优化条件下,研究了腐殖酸重复使用对苯甲醛与盐酸羟胺反应的影响。由表4可知,腐殖酸重复使用5次,催化效果依旧很好,说明腐殖酸是一种优良的可回收再使用催化剂。
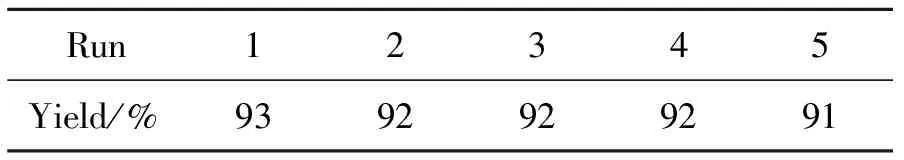
表4 腐殖酸催化剂重复使用情况*
2.2 底物拓展
确定了较佳反应条件后,以NMP为溶剂,反应温度为110 ℃,研究了腐殖酸催化不同醛和盐酸羟胺的一锅反应合成腈(Scheme 1)。由Scheme 1可以看出,腐殖酸对芳香醛、脂肪醛和α,β-不饱和醛都有很好的催化活性,所有反应都可以在5~8 min内完成,产率均在83%以上。对于芳香醛来说,苯环上的吸电子基有利于反应,而供电子基则不利于反应的进行。α,β-不饱和醛的产率为95%(Scheme 1,2n)。与芳香腈相比,脂肪腈产率较低(Scheme 1,2o和2p),但在5 min内反应可以完成。
N-甲基吡咯烷酮具有良好的化学稳定性和热稳定性,无腐蚀、毒性小、生物降解能力强、是一种环境友好的溶剂。腐殖酸也具有很好的热稳定性,是一种能回收并重复使用的绿色催化剂。本文报道的由醛与盐酸羟胺反应合成腈类化合物方法具有反应条件温和、反应时间短、产品产率高、催化剂环境友好等特点。
