微波辅助酸水解褐藻糖胶的研究
2022-06-16冯金华刘红英姜帅郑文静
冯金华 刘红英 姜帅 郑文静
摘要 [目的]研究微波辅助酸解在低分子量海带褐藻糖胶制备中的可行性。[方法]采用酸提取法制备海带褐藻糖胶,测定在不同HCl浓度(0、1、2 mol/L)、不同降解时间(40、50、60 min)、不同降解温度(70、80、90 ℃)条件下微波辅助酸解得到的褐藻糖胶的分子量,分析不同降解条件对褐藻糖胶分子量的影响,并与水浴辅助酸解的结果进行对比分析。[结果]随着HCl浓度、降解时间、降解温度的升高,酸解产物的分子量降低,且温度对降解产物分子量的影响最大。与水浴加热相比,微波辅助酸解降解产物的分子量更低。在80 ℃,HCl浓度为1 mol/L,降解40 min以上,比较容易制备低分子量褐藻糖胶。微波比水浴加热更容易对褐藻糖胶的硫酸基造成破坏。在2 mol/L HCl条件下,微波和水浴辅助酸解60 min,分别在70和90 ℃观察到明显的硫酸基脱除现象。[结论]采用微波辅助酸解法制备低分子量褐藻糖胶时,要注意硫酸基脱除的问题。
关键词 褐藻糖胶;酸解;微波辅助;分子量
中图分类号 TQ461 文献标识码 A 文章编号 0517-6611(2022)11-0154-05
doi:10.3969/j.issn.0517-6611.2022.11.040
开放科学(资源服务)标识码(OSID):
Study on Microwave-Assisted Acid Hydrolysis of Fucoidan
FENG Jin-hua1, LIU Hong-ying1, JIANG Shuai2 et al
(1. Ocean College of Hebei Agricultural University, Qinhuangdao,Hebei 066003;2. College of Fisheries and Life Science, Shanghai Ocean University, Shanghai 201306)
Abstract [Objective] To study the feasibility of microwave-assisted acidolysis in the preparation of low molecular weight kelp fucoidan. [Method]Kelp fucoidan was prepared by acid extraction. The molecular weight of fucoidan obtained by microwave-assisted acidolysis under different HCl concentration (0, 1, 2 mol/L), different degradation time (40, 50, 60 min) and different degradation temperature (70, 80, 90 ℃), was measured. The effects of different degradation conditions on the molecular weight of fucoidan were analyzed and compared with the results of water bath assisted acidolysis. [Result]With the increase of HCl concentration, degradation time and degradation temperature, the molecular weight of acid hydrolysis products decreased, and the temperature had the greatest influence on the molecular weight of degradation products.Compared with water bath heating, the molecular weight of microwave-assisted acid hydrolysis degradation products was lower. It was easy to prepare low molecular weight fucoidan at 80 ℃, HCl concentration of 1 mol/L and degradation for more than 40 min. Microwave was easier to destroy the sulfate group of fucoidan than water bath heating. Under the condition of 2 mol/L HCl, microwave and water bath assisted acidolysis for 60 min, obvious sulfate removal was observed at 70 ℃and 90 ℃ respectively. [Conclusion]When preparing low molecular weight fucoidan by microwave-assisted acidolysis, attention should be paid to the removal of sulfate group.
Key words Fucoidan;Acidolysis;Microwave-assisted;Molecular weight
褐藻糖膠是来自海洋褐藻的一种含硫酸酯的水溶性多糖,单糖组成主要为岩藻糖,所以又被称为岩藻聚糖硫酸酯[1]。除褐藻外,岩藻聚糖硫酸酯在无脊椎动物如海参中也存在[2-3]。褐藻糖胶已被证实是一种具有多种功能的多糖,如具有明显的抗氧化[1,4]、抗凝血[5]、免疫调节[6]、抗肿瘤[7-8]、抗病毒[9]、抗辐射[10]等功能。褐藻糖胶在日本、美国作为预防和治疗癌症及血栓疾病的药物已进入市场。在中国,研究发现褐藻糖胶治疗肾衰有一定作用,开发出海昆肾喜胶囊,已获得新药证书。褐藻糖胶对于单纯孢疹病毒、艾滋病病毒、烟草花叶病毒等病毒均有一定的抑制作用,加上褐藻糖胶具有明显的抗氧化活性及免疫调节活性,在治疗新冠肺炎感染上也可能具有一定的应用潜力。所以褐藻糖胶的研究有较大的应用前景和市场潜力。
褐藻糖胶的功效与其独特的多糖结构和相对分子质量有一定的关系。有研究认为,褐藻糖胶的分子量大小可以影响多糖的吸收效果,且吸收效率大致与分子量成反比[9],低分子量褐藻糖胶在很多情况下表现出比大分子量较好的生物活性[11-12],且低分子量褐藻糖胶具有黏度低、易吸收、生物利用率好等优点。所以低分子量褐藻糖胶也是目前的一个研究热点。
现在应用于制备低分子量褐藻糖胶的方法主要有酶降解法[13]、酸降解法[14]、H2O2降解法[15]和超声波降解法[16]等。物理方法辅助降解多糖已有很多报道,常用的为紫外线、γ射线、微波辐射等。与传统加热相比,发现微波辐射可以提高降解速率,改善反应条件,大大减少了反应时间,有利于节约能源。采用微波辅助降解褐藻糖胶,目前研究还比较少。笔者就微波辅助褐藻糖胶酸降解进行研究,通过比较在不同降解条件下微波辅助和水浴辅助盐酸降解褐藻糖胶所得降解产物的分子量和结构,探讨微波辅助酸降解在低分子量褐藻糖胶制备中应用的可行性。
1 材料与方法
1.1 试验材料
1.1.1 原材料。干海带,购买于河北省黄骅市市场。
1.1.2 主要仪器。FM100型高速万能粉碎机,由天津市泰斯特仪器有限公司生产;HH-8型恒温水浴锅,由江苏省金坛市荣华仪器制造有限公司生产;H185OR型台式高速冷冻离心机,由湖南湘仪实验室仪器开发有限公司生产;D2F-6050AB型电热真空干燥箱,由天津工兴实验室仪器有限公司生产;WGH-30A型双光束红外分光光度计,由天津港东科技发展股份有限公司生产;MDS-8G型微波消解仪,由上海新仪微波化学科技有限公司生产;78HW-1型恒温磁力搅拌器,由江苏省金坛市荣华仪器制造有限公司生产;FA2104N型精密分析电子天平,由上海菁海仪器有限公司生产;Scout SE型电子天平,由梅特勒-托利多国际贸易(上海)有限公司生产;DF-4型压片机,由天津港东科技发展股份有限公司生产;Agilent 1260型高效液相色谱仪,由美国安捷伦公司生产;示差检测器,由美国安捷伦公司生产;TSK G4000-PWXL和 TSK G3000-PWXL凝胶色谱柱,由日本TOSOH公司生产。
1.1.3 主要试剂。葡聚糖标准品,分子量 410 000、270 000、25 000、12 000、5 000和1 000 Da,由美国Sigma公司生产;溴化钾(AR),由天津天光光学仪器有限公司生产;盐酸(AR),由上海环发化工有限公司生产。
1.2 试验方法
1.2.1 褐藻糖胶的提取与纯化。海带清洗风干后粉碎至粉状,200 g海带粉中加入2 L 0.17 mol/L的盐酸溶液搅拌均匀。在70 ℃水浴锅中水浴1 h,离心后吸取上清液保留备用,沉淀再次用盐酸提取,重复3次,合并上清液,用NaOH调pH到中性,加热蒸发样品至1 250 mL,室温冷却后加540 mL无水乙醇(使无水乙醇体积分数为30%),保鲜膜封口静置过夜,离心去沉淀,继续加无水乙醇,使无水乙醇体积分数达到60%,离心取沉淀,干燥得褐藻糖胶粗品,干燥器中保存,备用。重复此酸提取过程,大量制备褐藻糖胶粗品,称重,贮存备用。
将褐藻糖胶粗品溶于蒸馏水中,加入无水乙醇至20%,离心去沉淀(除去溶解的褐藻酸和色素杂质),上清液再加入无水乙醇至其体积分数为60%,将褐藻糖胶沉淀出来,最后对沉淀物按0.886 g和9 mL水的比例溶解,加乙醇至30%,看是否有沉淀生成,如果离心后有沉淀,继续加入无水乙醇至体积分数为70%,使褐藻糖胶呈半胶体状态,按0.1 g NaCl/1 mL水的比例加入氯化钠使半胶体物质迅速絮凝,离心干燥得到呈褐色的砂状褐藻糖胶纯品。将褐藻糖膠纯品用水溶解,透析2 d,然后在透析后的褐藻糖胶溶液中加入无水乙醇使乙醇浓度为80%,密封静置一夜,离心,收集沉淀,60 ℃烘干,得到焦黄色褐藻糖胶块状儿纯品,称其质量,贮存备用[17]。
1.2.2 褐藻糖胶的降解。采用盐酸进行褐藻糖胶的降解。配制0.5%褐藻糖胶水溶液,并加入不同体积的浓盐酸使溶液呈酸性,进行水浴和微波辅助降解。降解条件分别为HCl浓度0、1、2 mol/L,降解时间40、50、60 min,降解温度70、80、90 ℃。
反应结束冷却至室温,将样品用NaOH中和至pH 7.0,并加入3倍乙醇,醇沉过夜,离心收集沉淀样品,干燥后称重,储存备用。
1.2.3 褐藻糖胶分子量表征。采用高效凝胶排阻色谱方法对褐藻糖胶原样及降解后的褐藻糖胶各样品进行分子量的检测[18]。
具体分析条件如下:色谱柱为TSK G4000-PWXL和TSK G3000-PWXL;流动相为0.2 mol/L醋酸/0.1 mol/L醋酸钠溶液;流速1 mL/min;柱温30 ℃;检测器为示差检测器。样品浓度为0.4%( W/V )。采用不同分子量的葡聚糖(410 000、270 000、25 000、12 000、5 000和1 000 Da)对凝胶色谱柱进行校准。
1.2.4 褐藻糖胶样品红外光谱分析(FT-IR)。采用KBr压片法,在WGH-30A型双光束红外分光光度计上对褐藻糖胶原样及降解后的褐藻糖胶样品进行分析,波长扫描范围4 000~400 cm-1,记录红外光谱图并分析。
2 结果与分析
2.1 褐藻糖胶的提取
4 000 g海带干粉共制备褐藻糖胶粗品78 g,产率为1.95%。粗品进一步经乙醇分级纯化、透析后,共得到褐藻糖胶纯品16 g,纯品产率为0.4%。
经检测,褐藻糖胶纯品平均相对分子量为2.660×105 Da。张全斌等[1]采用水提法制备的海带褐藻糖胶的平均分子量为10.890×105 Da。徐祖洪等[19]研究的从海带中制备褐藻糖胶的方法,得率为0.20%~0.35%,与该试验的研究结果相近。
2.2 降解时间对褐藻糖胶分子量的影响
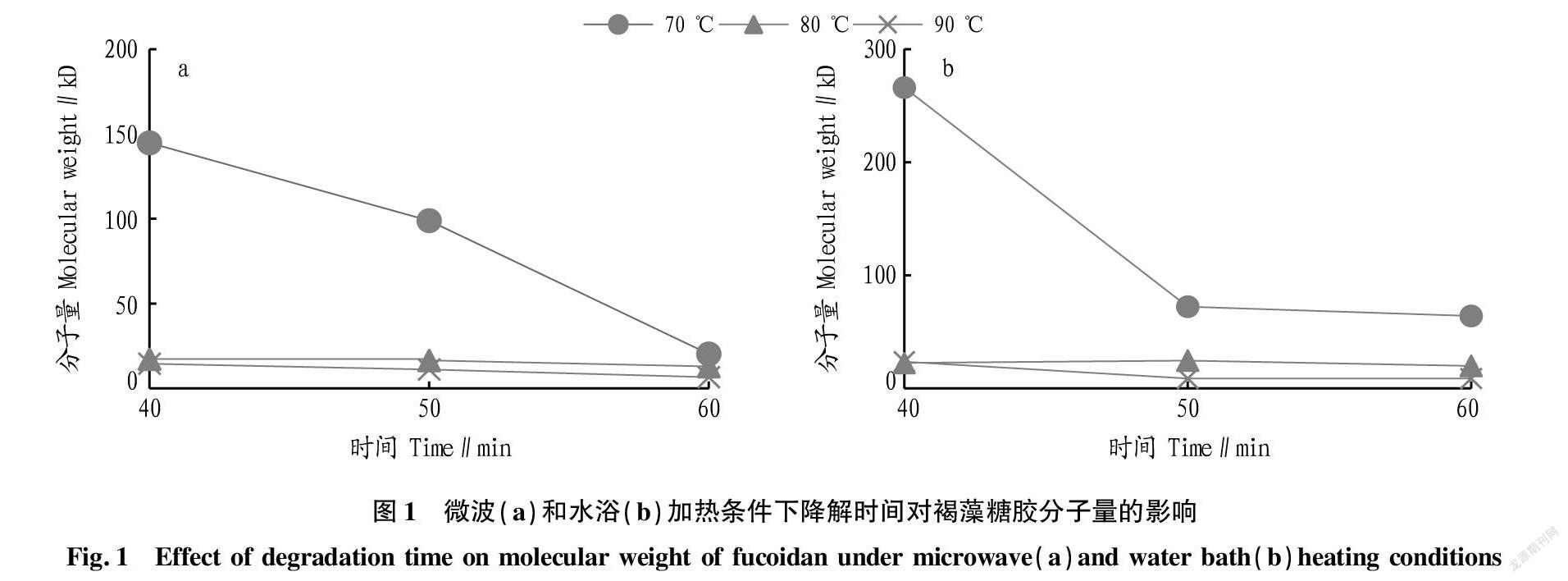
从图1可以看出,在HCl浓度为1 mol/L,降解温度分别为70、80、90 ℃时,在水浴加热和微波加热条件下,褐藻糖胶的分子量随着降解时间的延长都逐渐降低。但都是在70 ℃时褐藻糖胶的分子量随降解时间延长降低较明显,80和90 ℃时分子量的降低速度变慢。可能是由于在70 ℃、降解40 min时,降解后产品的分子量还比较高,微波和水浴加热条件下分别为144.730、265.990 kD,继续降解,分子量还有比较大的下降空间,而80 ℃、1 mol/L HCl降解40 min,分别降至17.289、22.515 kD,分子量较小,继续降解比较困难。由图1可知,微波加热比水浴加热对褐藻糖胶酸降解有更强的辅助降解作用;但是无论采用微波还是水浴加热,当温度为70 ℃、HCl浓度为1 mol/L、降解40 min时,对褐藻糖胶的降解程度均较小;在HCl浓度1 mol/L时,采用70 ℃、降解60 min以上,80、90 ℃降解40 min以上,都比较容易得到低分子量褐藻糖胶。
微波辅助酸解与水浴辅助酸解相比,在相同的降解条件下,降解后的褐藻糖胶的分子量数量级相似,不同点主要体现在:①同等条件下,微波辅助比水浴加热后的褐藻糖胶的分子量更低;②从分子量随降解时间延长的降低趋势来看,微波辅助酸解褐藻糖胶分子量变化趋势比较平缓,水浴加热的分子量变化趋势出现突变(如70、90 ℃趋势线),说明微波辅助加热比较均匀,水浴加热可能容易出现加热不均匀,造成降解效果出现微小偏差。
微波条件下,HCl 浓度为1 mol/L时,70 ℃,降解60 min以上,褐藻糖胶分子量降至20.268 kD;80 ℃,在60 min附近,分子量降至12.933 kD;90 ℃,在50 min左右,分子量降至11.117 kD,时间升至60 min时,分子量降至6.599 kD。
2.3 HCl浓度对褐藻糖胶分子量的影响
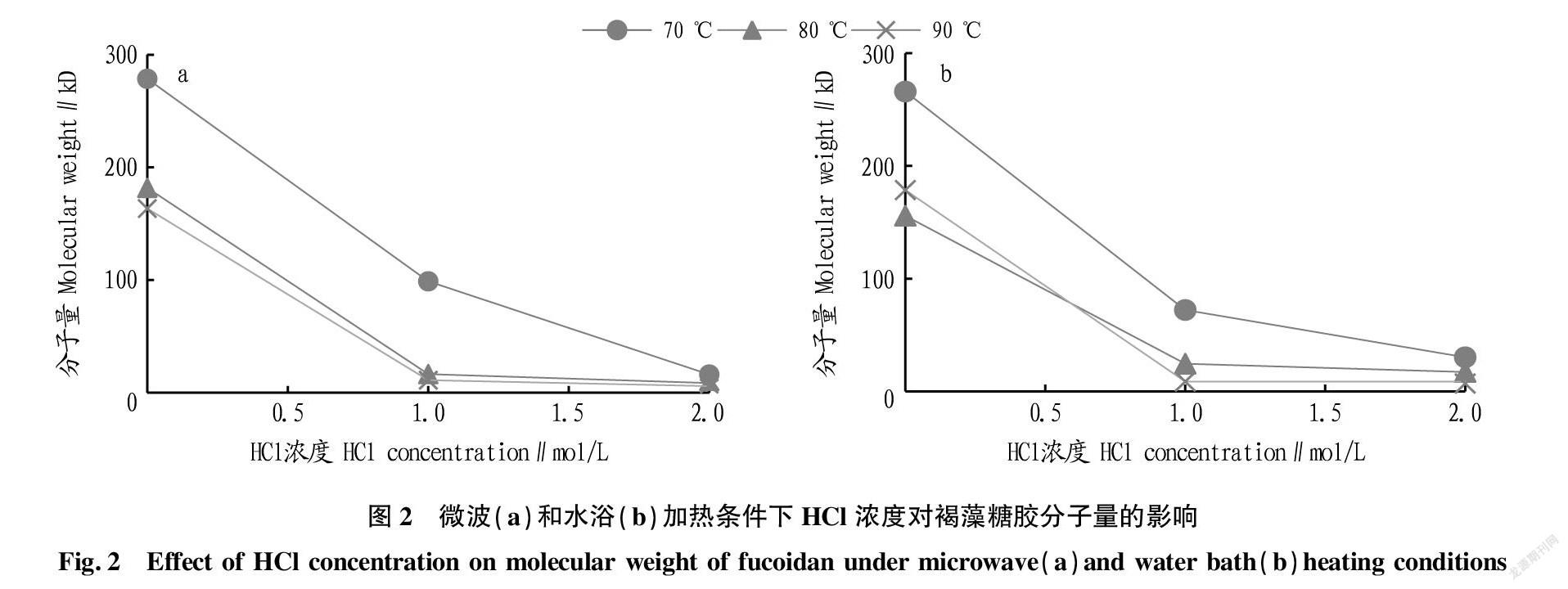
降解时间选择50 min,HCl浓度选择0、1、2 mol/L,考察褐藻糖胶分子量随酸度的变化趋势。从图2可以看出,在HCl浓度为0时,单纯的微波和水浴加热也会引起褐藻糖胶分子量的降低,降解温度和降解时间相同时,褐藻糖胶分子量在这2种加热方式下,降低程度相差不大。但是在2种加热条件下,70 ℃加热50 min,分子量与降解前(265.990 kD)相比,基本没降低;80 ℃加热50 min,不论是微波加热还是水浴加热,分子量降低开始明显;90 ℃加热50 min,分子量降低更明显。所以,在HCl浓度为0时,温度在80 ℃以上时,加热本身可以引起褐藻糖胶分子量比较明显的降低。说明褐藻糖胶水提取时,加热温度在低于70 ℃时,对褐藻糖胶分子量的影响较小。
在微波辅助条件下,随着HCl浓度的增加,褐藻糖胶分子量逐渐降低。HCl浓度从0升至1 mol/L,在70、80、90 ℃ 3个温度下分子量都迅速降低,分子量分别降低至98.869、16.497、11.117 kD。显然,80 ℃与70 ℃相比,分子量要低很多;80 ℃与90 ℃相比,差别不是特别明显。当HCl浓度从1 mol/L升至2 mol/L,70 ℃时,分子量降至16.134 kD,而80、90 ℃时,分子量分别降至8.560、5.836 kD。
从图2可以看出,在降解温度、降解时间、HCl浓度相同的条件下,与水浴辅助相比,微波辅助加热可使褐藻糖胶的分子量降至更低,但二者差距不大。采用微波加热,随降解温度升高,褐藻糖胶分子量逐渐降低,而水浴加热80 ℃的趋势线与90 ℃的趋势线出现交叉,可能是由于水浴不如微波加热均匀,所以使结果出现了微小偏差。
2.4 降解温度对褐藻糖胶分子量的影响
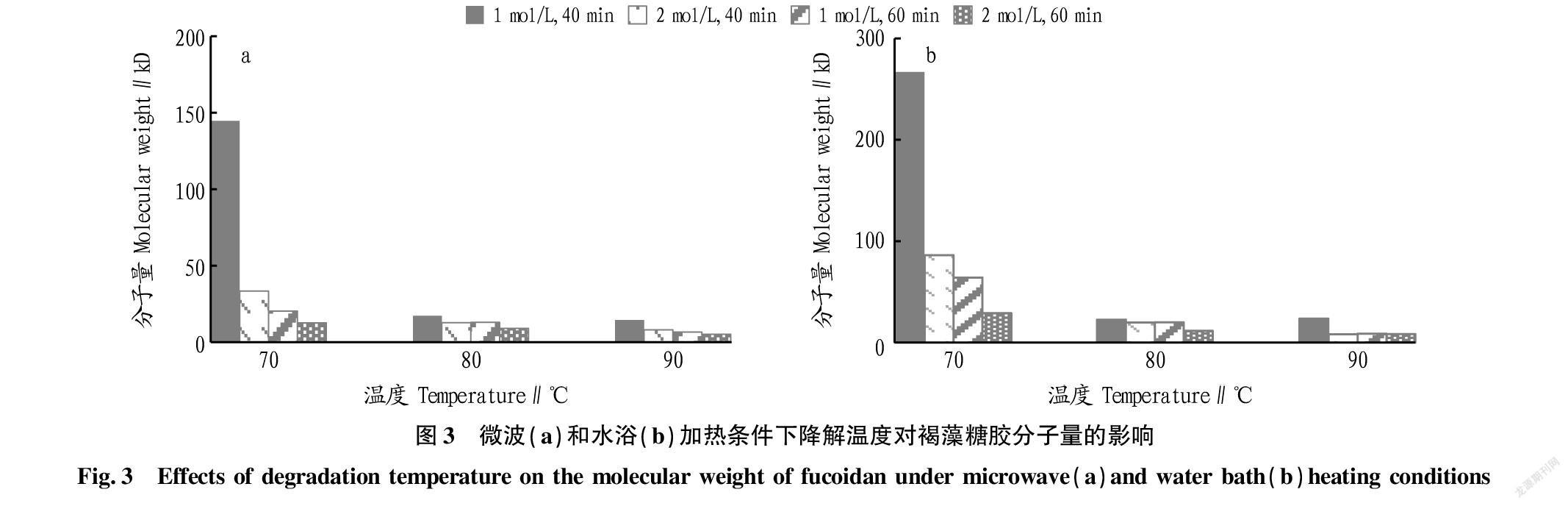
从图3可以看出,不论是微波辅助酸解还是水浴辅助酸解,在不同HCl浓度、降解时间和降解温度条件下,降解后褐藻糖胶分子量大小顺序基本是70 ℃>80 ℃>90 ℃,所以降解温度比降解时间和HCl浓度对褐藻糖胶分子量的影响可能要更大。
微波辅助加热时,2 mol/L、60 min条件下,70、80、90 ℃分别将褐藻糖胶从分子量265.990 kD降解至12.678、9.019、5.184 kD。水浴辅助加热时,2 mol/L、60 min条件下,70、80、90 ℃分别将褐藻糖胶从分子量265.990 kD降解至28.894、11.603、8.269 kD。从图3可以看出,微波辅助酸解与水浴辅助酸解相比,同等条件下分子量普遍可以降至更低。
2.5 红外光谱分析
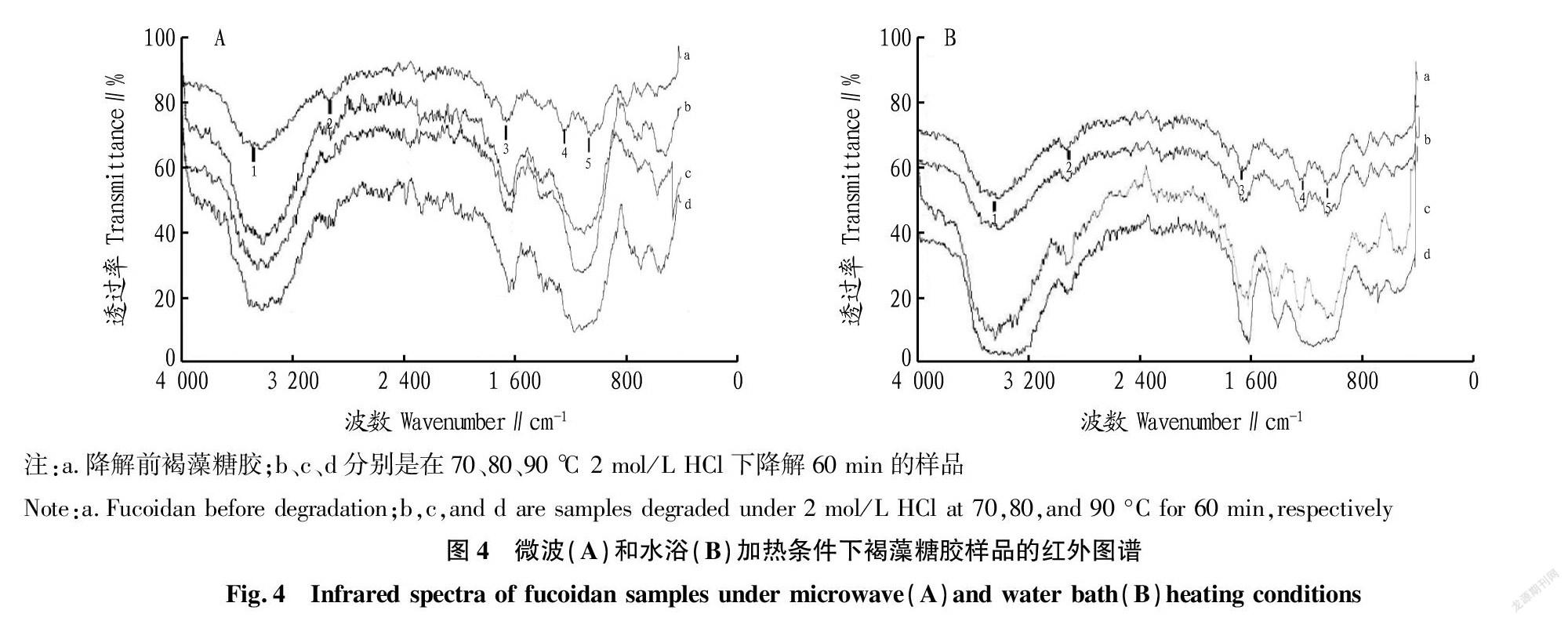
由图4可知,降解前,褐藻糖胶红外图谱有5个特征吸收峰,分别为峰1,3 438 cm-1的多糖的O—H伸缩振动吸收峰;峰2,2 930 cm-1的糖类的C—H伸缩吸收峰,也是岩藻糖中甲基的吸收峰;峰3,1 642 cm-1的多糖类物质常见的微量水分缔合羟基造成的吸收峰,也是糖醛酸的特征吸收峰;峰4,1 245 cm-1处的强峰为硫酸根基团的S==O伸缩振动吸收峰,这个峰说明物质中有硫酸基;峰5,1 046 cm-1处的吸收信号为C—O—C环内醚的C—O伸缩振动,是吡喃糖环的特征吸收峰,也是其糖苷键C—O—C的非对称伸缩振动峰。
从图4可以看出,不论是水浴加热辅助酸降解还是微波辅助酸降解,与降解前样品的红外图谱相比,各降解样品红外图谱中的峰1、峰2、峰3基本没有变化,主要变化发生在峰4和峰5。
水浴加热时,在HCl浓度为2 mol/L,70、80 ℃降解60 min,降解产物的红外图谱(b、c)与降解前样品的红外图谱(a)基本一样,即在这些条件下降解,样品结构基本没有变化;90 ℃降解60 min的样品的红外图谱(d)的变化比较大,峰4变得很小甚至消失,峰4和峰5变成一个宽峰;峰4是硫酸根基团的S==O伸缩振动吸收峰,这个峰的改變说明样品中硫酸根的变化;硫酸根在此条件下可能发生了脱除。
类似的变化也同样出现在微波辅助降解后的褐藻糖胶样品b、c和d的红外图谱中;3个样品的红外图谱中峰4都变得很小甚至消失,与峰5结合成了一个宽峰;说明微波辅助酸解褐藻糖胶使得褐藻糖胶的硫酸基基团发生了变化,很可能是发生了硫酸基脱除。
3 讨论与结论
酸水解是一种常用的降解多糖的方法。在酸水解法降解多糖时,可以选择无机酸和有机酸,而且一般选择辅助加热手段。辅助加热的常用方法有水浴加热和微波加热。该研究比较了酸解时采用水浴加热和微波辅助加热2种方式,在不同时间、温度和酸度下对褐藻糖胶的降解效果和差异。
该研究表明,在同等条件下,与传统水浴加热相比,微波辅助酸解可以使降解产物的分子量降到更低,而且样品加热更均匀。在2种加热条件下,随着HCl浓度、降解时间、降解温度的升高,褐藻糖胶分子量都逐渐降低,但是从数据可以看出,温度对褐藻糖胶分子量的影响比时间、酸度的影响要大。70、80、90 ℃,2 mol/L HCl条件下,降解60 min,微波和水浴加热,褐藻糖胶分别降至12.678、9.019、5.184和28.894、11.603、8.269 kD。
在该研究设定的条件下,最终降解产物的最低分子量与其他研究中报道的差不多。据报道,采用自由基方法,琥珀酸+H2O2+VC(CHV)体系降解海带硫酸多糖,分子量分别可以降至10 000~15 000 Da[20]。采用Harber-Weiss 反应体系和Fenton反应体系,分子量分别可达10 000和8 000 Da[12]。用Cu2+-H2O2自由基氧化体系降解褐藻糖胶,9.0%和4.5%H2O2氧化降解粗糖得到的低分子量糖在2 500~6 000 Da[21]。超临界CO2脱脂后的裙带菜提取的褐藻糖胶,应用微波辐射在110~200 ℃处理5~120 min,可将褐藻糖胶降解到低分子量范围(5~30 kD)[22]。
微波比水浴加热的反应速率快,在很多微波辅助多糖降解中都有报道。李克成[18]研究了微波輔助下H2O2氧化降解壳聚糖,微波下可以在低温低过氧化氢浓度的条件下降解壳聚糖,并且效率是传统加热条件下的5倍。裙带菜( Undaria pinnatifida )孢子叶中天然岩藻聚糖(5 100 kD),用0.01 mol/L HCl在沸水浴酸解5、15 min,岩藻聚糖硫酸酯的分子量分别降至490和260 kD;用0.01 mol/L HCl微波辅助加热90、120 s,分子量分别降至300和30 kD[23]。
从该研究结果看出,采用微波加热时,褐藻糖胶在2 mol/L HCl 70 ℃以上温度,酸解60 min,硫酸基的红外吸收峰有了明显的变化,采用水浴加热时,褐藻糖胶在2 mol/L HCl 70、80 ℃,酸解60 min,硫酸基的红外吸收峰没有明显的变化,90 ℃时硫酸基吸收峰也有了明显的变化。由此可见,不论是水浴还是微波辅助酸解,都有可能对产物的硫酸基的含量造成影响,都有可能造成硫酸基的脱除。而且微波比水浴辅助酸解更容易对褐藻糖胶的硫酸基造成破坏。微波辐射可以造成一些硫酸多糖硫酸基的脱除,在其他研究中也有相关报道。如微波法提取龙须菜琼胶时,发现随微波功率的增加,琼胶分子链上的硫酸基团脱除[24]。武晓琳等[25]研究海参岩藻聚糖硫酸酯的降解发现,酸降解法可以通过调节反应温度和酸浓度来控制反应速度,但重现性不好,并且存在着硫酸根脱落现象;酶解法反应条件温和,重现性好,不存在硫酸根脱落现象。Yang等[23]研究还发现,裙带菜孢子叶中天然岩藻聚糖(5 100 kD)用0.01 mol/L HCl在沸水浴酸解5 min制备的岩藻多糖聚合物(490 kD,1 mg/mL)能显著提高抗癌活性到75.9%;用0.01 mol/L HCl微波辅助加热90 s的产物对癌细胞的抑制作用甚至低于30%;推测可能是由于经苛刻的微波处理后岩藻多糖上硫酸盐的部分去除的原因。
所以虽然微波辅助酸解与水浴辅助酸解相比,在同等条件下,可以将褐藻糖胶降解到更低分子量,但要注意微波造成的降解产物中硫酸基含量降低的问题。可以通过控制降解时间、酸度、降解温度等来控制微波对褐藻糖胶硫酸基的破坏,或者将其作为一种制备低分子量褐藻糖胶的前期预处理手段使用。该研究可以为微波辅助酸解褐藻糖胶的应用提供一定的研究依据。
参考文献
[1] 张全斌,于鹏展,周革非,等.海带褐藻多糖硫酸酯的抗氧化活性研究[J].中草药,2003,34(9):824-826.
[2] 于龙.几种海参岩藻聚糖硫酸酯结构解析及构效关系初步研究[D].青岛:中国海洋大学,2014.
[3] 张珣,王静凤,徐雷,等.海地瓜和冰岛刺参海参岩藻聚糖硫酸酯抗肿瘤作用的比较研究[J].食品科学,2012,33(7):251-255.
[4] 崔艳秋,罗鼎真,王晓民.褐藻多糖硫酸酯的抗炎与抗氧化活性研究进展[J].药学学报,2008,43(12):1186-1189.
[5] 王春玲,张全斌.褐藻多糖硫酸酯抗凝血活性的研究[J].中国海洋药物,2005,24(5):36-38.
[6] 刘宪丽,刘东颖,汪艳秋,等.褐藻多糖硫酸酯免疫调节和抗肿瘤活性研究[J].中国微生态学杂志,2010,22(12):1074-1076.
[7] 付志飞,管华诗,刘红兵.褐藻糖胶的抗肿瘤作用及构效关系研究进展[J].中国海洋药物,2013,32(4):76-82.
[8] 张婷,薛美兰,刘佳,等.褐藻糖胶对乳腺肿瘤大鼠肠道屏障损伤的保护作用[J].营养学报,2018,40(1):59-63.
[9] 李芳.不同分子量海带岩藻聚糖硫酸酯消化吸收、免疫及抗病毒活性的比较研究[D].青岛:中国海洋大学,2012.
[10] 吴晓旻.褐藻糖胶抗辐射和抗白血病作用及其机制研究[D].武汉:武汉大学,2004.
[11] 李芳,李八方,董诗竹,等.低分子量海带岩藻聚糖硫酸酯的制备及流感病毒神经氨酸酶抑制活性研究[J].中国海洋大学学报(自然科学版),2012,42(S1):106-112.
[12] 刘静文,史姣霞,谢洁玲,等.海带低分子量岩藻聚糖硫酸酯的制备和抗血小板聚集活性研究[J].中国海洋药物,2017,36(1):19-26.
[13] 王雪迎.一种海洋硫酸多糖降解酶降解岩藻聚糖硫酸酯和糖胺聚糖的研究[D].青岛:中国海洋大学,2014.
[14] KARLSSON A,SINGH S K.Acid hydrolysis of sulphated polysaccharides.Desulphation and the effect on molecular mass[J].Carbohydr Polym,1999,38(1):7-15.
[15] 郭峰君,胡靖,赵雪.海带岩藻聚糖硫酸酯降解及基本结构分析[J].食品工业科技,2014,35(18):93-97.
[16] 郭欣.超声处理对海洋岩藻聚糖硫酸酯分子链及结构和抗氧化活性影響的研究[D].杭州:浙江大学,2014.
[17] BLACK W A P,DEWAR E T,WOODWARD F N.Manufacture of algal chemicals.IV-Laboratory-scale isolation of fucoidin from brown marine algae[J].J Sci Food Agric,1952,3(3):122-129.
[18] 李克成.单一聚合度和特定N-乙酰化壳寡糖的分离及抗氧化活性研究[D].青岛:中国科学院大学(中国科学院海洋研究所),2013.
[19] 徐祖洪,李智恩,张星君,等.褐藻多糖硫酸酯在制备治肾衰病药品中的应用:CN98120283.7[P].1999-09-22.
[20] 岳真.自由基降解海带硫酸多糖的研究[D].济南:山东大学,2006.
[21] 董诗竹.海带低分子量岩藻聚糖硫酸酯的制备及其抗血栓活性研究[D].青岛:中国海洋大学,2011.
[22] QUITAIN A T,KAI T,SASAKI M,et al.Microwave-hydrothermal extraction and degradation of fucoidan from supercritical carbon dioxide deoiled Undaria pinnatifida [J].Ind Eng Chem Res,2013,52(23):7940-7946.
[23] YANG C,CHUNG D,SHIN I S,et al.Effects of molecular weight and hydrolysis conditions on anticancer activity of fucoidans from sporophyll of Undaria pinnatifida [J].Int J Biol Macromol,2008,43(5):433-437.
[24] 王连杰,沈照鹏,穆惠敏,等.微波法提取龙须菜琼胶及其理化性质的研究[J].水产学报,2017,41(6):854-860.
[25] 武晓琳,常耀光,王静凤,等.不同分子量海参岩藻聚糖硫酸酯的制备及消化吸收特性的初步研究[J].中国海洋药物,2011,30(3):20-24.
