钢渣对Ni2+与Cu2+的竞争吸附研究
2022-06-15冯珊珊汪凯举章蓝月顾子萱李灿华
冯珊珊,汪凯举,章蓝月,顾子萱,李灿华,3
(1.安徽工业大学冶金工程学院,马鞍山 243000;2.宣城市宣城经开区科技创业服务中心,宣城 242000; 3.宣城市安工大工业技术研究院有限公司,宣城 242000)
0 引 言
重金属污染的废水很难通过生物降解,给生物环境造成极大污染[1]。常见的重金属废水处理技术主要包括化学法、物理化学法、生物法等[2]。吸附法作为一种物理化学法,处理重金属废水时具有成本低、工艺流程简单、不产生二次污染的特点。
钢渣由于成分复杂,其综合利用率仅为30%左右[3]。传统的直接堆存处理方式在浪费资源的同时会对环境造成污染,成为了钢企绿色生态治理的一大难题。然而,钢渣疏松多孔,具有较大的比表面积,在水溶液中易水解电离出Ca2+、Fe2+、OH-、羟基化基团SOH等,能快速高效地去除废水中重金属离子[4]。
近年来,国内外学者对钢渣分别吸附Ni2+与Cu2+进行了广泛研究。王士龙等[5]证明用钢渣吸附Ni2+可以达到很好的效果且温度对钢渣吸附Ni2+的影响很小。赵艳锋等[6]证明钢渣吸附Ni2+的效率在一定条件下可超过99%。Yusuf等[7]研究表明在1 000 mg·L-1初始浓度下,最佳Ni2+摄取量为160.92 mg·g-1,平衡时间为216 h。张从军等[8]证明用钢渣处理含Cu2+废水,Cu2+最优去除率可达99.14%。云玉攀等[9]研究表明钢渣吸附Cu2+的最佳投加量为50 g·L-1。
然而,由于Ni2+与Cu2+在废水中共存现象较普遍,现有的处理工艺很难将Ni2+与Cu2+分离[10]。为此,通过设定吸附条件并探究溶液中Ni2+与Cu2+对钢渣竞争吸附的现象,确定对一定浓度Ni2+废水中含有不同浓度Cu2+的最佳钢渣用量和其他最适条件,对废水中Ni2+与Cu2+分离研究提供一定的参考。
1 实 验
1.1 材 料
试验所用钢渣取自某钢铁集团有限公司,表1为钢渣的主要化学成分。试验前将钢渣磨碎,过200目(0.074 mm)筛筛分备用,经X-射线荧光光谱仪(XRF)测定分析其化学成分,结果见表1。

表1 钢渣的化学成分Table 1 Chemical compositions of steel slag
图1为钢渣的XRD谱。在30°~35°的位置一个较高峰,钢渣的物相组成主要取决于其化学成分,特别是其碱度(CaO/SiO2)[11]。通过分析可知本试验钢渣的物相极其复杂,主要是硅酸二钙(Ca2SiO4)、钙铁氧化物(Ca2Fe9O13、CaFe3O5)、钙和铁的固溶体(RO)等。
图2为过200目筛筛分的钢渣粒度分布图,小于74 μm的钢渣所占比例为99.53%。

图1 钢渣的XRD谱Fig.1 XRD pattern of steel slag
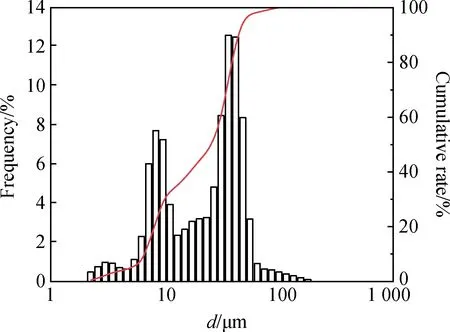
图2 钢渣的粒度分布图Fig.2 Particle size distribution of steel slag
表2为钢渣的BET分析数据,由数据可知,钢渣的比表面积为5.873 m2·g-1,表明钢渣具有一定的吸附位点,具有吸附的基本条件。

表2 钢渣的BET数据Table 2 BET dates of steel slag
1.2 主要仪器
DHG-9425A电热鼓风干燥机,FA2004型万分之一电子天平,PHS-3E型pH计,SM-500 TEST MILL型球磨机,DBS-300型顶击式标准筛振筛机,B13-3型智能恒温定时磁力搅拌器。
1.3 主要溶液配制
为了排除其他离子可能的干扰,配置溶液所采用的水均为去离子水。
含镍试液:称取分析纯硫酸镍(NiSO4·6H2O),充分溶解后移至容量瓶定容储存,此液含Ni2+浓度为500 mg·L-1。
含铜试液:称取分析纯硫酸铜(CuSO4·5H2O),充分溶解后移至容量瓶定容储存,此液含Cu2+浓度为100 mg·L-1。
混合溶液(含Ni2+、Cu2+试液):混合溶液的容量为100 mL,其中Ni2+的浓度为50 mg·L-1,量取10 mL含Ni2+试液,剩下的90 mL根据不同的变量分别量取稀释不同浓度的含Cu2+试液。
用0.1 mol·L-1的硫酸滴定配置酸性溶液。
1.4 试验方法
采用平行对照原则,设定的恒温定时磁力搅拌器速度为200 r·min-1。人工模拟Ni2+、Cu2+废水,控制单一变量,对吸附后的溶液进行过滤,使用电感耦合等离子体发射光谱仪(inductively coupled plasma, ICP)分析溶液剩余离子浓度。
确定钢渣与Ni2+的最适配比。取7份10 mL浓度为500 mg·L-1的硫酸镍溶液分别稀释至100 mL,依次投加0 g、0.05 g、0.075 g、0.10 g、0.125 g、0.15 g、0.20 g钢渣,在25 ℃的条件下用磁力搅拌器搅拌50 min。
确定钢渣吸附Ni2+的最佳时间,并用动力学吸附模型分析。取9份10 mL浓度为500 mg·L-1的硫酸镍溶液依次稀释至100 mL,均投加0.15 g钢渣,在25 ℃的条件下用磁力搅拌器分别搅拌1 min、3 min、5 min、10 min、15 min、20 min、25 min、30 min、40 min。
准一级动力学吸附方程为:
q=qe-exp(lnqe-k1t)
(1)
准二级动力学吸附方程为:
(2)
式中:qe为平衡吸附量,mg·g-1;t为吸附的时间, min;q为t时刻的吸附量,mg·g-1;k1为准一级吸附速率常数,min-1;k2为准二级吸附速率常数,g·mg-1·min-1
通过等温吸附模型来分析钢渣吸附Ni2+的过程。各取浓度为500 mg·L-1的硫酸镍溶液10 mL、15 mL、20 mL、25 mL、30 mL依次稀释至100 mL,得到浓度分别为50 mg·L-1、75 mg·L-1、100 mg·L-1、125 mg·L-1、150 mg·L-1的Ni2+溶液,均投加0.15 g钢渣,在25 ℃的条件下用磁力搅拌器搅拌50 min。
Langmuir等温式为:
(3)
Freundlich等温式为:
qe=kc1/n
(4)
式中:qe为平衡吸附量,mg·g-1;qm为饱和吸附量,mg·g-1;c为平衡浓度,mg·L-1;b为吸附系数;k为吸附系数;1/n为吸附强度。
试验探究Ni2+与Cu2+的竞争吸附关系。由于近些年来许多电镀镍废水Ni2+浓度低于50 mg/L[12-15],笔者主要取50 mg/L的镍溶液模拟工业废水进行试验分析。配置100 mL Ni2+浓度为50 mg/L,Cu2+浓度分别为10 mg/L、20 mg/L、30 mg/L、40 mg/L、50 mg/L的混合溶液,与100 mL Ni2+浓度为50 mg/L的溶液作吸附对照。分别投加0.15 g钢渣,在25 ℃的条件下用磁力搅拌器搅拌10 min、20 min、30 min、40 min、50 min。
试验探究酸性条件对钢渣吸附Ni2+与Cu2+的影响。由于电镀镍废水为酸性,且Cu2+在碱性条件下为沉淀,所以仅探究酸度的影响。配置100 mL Ni2+浓度与Cu2+浓度均为50 mg/L的混合溶液,用硫酸滴定,在25 ℃的条件下用磁力搅拌器搅拌30 min。
探究钢渣对Ni2+与Cu2+的吸附能力可以用吸附量和吸附率表示,吸附量和吸附率分别可以按照式(5)~(6)计算:
(5)
(6)
式中:qe为平衡吸附量,mg·g-1;V为溶液体积,L;η为吸附率,%;c0为初始浓度,mg·L-1;c为平衡浓度,mg·L-1。
2 结果与讨论
2.1 钢渣投加量的影响
图3为钢渣投加量对Ni2+吸附率的影响。当吸附时间为50 min,Ni2+浓度和溶液用量不变时,随着钢渣投加量的增多,Ni2+吸附率不断增大。投加量为0.15 g时,钢渣对Ni2+的吸附率为99.88%。确定钢渣的最适投加量为0.15 g。
2.2 动力学吸附
图4为钢渣吸附Ni2+的动力学方程拟合曲线。由图4可知,钢渣对Ni2+的吸附量随时间递增而增大,吸附速率先快后慢。在30 min时,钢渣对Ni2+的吸附率为99.88%,因此,确定钢渣吸附单一Ni2+溶液的最短时间为30 min。
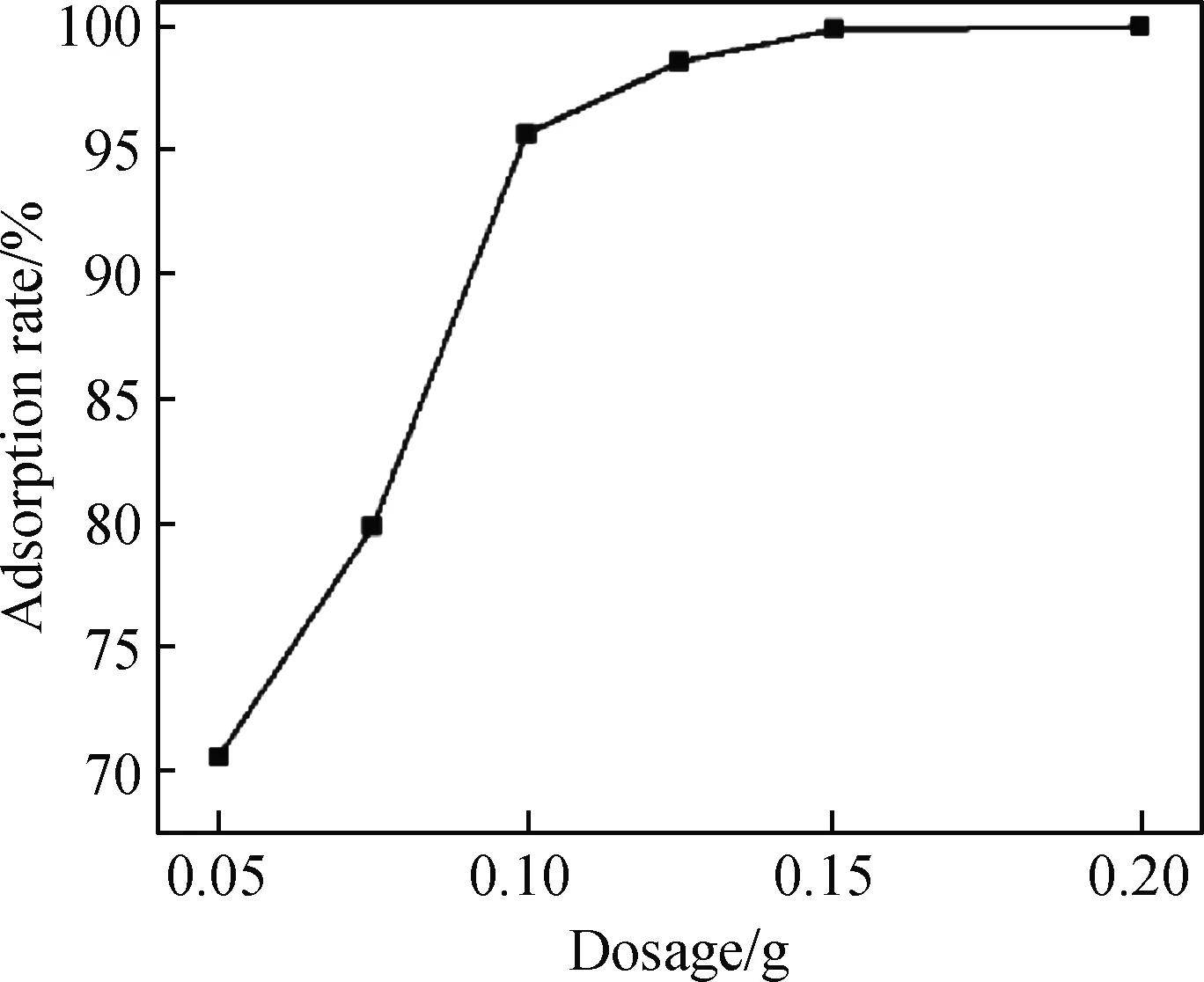
图3 钢渣投加量对Ni2+吸附率的影响Fig.3 Effect of steel slag dosage on Ni2+ adsorption rate
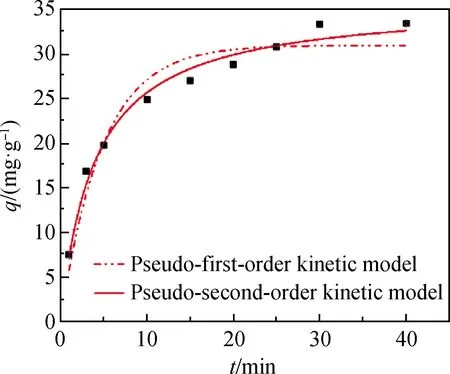
图4 钢渣吸附Ni2+的动力学方程拟合曲线Fig.4 Kinetic equation fitting curves of nickel adsorption by steel slag
利用试验数据拟合,得到钢渣吸附Ni2+的动力学模型基本参数见表3。试验测得的吸附量qexp为33.290 mg·g-1。准一级动力学方程拟合出的平衡吸附量qe=30.922 mg·g-1,R2=0.940;准二级动力学方程拟合出的平衡吸附量qe=34.813 mg·g-1,R2=0.984。综上可见,钢渣吸附Ni2+的过程更符合准二级动力学吸附方程。

表3 钢渣吸附Ni2+的动力学模型参数Table 3 Kinetic model parameters of Ni2+ adsorption by steel slag
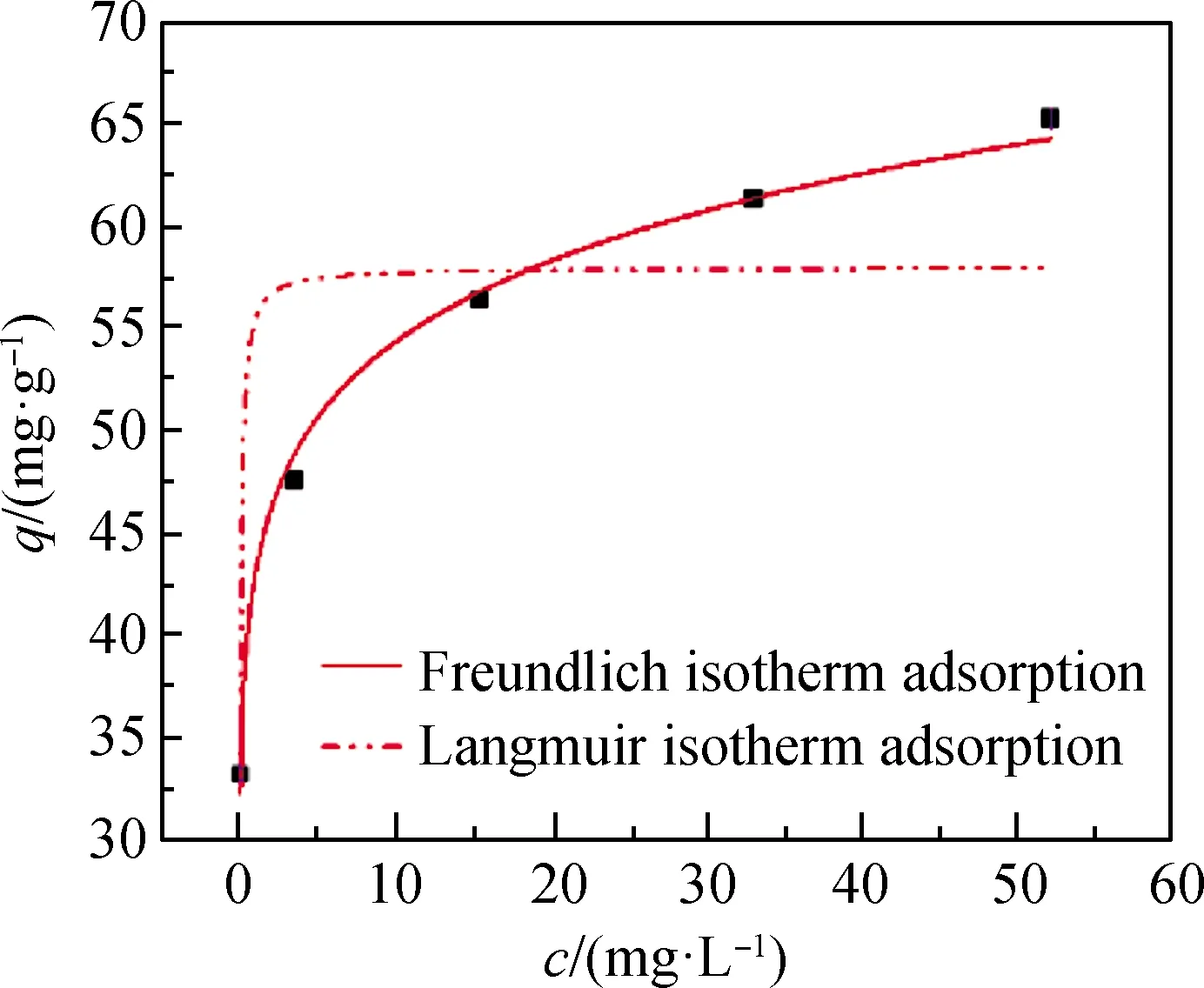
图5 钢渣吸附Ni2+的Freundlich和Langmuir吸附等温线Fig.5 Freundlich and Langmuir adsorption isotherms of Ni2+ on steel slag
2.3 等温吸附
图5为钢渣吸附Ni2+的Freundlich和Langmuir吸附等温线。在溶液浓度较低时,钢渣有许多吸附位点,随着Ni2+浓度的增加,钢渣吸附Ni2+的位点逐渐减少,曲线趋于平缓。
利用试验数据拟合,得到钢渣吸附Ni2+的等温吸附方程相关参数如表4所示,Freundlich和Langmuir的拟合系数分别是0.994,0.753。Freundlich等温式的相关系数n=9.856,即1/n=0.101,表示钢渣对单一水溶液中的Ni2+符合易发生吸附的多分子层吸附。综上可见,钢渣吸附Ni2+的过程符合Freundlich等温吸附模型。试验测得钢渣对Ni2+的实际饱和吸附量qe为70.66 mg·g-1,吸附时间为50 min。

表4 钢渣吸附Ni2+的等温吸附方程相关参数Table 4 Parameters of isothermal adsorption equation for Ni2+ adsorption by steel slag
2.4 竞争吸附
通过图6 Ni2+与Cu2+的竞争吸附情况可以发现,钢渣对Ni2+和Cu2+的吸附量总体随时间呈递增趋势。钢渣对Cu2+的吸附能力明显大于对Ni2+的吸附能力:在50 min时,5组溶液Cu2+的吸附率均达到100%,而Ni2+的吸附量分别是33.33 mg·g-1、33.25 mg·g-1、22.73 mg·g-1、18.57 mg·g-1、17.21 mg·g-1、11.22 mg·g-1,对应的吸附率分别是100%、99.76%、68.20%、55.72%、51.62%、33.66%。
在图6(b)和(c)中20~30 min钢渣对Ni2+的吸附量有递减趋势,存在较明显脱附现象,表明钢渣存在物理吸附。实际微观粒子的脱附现象应发生在该时间段之前,为15~25 min阶段。在15~25 min存在明显脱附,其原因可能是受磁力搅拌器作用的化学吸附过程中极性分子的极性减小,使部分以物理吸附方式吸附的Ni2+脱附,而钢渣吸附Cu2+的性能较好,Cu2+没有明显脱附现象。随着Cu2+浓度增加,Cu2+占据更多的吸附位点,使得钢渣对Ni2+的吸附能力下降。在图6(a)中Ni2+不存在明显脱附是因为钢渣比表面积较大,吸附位点较多,在图6(d)、(e)和(f)中Ni2+不存在明显脱附是因为钢渣对其吸附量较少。
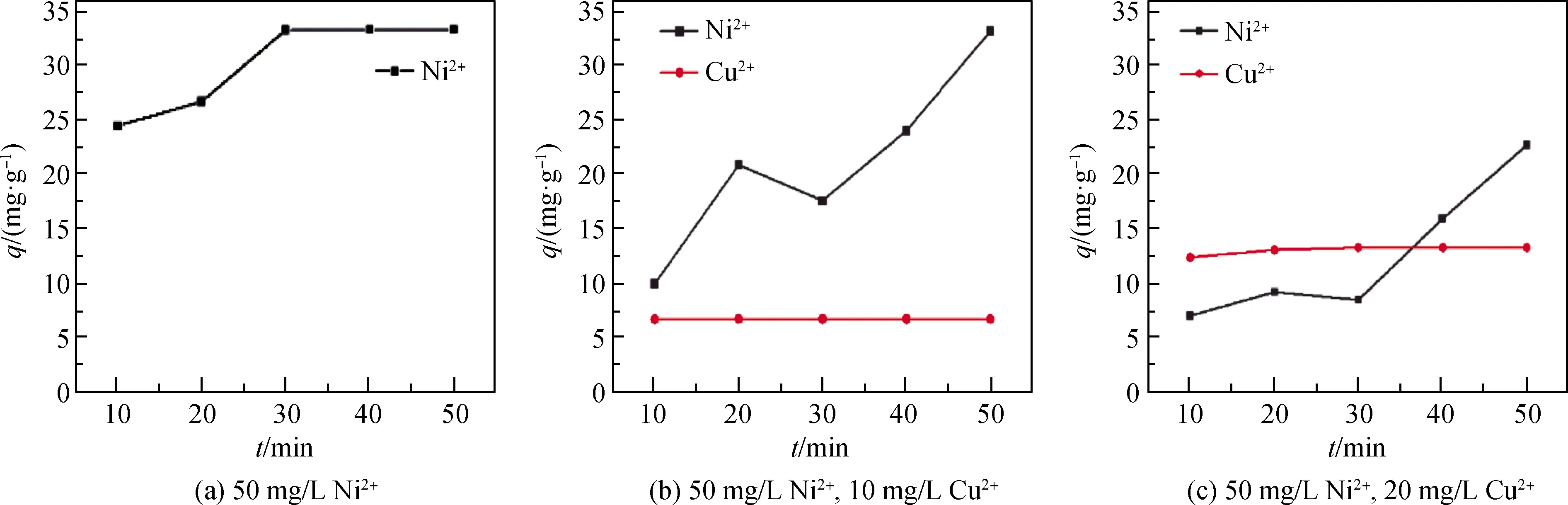
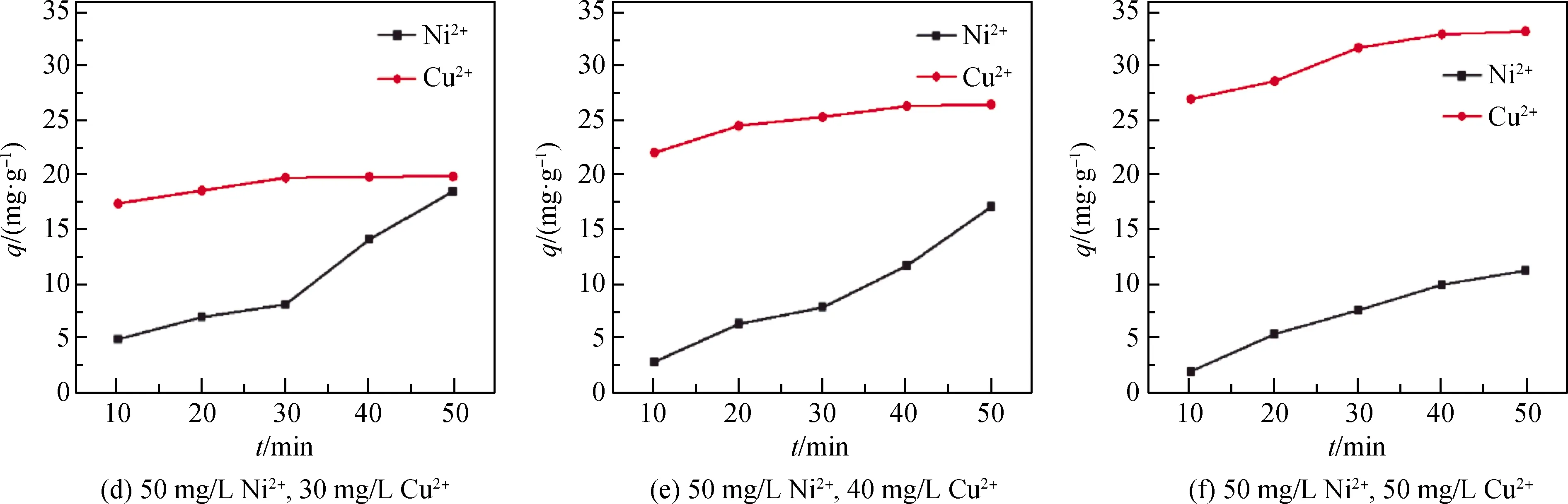
图6 Ni2+和Cu2+的竞争吸附情况Fig.6 Competitive adsorption of Ni2+ and Cu2+
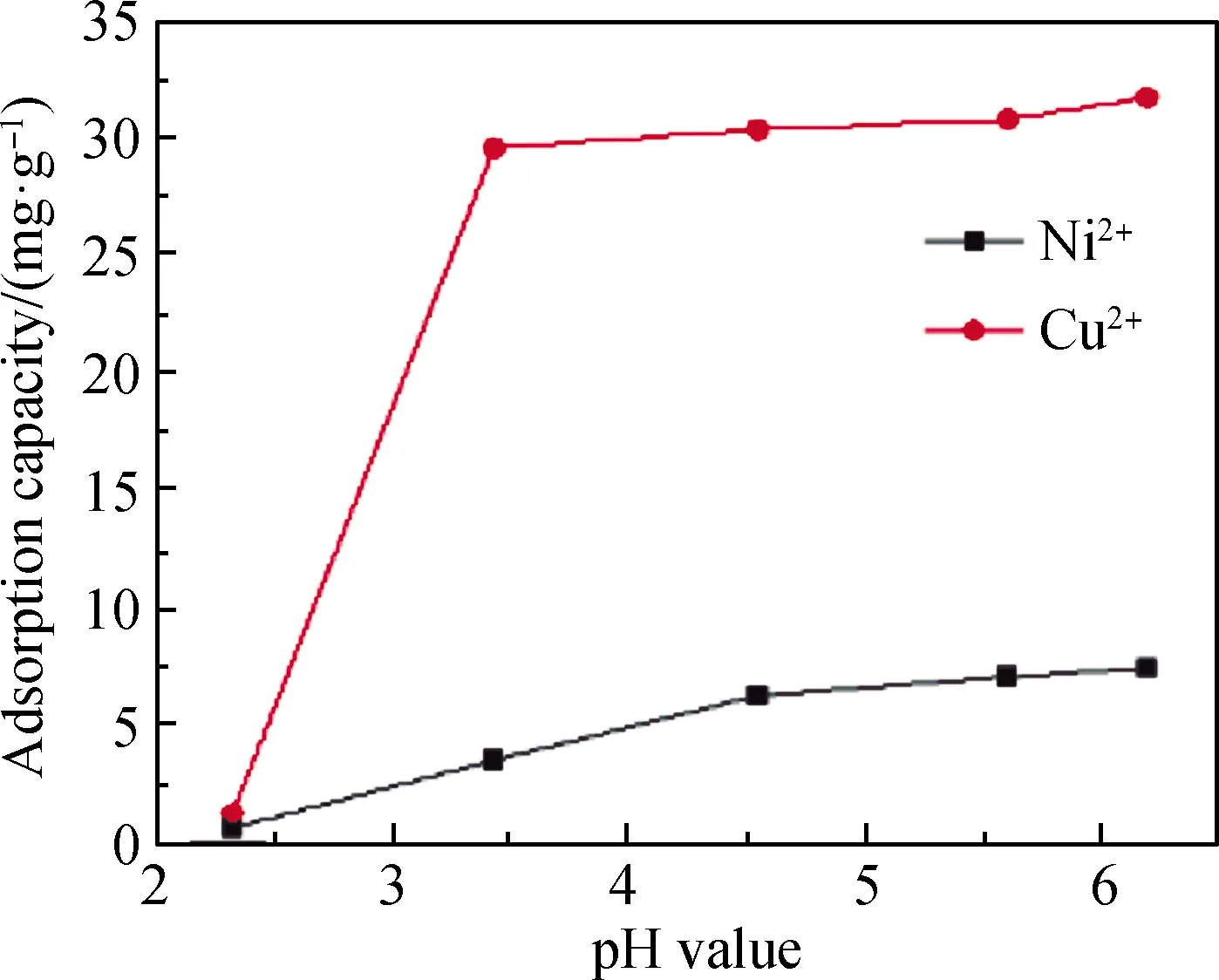
图7 酸度对钢渣吸附Ni2+和Cu2+的影响Fig.7 Effect of acidity on adsorption of Ni2+ and Cu2+ by steel slag
2.5 酸性条件的影响
酸度对钢渣吸附Ni2+和Cu2+的影响如图7所示。硫酸滴定Ni2+和Cu2+的混合溶液,吸附前pH值分别为2.32、3.43、4.55、5.61、6.20,吸附30 min后pH值分别为3.83、5.93、6.15、6.50、6.78。在酸性条件下,钢渣对Cu2+的吸附能力优于对Ni2+的吸附能力,钢渣对Ni2+和Cu2+的吸附能力随pH值升高而增强。pH值过低的情况下,钢渣对Ni2+和Cu2+的吸附效果都很差。当pH值从2.32过渡到3.43后,钢渣对Cu2+的吸附能力明显增强。钢渣去除重金属离子的效率在初始pH值较低时较低,但随着初始pH值增加而急剧增加并趋于稳定,与文献[16]所得结论一致。
2.6 SEM分析
图8为吸附前后钢渣的SEM照片和面扫描的EDS谱。图8(a)、(b)和(c)为放大5 000倍的SEM照片,图8(d)、(e)和(f)为放大15 000倍的SEM照片,其中,图8(a)和(d)为未作吸附处理的钢渣的SEM照片,图8(b)和(e)为吸附50 min浓度为50 mg·L-1的Ni2+溶液后的钢渣的SEM照片,图8(c)和(f)为吸附Cu2+与Ni2+混合溶液达到饱和后钢渣的SEM照片。图8(g)、(h)和(i)为面扫的EDS谱,分别对应着图8(a)、(b)和(c)。钢渣中含有大量的Ca以及Fe、Si、Al、Mg等,其物相极其复杂,未作处理前的钢渣呈棉状的絮凝态(见图8(d))。钢渣吸附是一个动态平衡过程,既存在化学吸附也存在物理吸附,化学吸附占主要作用。Ca在钢渣中的主要存在形式为钙硅酸盐相、钙与铝铁氧体相、游离钙的氧化物。研究发现吸附处理后Ca的含量远远低于处理前的,可能是在化学吸附过程中Ni2+和Cu2+置换出了钙硅酸盐相、钙与铝铁氧体相、游离钙的氧化物中的Ca;吸附后钢渣中的O含量升高,可能是水解后的OH-与金属元素形成了难溶解的沉淀。化学吸附方式主要为沉淀和阳离子交换,产物为Ni(OH)2与Cu(OH)2。吸附Ni2+后的钢渣一部分絮凝态被破坏,解离成了大量粒状的颗粒(见图8(e))。饱和吸附后的钢渣在显微观察下有趋于结晶的形态,呈针状(见图8(f))。

图8 吸附前后钢渣的SEM照片和EDS谱Fig.8 SEM images and EDS spectra of steel slag before and after adsorption
3 结 论
(1)25 ℃时,100 mL浓度为50 mg·L-1的Ni2+溶液,最佳的钢渣投入量与吸附时间分别是0.15 g、30 min,此时Ni2+的吸附率为99.88%。通过吸附动力学研究,钢渣吸附Ni2+符合准二级动力学模型,相关系数R2为0.984;通过等温吸附模型研究,钢渣吸附Ni2+符合Freundlich等温式,相关系数R2为0.994。
(2)钢渣物相组成复杂,表面呈棉状的絮凝态。钢渣吸附Ni2+的方式既存在化学吸附,也存在物理吸附,以化学吸附为主。Ni2+和Cu2+对钢渣吸附属于竞争吸附关系,且钢渣对Cu2+的吸附能力明显强于对Ni2+的吸附能力。随着Cu2+浓度的升高,钢渣对Ni2+的化学吸附逐渐取代物理吸附,即钢渣对Ni2+的物理吸附在吸附的前期更为明显。
(3)酸性条件对钢渣吸附Ni2+和Cu2+均有抑制作用。随pH值增大,钢渣吸附Ni2+和Cu2+的效果不断增强。
