影响新生儿并发高胆红素血症的危险因素分析
2022-06-15王利春
高 翠,王利春
(呼和浩特市第一医院新生儿科,内蒙古 呼和浩特 010030)
新生儿高胆红素血症多见于新生儿期,主要是由于新生儿体内胆红素大量积聚,导致胆红素水平高于正常参考范围,使新生儿出现较为严重的皮肤黏膜黄染。血清胆红素具有潜在神经毒性,由于新生儿血脑屏障尚未发育成熟,过多的血清间接胆红素可透过血脑屏障引起急性胆红素脑病,导致新生儿出现视听障碍、脑性瘫痪等严重神经系统后遗症[1]。因此高胆红素血症需要根据病因和病情严重程度及时进行治疗,避免新生儿脑神经出现不可逆性损伤。有研究显示,新生儿高胆红素血症会受到多种因素的影响,如产妇的孕周、产妇在妊娠期是否合并其他妊娠期疾病等,其中尤以围产因素最为突出,如果可以对新生儿高胆红素血症的发病风险进行较为有效的预测,可在一定程度上降低新生儿高胆红素血症的发病率,还可以有效减轻患病新生儿的病情严重程度[2-3]。基于此,本研究旨在探讨影响新生儿并发高胆红素血症的危险因素,为临床治疗提供参考价值,现报道如下。
1 资料与方法
1.1 一般资料 回顾性分析呼和浩特市第一医院2019年1月至2022年1月收治的97例高胆红素血症新生儿的临床资料,将其作为高胆红素血症组,另回顾性分析同期98例健康新生儿的相关临床资料,将其作为健康组。诊断标准:高胆红素血症组新生儿均符合《新生儿高胆红素血症诊断和治疗专家共识》[4]中的相关诊断标准。纳入标准:高胆红素血症组新生儿均符合上述诊断标准者;出生日龄≤ 7 d者;无遗传代谢性疾病者等。排除标准:先天发育畸形者;无法进行调研者;合并多种脏器功能性病变者;合并消化系统疾病者等。呼和浩特市第一医院医学伦理委员会审核并批准此研究。
1.2 研究方法 收集所有新生儿的相关资料,其中新生儿方面一般资料包括:是否为早产儿、性别(男性、女性)、出生时体质量(≤ 2.5 kg、> 2.5 kg)、是否缺乏母乳、是否胎儿窒息、是否合并新生儿感染、首次胎便排出时间(> 24 h、≤ 24 h),并分别抽取两组新生儿空腹静脉血3 mL,静置待其凝固,离心(离心时间15 min,离心半径8 cm,离心转速3 000 r/min)分离血清,采用全自动生化分析仪检测新生儿血清肝功能指标,主要包括血清天门冬氨酸氨基转移酶(AST)、丙氨酸氨基转移酶(ALT)、总胆红素(TBiL)水平;母体方面一般资料包括,母体是否胎膜早破、母体分娩方式(剖宫产、顺产)、产妇是否为妊娠期糖尿病、产妇是否为妊娠期高血压,是否为高龄产妇、产妇是否贫血等。
1.3 观察指标 ①单因素分析。对影响新生儿并发高胆红素血症的相关因素进行单因素分析。②通过多因素Logistic回归分析筛选影响新生儿并发高胆红素血症的危险因素。
1.4 统计学方法 采用SPSS 22.0统计软件分析数据,计量资料、计数资料分别以(±s)、[ 例(%)]表示,组间比较分别行t、χ2检验;采用多因素Logistic回归模型进行危险因素分析。以P<0.05表示差异有统计学意义。
2 结果
2.1 单因素分析 单因素分析结果显示,高胆红素血症组为早产儿、出生时体质量≤ 2.5 kg、缺乏母乳、胎膜早破、胎儿窒息、新生儿感染、首次胎便排出时间> 24 h的新生儿占比及血清AST水平均显著高于健康组,差异均有统计学意义(均P<0.05),见表1。
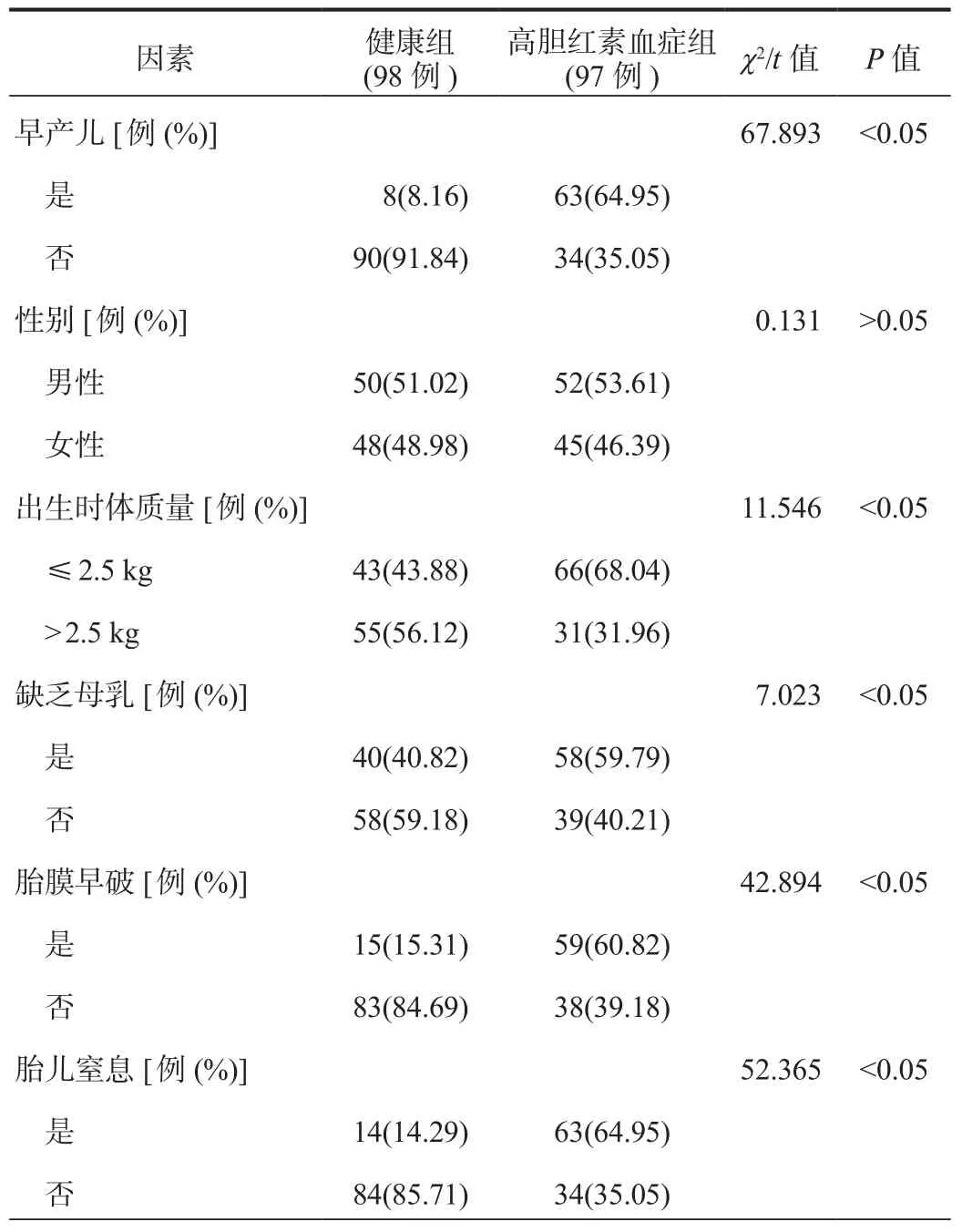
表1 影响新生儿并发高胆红素血症的单因素分析
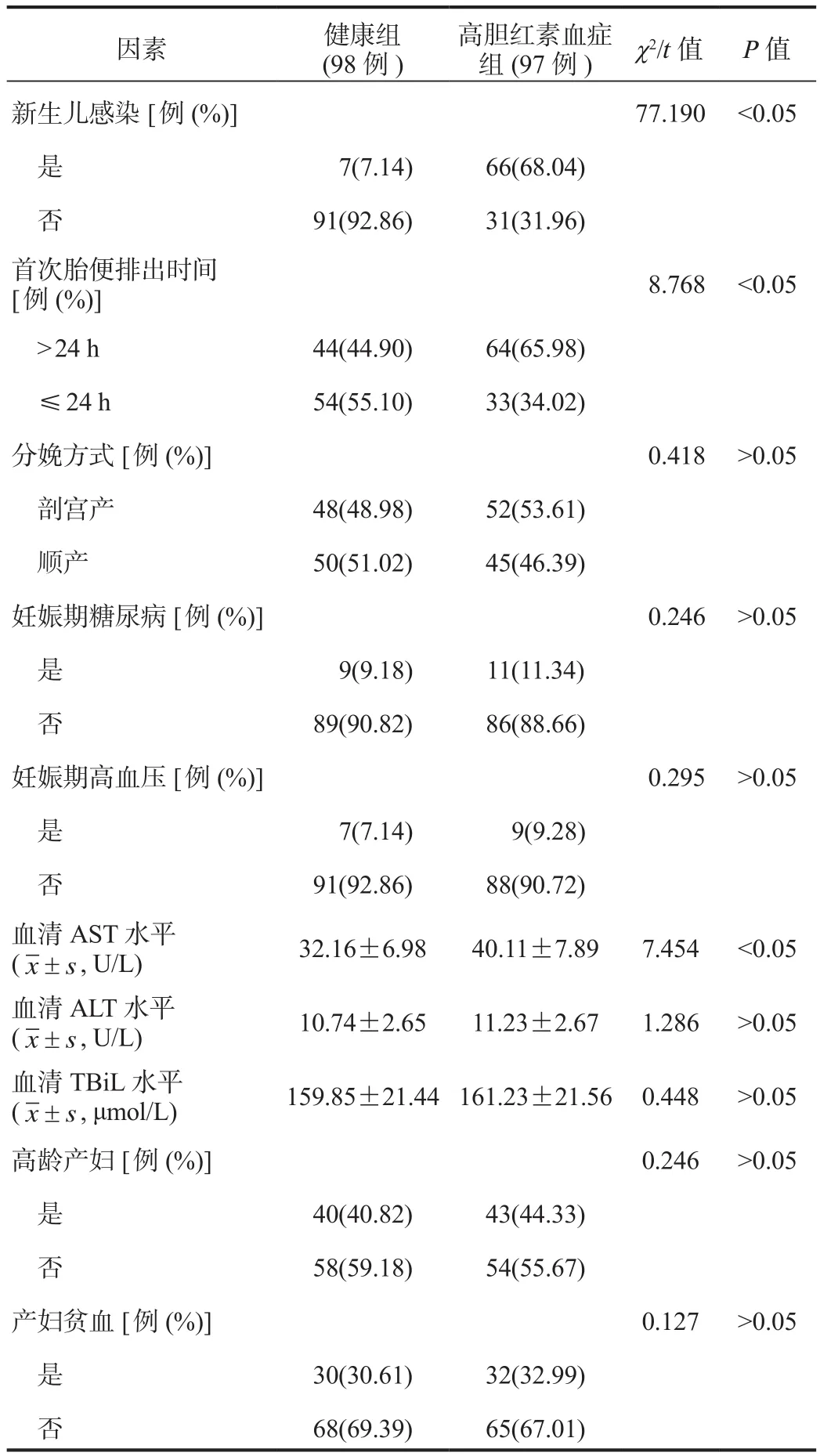
续表1
2.2 多因素Logistic回归分析 以单因素分析中差异有统计学意义的指标作为自变量,是否并发高胆红素血症为因变量,进行多因素Logistic回归分析,结果显示,出生时体质量≤ 2.5 kg、血清AST水平偏高、早产儿、胎儿窒息、新生儿感染、首次胎便排出时间 > 24 h、母乳缺乏、胎膜早破均为导致新生儿并发高胆红素血症的独立危险因素,差异均有统计学意义(OR= 1.436、1.530、1.470、1.501、1.754、1.684、1.640、1.531,均P<0.05),见表 2。

表2 影响新生儿并发高胆红素血症的多因素Logistic回归分析
3 讨论
新生儿高胆红素产生的原因可能是新生儿出后在适应环境的过程中,红细胞损伤较为严重,导致产生的胆红素水平升高。一般症状比较轻的新生儿可能只需要蓝光照射进行治疗,而较为严重者的新生儿,需要输注人免疫球蛋白和白蛋白,更严重者则可能引起胆红素脑病,致使新生儿出现不可逆性的脑损伤[5]。此外,高胆红素血症还可影响新生儿的全身器官,并可对新生儿的心肌细胞、免疫功能、肾功能等产生危害,故临床对其危险因素的评估尤为重要。及时有效了解影响新生儿并发高胆红素血症的相关因素并对此采取相应措施,以便对其进行预防,还有利于减少新生儿高胆红素血症的发生,降低胆红素脑病、神经性脑病等并发症的发生风险。
本研究多因素Logistic回归分析结果显示,出生时体质量≤ 2.5 kg、血清AST水平偏高、早产儿、胎儿窒息、新生儿感染、首次胎便排出时间 > 24 h、母乳缺乏、胎膜早破均为导致新生儿并发高胆红素血症的独立危险因素,与张微等[6]研究结果相符。分析其原因在于,新生儿刚出生时的体质量较低,意味着新生儿体内各个部位的器官均没有发育完善,尤其肝脏功能较正常新生儿差,导致低体质量的新生儿肝细胞处理肝内胆红素的能力相对较差,因此发生高胆红素血症的风险相对较高[7]。针对出生时体质量过低的新生儿,应予以一定的营养支持,帮助完善新生儿体内脏器系统,从而降低高胆红素血症的发生率。血清AST主要存在于心、肝脏等部位,当其在人体内水平过高时提示肝细胞受到损害,使肝脏功能较为低下,因此发生高胆红素血症的概率相对较高[8]。临床医师应及时对新生儿体内的血清AST水平进行监控,必要时可使用肝酶诱导剂、血红素加氧酶抑制剂等帮助提高新生儿体内肝脏功能,最终达到减少高胆红素血症发生的目的。早产儿机体内的血清胆红素代谢反应不完全,新生儿体内葡萄糖醛酸转移酶含量低,故生理性高胆红素血症维持时间长,症状相对严重,因而高胆红素血症的发病风险较高[9]。对于早产儿更应对其体内胆红素水平进行监测,以降低高胆红素血症的发生率。胎儿窒息而引起的缺氧会对新生儿机体内的血清白蛋白与非结合胆红素的结合发挥抑制的作用,从而致使新生儿体内的胆红素增加,对于未结合的胆红素会进入到脑部,最终增加胆红素脑病的风险[10]。因此在帮助产妇进行生产时,应选择合适的生产方式,尽量避免造成胎儿窒息情况的发生。由于新生儿免疫功能不完善,机体抗感染能力低下,一旦遭受细菌、病毒感染,细胞膜受到破坏,从而引发溶血,影响葡萄糖醛酸转移酶的活性,使肝脏对胆红素的代谢能力下降,生成过多的胆红素;且感染较为严重的新生儿还会增加机体耗氧量,引发代谢性酸中毒,降低胆红素代谢活性,从而诱发高胆红素血症。因此在新生儿住院期间应做好产房消毒隔离工作,尽量避免新生儿出现感染情况,以减少高胆红素血症的出现。当新生儿首次胎便排出时间>24 h时,会导致其体内胆红素的排出量降低,而胆红素经肠肝循环吸收进入血液量则随之增加,提高了高胆红素血症发生的风险[11]。母乳缺乏会对新生儿的摄乳量产生影响,降低新生儿液体量,减少能量的摄入,阻碍了肠胃的蠕动,使肠肝循环增加,最终造成高胆红素血症的发生[12]。因此临床应及时指导产妇掌握正确的母乳喂养方法和分泌母乳的方法,以保证新生儿摄入足够的奶量,而充足的奶量便于胎便及时排出,避免了肠肝循环负荷过重,从而有利于减少胆红素经肠道的吸收,降低了新生儿高胆红素血症的发生率。胎膜早破后由于细菌上行,可使羊水受到污染,若未能及时给予抗感染治疗则可能引发胎儿宫内感染,感染后病情变化快,少数严重感染的新生儿还可能发生败血症,而新生儿败血症的重要表现即是高胆红素血症[13]。针对胎膜早破的孕妇,应及时予以抗感染治疗以帮助降低新生儿高胆红素血症的发生率。
综上,出生时体质量≤ 2.5 kg、血清AST水平偏高、早产儿、胎儿窒息、新生儿感染、首次胎便排出时间 > 24 h、母乳缺乏、胎膜早破均为导致新生儿并发高胆红素血症的独立危险因素,因此临床医师应加强对以上各个因素的监控,并进行专业的临床指导,以降低新生儿并发高胆红素血症的发生率。
