高稳定性金红石型TiO2-SiO2载体的制备及表征
2022-06-13潘喜强李玉洁陈雪莲
潘喜强,韦 萌,李玉洁,陈雪莲,李 飞
(1.西北化工研究院有限公司,陕西 西安 710061;2.西安石油大学材料科学与工程学院,陕西 西安 710065)
在二氧化钛所有晶型中,金红石相是热力学最稳定的,传统金红石型二氧化钛的制备需经高温固相反应,经历无定形、锐钛矿、金红石的转化过程[1-2]。经过高温焙烧后的二氧化钛往往烧结严重,颗粒尺寸增大,甚至变成无孔材料[3-4]。然而,在锂离子电池、光催化、工业催化等应用领域内,为了提高应用性能,往往要求金红石二氧化钛具有纳米尺寸以及高比表面积[1,5-8]。因此,制备具有高比表面积金红石型纳米二氧化钛,并保持高温稳定性十分具有挑战性。
利用纳米尺寸效应改变晶型转变顺序,低温液相法实现了低温合成金红石型纳米二氧化钛,可以有效提高金红石型二氧化钛比表面积[9-11]。Zhang Qinghong等[10]通过中低温水热法制备了棒、球和花生形状等形貌的纯金红石型二氧化钛,最小晶粒尺寸达到7.3 nm,最大比表面积202.2 m2·g-1。Kim S J等[11]采用低温均匀沉淀法,将TiOCl2水解温度控制在室温~65 ℃,制备了直径(200~400) nm的纯金红石型纳米TiO2。虽然低温液相合成解决了高比表面积金红石型二氧化钛的制备难题,但是小粒径(<15 nm)的纳米金红石二氧化钛具有较高的表面能,热稳定性显著降低,限制了其高温应用性能[3,12-13]。
复合结构对TiO2粒子的分散和稳定十分有益,活性炭、沸石和SiO2等多孔材料通常与TiO2复合以获得高比表面积以及高温稳定性[14-17]。Yener H B等[14-15]采用TiCl4快速水解法将金红石TiO2负载在沸石和SiO2表面,提高了TiO2的分散性。但是该方法采用预制的微米级多孔材料,然后再负载形成复合物,不仅复合结构受多孔材料的颗粒尺寸影响较大,而且负载量可调节范围较窄,无法合成高TiO2含量的复合物。溶胶-凝胶法是制备多孔材料的常用手段,制备条件可调范围广,得到的凝胶材料具有高比表面积,且易于得到多组分材料[18]。与Yener H B等[15]采用的微米级SiO2颗粒负载TiO2相比,SiO2溶胶颗粒大小一般为(1~5) nm,且在溶液中分散均匀,是分散TiO2纳米粒子的理想材料。本文结合了低温均匀沉淀法和溶胶-凝胶法的优点,首先采用低温均匀沉淀法制备金红石TiO2纳米颗粒,然后在溶胶-凝胶法制备SiO2凝胶的过程中,将TiO2纳米颗粒在溶胶溶液中分散,最后通过凝胶化制备高分散性TiO2-SiO2复合物载体,并考察了TiO2-SiO2载体的高温稳定性。
1 实验部分
1.1 TiO2-SiO2载体制备
实验用四氯化钛、正硅酸乙酯、乙醇、盐酸、氨水均为分析纯,购自国药集团化学试剂有限公司。参照低温均匀沉淀法制备纯金红石型TiO2纳米颗粒[19]:首先,在冰浴条件下,将TiCl4缓慢加入去离子水中,配置成0.5 mol·L-1的 TiOCl2溶液;将50 mL 0.5 mol·L-1的TiOCl2溶液加入三口烧瓶中,然后在油浴中加热到80 ℃并反应6 h,待溶液冷却后,离心分离沉淀物,用蒸馏水和乙醇各洗3次,80 ℃烘干即得到纯TiO2粉末。
采用溶胶凝胶法制备TiO2-SiO2载体[20]:按照正硅酸乙酯(TEOS)、乙醇、去离子水物质的量比为1∶7∶4 配制TEOS溶液。然后将配制的TEOS溶液与上述的纯TiO2粉末进行混合,混合过程中TiO2的用量保持不变,只改变TEOS的浓度,使得TiO2/SiO2的质量比分别为0.1、0.2、0.4和0.6。将混合后的溶液超声分散,然后在磁力搅拌下用0.2 mol·L-1的盐酸将其pH调节至2,继续搅拌2 h形成溶胶溶液。随后逐滴加入2 mol·L-1氨水使溶胶溶液快速凝胶化,陈化3天后,在70 ℃下干燥即得到TiO2-SiO2载体,样品编号分别为0.1TiO2-SiO2、0.2TiO2-SiO2、0.4TiO2-SiO2、0.6TiO2-SiO2。
1.2 TiO2-SiO2表征
比表面积与孔径分析采用美国康塔仪器公司NOVA4200,样品测试前200 ℃真空处理4 h。
粉末X射线衍射表征(XRD)采用荷兰帕纳科X’Pert Powder测定,Cu Kα,工作电压40 kV,工作电流40 mA,步长0.02°,扫描范围2θ=10°~80°。
样品的微观形貌采用日立SU-8010场发射扫描电子显微镜(SEM)测定。
傅里叶变换红外光谱(FT-IR)采用布鲁克Vertex 70v测试,粉末样品与溴化钾混合压片后测试吸收光谱。
紫外-可见漫反射光谱(UV-vis DRS)采用岛津UV-2700型分光光度计,测量样品的相对反射率。
1.3 热稳定性评价
样品烧结实验:采用程序升温控制的马弗炉,将TiO2-SiO2载体粉末在不同温度下焙烧一定时间,升温速率为5 ℃·min-1,然后分析和表征烧结前后样品,研究不同样品的热稳定性。
2 结果与讨论
2.1 TiO2-SiO2载体结构表征
图1为不同载体500 ℃焙烧后的孔结构图。由图1N2吸附-脱附等温线可知,纯TiO2的N2吸附-脱附等温线属于第IV种等温线,在相对压力为0.4位置出现H1型滞后环,表明纯金红石TiO2样品含有介孔,不同TiO2-SiO2载体的等温线类型不变,在相对压力0.4出现滞后环,低于纯TiO2,表明TiO2-SiO2载体中的介孔孔径较小。由图1介孔孔径分布曲线可以看出,纯TiO2的孔径分布较广,主要集中在12 nm,而TiO2-SiO2载体的孔径分布曲线不随TiO2含量的变化而变化,孔径分布范围较广且孔径分布较为均匀,与典型的SiO2凝胶孔径分布一致,说明TiO2-SiO2载体的孔结构主要是由SiO2提供的[21]。TiO2-SiO2载体的滞后环和孔容随着TiO2含量的增加而逐渐减小,表明TiO2导致介孔含量减少,而TiO2-SiO2载体中无纯TiO2的特征孔径,说明TiO2能够均匀的分散在SiO2的骨架中,无TiO2粒子堆积孔的形成。整体上,TiO2-SiO2载体的比表面积较大,0.1TiO2-SiO2、0.2TiO2-SiO2、0.4TiO2-SiO2、0.6TiO2-SiO2载体的比表面积分别为746.2 m2·g-1、657.0 m2·g-1、542.9 m2·g-1、463.1 m2·g-1,而纯TiO2比表面积仅为16.0 m2·g-1。

图1 不同载体的N2吸附-脱附等温线和孔径分布图Figure 1 N2 adsorption-desorption isotherms and pore size distribution of samples
图2为未焙烧载体的XRD图。
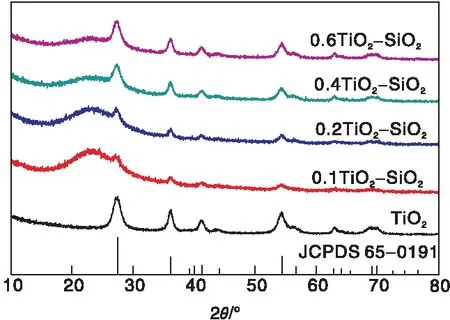
图2 未焙烧载体的XRD图Figure 2 XRD patterns of uncalcined samples
由图2可知,纯TiO2的所有衍射峰与金红石TiO2的标准卡片JCPDS 65-0191完全一致,无其他杂质的衍射峰,且溶胶-凝胶法制备的所有TiO2-SiO2载体中TiO2均保持了纯金红石晶相。由(110)晶面衍射峰通过Scherrer公式计算TiO2晶粒尺寸,0.1TiO2-SiO2、0.2TiO2-SiO2、0.4TiO2-SiO2、0.6TiO2-SiO2载体中TiO2晶粒尺寸分别为5.5 nm、5.5 nm、5.6 nm、5.6 nm,与5.6 nm的纯TiO2基本相同,表明溶胶凝胶法制备过程不影响均匀沉淀法制备的纯TiO2纳米颗粒的稳定性和晶粒尺寸。
图3为500 ℃焙烧后载体的SEM照片。由图3可以看出,0.1TiO2-SiO2、0.2TiO2-SiO2为不规则颗粒状,聚集成球形,初级粒子间分布较为均匀,主要是SiO2凝胶的形貌,0.4TiO2-SiO2、0.6TiO2-SiO2中可观察到针状初级粒子聚集的球形颗粒,与SiO2初级粒子明显不同,为不规则的TiO2颗粒。焙烧后的纯金红石TiO2初级粒子为规则颗粒状,二次颗粒聚集成球形或花状,各晶粒间无明显边界,表明500 ℃焙烧已造成烧结。由此推断,随着TiO2-SiO2载体中TiO2含量的增加,部分TiO2纳米颗粒聚集,但是整体上TiO2仍均保持了较高的分散性,与XRD和孔结构分析结果一致。

图3 500 ℃焙烧载体的SEM照片Figure 3 SEM images of supports calcined at 500 ℃
2.2 TiO2-SiO2载体的稳定性
以0.6TiO2-SiO2载体为例,考察载体经过500 ℃、600 ℃、700 ℃焙烧后的孔结构稳定性。不同温度焙烧的0.6TiO2-SiO2载体的吸附等温线和孔径分布如图4所示。由图4可以看出,未焙烧和不同温度焙烧后的0.6TiO2-SiO2载体的N2吸附-脱附等温线均属于IV型。所有样品的孔径均分布较广,仍保持了凝胶特有的孔分布特点。0.6TiO2-SiO2经过500 ℃、600 ℃、700 ℃焙烧处理后,比表面积由未焙烧的486.1 m2·g-1分别降至463.1 m2·g-1、441.0 m2·g-1、371.5 m2·g-1,孔径分布曲线基本保持一致,仅在(21~25) nm处分布稍有波动,孔容则由0.102 ml·g-1分别降至0.085 mL·g-1、0.077 mL·g-1、0.077 mL·g-1。由此可见,500 ℃焙烧对孔结构影响不明显,600 ℃焙烧对孔结构影响较小,而700 ℃焙烧后孔结构变化明显,表明载体发生了烧结,与文献报道的TiO2-SiO2凝胶结果一致[21]。与纯TiO2相比,焙烧后的0.6TiO2-SiO2载体仍具有较高的比表面积和孔容,表明0.6TiO2-SiO2载体的孔结构具有优异的高温稳定性。

图4 不同温度焙烧的0.6TiO2-SiO2载体的吸附等温线和孔径分布图Figure 4 Adsorption isotherms and pore size distribution of 0.6TiO2-SiO2 calcined at different temperature
图5是不同载体高温焙烧后XRD图及晶粒尺寸。由图5可以看出,所有样品经500 ℃、600 ℃和700 ℃焙烧后,TiO2仍为金红石晶型,未观察到TiO2的锐钛矿和板钛矿的特征峰,表明焙烧过程中金红石相未向其他晶型转变[22]。与未焙烧时相比,载体样品经500 ℃焙烧后,纯TiO2的衍射峰强度明显变大,峰型明显尖锐,半高宽变窄,表明晶粒尺寸显著增大,而其他TiO2-SiO2载体中TiO2的衍射峰基本无变化。不同样品经过600 ℃和700 ℃焙烧后,衍射峰的变化趋势与500 ℃保持一致。由TiO2晶粒尺寸对比可以看出,未焙烧时,0.1TiO2-SiO2、0.2TiO2-SiO2、0.4TiO2-SiO2、0.6TiO2-SiO2等载体中TiO2晶粒尺寸和纯TiO2晶粒尺寸一致,所有TiO2-SiO2载体在不同温度焙烧过程中TiO2晶粒尺寸基本保持不变,而纯TiO2晶粒尺寸在经过500 ℃、600 ℃、700 ℃焙烧后,晶粒尺寸由5.6 nm分别增大至22.1 nm、39.7 nm、100 nm (实际大于100 nm,超过Scherrer公式适用范围),发生了严重烧结。由此可见,所有TiO2-SiO2载体中的TiO2均未发生烧结,表明SiO2提高了TiO2的高温稳定性。
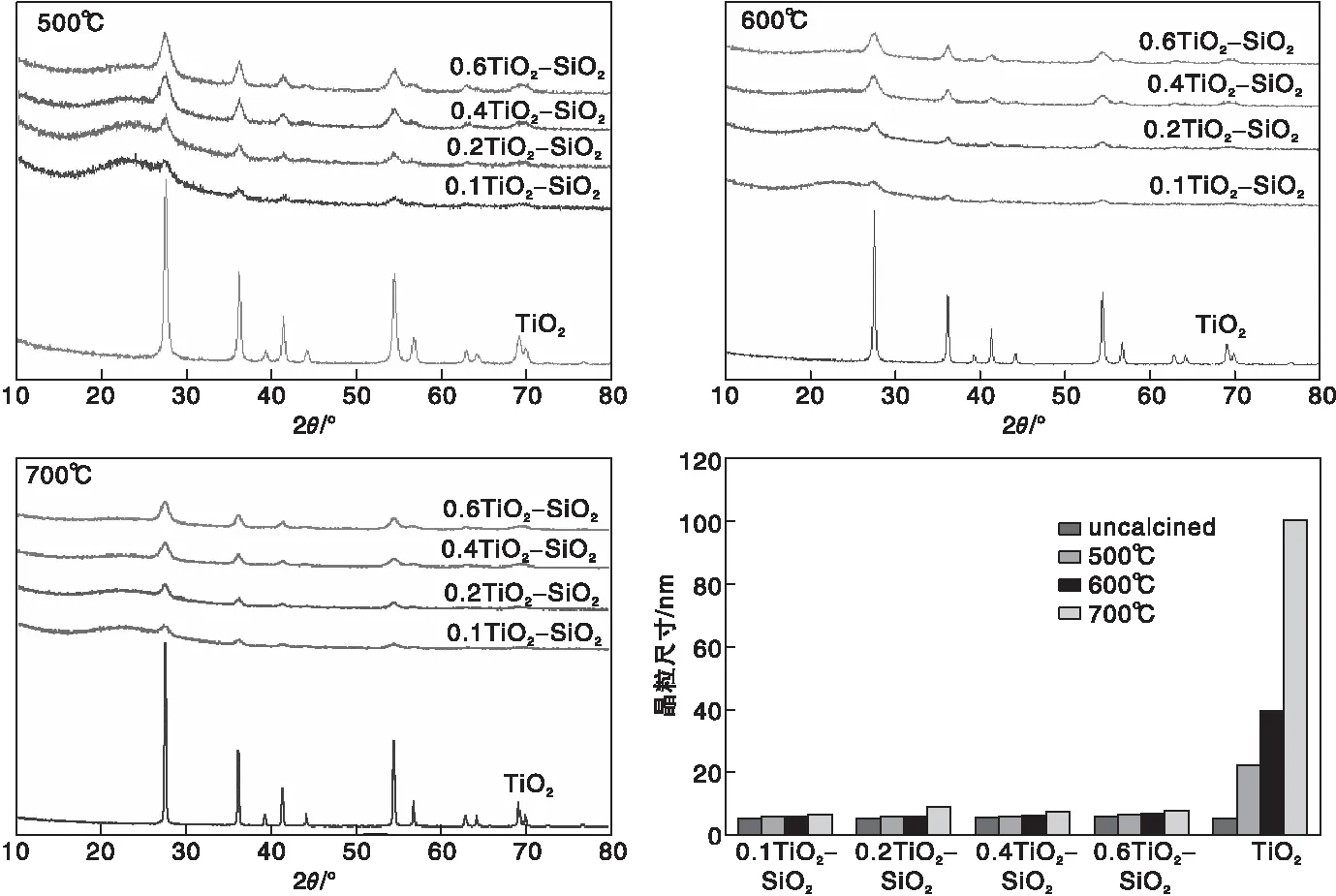
图5 不同温度焙烧的载体XRD图及晶粒尺寸Figure 5 XRD patterns and crystallite size of samples
不同TiO2含量载体500 ℃焙烧和不同温度焙烧0.6TiO2-SiO2载体的FT-IR谱图如图6所示。由图6可以看出,460 cm-1和624 cm-1吸收峰分别为Si-O键对称伸缩振动峰和Ti-O键对称伸缩振动峰,1 078 cm-1的吸收带为Si-O-Si键反对称伸缩振动峰[21]。随着TiO2含量增加,0.1TiO2-SiO2、0.2TiO2-SiO2、0.4TiO2-SiO2、0.6TiO2-SiO2样品的624 cm-1和1 078 cm-1峰强度比分别为0.05、0.25、0.31、0.43,与TiO2-SiO2载体合成时的TiO2/SiO2比例大小顺序一致。由图6还可以看出, 0.6TiO2-SiO2载体经不同温度焙烧后,Si-O键、Ti-O键、Si-O-Si键的特征吸收峰波数基本不变,而且均未在(910~960) cm-1范围内观察到Ti-O-Si特征峰,表明TiO2和SiO2并未生成化学键[21-23]。由此推断,TiO2-SiO2载体中TiO2颗粒主要由SiO2基底的空间结构来保持高温稳定性。
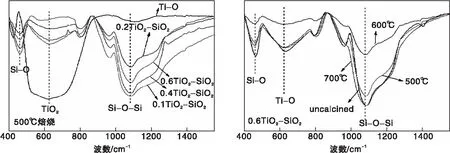
图6 不同TiO2含量载体500 ℃焙烧和不同温度焙烧的0.6TiO2-SiO2的FT-IR谱图Figure 6 FT-IR spectra of samples with different TiO2 content calcined at 500 ℃ and 0.6TiO2-SiO2calcined at different temperature
紫外可见漫反射光谱可以表征TiO2的电子结构,图7为不同载体的UV-vis DRS谱图及[F(R∞)hν]1/2~hν曲线。由图7可知,500 ℃焙烧后,纯TiO2的带边吸收波长为400 nm,而其他TiO2-SiO2载体带边吸收波长发生蓝移。根据Kubelka-Munk理论,通过[F(R∞)hν]1/2~hν曲线,求得纯TiO2的间接禁带宽度为3.05 eV,与文献报道的金红石TiO2禁带宽度3.03 eV一致[24]。0.1TiO2-SiO2、0.2TiO2-SiO2、0.4TiO2-SiO2、0.6TiO2-SiO2等样品的禁带宽度分别为3.06 eV、3.05 eV、3.06 eV、3.06 eV,与纯TiO2相同,说明所有TiO2-SiO2载体中的TiO2仍然为金红石相。由XRD分析可知,TiO2-SiO2载体中的TiO2晶粒尺寸为(5.8~6.2)nm,而纯TiO2为22.1 nm,表明在这些晶粒尺寸范围内TiO2量子尺寸效应不明显,可能与TiO2的波尔半径较小有关[25]。TiO2和0.4TiO2-SiO2样品经500 ℃、600 ℃和700 ℃焙烧后, TiO2的带边吸收波长随着焙烧温度的升高而红移,而0.4TiO2-SiO2载体中的TiO2带边吸收波长基本不变,但是二者的禁带宽度仍相同。由此可见,纯TiO2的焙烧过程,以及TiO2与SiO2复合过程均有结构变化并影响了带边吸收波长移动,但是整体上对TiO2的能带结构影响较小,均保持典型的金红石型TiO2特点。因此,证明了TiO2-SiO2载体中的TiO2和SiO2无相互作用。
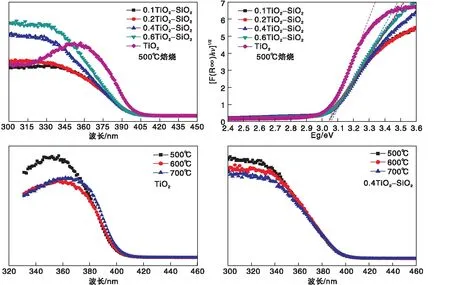
图7 不同载体的UV-vis DRS谱图及[F(R∞)hν]1/2~hν曲线Figure 7 UV-vis DRS spectra of carriers and [F(R∞)hν]1/2~hν curves
3 结 论
(1) 溶胶-凝胶法制备的TiO2-SiO2载体具有典型的SiO2凝胶多孔结构,0.6TiO2-SiO2的比表面积达到463.1 m2·g-1,而纯TiO2为16.0 m2·g-1。TiO2-SiO2载体中TiO2晶型和晶粒尺寸与纯TiO2相同,其制备过程不影响TiO2的稳定性。
(2) 高温焙烧后,TiO2-SiO2载体中的SiO2发生轻微烧结,比表面积和孔容减小,而其中的TiO2仍保持高分散性,晶粒尺寸未发生烧结,表明载体中的SiO2提高了TiO2的稳定性。整体上,与纯TiO2严重烧结相比,TiO2-SiO2载体具有优异的高温稳定性。
(3) TiO2-SiO2载体中的TiO2和SiO2并未生成Ti-O-Si化学键,只是纳米尺度上的混合,而且复合结构对TiO2的能带结构影响较小,仍保持典型的金红石型TiO2特点。TiO2-SiO2载体中TiO2颗粒的高温稳定性主要由SiO2基底的空间结构维持。
