黑枣醋蛋液理化特性、挥发性物质变化及抗氧化能力比较分析
2022-06-11孔炜浩颜景焱张仁堂
孔炜浩,高 琳,颜景焱,张仁堂,
(1.山东农业大学食品科学与工程学院,山东泰安 271018;2.山东枣尚好农业科技有限公司,山东泰安 271000;3.山东土地乡村振兴集团有限公司,山东济南 250000)
醋蛋液是由禽蛋浸泡于醋中而成,同时具有醋与鸡蛋的各种营养成分。醋蛋液营养保健价值极高,在国内外均属传统食疗保健品[1-2],具有提高免疫力、降血压、降血脂、抗氧化、补钙、防治心血管疾病、治疗扁平疣等作用[3-6]。红枣,又名大枣,为鼠李科果实,原产地为中国,历史悠久,被誉为“滋补佳品”,是一种药食同源的水果。红枣中富含酚类、黄酮类、多糖等多种化合物,并表现出良好的抗氧化能力[7-8]。黑枣是由红枣经控温控湿发酵而成[9]。红枣黑化过程中通过非酶褐变反应使其口感、原有成分及功能发生变化[10]。同时黑枣还兼具红枣抑制癌细胞、保肝护脾、美容护肤、补气养血、增强人体免疫力、预防心血管疾病等主要作用[11]。
杨萍芳等[12]优化得到醋蛋浸泡的条件为:醋蛋比值3.2,浸泡时间64 h,浸泡温度24 ℃,蛋白质水解度可达37.19%。艾华等[13]的研究表明醋蛋液有良好的调节血脂和抗氧化作用。李琳等[14]研究表明,醋蛋液具有降压作用。前人研究主要集中在工艺优化及功能方面,对于浸泡过程中各成分变化研究较少。另外,传统醋蛋液多以米醋浸泡,酸度高、刺激性大,并具有蛋腥及冰醋酸的异味,风味较差且质量不稳定、保质期短等问题影响了传统醋蛋液的推广。本实验以黑枣醋浸泡禽蛋,一方面减少蛋腥味,增加枣香味,同时也会增加其营养成分,提高功能,明确其工艺及浸泡过程中成分变化规律对醋蛋液产品的推广具有十分重要的价值。
1 材料与方法
1.1 材料与仪器
鸡蛋 大小均匀且无损伤的红壳鸡蛋,购于山东泰安批发市场;9 g/100 mL白醋(多酚含量很低,可忽略不计;初始pH为2.4) 山东统食食品有限公司;9 g/100 mL黑枣醋(多酚含量为0.164 mg/mL;初始pH为3.4) 山东农业大学果蔬加工实验室发酵;甘氨酸、果糖 分析纯,北京索莱宝科技有限公司;茚三酮试剂 分析纯,上海科丰实业有限公司;磷酸氢二钠、磷酸二氢钾、无水乙醇、甘氨酸、亚硝酸钠、铁氰化钾、碳酸钠、没食子酸、浓硫酸、柠檬酸钠、浓硝酸、浓盐酸、氢氧化钠、氯化锌、氯化钙、氯化钠、三氯乙酸、Folin酚试剂、抗坏血酸、DPPH、ABTS
分析纯,天津市凯通化学试剂有限公司;钼酸铵、无水亚硫酸钠、氯化亚铁、氯化铜、芦丁标准液 分析纯,上海源叶生物科技有限公司;甲醇 色谱纯,山东禹王实业有限公司;钙红指示剂 分析纯,天津市巴斯夫化工有限公司;氢氧化钾 分析纯,天津市科密欧化学试剂开发中心。
AX124ZH分析天平 奥豪斯仪器(常州)有限公司;YP2003电子天平 上海光正医疗仪器有限公司;KSL系列箱式高温烧结炉 合肥科晶材料技术有限公司;TG16台式高速离心机 长沙英泰仪器有限公司;平行蒸发仪 杭州嘉维创新科技有限公司;氨基酸分析仪 武汉恒信世纪科技有限公司;TQ8030气相色谱-质谱联用仪 日本岛津;VF-waxmS柱(0.25 mm×60 m,0.25 μm) 美国瓦里安;PB-10型pH计、PH-070A培养箱、磁力搅拌器 上海一恒科学仪器有限公司;101-2ES电热鼓风干燥箱 北京市永光明医疗仪器厂;HH-6数显恒温水浴锅 江苏省金坛市荣华仪器制造有限公司;KQ2200DE型数控超声波清洗器 昆山市超声仪器有限公司。
1.2 实验方法
1.2.1 黑枣醋蛋液工艺研究
1.2.1.1 浸泡工艺流程选择 实验分别研究黑枣醋蛋液两种浸泡工艺,一次浸泡与二次浸泡,以外观为评价指标,通过观察感官评价的结果来确定最适浸泡工艺。
一次浸泡:鸡蛋→破壳→加枣醋浸泡(醋的质量:蛋的质量=3:1)60 h→搅拌→过滤→醋蛋原液
二次浸泡:鸡蛋→加枣醋浸泡(醋的质量:蛋的质量=3:1)→浸泡24 h后,蛋壳完全溶解,搅拌均匀→继续二次浸泡至60 h→过滤→醋蛋原液
1.2.1.2 感官评价 挑选10名经过培训的食品营养与检测人员,男女各五名,平均年龄为20±3岁,于特定环境下对黑枣醋蛋液进行感官评定,感官评价表如表1所示。最后以平均得分呈现黑枣醋蛋液形态。

表1 黑枣醋蛋液形态感官评价标准Table 1 Sensory evaluation of black jujube vinegar egg liquid
1.2.2 黑枣醋蛋液浸泡过程中各成分的变化
1.2.2.1 黑枣醋蛋液浸泡过程中多酚、磷的变化 称取红壳鸡蛋若干份,按醋蛋质量比3:1的比例添加9 g/100 mL黑枣醋,于25 ℃下浸泡,每8 h取样分别检测多酚和磷的变化,平行操作三次。
1.2.2.2 黑枣醋蛋液浸泡过程中氨基酸的变化 参照1.2.2.1的处理方法,取样检测黑枣醋蛋液浸泡24与64 h氨基酸的变化,平行操作三次。
1.2.3 黑枣醋蛋液与白醋醋蛋液浸泡过程中挥发性成分的变化 参照1.2.2.1的处理方法,分别于浸泡0、24、64 h取样,将样品过滤,除去浮沫,离心(5000r/min、3 min),取上清液,零下4 ℃避光保存,备用。
样品处理:分别量取黑枣醋蛋液与白醋醋蛋液样品8 mL于15 mL样品瓶中,加2 g NaCl,加盖密封,放入30 ℃水浴中平衡10 min。将老化好的固相微萃取器插在样品瓶上,吸附40 min后拔出,插入气相色谱仪进样口,于250 ℃解析3 min。
GC-MS联用分析条件[15]:VF-waxmS色谱柱(0.25 mm×60 m,0.25 μm),进样口温度250 ℃;进样时间3 min;升温程序为初始温度50 ℃,以10 ℃/min升至200 ℃,以4 ℃/min升至260 ℃,再以10 ℃/min升至270 ℃,保持10 min;汽化室温度250 ℃,进样量1 μL,载气(He)流量1 mL/min,分流比25:1。电子轰击离子源,离子源温度230 ℃,接口温度220 ℃,检测器电压0.1 kV,电子能量70 eV,发射电流34.6 μA,质量扫描范围(m/z)45~500,溶剂延迟时间3 min,FullScan模式。通过标准品与NIST-11数据库进行定性,峰面积归一化法定量。
1.2.4 黑枣醋蛋液与白醋醋蛋液抗氧化能力比较
1.2.4.1 DPPH自由基清除率的测定 参考Brand等[16]的方法进行测定。各取不同浓度的黑枣醋蛋液及白醋醋蛋液0.5 mL与5 mL DPPH乙醇溶液(39.4 mg/mL)剧烈摇晃后,避光静置30 min。用去离子水调零,测定517 nm处的吸光度。对比黑枣醋蛋液及白醋醋蛋液的抗氧化能力。DPPH自由基清除率(%)=(A0-A1)/A0×100(A0:1 mL无水乙醇与5 mL DPPH混合,经处理后,于517 nm处测定的吸光度;A1:1 mL样品溶液与5 mL DPPH混合,经处理后,于517 nm处测定吸光度)。
1.2.4.2 FRAP还原能力的测定 总还原力按照Yao等[17]的方法检测。各取不同浓度成品黑枣醋蛋液和白醋醋蛋液0.6 mL,加入2.5 mL磷酸缓冲溶液(0.2 mol/L,pH6.6),2.5 mL铁氰化钾(1%)混和均匀后在50 ℃恒温水浴锅中静置20 min,冷却后,加入2.5 mL三氯乙酸(10%),摇匀,4000 r/min离心,取2.5 mL上清液加入试管中,分别加入2.5 mL去离子水和2.5 mL三氯化铁(0.1%),摇匀,反应8 min,检测其在700 nm处的吸光度值A1。空白以蒸馏水代替样液为A0,重复三次平行实验。吸光度越大,还原能力越强。亚铁还原能力=A1-A0。
1.2.4.3 ABTS+自由基清除率的测定 参考Trabelsi等[18]的方法进行测定。各取不同浓度黑枣醋蛋液溶液及白醋醋蛋液溶液0.04 mL,加入5 mL ABTS储备液混匀,在室温下反应8 min,4000 r/min离心,取上清液,以去离子水为参比,测定其在734 nm处的吸光度值。ABTS+自由基清除率(%)=1-(A1-A0)×100(A0:0.04 mL去离子水与5 mL ABTS混合,经处理后,于734 nm处测定的吸光度;A1:0.04 mL样品与5 mL ABTS混合,经处理后,于734 nm处测定的吸光度)。
1.2.5 指标测定方法
1.2.5.1 多酚测定方法 参考文献[19-20]的方法。标曲的制作:准确量取0、0.1、0.3、0.5、0.7、0.9 mL没食子酸溶液(0.2 mg/mL),分别向没食子酸溶液中加入稀释一倍的Folin酚试剂0.5 mL,混合均匀,然后向没食子酸溶液中加入1.5 mL碳酸钠溶液(10%),加水定容至10 mL,摇匀后75 ℃水浴加热10 min,冷却后,测定其在760 nm处的吸光值。得出吸光值与没食子酸溶液浓度(mg/mL)之间的曲线方程为:Y=62.923X+0.048;R2=0.9933。
样品的测定:准确量取0.2 mL样品,加入稀释一倍的Folin酚试剂0.5 mL,混合均匀,然后向样品溶液中加入1.5 mL碳酸钠溶液(10%),加水定容至10 mL,摇匀后放入水浴锅中75 ℃水浴加热10 min,冷却后,测定其在760 nm处的吸光值。
1.2.5.2 磷测定方法 磷的检测:参照GB 5009.87-2016[21]。
1.2.5.3 氨基酸测定方法 氨基酸的检测:参照GB 5009.124-2016[22]。
1.3 数据处理
实验采用SPSS18.0软件进行数据分析,采用Origin Pro 8.5进行作图。
2 结果与分析
2.1 黑枣醋蛋液加工工艺优化
由表2可知,一次浸泡感官较差,蛋壳未完全溶解,可能是由于浸泡前先打破鸡蛋壳,蛋液流出与枣醋混合,降低了枣醋的酸度,致使鸡蛋壳溶解不充分;而二次浸泡则是待鸡蛋壳完全溶解后再打破蛋壳,因此最终醋蛋液中不会残留蛋壳,且蛋壳溶解后立即破衣,蛋液与枣醋充分混合继续浸泡反应,得到的醋蛋液感官评价效果较好。因此,选择二次浸泡得到的醋蛋液浸泡效果最好。

表2 不同浸泡工艺对醋蛋液感官评价结果的影响Table 2 Effects of different soaking process on sensory evaluation results of vinegar egg liquid
2.2 黑枣醋蛋液浸泡过程中理化成分变化
2.2.1 黑枣醋蛋液浸泡过程中多酚的变化 由图1可知,黑枣醋蛋液中多酚浓度随着浸泡时间的增加整体呈现先降低后升高的趋势。0~16 h醋蛋液中多酚浓度不断降低,16 h时多酚浓度最低为0.11 mg/mL,16~40 h醋蛋液中多酚浓度不断升高,40 h时达到最高0.39 mg/mL,是0 h的2.38倍,40~64 h呈下降趋势,但经显著性分析发现40与64 h时多酚浓度有着显著性差异(P<0.05)。0~16 h由于初始黑枣醋酸度较高,导致小分子多酚物质不稳定,发生水解,浓度降低;24 h打破蛋壳,将蛋液与黑枣醋搅拌均匀,降低了黑枣醋的酸度,小分子多酚物质在此酸度条件下相对稳定,另外大分子多酚类物质发生裂解,使得带有酚羟基的小分子物质增多,因此,多酚浓度不断升高,最后趋于稳定[23]。另外,多酚浓度的增加使醋蛋液抗氧化能力增强[24-26]。

图 1 多酚浓度随浸泡时间的变化Fig.1 Changes of polyphenol concentration with soaking time
2.2.2 黑枣醋蛋液浸泡过程中磷的变化 黑枣醋蛋液中磷的浓度随浸泡时间的变化如图2所示。由图2可知,随着黑枣醋蛋液浸泡时间的增加,磷的浓度整体呈升高趋势。0~24 h醋蛋液中磷浓度增加速率较慢,24 h后增加速率较快,浸泡64 h时含量达到最高为0.13 mg/mL,浓度是0 h的10倍以上。0~24 h醋蛋液中磷浓度小幅增加,主要来自于鸡蛋壳中溶出的磷;24 h鸡蛋破壳,蛋液流出,与黑枣醋混合,蛋液中磷不断释放到枣醋中,使醋蛋液中磷浓度迅速升高。磷是人体内除钙以外含量较多的一种元素,具有参与人体内细胞核蛋白构成、释放能量等多种重要的功能作用[27]。随着浸泡时间的增加,黑枣醋蛋液中小分子磷的含量不断增加,更有利于人体的吸收。
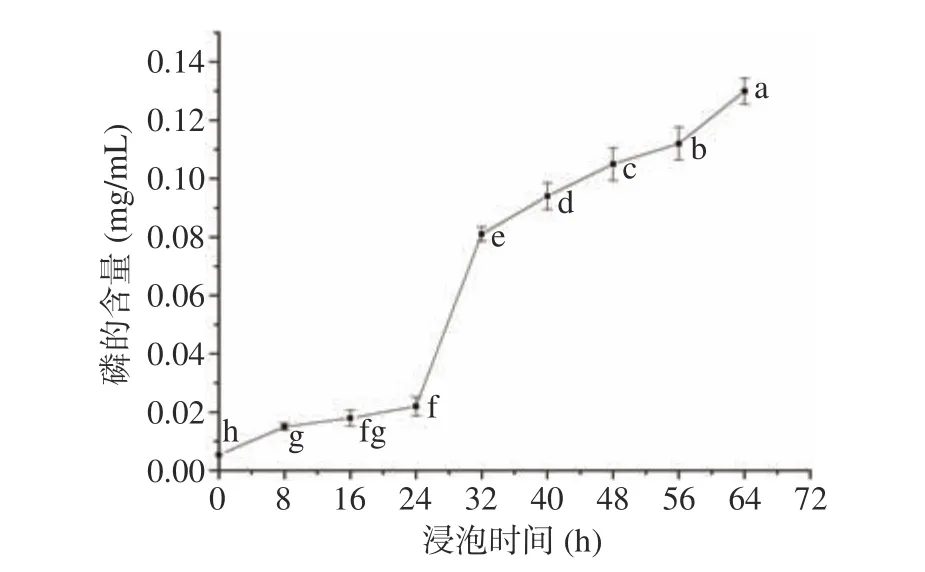
图 2 磷的浓度随浸泡时间的变化Fig.2 Changes of phosphorus concentration with soaking time
2.2.3 黑枣醋蛋液浸泡过程中氨基酸的变化 黑枣醋蛋液浸泡24与64 h的氨基酸变化情况如表3所示。24 h为鸡蛋破壳,蛋液与黑枣醋混合均匀时的时间点;64 h为蛋液与黑枣醋混合均匀后继续浸泡40 h后的黑枣醋蛋液。通过表3可知,浸泡64 h的黑枣醋蛋液氨基酸总量比浸泡24 h的黑枣醋蛋液氨基酸总量增加42.62%,这说明蛋液在酸性环境下继续进行水解,释放出更多的氨基酸。黑枣醋蛋液中共测定出16种氨基酸,其中包括7种必需氨基酸。而且,随着浸泡时间的增加,16种氨基酸的含量均升高,升高最多的氨基酸为蛋氨酸、脯氨酸和异亮氨酸,增加量均超过50%。当浸泡时间为64 h时,黑枣醋蛋液中谷氨酸、亮氨酸、门冬氨酸含量较高,分别为0.50、0.32和0.36 g/100 g,三种氨基酸总量占醋蛋液氨基酸总量的33.91%;其次为赖氨酸、丝氨酸、精氨酸、缬氨酸、丙氨酸和苯丙氨酸,六种氨基酸总量占醋蛋液氨基酸总量的39.10%;剩余7种含量相对较低,占醋蛋液氨基酸总量的27%。随着浸泡时间的增加,醋蛋水解度增加,释放出更多小分子的氨基酸,更有助于人体吸收。氨基酸是组成蛋白质的基本单位,不仅能合成蛋白质,还具有养肝护肝、提高免疫力、增强记忆力等多种功能作用。因此,浸泡64 h的黑枣醋蛋液比浸泡24 h的黑枣醋蛋液功能性更强。
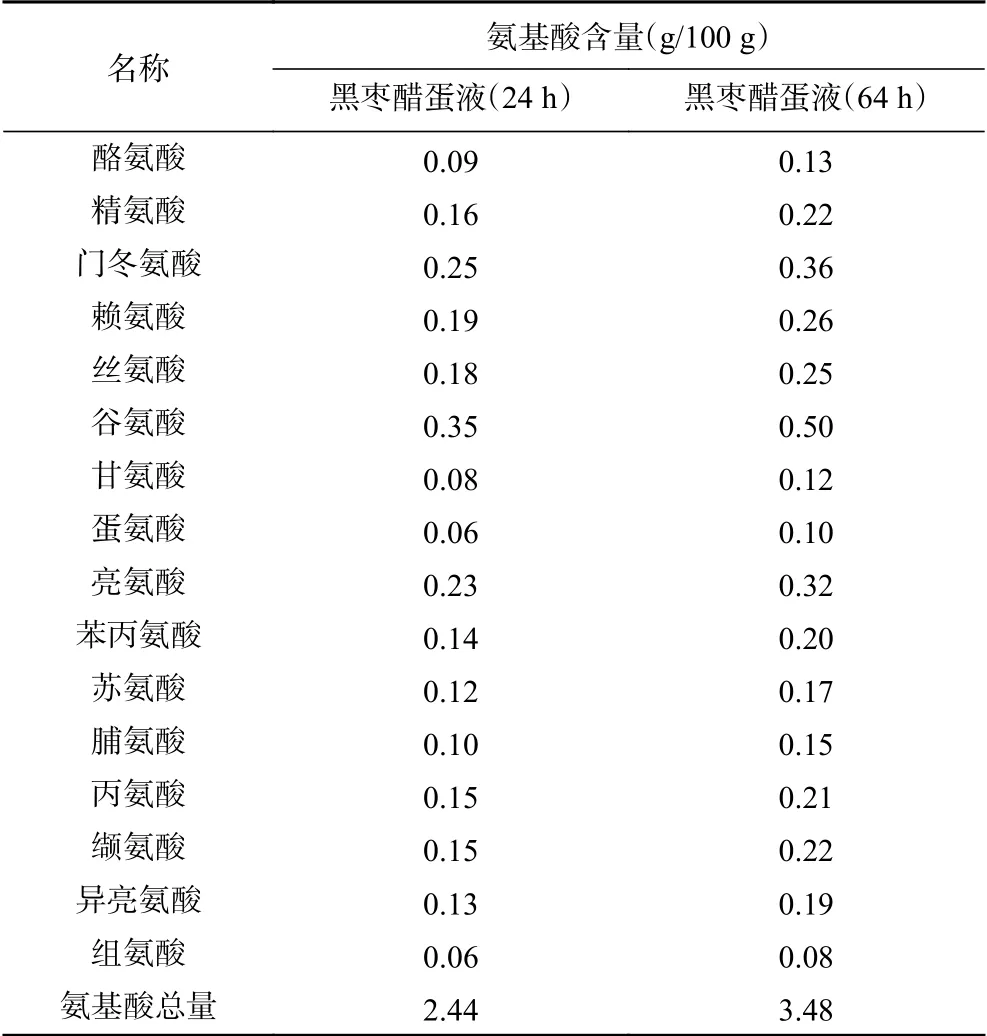
表3 黑枣醋蛋液浸泡24、64 h氨基酸含量对比Table 3 Comparison of amino acid content in black jujube vinegar egg liquid after soaking for 24 and 64 h
2.3 黑枣醋蛋液与白醋醋蛋液浸泡过程中挥发性成分比较
2.3.1 黑枣醋蛋液与白醋醋蛋液浸泡过程中挥发性物质变化比较 现今市场上的醋蛋液大多是用白醋或米醋来浸泡禽蛋制作而来,实验对比分析黑枣醋蛋液与白醋醋蛋液在浸泡过程中挥发性成分的变化规律,研究两种醋蛋液的差异。
白醋醋蛋液浸泡过程中共检测出14种挥发性成分,包括:3种酸类物质、2种酯类物质、1种酮类物质、5种醇类物质、1种醛类物质、1种烷烃和1种酚类物质;黑枣醋蛋液浸泡过程中共检测出26种挥发性物成分,包括:2种酸类物质、3种酯类物质、3种酮类物质、5种醇类物质、4种醛类物质、2种烷烃和7种苯类物质。黑枣醋蛋液浸泡过程中检测出的挥发性成分种类是白醋醋蛋液的两倍,因此黑枣醋蛋液挥发性成分更丰富,香气更加饱满。
2.3.1.1 黑枣醋蛋液与白醋醋蛋液浸泡过程中酸类物质比较 由表4所示,白醋醋蛋液在浸泡过程中共检测出3种酸类物质,其总量呈降低趋势,由0 h的60.18%降至64 h的45.38%,其中丙二酸含量最高。黑枣醋蛋液在浸泡过程中共检测出2种酸类物质,其总量也呈现下降趋势,由0 h的68.19%降至64 h的32.88%。在浸泡后期,两种醋蛋液中均只含有丙二酸和乙酰氧基乙酸,且丙二酸含量最高。

表4 黑枣醋蛋液与白醋醋蛋液浸泡过程中挥发性物质变化对比Table 4 Comparison of volatile compounds in black jujube vinegar egg liquid and white vinegar egg liquid during soaking
2.3.1.2 黑枣醋蛋液与白醋醋蛋液浸泡过程中酯类物质比较 由表4所示,白醋醋蛋液和黑枣醋蛋液在浸泡过程中,酯类物质的总量均逐渐降为0。但两种醋蛋液浸泡过程中酯类物质的种类不同,白醋醋蛋液中含有正己酸乙酯和乙酰氧基乙酸甲酯两种酯,而黑枣醋蛋液含有正己酸乙酯、乙酰氧基乙酸甲酯和1,2-丙二醇二乙酸酯三种酯。乙酰氧基乙酸甲酯具有芳香气味,正己酸乙酯具有油香、菠萝香型的气味,在两种醋蛋液浸泡过程中均提供了酯类部分的香气特征[28]。
2.3.1.3 黑枣醋蛋液与白醋醋蛋液浸泡过程中酮类物质比较 由表4所示,白醋醋蛋液浸泡过程中只检测出3-辛酮一种酮类物质,其含量呈现先升高后降低的趋势。而黑枣醋蛋液中检测出三种酮类物质3-辛酮、甲基庚烯酮和香叶基丙酮,三种酮类总含量呈现降低趋势,其中,甲基庚烯酮和香叶基丙酮含量在浸泡过程中逐渐降为0。因此,在浸泡后期,两种醋蛋液中均只含有3-辛酮一种酮类物质,且黑枣醋蛋液中其含量高于白醋醋蛋液。3-辛酮具有刺激性果香,构成了酮类部分的香气特征。
2.3.1.4 黑枣醋蛋液与白醋醋蛋液浸泡过程中醇类物质比较 由表4可知,两种醋蛋液浸泡过程中均检测出5种醇类物质,但种类不同。白醋醋蛋液在浸泡过程中(S)-(+)-5-甲基-1-己醇和2-乙基己醇逐渐减少至0,而黑枣醋蛋液中(S)-(+)-5-甲基-1-己醇和3-辛醇在浸泡过程中均减少至0。另外,两种醋蛋液中异戊醇和苯乙醇含量均先增后减,2,4-二甲基庚醇含量均逐渐升高。异戊醇具有浓郁的香油香,苯乙醇则具有清甜的花香[29]。在浸泡后期,2,4-二甲基庚醇均成为两种醋蛋液中主要醇类物质,分别占白醋醋蛋液和黑枣醋蛋液醇类总量的99.2%和99.4%。2,4-二甲基庚醇为醋蛋液提供了特殊的叶香和木香气味[28]。
2.3.1.5 黑枣醋蛋液与白醋醋蛋液浸泡过程中醛、酚、烷、苯等物质比较 由表4可知,白醋醋蛋液浸泡过程中共检测出一种醛类物质糠醛,其含量先升高后趋于稳定0.03%,但目前关于糠醛的安全性仍存在争议[30];一种酚类物质2,4-二叔丁基苯酚和一种烷烃三氯甲烷,其含量均随浸泡时间的增加降为0。而黑枣醋蛋液中检测出四种醛类物质,随浸泡时间的增加其含量均降为0;两种烷烃三氯甲烷和十七烷,三氯甲烷在浸泡过程中呈现先升高后降低的趋势,最终含量为0.37%,而十七烷含量最终降为0。黑枣醋蛋液浸泡初期检测出7种苯类物质,但随浸泡过程增加其含量均降为0。
2.3.2 黑枣醋蛋液与白醋醋蛋液成品挥发性物质比较 由图3~图4可知,黑枣醋蛋液与白醋醋蛋液浸泡结束时共检测出9种挥发性成分,其中丙二酸、乙酰氧基乙酸、3-辛酮、异戊醇、2,4-二甲基庚醇和苯乙醇是共有挥发性成分,而乙酰氧基乙酸甲酯和糠醛只在白醋醋蛋液中检出,三氯甲烷只在黑枣醋蛋液中检出。黑枣醋蛋液中主要挥发性成分是2,4-二甲基庚醇,占挥发性成分总量的63.4%,其次是丙二酸,占挥发性成分总量的35.1%,两种物质构成黑枣醋蛋液的主要香气来源;而白醋醋蛋液中主要挥发性成分也是2,4-二甲基庚醇和丙二酸,但两种物质含量相差不大,分别占挥发性成分总量的49.3%和49.4%。黑枣醋蛋液中丙二酸含量要低于白醋醋蛋液,挥发性酸类物质大多有刺激性气味,低浓度的酸会赋予醋蛋液令人愉快的香味,但浓度过高时则会对醋蛋液香气品质产生消极影响,因此黑枣醋蛋液刺激性味道更少[31]。另外,2,4-二甲基庚醇具有叶香和木香气息,并有油脂和玫瑰香调,黑枣醋蛋液中其相对含量明显高于白醋醋蛋液,香气更加突出。其他挥发性物质在两种醋蛋液中含量差距不大且含量较少,表现出的香气差异并不明显。综上所述,黑枣醋蛋液的挥发性物质要优于白醋醋蛋液,特征香气更明显。
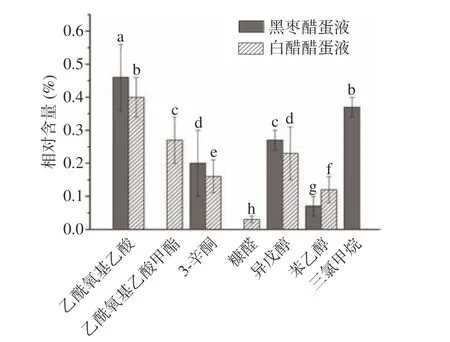
图 3 黑枣醋蛋液与白醋醋蛋液挥发性物质比较Fig.3 Comparison of volatile substances between black jujube vinegar egg liquid and white vinegar egg liquid
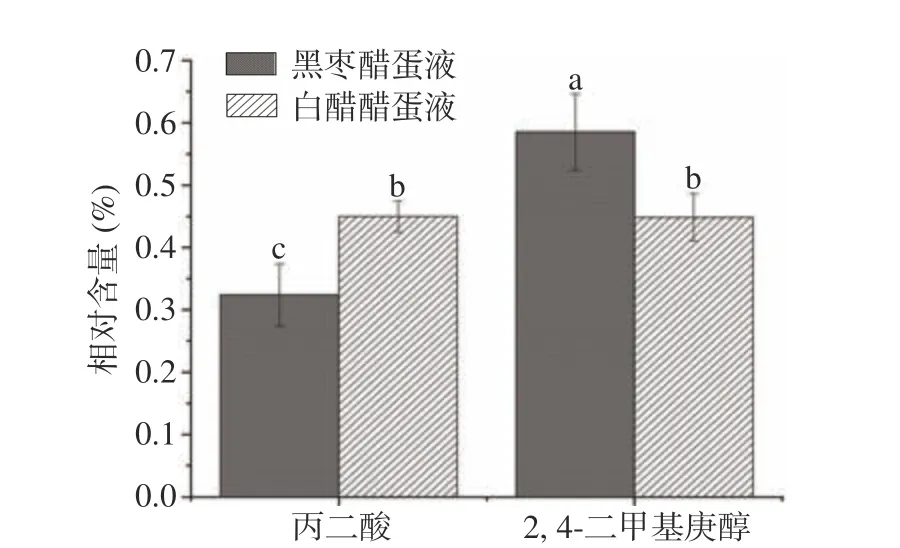
图 4 黑枣醋蛋液与白醋醋蛋液挥发性物质比较Fig.4 Comparison of volatile substances between black jujube vinegar egg liquid and white vinegar egg liquid
2.4 黑枣醋蛋液与白醋醋蛋液抗氧化能力比较
由图5可知,黑枣醋蛋液对DPPH·、ABTS+·清除率及FRAP的IC50值均低于白醋醋蛋液的IC50值,分别为0.19、0.31和0.66 mg/mL。说明黑枣醋蛋液对DPPH·、ABTS+·清除能力以及FRAP均高于白醋醋蛋液。因此,黑枣醋蛋液的抗氧化活性要明显高于白醋醋蛋液。产生这种结果的原因可能是以黑枣醋代替白醋浸泡鸡蛋,黑枣内具有抗氧化能力的营养物质如多酚进入黑枣醋蛋液,多酚是有效的自由基终止剂,具有着清除自由基的机制,是天然的抗氧化剂,且在产品中起主要的抗氧化作用。多酚等物质的进入,使黑枣醋蛋液内抗氧化物质增多,进而增加了黑枣醋蛋液的抗氧化能力[20]。
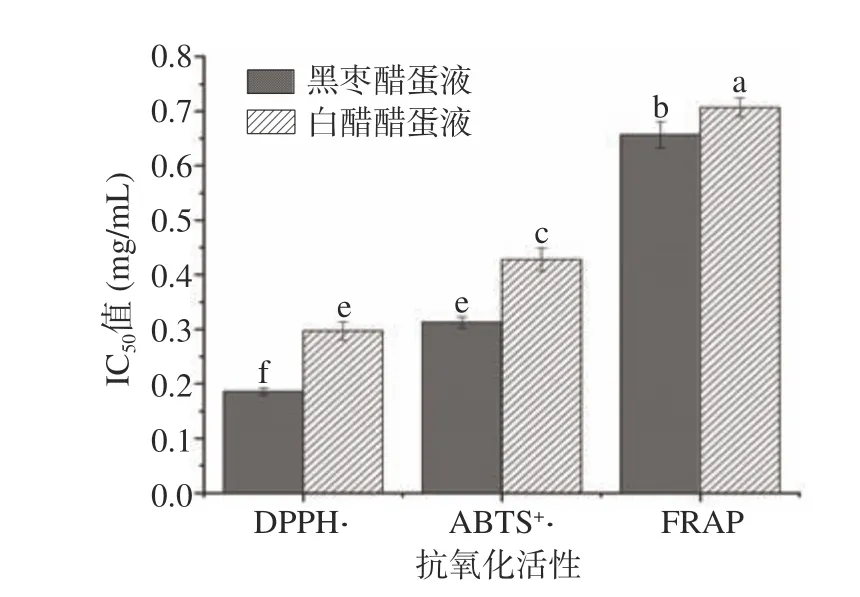
图 5 黑枣醋蛋液与白醋醋蛋液抗氧化能力比较Fig.5 Comparison of antioxidant capacity between black jujube vinegar egg liquid and white vinegar egg liquid
3 结论
本研究确定了黑枣醋蛋液浸泡工艺流程为二次浸泡。研究发现黑枣醋蛋液浸泡过程中多酚浓度在40 h时达到最高0.39 mg/mL,浸泡前多酚浓度为0.164 mg/mL,浸泡40 h后是浸泡前的2.38倍,磷的浓度整体呈升高趋势,浸泡64 h的黑枣醋蛋液氨基酸总量比浸泡24 h增加了近50%;浸泡过程中两种醋蛋液挥发性成分差异较大,黑枣醋蛋液挥发性成分的种类是白醋醋蛋液的2倍左右,香气更加饱满;黑枣醋蛋液对DPPH·、ABTS+·的清除率及FRAP的IC50值均低于白醋醋蛋液的IC50值,分别为0.19、0.31和0.66 mg/mL,说明黑枣醋蛋液的抗氧化能力明显高于白醋醋蛋液。
本研究优化确定了黑枣醋蛋液工艺、浸泡过程中理化成分及挥发性成分变化、抗氧化能力,不仅拓宽了黑枣应用领域,弥补传统醋蛋液生产工艺的不足,同时对醋蛋液产品的推广具有重要意义。
