响应面法优化蔗叶纤维素乙酸酯的制备工艺
2022-06-10周永升张思原龙勇益韦巧艳蔡吉祥柳富杰
周永升,张思原,龙勇益,苏 龙,韦巧艳,蔡吉祥,唐 森,柳富杰*
(1广西科技师范学院,广西现代蔗糖业发展研究院,广西来宾 546199;2广西大学轻工与食品工程学院,广西南宁 530004)
0 引言
纤维素(Cellulose)是由β-D-葡萄糖基之间以β-1,4-糖苷键形成的链状高分子,其分子链中每个葡萄糖单元上有3个活跃羟基,可以进行羟基的醚化反应、酯化反应及接枝共聚反应等[1]。由于纤维素具有可降解、无毒、无环境污染、来源广泛等特点[2],纤维素已广泛应用于建筑[3]、造纸[4]、食品[5]、医药[6]等多个领域。纤维素广泛存在于自然界中,植物纤维素的提取方法主要有碱处理法[7]、生物酶法[8]、蒸汽爆破法[9]、有机溶剂法[10]等。现如今,纤维素改性主要集中在以下3种方法:①物理改性,如高能电子辐照处理[11]、溶剂交换[12]、微波[13]和超声波[14]处理等;②化学改性,如酯化反应[15]、醚化反应[16]、接枝共聚反应[17]等;③生物改性,包括酶的水解[18]、微生物降解氧化[19]等。
近年来,甘蔗叶资源浪费已经成为我国较大的环境问题,甘蔗叶是制糖工业过程中的废弃物,是一种可再生生物质资源,甘蔗叶中含有50%左右的纤维素[20]。但是国内对甘蔗叶的利用不合理,在采集甘蔗时直接对甘蔗叶进行丢弃或者就地焚烧,大大浪费了资源且污染环境[21]。因此,为了合理利用废弃物资源,可以从甘蔗叶中提取出优质的纤维素并进行高附加值的加工生产,将很大程度上拓宽甘蔗叶的综合利用渠道。
本研究是利用碱处理手段提取蔗叶纤维素,并且对蔗叶纤维素进行乙酰化改性,制备出取代度较高的蔗叶纤维素乙酸酯(Sugarcane Leaf Cellulose Acetate,SLCA)。纤维素乙酸酯(Cellulose Acetate,CA)是一种食品、化工的重要原辅材料,本研究主要以蔗叶纤维素为原料,考虑酰化剂与蔗叶纤维素的液料比、酰化剂的组成比例、浓硫酸用量、反应温度、反应时间作为考察因素,探索它们与酯化取代度(Degree of Substitution,DS)的关系,再通过响应面设计试验优化蔗叶纤维素乙酰化改性的条件。
1 材料与方法
1.1 材料与仪器
甘蔗叶是甘蔗梢和种植期间剥离的混合样品。酶制剂:热稳定α-淀粉酶(酶活≥3.5 U/mg,上海颖心实验室设备有限公司);碱性蛋白酶(酶活≥200 U/mg,合肥博美生物科技有限责任公司);脂肪酶(酶活≥30 U/mg,上海源叶生物有限公司)。其他试剂均为分析纯。仪器设备:FW177型中草药粉碎机(天津市泰斯特仪器有限公司);FA2004型分析天平(上海越平科学仪器有限公司);SHZ-D(Ⅲ)型循环水多用真空泵(巩义市科瑞仪器有限公司);DZF6050型真空干燥箱(上海识捷实业有限公司);GZX-GF101-3 BS型电热恒温鼓风干燥箱(上海跃进医疗器械有限公司);HH-S8型恒温水浴锅(金坛市医疗仪器厂);H1850型台式高速离心机(湖南湘仪实验室仪器开发有限公司)。
1.2 试验方法
1.2.1 蔗叶的预处理
⑴粉碎过筛:将清洗过的甘蔗叶在65℃±5℃下烘干,然后剪切成小段,用粉碎机粉碎后过40目筛密封保存。
⑵参考林杰[22]等人的方法去除蛋白质、淀粉和脂肪:用相对于蔗叶粉末质量分数0.3%混合酶(蛋白酶和α-淀粉酶质量比为1∶3)溶液浸泡蔗叶粉末,其中液料比为20∶1,在65℃下酶解90 min,过滤,再将酶解后的滤渣用蒸馏水洗净。将滤渣用液料比为20∶1的脂肪酶溶液进行酶解,脂肪酶用量为0.4%、温度为50℃、酶解时间为60 min,之后使用100℃水浴灭酶10 min,再用蒸馏水将滤渣洗至中性,放入65℃±5℃烘干,粉碎过40目筛备用。
⑶参考李春光[23]、Gil-López[24]、Ann[25]等人的方法去除木质素和半纤维素:称取上述粉末,按液料比30∶1加入体积分数0.7%的H2O2和质量分数4%的NaOH混合溶液,在85℃下搅拌4 h,滤渣用蒸馏水洗净,65℃±5℃干燥后粉碎过40目筛。然后取碱液处理后的粉末,按液料比30∶1加入31 mL/L乙酸和9.5 g/L NaClO2混合溶液,在75℃下处理1 h,过滤后用蒸馏水洗涤至中性,65℃±5℃烘干后粉碎过100目筛备用。纤维素含量的测定按照李春光[23]的方法平行测定3次。
1.2.2 乙酰化蔗叶纤维素的制备
将2 g蔗叶纤维素和一定体积的乙酸酐-冰乙酸混合溶液加入到圆底烧瓶中,并且加入一定量的浓硫酸作为反应催化剂。在一定温度下,于回流冷凝装置中反应一段时间,反应结束后,将圆底烧瓶取出,冷却至室温后加入50 mL的无水乙醇沉淀1 h,抽滤,用蒸馏水冲洗滤渣至中性,除去没有反应完全的乙酸。最后将滤渣在30℃下真空干燥至恒重,测定DS值。按照傅七兰[26]的醇皂法平行测定3次。
1.2.3 制备乙酰化蔗叶纤维素的单因素试验设计
按照1.2.2节的制备步骤进行。考虑液料比(15∶1,20∶1,25 1∶,30∶1,35 1∶)、相对于冰乙酸的乙酸酐体积分数(40%、45%、50%、55%、60%)、相对于乙酸酐-冰乙酸混合溶液的浓硫酸体积分数(0、0.25%、0.5%、0.75%、1%)、酯化温度(80、85、90、95、100℃)、酯化时间(1.5、2、2.5、3、3.5 h)等因素和水平。固定相对于冰乙酸的乙酸酐体积分数为50%、相对于乙酸酐-冰乙酸混合溶液的浓硫酸体积分数为0.5%、酯化温度为90℃、酯化时间为2.5 h,以DS为指标,进行单因素试验得到最佳液料比,再依次确定其他因素的水平。最后进行单因素方差分析结果,筛选合适的3个因素进行制备工艺的优化。
1.2.4 Box-Behnken响应面试验设计及验证实验
根据单因素试验结果,以DS为指标进行3因素3水平Box-Behnken响应面试验,试验设计见表1。确定最佳制备工艺,并建立数学模型,分析因素间的相互作用。通过规划求解后得到工艺条件的理论值,重复5次实验,并进行t检验,检查工艺的稳定性、模型的准确性。

表1 Box-Behnken响应面试验设计表
1.3 数据处理
通过Excel 2016进行数据统计、标准偏差计算及表格制作,使用Minitab 18进行Tukey多重比较分析(α=0.05),运用Excel 2016和Origin 2018绘图。
2 结果与分析
2.1 单因素结果
2.1.1 液料比
蔗叶经过预处理后得到了纤维素含量为92.56%的样品。使用该样品进行乙酰化改性,研究料液比对DS的影响,结果见图1。液料比在15~35 mL/g范围内,DS呈先上升后下降的趋势,但是不具有统计学差异(P>0.05)。液料比过低时底物较少,乙酰化效果不好,随着液料比的升高,酯化反应向正方向进行,DS也在上升,在液料比达到25 mL/g时,DS为2.248。但当液料比超过25 mL/g时,DS反而减小。原因可能有2方面:一是过量的乙酰化试剂抑制了反应的进行,二是过量的乙酸酐使得反应体系呈较强的酸性,导致生成的纤维素乙酸酯发生分解[27]。综上,确定最佳液料比为25 mL/g。 2.1.2 乙酸酐体积分数

图1 料液比对DS的影响
试验考察了乙酸酐体积分数(相对于冰乙酸40%~60%)对DS的影响,由图2可知,DS先显著上升后(P<0.05)再略微下降,即当乙酸酐体积分数大于45%之后,DS差异不显著(P>0.05)。DS随着乙酸酐体积分数的增加逐渐上升,在乙酸酐体积分数为50%时DS达到最大,DS等于2.250。因为当乙酸酐体积分数增加时,酯化反应平衡向正方向移动;同时,随着酯化反应的进行,酯化反应生成的水会参与水解反应,促进酯化反应,有利于提高DS[28]。当乙酸酐体积分数继续增大时,会导致DS逐渐下降。因为酯化反应是可逆的,而且酸对纤维素有一定的降解作用,所以DS低于理论值3.0[28]。综上,确定最佳乙酸酐体积分数为50%。

图2 乙酸酐体积分数对DS的影响
2.1.3 浓硫酸体积分数
试验考察了浓硫酸体积分数(相对于乙酸酐-冰乙酸混合溶液0~1%)对DS的影响,由图3可知,DS先显著上升后再显著下降(P<0.05),当浓硫酸体积分数为0.50%时DS达到最大,DS等于2.231。因为纤维素的乙酰化反应需要在无水体系中进行,使用浓硫酸作催化剂可以减少反应体系中的水,从而减少产物水解;当浓硫酸用量过大时,纤维素发生氧化降解,且在乙酰化过程中会生成少量的纤维素硫酸酯、纤维素磺醋酸混合酯、乙酰硫酸等[26,28]。综上,确定最佳浓硫酸体积分数为0.50%。

图3 催化剂用量对DS的影响
2.1.4 酯化温度
试验考察了酯化温度(80~100℃)对DS的影响,由图4可知,DS先显著上升后(P<0.05)再略微下降。DS随着酯化温度的增加逐渐上升,在酯化温度为95℃时DS达到最大,DS为2.252。因为温度较低时,酯化反应不完全导致DS不高;当温度过高时,少量的纤维素在高温酸环境中会发生脱水、氧化、缩水等副反应,造成DS降低[26]。综上,确定最佳酯化温度为95℃。

图4 反应温度对DS的影响
2.1.5 酯化时间
试验考察了酯化时间(1.5~3.5 h)对DS的影响,由图5可知,DS先显著上升后再显著下降(P<0.05),当酯化时间为2.5 h时DS达到最大,DS等于2.246。因为在酸的作用下,随着时间的延长,纤维素分子原有结构受到破坏,羟基不断暴露出来,DS增加;而作用时间过长导致纤维素在酸性环境中发生轻度降解导致DS略微减小。综合考虑,确定反应时间以2.5 h为宜。

2.1.6 单因素方差分析
各因素的方差分析见表2,由表可知,各因素对DS的影响显著性程度依次是:酯化温度、浓硫酸体积分数、酯化时间、乙酸酐体积分数、液料比。选取影响较显著的3个因素进行响应面试验,优化酯化工艺。

表2 各因素方差分析表
2.2 Box-Behnken响应面试验结果及验证
2.2.1 响应面试验结果与分析
在单因素试验的基础上,以酯化温度、浓硫酸体积分数、酯化时间为考察因素,以DS为指标,设计Box-Behnken响应面试验,实验结果见表3。利用Design-Expert软件对试验数据进行分析,可以得到DS的多项式回归方程(自然变量)。方程为:

表3 响应面试验结果

对回归方程进行方差分析,结果见表4。F值可用于测试每个变量对响应值的意义。F越大,则相应变量的显著程度越高。当显著性检验P<0.05时,说明其具有统计学意义。从表4可以得出结论,模型P<0.0001,该模型已达极显著水平;失拟项P=0.5276>0.05(不显著),决定系数R2=0.9883,说明具有较高的显著性,而R2adj=0.9732,能够解释实验 97.32%的响应值变化,且预测相关系数R2Pred=0.9150,C.V.%=3.36,说明此实验模型与真实数据拟合程度良好,拟合度较高,可用于分析和预测蔗叶纤维素乙酸酯的制备效果。回归方程系数的显著性分析:A、B、C、A2、B2、C2对DS的影响达到极显著水平,AC达显著水平。A、B、C 3个因素对DS影响大小顺序为:A>C>B,即反应温度>催化剂用量>反应时间。
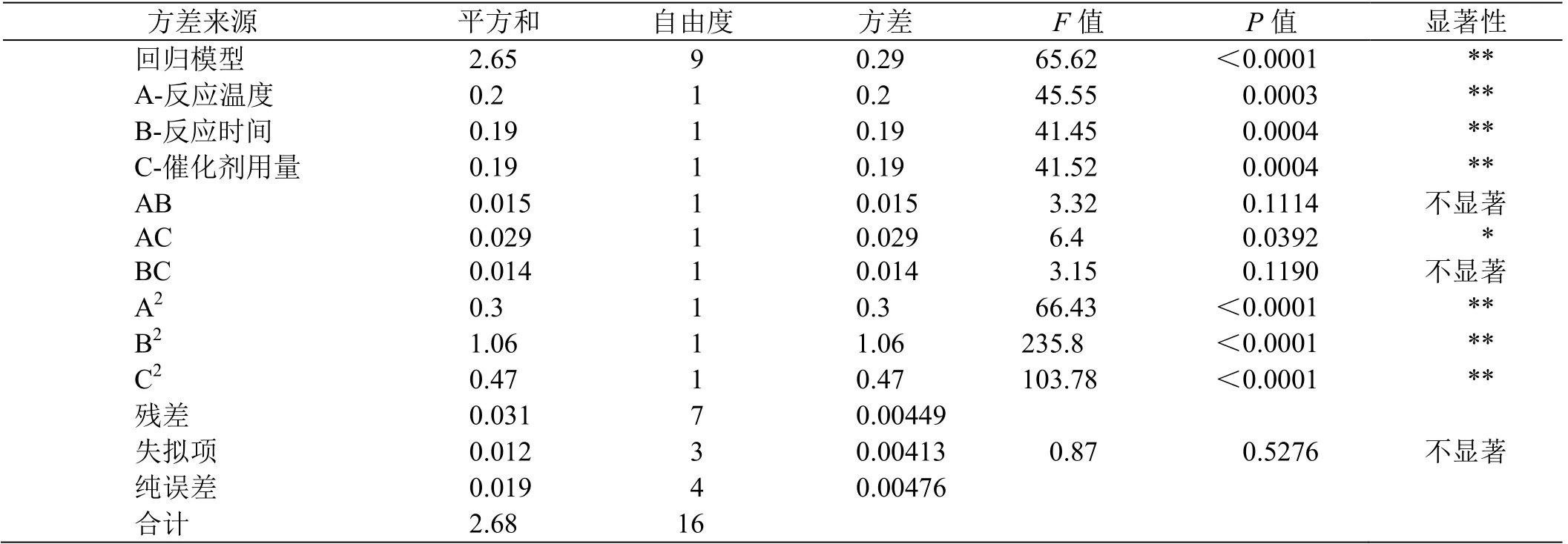
表4 方差分析结果
图6是根据上述回归方程绘出的各因素交互作用对DS影响的等高线图和响应曲面图。等高线越接近椭圆表明两因素交互作用越强,且等高线越密集则影响效果越大;响应曲面图呈凸面,直观地反映了这些因素对DS的影响。在所研究的区域内均存在一个极值点,随着各因素从小到大变化,DS呈现先增后减(或先增后缓)的趋势,这与单因素实验结果相一致。其中,结合表4可知,交互项AC的P值为0.0392,表明反应温度和催化剂用量之间的交互影响达到显著水平。
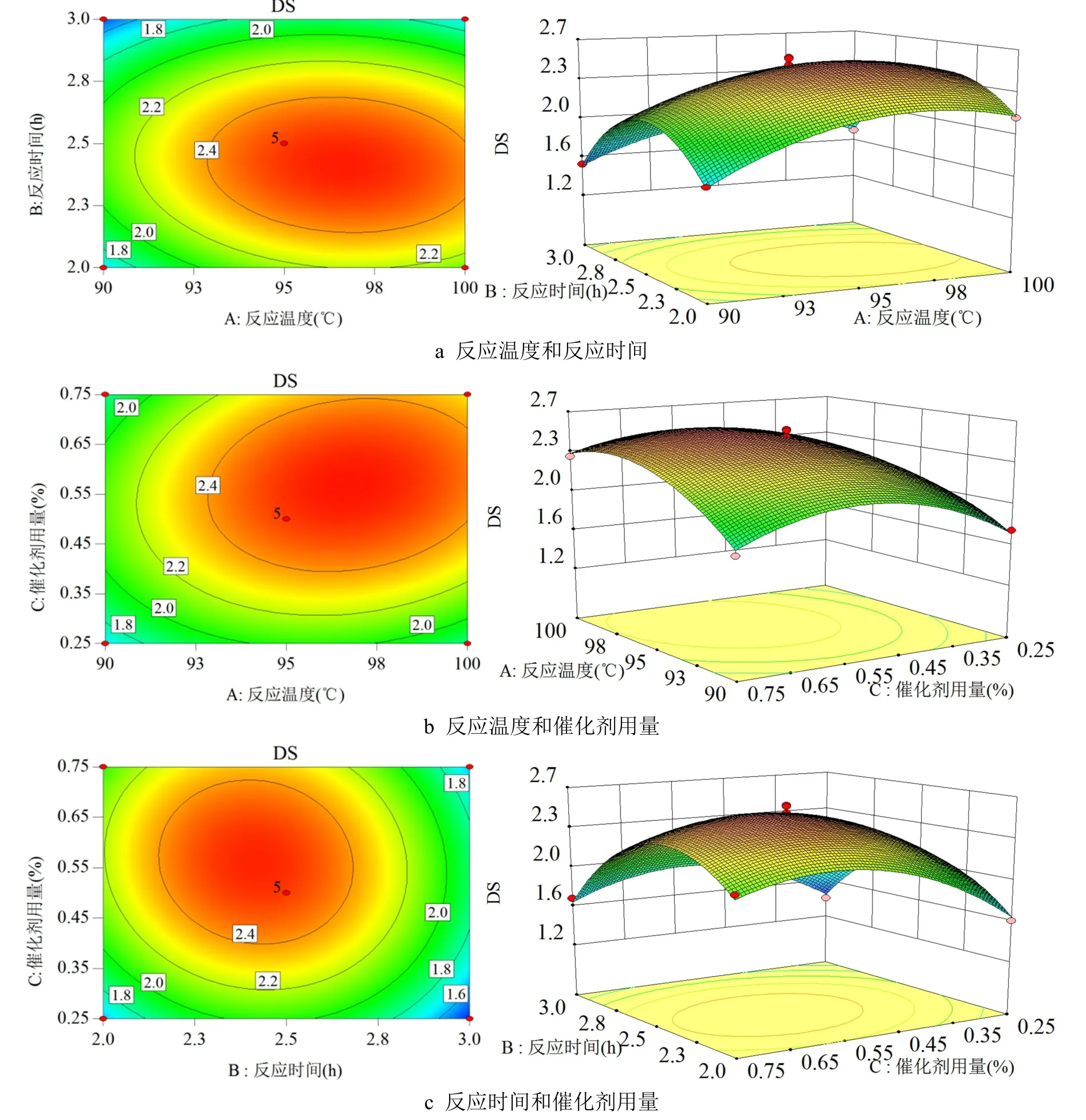
图6 各因素交互作用对DS影响的等高线及响应面图
2.2.2 最佳条件的确定及验证
通过对试验数据的处理与分析,得到最佳条件为:反应温度97℃、反应时间2.4 h、催化剂用量0.57%,此时模型理论结果为DS=2.600。进行5次重复实验,DS分别为2.484、2.591、2.561、2.624、2.555,DS平均值2.563与模型预测结果接近。通过t检验分析(α=0.05),经过双尾检验可知重复实验值和预测值没有显著差异,再经过单尾检验可知重复实验的DS没有显著减小,表明所建回归模型具有良好的预测效果。
3 结论
本实验以蔗叶纤维素为原料进行乙酰化反应,制备蔗叶纤维素乙酸酯。通过单因素试验和响应面试验结果可知,蔗叶纤维素乙酸酯最佳制备条件为液料比25 mL/g、乙酸酐体积分数50%、反应温度97℃、反应时间2.4 h、催化剂用量0.57%,此时蔗叶纤维素乙酸酯DS为2.600。建立的数学模型与真实数据拟合度较高,可用于分析和预测蔗叶纤维素乙酸酯的制备效果。研究成果为蔗叶纤维素乙酸酯的制备及应用提供了参考依据。
