苦槛蓝叶的黄酮类成分及其荔枝霜疫霉抑制活性研究
2022-06-10叶慧娟谷文祥
叶慧娟, 谷文祥
(1. 肇庆市食品检验所,广东 肇庆526000; 2. 华南农业大学材料与能源学院,广州 510642)
苦槛蓝科(Myoporaceae)植物为多年生的常绿灌木或乔木,有荒漠木属(Eremophila)、苦槛蓝属(Myoporum)和假瑞香属(Bontia)。在我国,苦槛蓝(M.bontioides)是唯一1 种苦槛蓝属植物,广泛分布于广东、广西、福建和台湾等沿海地区[1]。关于苦槛蓝的化学成分,已报道有萜类、黄酮、甾醇和糖苷类等多种化学成分[2-3]。本实验室前期从苦槛蓝叶中分离得到了多个单体化合物[4-6],化合物的结构类型多样,其中黄酮类化合物19 个,主要是黄酮类、二氢黄酮类化合物。前期的研究表明,苦槛蓝叶粗提物不仅对小菜蛾(Plutella xylostella)、菜粉蝶(Pieris rapae)、斜纹叶蛾(Lepidoptera noctuidae)、亚洲玉米螟(Ostrinia furnacalis)和蚜虫(Hemiptera aphidoidea)等多种害虫具有强烈的产卵驱避、拒食、生长发育抑制作用,而且还表现出较强的抗菌和影响某些植物生长的作用[6-8]。苦槛蓝叶挥发油对小菜蛾成虫具有强烈的趋避作用[9-10],其中的苦槛蓝酮对小菜蛾也有产卵忌避作用[11]。苦槛蓝叶乙醇提取物石油醚萃取部分对稻瘟菌(Pyriculariasp.)和香蕉炭疽菌(Colletotrichum musae)有很强的抑制活性[12-13],分离得到的(2R,3R)-3,5,7-trihydroxy-flavanone-3-acetate 对稻瘟菌有强抑菌活性[4];5,7-二羟基二氢黄酮、5,7-二羟基黄酮醇、3,4′-二甲氧基-5,7-二羟基黄酮醇对小菜蛾具有产卵忌避、拒食作用[8];桔皮素、甜橙素、二氢山奈酚和木犀草素对香蕉炭疽菌具有较好的抑菌活性[5];5,7-二羟基二氢黄酮、7-甲氧基香橙素、去甲基川陈皮素对大肠杆菌(Escherichia coil)与金黄色葡萄球菌(Staphyloccocus aureus)均有明显的抑制作用[6]。在前期研究的基础上,本文对苦槛蓝叶乙醇浸提乙酸乙酯萃取部分的化学成分进行了分离鉴定,并测定了部分化合物对荔枝霜疫霉菌的抑菌活性,为促进苦槛蓝植物资源更有效的开发利用提供理论依据。
1 材料和方法
1.1 材料和仪器
试验材料采自广东雷州半岛,经华南农业大学林学院李秉滔教授鉴定为苦槛蓝(Myoporumbontioides)。叶片晒干粉碎,过60 目筛,密封保存备用。荔枝霜疫霉菌(Peronophythora litchi)由华南农业大学资环学院姜子德教授提供。
5L-SFE 超临界CO2萃取仪(广州美晨高新分离技术有限公司);LC-6AD 型高效液相色谱仪(日本岛津公司);中压半制备(上海利穗科技有限公司);Bruker AVANCE 600 型核磁共振仪(瑞士Brucker 公司);电喷雾质谱(ESI-MS) MDS SCIEX API 2000 LC/MS/MS 仪;BSA224S 赛多利斯电子分析天平(德国);V-850 旋转蒸发仪(瑞士布琦公司);柱层析正相硅胶(青岛谱科分离材料有限公司);凝胶Sephadex LH-20 (瑞典Amersham Biosciences 公司);薄层层析硅胶板GF254(青岛海洋化工分厂)。
1.2 提取和分离
取苦槛蓝叶粉末32.50 kg,先用超临界二氧化碳在压力15 MPa,在30 ℃下提取15 min,然后在室温下用95%乙醇(3 BV)浸提3 次,每次浸泡7 d,过滤,合并滤液,减压蒸馏除去乙醇至无醇味。浓缩后的乙醇提取液用乙酸乙酯溶剂萃取3 次,合并萃取溶液,得到700 g 乙酸乙酯萃取物。
将乙酸乙酯萃取部分经正相硅胶柱色谱(200~300 目),以氯仿-甲醇[100∶1、50∶1、25∶1、10∶1、5∶1、2∶1 和0∶100,V/V(下同)]进行梯度洗脱,经TLC 薄层色谱检测合并主点相同的流分,得到16 个组分(E1~E16)。E10 (23.0 g)经中压液相色谱分离,以甲醇-水(10∶100~100∶0)梯度洗脱,利用TLC 检测合并主点相同的流分,得到E10-1~E10-8 共8 个亚组分。E10-3 (1.2 g)经Sephadex LH-20柱层析(流动相∶ 甲醇),再经正相硅胶柱层析, 以甲醇-氯仿(4∶96)洗脱,得到化合物9 (26.0 mg); E10-6组分(2.6 g)经Sephadex LH-20 柱层析(流动相: 甲醇),再经正相硅胶柱层析,以甲醇-氯仿(8∶92)洗脱,得到化合物7 (23.8 mg);E10-8 组分(1.8 g)经正相硅胶柱层析,用氯仿-甲醇(25∶1~1∶1)进行梯度洗脱,再经Sephadex LH-20 柱层析(流动相: 甲醇)得到化合物2 (17.0 mg)。E12 组分(80.0 g)经正相硅胶柱层析,用氯仿-甲醇(50∶1~0∶100)进行梯度洗脱,利用TLC 检测合并主点相同的流分, 得到E12-1~E12-10 共10 个亚组分。E12-3 组分(32.4 g)经中压液相色谱分离,以甲醇-水(20∶100~100∶0)梯度洗脱,再经Sephadex LH-20 柱层析(流动相: 甲醇),得到化合物1 (15.0 mg)和10 (12.0 mg)。E12-4 组分(26.0 g)经中压液相色谱分离,以甲醇-水(40∶100~100∶0)梯度洗脱,利用TLC 检测合并主点相同的流分,得到E12-4-1~E12-4-11 共11 个亚组分。E12-4-4 组分(3.5 g)经Sephadex LH-20 柱层析,以甲醇-氯仿(4∶1)洗脱,得到化合物8 (24.5 mg); E12-4-5组分(4.5 g)经Sephadex LH-20 柱层析,以甲醇-氯仿(4∶1)洗脱,得到化合物11 (24.0 mg); E12-4-8 (3.8 g)经Sephadex LH-20 柱层析,以甲醇-氯仿(41)洗脱,得到化合物4 (38.0 mg);E12-4-11 组分(4.2 g)经Sephadex LH-20 柱层析[流动相: 甲醇;甲醇-氯仿(4∶1)],得到化合物3 (38.0 mg)和5 (23.3 mg)。E14组分(10.0 g)经中压液相色谱分离, 以甲醇-水(20∶100~100∶0)梯度洗脱,利用TLC 检测合并主点相同的流分,得到E14-1~E14-4 共4 个亚组分。E14-1组分(1.8 g)经Sephadex LH-20 柱层析,以甲醇-氯仿(4∶1)洗脱,再经正相硅胶柱层析, 以甲醇-氯仿(4∶96)洗脱,得到化合物6 (9.0 mg)。
1.3 结构鉴定
5,7,3′-三羟基-4′-甲氧基黄酮 (1)黄色针状结晶,易溶于丙酮。分子式C16H12O6, ESI-MSm/z:301 [M + H]+, 299 [M - H]-。1H NMR (CD3COCD3,600 MHz):δ6.55 (1H, s, H-3), 6.22 (1H, d,J= 1.8 Hz,H-6), 6.46 (1H, d,J= 1.8 Hz, H-8), 7.42 (1H, d,J=1.8 Hz, H-2′), 7.10 (1H, d,J= 8.4 Hz, H-5′),7.55 (1H,dd,J= 8.4, 1.8 Hz, H-6′), 3.97 (3H, s, OCH3);13C NMR (CD3COCD3, 150 MHz):δ163.6 (C-2), 103.9(C-3), 182.3 (C-4), 157.5 (C-5), 91.5 (C-6, C-8), 164.2(C-7), 161.7 (C-9), 99.6 (C-10), 119.6 (C-1′), 112.9(C-2′), 146.9 (C-3′), 151.2 (C-4′), 124.0 (C-6′), 55.7(4′-OCH3)。核磁数据与文献[14]数据基本一致,故鉴定为5,7,3′-三羟基-4′-甲氧基黄酮。
3,5,7,4′-四羟基-3′-甲氧基黄酮 (2)淡黄色固体,溶于甲醇。分子式为C16H12O7, ESI-MSm/z:317 [M + H]+, 315 [M - H]-。1H NMR (DMSO-d6,600 MHz):δ3.90 (3H, s, -OCH3), 6.42 (1H, d,J= 2.1 Hz,H-6), 6.17 (1H, d,J= 1.8 Hz, H-8), 7.01 (1H, d,J=2.0 Hz, H-2′), 6.91 (1H, d,J= 8.5 Hz, H-5′), 6.91 (1H,dd,J= 8.5, 2.0 Hz, H-6′), 12.47 (1H, s, OH);13C NMR (DMSO-d6, 150 MHz):δ146.1 (C-2), 135.5 (C-3), 175.8 (C-4), 160.6 (C-5), 98.1 (C-6), 163.8 (C-7),93.3 (C-8), 156.1 (C-9), 102.9 (C-10), 121.6 (C-1′),110.3 (C-2′), 150.8 (C-3′), 148.0 (C-4′), 115.8 (C-5′),120.3 (C-6′), 55.4 (3′-OCH3)。核磁数据与文献[15]数据基本一致,故鉴定为3,5,7,4′-四羟基-3′-甲氧基黄酮。
5,7,4′-三羟基-3′,5′-二甲氧基黄酮 (3)黄色针状固体,易溶于丙酮。分子式C17H14O7, ESI-MSm/z: 330.9 [M + H]+, 353.1 [M + Na]+,329.2 [M - H]-,365.5 [M + Cl]-。1H NMR (CD3COCD3, 600 MHz):δ13.01 (1H, s, 5-OH), 9.67 (1H, s, 7-OH), 8.18 (1H, s,4′-OH), 6.73 (1H, s, H-3), 6.25 (1H, d,J= 2.0 Hz,H-6), 6.55 (1H, d,J= 2.0 Hz, H-8), 7.38 (2H, s, H-2′, 6′),3.96 (6H, s, 2×OCH3);13C NMR (CDCl3, 150 MHz):δ165.4 (C-2), 105.1 (C-3), 183.6 (C-4), 159.2 (C-5),100.2 (C-6), 165.5 (C-7), 95.3 (C-8), 163.8 (C-9),105.7 (C-10), 122.8 (C-1′), 105.8 (C-2′, 6′), 149.6(C-3′, 5′), 141.4 (C-4′), 57.4 (OCH3)。核磁数据与文献[16]数据基本一致,故鉴定为5,7,4′-三羟基-3′,5′-二甲氧基黄酮。
木犀草素 (4)黄色针状结晶,溶于甲醇。分子式C15H10O6, ESI-MSm/z: 287 [M + H]+, 285 [M -H]-。1H NMR (DMSO-d6, 600 MHz):δ12.99 (1H, s,5-OH), 10.05 (1H, br s, 7-OH), 9.50 (2H, br s, 3′,4′-OH), 6.68 (1H, s, H-3), 6.19 (1H, d,J= 2.0 Hz, H-6),6.44 (1H, d,J= 2.0 Hz, H-8), 7.40 (1H, br s, H-2′),6.90 (1H, d,J= 8.2 Hz, H-5′), 7.43 (1H, d,J= 8.2 Hz,H-6′);13C NMR (DMSO-d6, 600 MHz):δ162.4 (C-2), 103.2 (C-3), 180.1 (C-4), 158.2 (C-5), 98.6 (C-6),165.6 (C-7), 94.1 (C-8), 161.4 (C-9), 101.4 (C-10),120.2 (C-1′),113.2 (C-2′), 143.8 (C-3′), 149.4 (C-4′),115.2 (C-5′), 120.1 (C-6′)。核磁数据与文献[17]数据基本一致,故鉴定为5,7,3′,4′-四羟基黄酮,即木犀草素。
山奈酚(5)黄色针晶,溶于甲醇。分子式为C15H10O6, ESI-MSm/z: 287 [M + H]+, 285 [M -H]-。1H NMR (DMSO-d6, 600 MHz):δ12.47 (1H, s,OH), 6.17 (1H, d,J= 1.8 Hz, H-6), 6.42 (1H, d,J=2.1 Hz, H-8), 8.02 (2H, d,J= 8.1 Hz, H-2′, 6′), 6.90(2H, d,J= 8.3 Hz, H-3′, 5′);13C NMR (DMSO-d6,150 MHz):δ159.1 (C-2), 135.5 (C-3), 175.8 (C-4),160.6 (C-5), 98.1 (C-6), 163.8 (C-7), 93.3 (C-8), 156.1(C-9), 102.9 (C-10), 121.6 (C-1′), 115.3 (C-2′), 129.3(C-3′), 146.8 (C-4′), 129.4 (C-5′), 115.3 (C-6′)。核磁数据与文献[18]数据基本一致,故鉴定为山奈酚。
鼠李黄素(6) 淡黄色固体,溶于甲醇。分子式为C16H12O7, ESI-MSm/z: 317 [M + H]+, 315 [M -H]-。1H NMR (DMSO-d6, 600 MHz): δ 3.90 (3H, s,-OCH3), 6.42 (1H, d,J= 2.1Hz, H-6), 6.17 (1H, d,J=1.8Hz, H-8), 7.50 (1H, d,J= 2.0 Hz, H-2′), 6.91 (1H,d,J= 8.5 Hz, H-5′), 7.54 (1H, dd,J= 8.5, 2.0 Hz, H-6′), 12.47(1H, s, OH);13C NMR (DMSO-d6, 150 MHz):δ146.1 (C-2), 135.5 (C-3), 175.8 (C-4), 160.6 (C-5),98.1 (C-6), 163.8 (C-7), 93.3 (C-8), 156.1 (C-9), 102.9(C-10), 122.1 (C-1′), 113.8 (C-2′), 146.2 (C-3′), 150.0(C-4′), 116.4 (C-5′), 119.3 (C-6′), 55.4 (-OCH3)。核磁数据与文献[15]数据基本一致,确定为鼠李黄素。
5,7-二羟基二氢黄酮 (7)淡黄色针状晶体,溶于丙酮。分子式为C15H10O4, ESI-MSm/z: 257 [M +H]+, 255 [M - H]-。1H NMR (DMSO, 600 MHz):δ5.43 (1H, dd,J= 3.2, 12.7Hz, H-2), 2.84 (1H, dd,J=3.2, 17.3 Hz, H-3), 3.11 (1H, dd,J=12.7, 17.2 Hz,H-3), 6.00 (1H, d,J= 2.0Hz, H-6), 6.03 (1H, d,J=2.0 Hz, H-8), 7.45 (2H, t,J= 3.2, 8.8 Hz, H-2′, 6′),7.44 (3H, dd,J= 3.2, 8.8 Hz, H-3′, 4′, 5′), 12.04(1H, s, 5-OH);13C NMR (DMSO, 150 MHz):δ79.2(C- 2), 43.3 (C-3), 195.8 (C-4), 164.4 (C-5), 96.8(C-6), 164.6 (C-7), 95.5 (C-8), 163.2 (C-9), 103.2(C-10), 138.3 (C-1′), 126.2 (C-2′,6′), 128.9 (C-3′, 4′,5′)。核磁数据与文献[8]数据基本一致,确定为5,7-二羟基二氢黄酮。
7,4′-二羟基二氢黄酮 (8)黄色油状物,溶于甲醇。分子式C15H10O5, ESI-MSm/z: 271 [M + H]+,269 [M - H]-。1H NMR (CD3OD, 600 MHz):δ5.38(1H, d,J= 12.8 Hz, H-2), 3.05 (1H, dd,J= 16.8, 13.2 Hz, Ha-3), 2.70 (1H, dd,J= 16.8, 2.4 Hz, Hb-3), 7.73(1H, d,J= 8.8 Hz, H-5), 6.50 (1H, dd,J= 8.8, 2.3 Hz,H-6), 6.36 (1H, d,J= 2.3 Hz, H-8), 7.32 (2H, d,J=8.5 Hz, H-2′, 6′), 6.82 (2H, d,J= 8.5 Hz, H-3′, 5′);13C NMR (CD3OD, 150 MHz):δ81.1 (C-2), 45.0 (C-3),115.0 (C-4a), 129.9 (C-5), 111.8 (C-6), 166.8 (C-7),103.9 (C-8), 165.6 (C-8a), 131.4 (C-1′), 129.0 (C-2′,6′), 116.4 (C-3′, 5′), 160.0 (C-4′), 193.6 (C=O)。核磁数据与文献[19]数据基本一致,故鉴定为7,4′-二羟基二氢黄酮。
5,7,3′,4′-四羟基二氢黄酮 (9)淡黄色针状晶体,溶于丙酮。分子式为C15H12O6, ESI-MSm/z:289 [M + H]+, 287 [M - H]-。1H NMR (DMSO-d6,600 MHz):δ5.43 (1H, dd,J= 3.2, 12.7 Hz, H-2),2.84 (1H, dd,J= 3.2, 17.3 Hz, H-3), 3.11 (1H, dd,J=12.7, 17.2 Hz, H-3), 6.00 (1H, d,J= 2.0 Hz, H-6),6.03 (1H, d,J= 2.0 Hz, H-8), 7.01 (1H, d,J= 2.0 Hz,H-2′), 6.91 (1H, d,J= 8.5 Hz, H-5′), 6.91 (1H, dd,J=8.5, 2.0 Hz, H-6′), 12.04 (1H, s, 5-OH);13C NMR(DMSO-d6, 150 MHz):δ79.2 (C-2), 43.3 (C-3), 195.8(C-4), 164.4 (C-5), 96.8 (C-6), 164.6 (C-7), 95.5 (C-8), 163.2 (C-9), 103.2 (C-10), 122.1 (C-1′), 113.8 (C-2′), 146.2 (C-3′), 150.0 (C-4′), 116.4 (C-5′), 119.4 (C-6′)。核磁数据与文献[20]数据基本一致,故鉴定为5,7,3′,4′-四羟基二氢黄酮。
5-O-乙酰基-3,7,3′,4′-四羟基二氢黄酮 (10)黄色针状晶体,溶于甲醇。分子式为C17H14O8, ESI-MSm/z: 347 [M + H]+, 345 [M - H]-。1H NMR (DMSOd6, 600 MHz):δ4.70 (1H, d,J= 11.4 Hz, H-2), 5.12(1H, d,J= 12.0 Hz, H-3), 6.05 (1H, d,J= 2.4 Hz, H-6), 6.09 (1H, d,J= 2.4 Hz, H-8), 7.01 (1H, d,J= 2.0 Hz,H-2′), 6.91 (1H, d,J= 8.5 Hz, H-5′), 6.91 (1H, dd,J=8.5, 2.0 Hz, H-6′), 2.45 (3H, 5-O-COCH3);13C NMR(DMSO-d6, 150 MHz):δ83.6 (C-2), 76.3 (C-3), 189.8(C-4), 163.8 (C-5), 94.8 (C-6), 168.4 (C-7), 93.8 (C-8), 163.1 (C-9), 101.2 (C-10), 122.1 (C-1′), 113.8 (C-2′), 146.2 (C-3′), 150.0 (C-4′), 116.4 (C-5′), 119.4 (C-6′), 21.2 (-OCOCH3), 169.4 (-OCO)。核磁数据与文献[15]基本一致,故鉴定为5-O-乙酰基-3,7,3′,4′-四羟基二氢黄酮。
7-甲氧基香橙素 (11)白色针状晶体,溶于甲醇。分子式为C16H14O6, ESI-MSm/z: 303 [M +H]+, 301 [M - H]-。1H NMR (CD3COCD3, 600 MHz):δ4.70 (1H, d,J= 11.4 Hz, H-2), 5.12 (1H, d,J= 12.0 Hz,H-3), 6.05 (1H, d,J= 2.4 Hz, H-6), 6.09 (1H, d,J=2.4 Hz, H-8), 7.44 (2H, dd,J= 8.4, 2.4 Hz, H-2′, 6′),6.91 (2H, dd,J= 8.4, 2.4 Hz, H-3′,5′), 3.86 (3H, s, 7-OCH3);13C NMR (CD3COCD3, 600 MHz):δ83.6(C-2), 72.3 (C-3), 197.8 (C-4), 163.8 (C-5), 94.8 (C-6), 168.4 (C-7), 93.8 (C-8), 163.1 (C-9), 101.2 (C-10),128.1 (C-1′), 129.4 (C-2′, 6′), 115 (C-3′, 5′), 158.0 (C-4′), 55.4 (7-OCH3)。以上数据与文献[21]一致,确定为7-甲氧基香橙素。
1.4 抗菌活性测试
采用菌丝生长速率法[22]测定化合物对荔枝霜疫霉菌的生长影响。分别取化合物0.25、0.5、1.0、2.0 和4.0 mg,用40µL DMSO 溶解,加入到10 mL灭菌后的PDA 培养基中,使化合物在培养基中的质量浓度分别为25、50、100、200 和400µg/mL。在含萃取物的PDA 平板中接入菌碟, 28 ℃培养7 d后测量菌落直径,每处理3 个重复,以不加萃取物为对照,计算菌丝生长抑制率,利用SPSS 软件计算毒力回归方程和半抑制浓度(IC50)。结果表明(表1),木犀草素 (4)、5,7-二羟基二氢黄酮 (7)、4′,7-二羟基二氢黄酮 (8)、3′,4′,5,7-四羟基二氢黄酮 (9)、7-甲氧基香橙素 (11)均对荔枝霜疫霉菌有明显的抑制作用;山奈酚 (5)的IC50为192.71µg/mL,具有中等抑制活性。

表1 部分化合物对荔枝霜疫霉菌的IC50 值Table 1 Antifungal activities (IC50) of compounds against Peronophythora litchi
2 结果和讨论
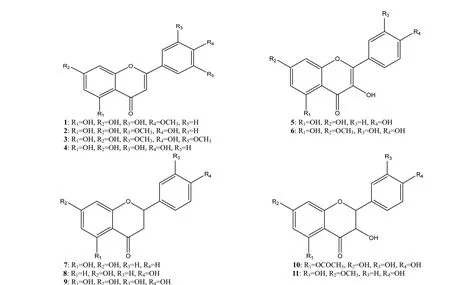
图1 化合物1~11 的结构Fig. 1 Structures of compounds 1-11
通过硅胶柱层析、葡聚糖凝胶柱层析和HPLC等色谱分离手段,从苦槛蓝叶的乙酸乙酯萃取部分分离得到11 个化合物。通过波谱分析及与文献数据对比,鉴定这些化合物结构分别为5,7,3′-三羟基-4′-甲氧基黄酮 (1)、3,5,7,4′-四羟基-3′-甲氧基黄酮(2)、5,7,4′-三羟基-3′,5′-二甲氧基黄酮 (3) 、木犀草素 (4)、山奈酚 (5)、鼠李黄素 (6)、5,7-二羟基二氢黄酮 (7)、7,4′-二羟基二氢黄酮 (8)、5,7,3′,4′-四羟基二氢黄酮 (9)、5-O-乙酰基-3,7,3′,4′-四羟基二氢黄酮 (10)和7-甲氧基香橙素 (11),其中化合物1~3、5~6、8~10 为首次从苦槛蓝植物中分离得到。部分化合物的体外抗菌活性实验结果表明,5,7-二羟基二氢黄酮 (7)对荔枝霜疫霉菌有很好的抑制作用,IC50为25.13µg/mL。据报道,5,7-二羟基二氢黄酮(7)对小菜蛾具有一定的产卵忌避、拒食作用[8];5,7-二羟基二氢黄酮 (7)、7-甲氧基香橙素 (11)对大肠杆菌与金黄色葡萄球菌均有明显的抑制作用[6];山奈酚 (5)具有良好的抗氧化活性和降血糖等作用[23-24];木犀草素 (4)具有抗肿瘤、抗氧化抗炎等作用[25],对香蕉炭疽菌具有明显的抑菌活性[5]。本研究结果进一步丰富了苦槛蓝叶中的化学成分数据库,对于推进苦槛蓝植物更有效的开发利用具有重要的意义。
