热量恒定下不同蛋白摄入量在肺结核合并糖尿病病人中的应用价值分析
2022-06-07曹春平王延芳董梦圆
曹春平,王延芳,董梦圆
随着经济发展进程的推进,我国居民生活水平明显提高,营养过剩问题较多,糖尿病(DM)等代谢性患病人数持续增长,2015年—2017年,我国成人DM患病率已达12.2%,其中2型糖尿病(T2DM)占比较大,在DM的膳食营养干预管理中,一般需要控制能量的摄入,推荐15%~20%的蛋白质占比[1]。肺结核(PTB)是一种慢性消耗性传染病,病人常表现出食欲下降、胃肠吸收功能不足和营养不良相关症状,而且结核病人常出现的低热症状也会加快病人的消耗,使其营养情况进一步恶化,所以结核病人常需要补充大量的能量物质[2]。由于DM病人的免疫力较差,与正常人相比,活动性PTB的发病率可增加至3倍,其中性别、体质指数(BMI)及DM确诊时间等因素对其有重要影响,肺结核合并糖尿病病人(PTB-DM)由于PTB本身的营养消耗问题以及DM病人的代谢紊乱等原因,常发生营养不良,其发病率可达60%上下,对于PTB病人的病情控制产生不利影响,容易造成PTB的初次治疗失败,其中蛋白质缺乏造成的营养不良占比较大,所以蛋白质相关的营养膳食管理对于PTB-DM的疾病控制和预后有着重要影响[3]。有证据显示,在能量保持的基础上添加1~1.5 g/(kg·d)蛋白质摄入可以促进疾病好转[4],现有以下实验探究PTB-DM病人不同蛋白质膳食方案的干预效果。
1 资料与方法
1.1 一般资料 从本科2018年8月—2020年8月接诊的肺结核合并糖尿病病人中选取研究对象107例,用掷币法将其分为对照组和观察组,其中对照组53例,男40例,女13例;年龄18~75(55.87±11.93)岁;血糖控制方法有单纯口服降糖药20例,加用胰岛素注射33例;体质指数(BMI)16~30(22.98±3.22)kg/m2。观察组54例,男42例,女12例;年龄18~75(56.40±12.05)岁;BMI 16~30(22.74±3.16)kg/m2;血糖控制方法有单纯口服降糖药23例,加用胰岛素注射31例。两组病人年龄、性别、病程等方面比较差异均无统计学意义(P>0.05)。纳入标准:①同时符合PTB和DM相关诊断[5-6];②可以经口进食;③愿意配合且签署知情同意书。排除标准:①合并有严重DM并发症;②血液、免疫系统疾病引发的贫血等;③合并有恶性肿瘤;④因为胃肠疾病引发营养不良;⑤肝肾功能不全。本研究已经伦理委员会审核批准。
1.2 方法 为两组病人进行疾病相关知识的宣教,遵医嘱采取相应的干预措施,为病人制定个体化营养膳食管理方案,必要时求助营养科医师。①计算每个病人膳食的基础热量。首先计算病人标准体重(kg),40岁及以上病人为身高(cm)-105,其他病人为身高(cm)-100。然后计算BMI值,并根据下表计算标准体重能量摄入并乘以110%为PTB-DM消耗,单位为kcal/(kg·d)(1 kcal=4.1 kJ),病人体温每上升1 ℃,总能量增加13%。②根据病人情况计算蛋白质摄入量,对照组标准为1.0 g/(kg·d),观察组标准为1.5 g/(kg·d)。③根据上述计算结果和病人喜好制定相应食谱。

表1 病人个体化营养膳食管理标准 单位:kcal/(kg·d)
1.3 观察指标 ①糖脂代谢水平:干预前后分别抽取两组病人清晨空腹静脉血6 mL,测定其空腹血糖(FBG)、糖化血红蛋白(HbA1c)、三酰甘油(TG)、低密度脂蛋白(LDL)及高密度脂蛋白(HDL)水平,从用餐第一口食物开始计时,测定其餐后2 h血糖(2 hPBG)值。②人体测量指标:干预前后测量两组病人体重、三头肌皮褶厚度(TSF)、上臂肌围(AMC),记录体重丢失率=[(干预后体重-干预前体重)/干预前体重]×100%。③氧化应激水平:两组病人干预前后各抽取清晨空腹静脉血5 mL,检测其中超氧化物歧化酶(SOD)、血清维生素C(VC)、血清维生素E(VE)及丙二醛(MDA)水平。
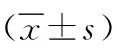

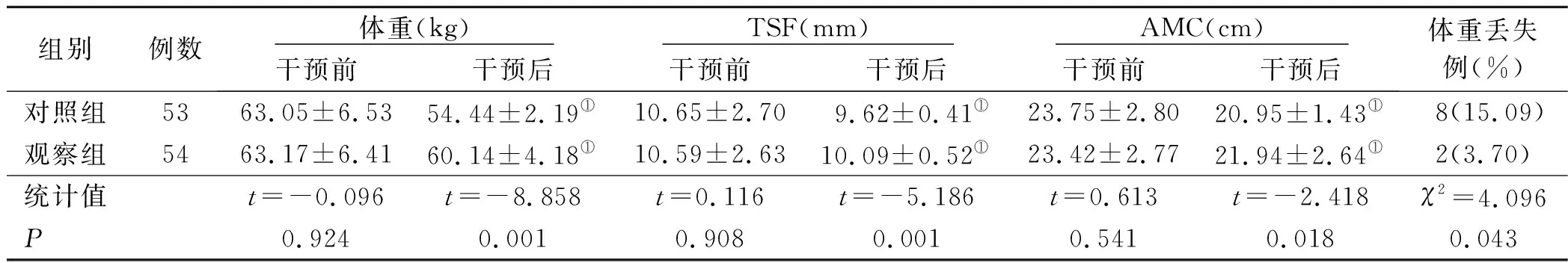
表3 两组病人干预前后人体测量指标比较

2 结果
3 讨论
与单纯的的PTB和DM病人相比,PTB-DM病人在治疗过程中的营养风险增加,更容易导致营养不良和药物损伤等并发症的发生,使得抗结核治疗的预后变差,不利于病人病情的干预和管理[7]。PTB和DM可以相互影响,其中不同严重程度的DM病人中PTB患病率最高可达36%,PTB病人中也有16%左右并发有DM[8-9]。其中DM病人由于糖和脂肪代谢紊乱,使体内能量过剩并降低组织抵抗力,使体内环境更利于结核杆菌生存,而且DM病人免疫功能下降,更易感染,此外DM的微血管和周围神经病变使肺部环境变差,更易导致结核病发生,而PTB病人的感染症状会加重胰岛细胞负担并且使胰高血糖素水平上升,加重DM病人病情,而且诸多抗结核药物容易引起肾功能损伤,促进糖代谢紊乱[10]。所以两病共同治疗的基础是营养干预,控制食物总体热量并调整蛋白质等物质的比例可以同时满足两者的营养需求,有利于病人的恢复[11]。
DM病人由于糖代谢紊乱等因素的影响,会导致包括糖脂代谢在内一系列内分泌物过程的异常,而PTB病人的感染等情况又会加重此过程,使得病人血糖和血脂水平上升,但是PTB病人消耗性疾病的特点,血脂水平上升不如血糖水平明显[12-13]。在PTB的病理过程中,由于发热感染情况的发生,蛋白质为主的营养物质的消耗量显著增加,在临床上常用体重、TSF、AMC等相关指标用作评价PTB病人的治疗效果[14-15]。干预后观察组体重、TSF、AMC、体重丢失率均优于对照组,提示经基础热量+1.5 g/(kg·d)的蛋白质摄入量可有效降低病人体重下降情况,改善营养状态。PTB病人因机体呈高分解代谢特点,大量瘦体组织遭受分解,蛋白质供能达到总能量消耗的15%以上甚至高达25%~30%,极易出现负氮平衡。据报告在PTB病人中,有38%病人并发低蛋白血症,蛋白质分解的主要终产物是尿素氮(BUN),当机体处于应激状态时,蛋白质分解增加,BUN合成增多,血浆BUN水平可增高,其变化可直接反映机体蛋白质代谢情况[16]。通过基础热量+1.5 g/(kg·d)的蛋白质摄入量干预可以有效增加神经肽Y和饱食激素等物质的分泌,促使病人减少包括果糖在内其他食物的摄入,可快速补充机体所消耗的蛋白质,有效缓解蛋白质进行性分解过程,减低体重丢失程度,纠正营养不良事件的发生[17]。
在PTB病人的病灶中,由于结核分枝杆菌的作用,往往会产生过量的氧化自由基超出人体自身的调节能力,发生氧化应激反应[18-19]。其中PTB-DM病人胰岛功能受损,使得线粒体偶联反应大量增加,调剂能力减弱,氧化应激水平更甚,造成体内VC、VE等抗氧化物质减少,MDA等反应产物增加,此外病人营养水平降低也会导致包括SOD抗氧化酶和氨基酸产物水平的降低[18-19]。观察组病人干预后MDA水平较干预前降低,VE、VC和SOD水平均较干预前升高,且干预后观察组各项指标水平变化幅度大于对照组(P<0.05)。高热量、高优质蛋白饮食一方面可以有效缓解病人营养状况,增加SOD等抗氧化酶的合成,增强抗氧化反应,另一方面,蛋白质等物质的足量补充可以改善体内无氧代谢情况,减少氧化自由基的产生,进而降低MDA等氧化应激反应产物水平,使VC和VE水平回升。
综上所述,基础热量+1.5 g/(kg·d)蛋白质膳食方案可以有效改善PTB-DM病人的糖脂代谢水平,恢复病人营养不良状态,降低氧化应激水平,临床疗效佳。
