RGB色彩模式识别多组分苏丹红含量
2022-06-06毕秀成郭英
周 佳,毕秀成,郭英
(汉江师范学院 化学与环境工程学院,湖北 十堰, 442000)
苏丹红是一类萘酚偶氮染料,包括苏丹红Ⅰ、苏丹红Ⅱ、苏丹红Ⅲ和苏丹红Ⅳ,具有颜色鲜艳、着色性强、价格便宜等特点[1]。由于苏丹红属于工业染色剂,人体摄入后会引起某些病变,因此该类物质严禁用于食品生产加工,食品检测机构在检测食品时,往往不会对其进行测定,因而添加了苏丹红的食物就不易被发现[2-3]。不法商家为了保证颜色稳定和延长保质期,往往添加多种染色剂,给检测带来较大困扰。
多组分苏丹红检测方法主要包括高效毛细管电泳法[4]、高效液相色谱法[5-6]、同步荧光检测法[7-8]等。上述方法普遍存在仪器成本高、操作步骤复杂、常规检测适用性不强等不足。
运用分光光度法测定多组分样品的含量,如果各种吸光物质的吸收曲线相互重叠,根据吸光度加和性特征,在某一波长下总吸光度等于各组分吸光度的和,一定条件下样品可不经过分离即可对混合物进行多组分含量分析[9]。图片比色法测定单一溶液的浓度时发现,吸光度与颜色量值存在一定的线性关系,可构建吸光度、颜色量值和浓度之间的函数关系。本文以苏丹红Ⅱ和苏丹红Ⅲ混合溶液为测试对象,建立了吸光度与颜色量值的数学模型。不同波长的情况下,测得混合溶液的吸光度,经模拟运算,获得混合溶液三原色值,根据各组分浓度与颜色量值的关系推算出各组分的浓度。该方法在多组分混合物浓度测定中具有一定的适用性。
1 实验部分
1.1 试剂与仪器
苏丹红Ⅱ号和苏丹红Ⅲ号(分析纯,天津致远化学试剂有限公司);正己烷(分析纯,国药集团化学试剂有限公司);实验用水为超纯水。722SP型分光光度计(上海棱光技术有限公司);EX124A型电子分析天平(厦门莱斯德科学仪器有限公司);自制拍摄箱体(长38 cm、宽25 cm、高15 cm),上部开圆孔放置光源,侧壁开矩形孔放置拍摄手机;iPhone 5S(苹果公司)、VIVO Y71(维沃移动通信有限公司)。
1.2 实验原理
同一溶液,不同浓度,最大吸收波长一样,吸收曲线的形状相似,吸光度A与浓度C成正比。对于多组分有色溶液,如果各组分之间无相互作用,组分与组分的吸光度可以进行加和计算,以式(1)表示:
(1)
图片比色法是近年来兴起的一种新型分析测试方法。在运用手机比色法测定苏丹红Ⅱ浓度时,发现不同浓度的溶液,吸光度与颜色量值存在线性关系。对于多组分苏丹红溶液,根据吸光度加和性特点,构建混合溶液吸光度与颜色量值之间的数学关系式,用式(2)表示:
(2)
(3)
(4)
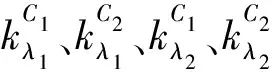
1.3 溶液的配制
称取3 mg苏丹红Ⅱ和3 mg苏丹红Ⅲ,用正己烷分别定容至100 mL,在4 ℃环境下保存。取4支25 mL比色管,分别加入1 mL、2 mL、3 mL、4 mL苏丹红Ⅱ标准液,再取4支25 mL比色管,分别加入1 mL、2 mL、3 mL、4 mL苏丹红Ⅲ标准液,用正己烷稀释至刻度。
2 结果与讨论
2.1 最大吸收波长的确定
向两只1 cm比色皿中分别添加苏丹红Ⅱ和苏丹红Ⅲ标准液,以正己烷为参比液,在400~600 nm范围内,每隔5 nm测定一次吸光度,最大吸收峰附近间隔2 nm测定一次。两组溶液的吸收曲线见图1,由图可知苏丹红Ⅱ的最大吸收波长为474 nm,苏丹红Ⅲ的最大吸收波长为504 nm。

图1 苏丹红Ⅱ和苏丹红Ⅲ吸收曲线
2.2 吸光度与颜色间接值关系的构建
由于拍摄过程中样品的图像采集容易受外界环境的影响,用获得的RGB值直接进行计算,会引起较大误差[10],因此引入误差传递原理[11],将直接测定的R、G、B值转化间接测定值XR、XG、XB,可以降低误差带来的影响,XR可用关系式(5)表示,XG、XB同理可得,其中Gr为颜色灰度值。
(5)
取配制好的苏丹红Ⅱ和苏丹红Ⅲ标准溶液各4组,依次加入8支比色皿,将比色皿放置在拍摄箱中距离拍摄手机正前方12 cm处,以VIVO手机的手电筒光为环境光源,iPhone 5S为取样手机。拍摄完毕后,将比色皿转入分光光度计,分别在474 nm和504 nm处测定对应组分的吸光度,吸光度A与XR、XG、XB趋势关系可用图2表示。

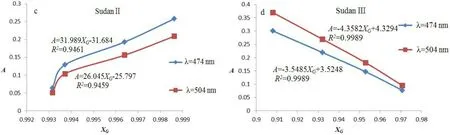
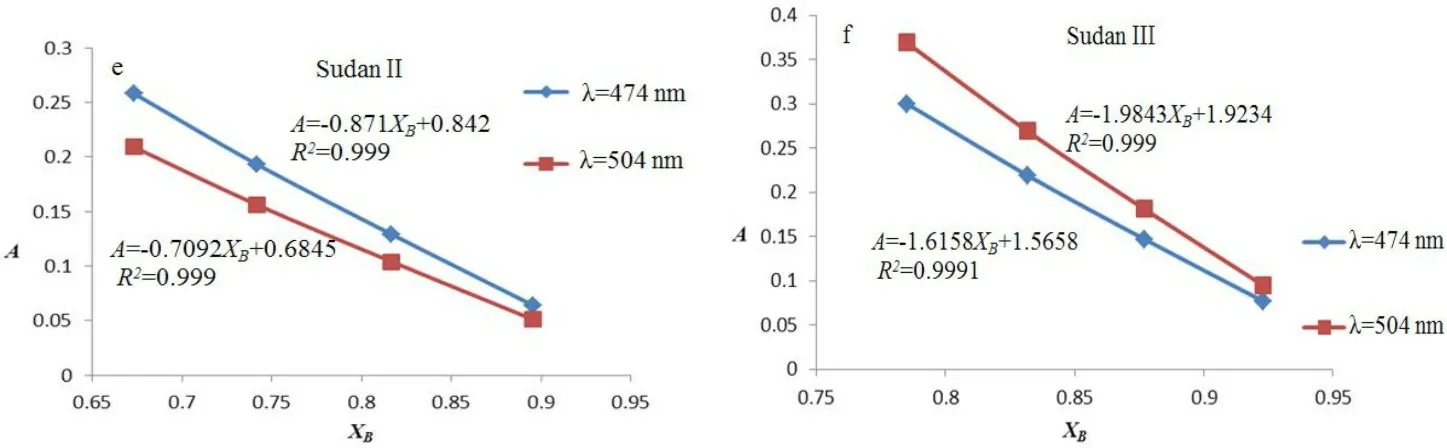
图2 吸光度与颜色测量值关系曲线
由图2可知,不同波长处,除苏丹红Ⅱ(c图)浓度与间接测量值XG线性拟合度较低,另外5组吸光度A与间接测量值XR、XG、XB的线性关系较好。以苏丹红Ⅱ和苏丹红Ⅲ浓度与XB的关系曲线作为测试组,将图2e和图2f中的线性方程带入到式(3)和式(4)得到组合方程式(6)和式(7),式(6)和式(7)分别是苏丹红Ⅱ和苏丹红Ⅲ混合溶液在波长474 nm和504 nm时吸光度与XB的组合方程。为了验证该方法的可靠性和稳定性,用苏丹红Ⅱ和苏丹红Ⅲ浓度与XR的关系曲线作为对照组,得到式(8)和式(9),比较两者测得的结果。
(6)
(7)
(8)
(9)
以苏丹红Ⅱ和苏丹红Ⅲ系列标准溶液为对象,用手机比色法获得间接测量值,建立苏丹红Ⅱ浓度C与XB、XR的线性方程,分别为C=-0.0617XB+0.9671(R2=0△.9991)和C=-0.0204XR+1.0308(R2=0.9955);苏丹红Ⅲ浓度C与XB、XR的线性方程,分别为C=-0.0382XB+0.9688(R2=1)和C=-0.0487XR+1.0255(R2=0.9978)。
取2 mL苏丹红Ⅱ标准溶液,加入到25 mL比色管中,添加2 mL苏丹红Ⅲ标准溶液,定容后摇匀,由测得的混合溶液吸光度A(474 nm)和A(504 nm)计算出苏丹红Ⅱ和苏丹红Ⅲ的XB、XR,分别带入两者的标准溶液浓度C与间接值XB、XR的关系式,将计算值与标准值进行比较,结果如图3所示。
图3可以看出,苏丹红混合溶液中,测定组的各组分浓度与对照组的各组分浓度基本一致,证实了构建的混合溶液与颜色间接测量值XB、XR的关系在测定各组分浓度的合理性。计算浓度与标准浓度对比,发现测定的苏丹红Ⅱ浓度准确度较高,苏丹红Ⅲ浓度偏高,说明该方法识别苏丹红混合溶液苏丹红Ⅱ的含量是有效的。

图3 测定浓度和标准浓度比较
2.3 样品的测定及回收率实验
取1 mL苏丹红Ⅱ标准溶液至10 mL比色管,添加1 mL苏丹红Ⅲ标准溶液,定容至刻度,按照2.2中测定方法,分别在λ=474 nm和λ=504 nm处采集混合溶液吸光度A。平行配制3组样液进行测定,得到不同颜色间接值时,苏丹红Ⅱ标准样品的测定结果,见表1和表2。
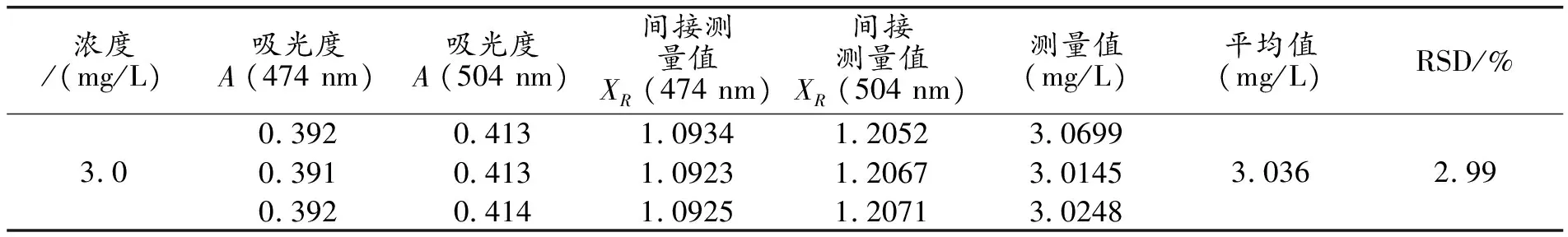
表1 XR时苏丹红Ⅱ的测定结果

表2 XB时苏丹红Ⅱ的测定结果
向1 mL苏丹红Ⅱ标准样品中依次添加2 mL苏丹红Ⅱ和2 mL苏丹红Ⅲ混合加标样,每份样品配制3次,摇匀后进行测定。间接测量值XR为测试变量时,苏丹红Ⅱ的加标回收率为101.9 %~105.6 %,苏丹红Ⅲ加标回收率为121.5 %~123.4 %;间接测量值XB为测试变量时,苏丹红Ⅱ的加标回收率为101.4 %~104.9 %,苏丹红Ⅲ加标回收率为121.4 %~123.2 %。两者均证实该方法在测定苏丹红二组分混合溶液中,苏丹红Ⅱ浓度的准确度较高,能初步预测苏丹红Ⅲ的浓度。
3 结论
基于吸光度具有加和性的特点,建立了分光光度法和图片比色法联用检测混合溶液的方法。引入误差传递规律降低了三原色值RGB的测定误差,构建了吸光度与颜色间接测定值的函数方程,测定了苏丹红Ⅱ和苏丹红Ⅲ混合溶液的各组分含量,具有较好的重复性,其中苏丹红Ⅱ测定的选择性和准确度高,为多组分溶液的测定提供了一种参考。
