微型实验在高中化学教学中的应用
2022-06-02钟天丽广西壮族自治区南宁市邕宁高级中学
钟天丽 广西壮族自治区南宁市邕宁高级中学
化学是一门与实验密切相关的自然学科。高中化学涉及很多实验,既能很好地激发学习者的学习兴趣,又能深化其对所学知识的理解,因此,实验不仅是教学的重要内容,而且是各类测试的必考知识点。但传统的实验具有准备时间长、操作复杂、使用仪器多、使用试剂量大等缺点。为更好地克服传统实验的弊端,教育工作者将微型实验应用于教学活动中,获得了良好的实验效果。高中化学教学中应认识到微型实验的优点,提高微型试验应用意识,结合具体教学内容积极查阅相关资料,做好微型实验的设计与展示,更好地提升学生的学习体验,提高课堂教学效率。
一、微型实验用于SO2性质教学中
二氧化硫是硫的重要氧化物,是高中化学学习的重要知识点,其性质主要有:漂白性、弱酸性、强还原性等。教学中为使学习者更好地理解与掌握二氧化硫的性质,并能够根据具体的反应现象准确地判断对应的性质,既要求学生牢固记忆二氧化硫性质以及对应的反应方程式,又要注重借助微型实验增加教学趣味性,给学习者留下深刻印象。
例如,在课堂上做微型实验,如图1所示,使用棉球分别蘸取品红溶液、NaOH酚酞溶液以及淀粉I2溶液,按照图示塞到硬质玻璃管中。

图1
为更好地激活高中化学课堂,驱使学生主动地思考,做上述实验之前要求学习者根据自己对SO2性质的理解,思考如下问题:(1)实验中制取二氧化硫的原理是什么?(2)棉球a、b、c分别有什么变化,分别反映了SO2的哪些性质?(3)使用什么化学试剂吸收尾气?
运用微型实验很好地吸引了学习者的注意力,并及时抛出问题引发学习者思考,能更好地激发其学习热情。认真观察不难发现,实验中通过挤压右侧的胶头,使浓硫酸滴加到亚硫酸钠固体上产生二氧化硫气体,对应的实验原理为该反应没有化合价变化,因此属于复分解反应。二氧化硫能够使品红溶液褪色,因此棉球a的颜色逐渐变淡,验证了二氧化硫的漂白性;SO2为酸性氧化物能够与NaOH溶液反应生成Na2SO3,使得棉球b中的碱性变弱,棉球逐渐褪色;I2遇到淀粉呈现蓝色,SO2具有还原性,和I2发生反应SO2+I2+2H2OH2SO4+2HI,因I2不断被消耗,棉球c的蓝色逐渐变淡。尾气中主要是未反应的SO2,因此,可使用碱性溶液进行吸收。
该微型实验使用的试剂量较少,操作方便,能研究SO2的很多性质。课堂上运用该微型实验不仅达到了传统实验的目的,而且通过对实验现象的深入分析,使学生理解了棉球褪色的不同原因,启发其在以后分析化学现象时透过现象看本质,多分析引起实验现象的内在原因,如此才能更好地把握化学知识精髓。
二、微型实验用于Cl2性质教学中
氯及其化合物是高中化学中非常重要的内容,而氯气的物理、化学性质以及制取方法更需要学习者深入理解,牢固掌握。在进行Cl2性质教学中考虑到氯气具有毒性,为确保安全,更好地激发学习者的学习热情,应认真分析课本中实验存在的弊端,结合自身授课经验做好相关微型实验的设计,运用微型实验与学习者一起探究氯气的化学性质。
例如,课堂上按照图2设计微型实验。将溴化钾溶液、含淀粉的KI溶液以及FeCl2溶液分别滴加到点滴板中a、b、c凹槽中。同时,取少量KMnO4晶体放到表面皿中,向KMnO4晶体上滴加浓盐酸后迅速使用烧杯盖住。课堂上为使学习者更好地理解该实验,围绕以下问题与学习者进行互动:(1)实验中是怎样制取氯气的?请写出化学反应方程式并判断化学反应类型。(2)点滴板a、b、c凹槽中的实验现象是什么?从中能够说明哪些问题?(3)实验中能否使用MnO2代替KMnO4,为什么?
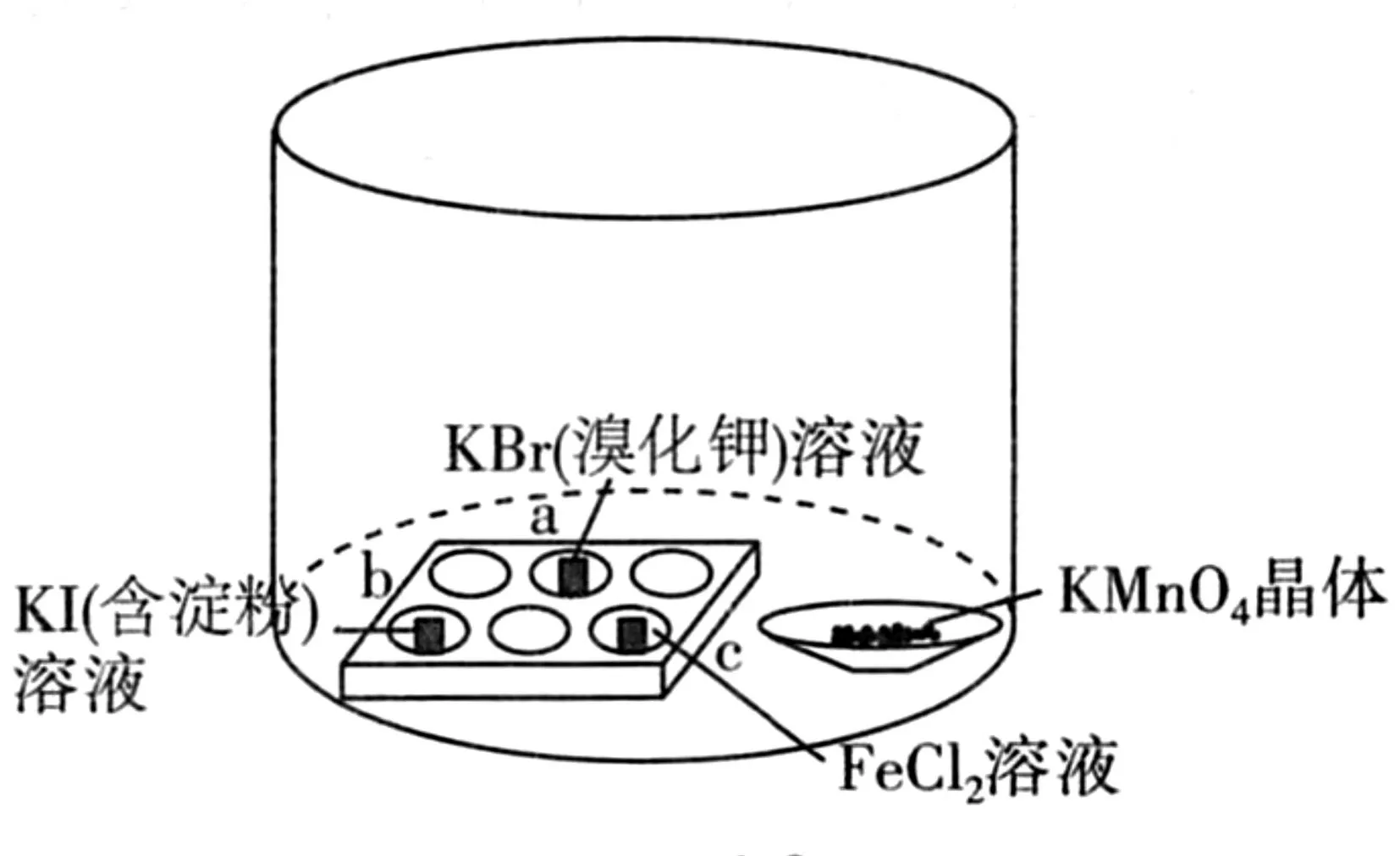
图2
认真分析不能发现实验中通过KMnO和浓盐酸反应制取氯气,对应的化学反应方程式为反应中Cl元素化合价发生变化,因此属于氧化还原反应。在a、b、c三个凹槽中分别发生反应结合氧化还原反应知识可得Cl2的氧化性强于Br2、I2、Fe3+。KMnO4和浓盐酸反应在常温下就能进行,但如果使用MnO2代替KMnO4则需要加热,因此,为确保实验的正常进行不能替换。
上述微型实验不仅制取了Cl2,而且验证了氯气与其他物质氧化性的强弱关系,实验虽小,但学习者从中学习到的内容并不少。课堂上为学生展示微型实验并与学生一起分析实验现象、实验原理,进一步提高其对氯气性质的认识。课堂上学习者表现非常积极,不仅认真观察实验过程、实验现象,而且积极讨论,共同探讨发生的化学反应,得出了正确的实验结论,顺利地完成了课堂教学目标。
三、微型实验用于电化学教学中
电化学是高中化学的重要知识点,是高考的必考内容。电化学主要分为原电池以及电解池两个重要部分,需要学习者深入理解原电池与电解池原理,并能灵活应用于相关问题的分析中。因原电池与电解池原理较为接近,相关知识点容易混淆,教学实践中应注重应用微型实验增加教学内容的趣味性,帮助学习者在头脑中形成清晰模型,遇到相关问题能够迅速地找到切入点。
例如,在讲解电化学知识时,在课堂上展示图3所示的微型实验,准备好两个试纸将其密切接触,使用铅笔芯当做电极,分别和表面皿上的试纸接触,接通电源后,观察实验现象。课堂上为加深学习者的理解,锻炼其学以致用能力,围绕微型实验提出以下问题,并提问学生代表,了解其回答问题的正误,检验学习者是否真正地掌握电解池知识:(1)与浸润饱和实验水的KI-淀粉试纸接触的铅笔芯对应的电极名称是什么?(2)两个试纸出现什么现象,原理是什么?(3)两个试纸中的离子是怎样运动的?

图3
该微型实验构成简单,实验过程不难理解,因其外加电源,因此,属于电解池。分析时需要正确、深入理解电解池原理,尤其不能死记硬背相关结论。课堂上与学习者一起回顾电解池原理,而后进行提问。联系所学的电解池知识可知,与电源正极相连的是阳极,与电池负机相连的是阴极。由电解池原理可知,阴极离子得到电子,即H+得到电子生成H2,导致试纸中OH-浓度变大,则pH试纸变蓝。阳极离子失去电子,Cl-失去电子生成Cl2,Cl2可将I-氧化成I2,而I2遇淀粉呈蓝色,KI-淀粉试纸呈蓝色。试纸中阴离子向左侧移动,阳离子向右侧移动。
上述微型实验使用的器材非常简单,而且使用的实验试剂非常少,实验现象非常明显,能很好地巩固学生所学。同时,通过提问学生代表驱使其进行深层次地思考,分析两极发生的电极反应以及反应中生成的物质,很好地锻炼了其分析问题的能力。不仅如此,学习者通过观察、思考微型实验,获得了良好的学习启发,在分析电化学相关问题时不仅要正确分析对应的电极名称,而且需要分析各电极中的离子种类,对比各离子的放电顺序。
四、微型实验用于浓硫酸性质教学中
浓硫酸是高中化学中较为重要的一类酸,其与稀硫酸的性质有所不同。教学实践中为使学习者更好地掌握浓硫酸的性质,包括强氧化性、酸性、催化性、脱水性等,搞清楚其与稀硫酸性质的区别,应提高实验在教学中的应用意识,增加教学趣味性的同时帮助学习者更好地记忆,尤其通过对课本中实验的改进,积极应用微型实验开展教学活动,更好地提高课堂教学效率。
例如,在进行蔗糖与浓硫酸反应教学中,使用分液漏斗、试管、导管等实验器材,按照如图4所示装置进行实验器材的组装。课堂上展示实验过程,通过旋转分液漏斗的旋塞使浓硫酸与蔗糖接触,要求学习者认真观察,填写如下空格:
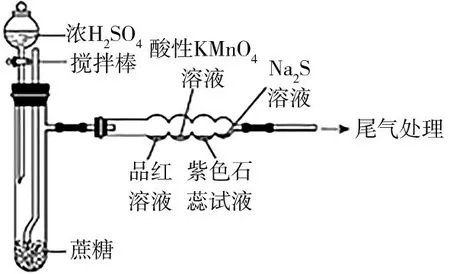
图4
(1)该实验体现了浓硫酸的_____性与______性。
(2)反应的实验现象有:____、____、____、____。
(3)该实验能证明SO2具有_____性、_____性。
(4)处理尾气时可使用_______(填写一种碱),也可以使用______(填写一种盐)。
要想正确地填写上述空格,需要明确该微型实验依据的原理。根据所学可知,浓硫酸与蔗糖反应,蔗糖先变黑后膨胀,变黑是因为浓硫酸具有强氧化性,而体积膨胀表现浓硫酸的脱水性。产生的二氧化硫气体具有漂白性,可使品红溶液褪色,而且SO2因具有还原性可使高锰酸钾溶液褪色,且能和Na2S反应生成淡黄色的单质硫沉淀。因二氧化硫污染空气,不能直接排放,因此可使用氢氧化钠溶液吸收尾气,当然也可使用高锰酸钾溶液对尾气进行处理。
实践中借助微型实验为学生展示浓硫酸与蔗糖反应的实验,吸引学习者的注意力,不仅能够使学习者清晰地看到实验现象,而且能验证反应产物的相关性质,尤其考虑了尾气的处理,避免了空气污染,一举多得,达到了常规实验无法取得的实验效果。课堂上学生认真观察实验过程,积极思考,尝试着填写空格中的内容,加深了印象,圆满地完成了课堂教学目标。
五、微型实验用于浓硝酸性质教学中
稀硝酸与浓硝酸是高中化学较为重要的酸,其中当硝酸的浓度超过69%时为浓硝酸。浓硝酸涉及的知识点较多,包括浓硝酸的保存、浓硝酸与金属的反应以及浓硝酸的强氧化性等。其与稀硝酸的性质较为接近,因此,很多学习者容易混淆相关知识点。讲解该部分知识时既要注重引导学习者尝试将浓硝酸与稀硝酸的性质进行对比记忆,又要注重运用微型实验开展教学活动,加深其对浓硝酸的印象。
例如,在进行浓硝酸和Cu反应的教学中,课堂上使用塑料瓶盛放适量浓硝酸并在干燥管中盛放适量铜片,将其按照图5所示装置连接起来。同时,在干燥管口塞上蘸有碱液的棉花,开展微型实验。实验过程中为使学习者更好地掌握所学内容,设计如下问题要求其思考、讨论:(1)该微型实验有哪些优点?怎么控制反应的进行与停止?(2)写出该实验涉及的化学反应方程式。(3)在干燥管口塞蘸碱液棉花的目的是什么?(4)使用该微型实验装置是否能够做木炭与浓硝酸反应的实验,为什么?
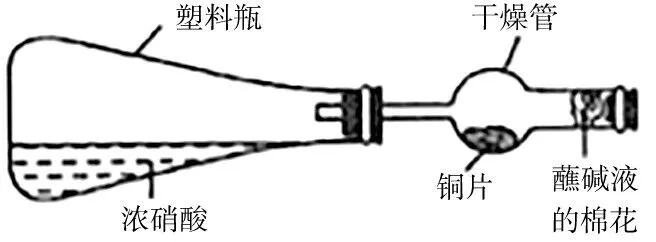
图5
通过挤压塑料瓶,浓硝酸进入到干燥管便可发生反应,当倾斜塑料瓶浓硝酸回流至塑料瓶中反应便停止,因此,该实验的优点是操作简单,容易控制反应过程,而且避免了产物NO2气体的逸出,较为环保。该实验的反应原理为Cu+4HNO3(浓)Cu(NO3)2+NO2↑+2H2O。因反应的产物中有NO2,会对空气造成污染,因此,运用碱液进行吸收。因浓硝酸和碳的反应需要加热,因此,使用该微型实验装置无法实现。
教学中鼓励学习者积极思考,相互讨论上述问题,不仅激活了化学课堂,而且使其更加透彻地理解与掌握了实验内容,尤其当学习者正确地回答出问题时,在课堂上及时进行表扬,使其尝到学习的成就感。从整个实验效果来看,达到了预期效果,学习者学习热情非常高涨。不仅如此,通过该微型实验的展示,给学习者带来一定启发,使其在以后的学习中善于思考,能够发现课本中实验的不足,并积极尝试设计相关微型实验进行改进。
众所周知,高中化学实验内容较多,如何提高实验教学质量与效率,激发学习者的学习热情与潜力,一直是教育工作者关注的重点。微型实验不仅能达到传统实验的效果,而且在实验器材、实验试剂的选择与应用上更为节省,在实践中的应用效果显著,深受广大师生的喜爱。借助微型实验开展教学活动,能获得良好的教学效果,教学中应做到:其一,积极主动地查阅相关资料,结合具体教学进度,在课堂上做微型实验,给学生带来不一样的视觉感受以及学习体验,增强化学课堂的新鲜感。其二,围绕微型实验设计问题,要么与学习者互动,要么要求学习者思考、作答,使其参与到实验过程中来,更好地掌握相关实验内容。其三,结合学习者的表现及时给予针对性的指引与点拨,纠正其理解上的误区,使其体会到学习的乐趣以及成就感,更加自觉地开展学习活动。
