紫外光活化过硫酸盐脱色处理甲基橙染料的研究
2022-06-01陈博凯李玉坤杨书申炊衣琦陈彬洁杨凯峰
张 丹,陈博凯,晁 聪,李玉坤,杨书申,炊衣琦,陈彬洁,杨凯峰
(1.中原工学院能源与环境学院,河南郑州 450007;2.河南省食品安全检测工程技术研究中心,河南郑州 450000)
随着工业的飞速发展,纺织行业需求快速增加, 大量的水被消耗,据统计,仅1 kg 纺织品的生产需要使用约200 L 水〔1〕,因而排放的废水越来越多。根据2015 年环境统计年报中工业行业废水排放情况〔2〕,纺织废水排放量位居41 个工业行业中第三,仅次于化学原料和化学制品制造业、造纸和纸制品业,年排放量为18.4 亿t,占重点行业废水排放总量的10.1%。纺织业废水具有水量大、有机物浓度高、可生化性差等特点,而且成分复杂,含有大量的染料、印染助剂、无机盐、浆料、纤维杂质等〔3〕,其中染料尤其是偶氮染料用量多、难降解,在环境中具有持久性,若不经过处理直接排放,将会严重影响周围水体、土壤的环境安全,危害人类健康〔4〕。因此,在废水排放前,高效去除废水中染料污染物至关重要,成为国内外研究的热点。传统的染料废水处理方法如:膜过滤、混凝/絮凝法、微生物或酶法、吸附法等,在应用中存在吸附、膜过滤方法仅凭分离难以对染料进行有效去除,生物过程通常需要足够的曝气、搅拌设备,投资成本高、预处理周期长等限制〔5-6〕。
近年来,高级氧化过程(Advanced oxidation processes,AOPs)因其在水和废水处理领域具有降解效率高、通用性好、环境友好等优点而受到广泛关注〔7-8〕,AOPs主要通过反应体系原位产生硫酸根自由基(SO4·-)、羟基自由基(HO·)等高活性氧化物种对有机污染物进行氧化去除,其中基于过硫酸盐的AOPs 产生的SO4·-相比于传统AOPs 产生的HO·,优势在于:(1)SO4·-半衰期更长,延长与污染物的作用时间;(2)可以在较宽的酸碱度范围存在;(3)与H2O2相比,过硫酸盐作为固体氧化剂,具有稳定性好,方便运输、储存和使用等优势;(4)SO4·-具有较强的氧化能力,氧化还原电位为2.6 V,与HO·接近〔9〕。但是过硫酸盐在室温和没有活化剂的条件下,氧化反应通常很缓慢,当通过加热、超声、光照、过渡金属、生物炭等方式活化时,过硫酸盐的O—O 键断裂产生活性氧化物种SO4·-〔10-12〕。其中紫外光活化过硫酸盐能够在温和条件下通过简单操作实现高效的有机污染物降解,已应用到酸性红37、罗丹明B、亚甲基蓝、酸性蓝129 等染料污染物的去除〔13-19〕。然而研究多集中在罗丹明B、亚甲基蓝等染料及过硫酸盐的活化方式,而纺织印染废水成分复杂,环境因素如无机阴离子、印染助剂等对染料去除效果影响的研究较少。
本研究以偶氮染料甲基橙为目标污染物,研究甲基橙在紫外光活化过硫酸盐体系的去除过程,探究甲基橙初始浓度、过硫酸盐(Persulfate,PS)用量对脱色效果的影响,同时考察纺织印染废水中无机阴离子(HCO3-、Cl-)、印染助剂〔柠檬酸钠、十二烷基苯磺酸钠(Sodium dodecyl benzene sulfonate,SDBS)〕等环境因素对染料去除效果的影响,利用自由基猝灭实验对反应的主要自由基种类进行探讨。研究有助于理解UV/PS 体系下甲基橙染料的反应过程,为AOPs 应用于实际纺织印染废水的处理提供理论基础和技术支撑。
1 实验部分
1.1 试剂与仪器
试剂:甲基橙、甲醇、乙醇、叔丁醇、NaHCO3、NaCl、柠檬酸钠均购于天津科密欧化学试剂有限公司,过硫酸钾购于国药集团化学试剂有限公司,SDBS 购于天津百伦斯生物技术有限公司。实验所用化学试剂均为分析纯,实验用水为电阻率18.2 MΩ·cm 的超纯水。
仪器:FA2004 型电子天平,上海舜宇恒平科学仪器有限公司;UV1901 型紫外可见分光光度计,上海棱光技术有限公司;ZQ-GHX-IV 型光化学反应仪,上海争巧科学仪器有限公司。
1.2 实验方法
紫外光活化过硫酸钾氧化去除甲基橙实验在光化学反应仪中进行,采用8 套磁力搅拌装置,搭配8套100 mL 容量的石英反应管,汞灯灯源放置在反应仪的中心,使每个反应管光照均匀。将初始浓度为40 μmol/L 甲基橙模拟染料废水转移到反应管中,加入一定量的过硫酸钾储备液,磁力搅拌使溶液充分混合均匀。开启汞灯辐照并记录反应时间,在不同的反应时间用移液器移取反应溶液,加入到添加甲醇猝灭剂的取样管中,避免样品储存期间缓慢形成自由基的影响。采用紫外可见分光光度计对反应前后溶液中甲基橙的浓度进行分析。基于控制变量法,考察甲基橙初始浓度(10~100 μmol/L)、过硫酸钾投加量(40~800 μmol/L)以及HCO3-、Cl-、柠檬酸钠、十二烷基苯磺酸钠等水体环境因子(浓度分别为0.05~5.0 mmol/L)对甲基橙去除效果的影响。
1.3 甲基橙分析方法
利用UV1901 型紫外可见分光光度计,以超纯水作为参比对照,对40 μmol/L 甲基橙溶液在400~800 nm 波长范围内进行全波长扫描,确定最大吸收波长为465 nm。在465 nm 处分别测定浓度范围为1~120 μmol/L 甲基橙标准溶液的吸光度,根据浓度与吸光度的标准曲线方程(y=0.011 8x+0.033 8,线性相关系数R2=0.999),外标法定量反应前后样品溶液中甲基橙的浓度。
2 结果与讨论
2.1 甲基橙初始浓度的影响
为探究紫外光活化过硫酸盐对甲基橙的去除效果,分别考察了单独过硫酸钾PS 氧化(CMO∶CKPS=1∶5)、单独汞灯辐照条件下甲基橙的去除趋势,结果见图1。

图1 不同反应条件下甲基橙的去除趋势Fig.1 Removal trend of methyl orange under different reaction conditions
由图1 可知,单独PS 氧化条件下,当自然光光照时间为180 min 时,甲基橙浓度变化(残余比例Ct/C0)仅降低了4.5%,持续光照420 min,浓度降低11.6%,表明自然光条件下PS 比较稳定,自身氧化能力有限,需要外界条件活化。单独汞灯辐照时,甲基橙在紫外光下发生缓慢降解,光照90 min 时甲基橙去除率为14.1%。将反应过程中甲基橙浓度随时间的变化趋势利用准一级反应动力学模型进行拟合,模型方程见式(1)。

式中:Ct、C0——分别代表反应时间为t时甲基橙的残余浓度和初始反应浓度,μmol/L;
t——反应时间,min;
k——准一级反应动力学速率常数,min-1。
利用准一级动力学方程模型描述反应过程,发现单独PS 氧化、单独汞灯辐照条件下甲基橙的反应过程均符合准一级反应动力学,且线性拟合相关系数R2≥0.984。单 独PS 氧 化 时,k为0.000 290 min-1;单独汞灯辐照,不加PS 时,紫外光光照甲基橙反应k为0.001 56 min-1;结果表明单独PS 氧化和单独汞灯对甲基橙的去除作用有限。
过硫酸钾投加量200 μmol/L,不同甲基橙初始浓度条件下,UV/PS 体系反应过程甲基橙残余比例Ct/C0的变化趋势见图2。
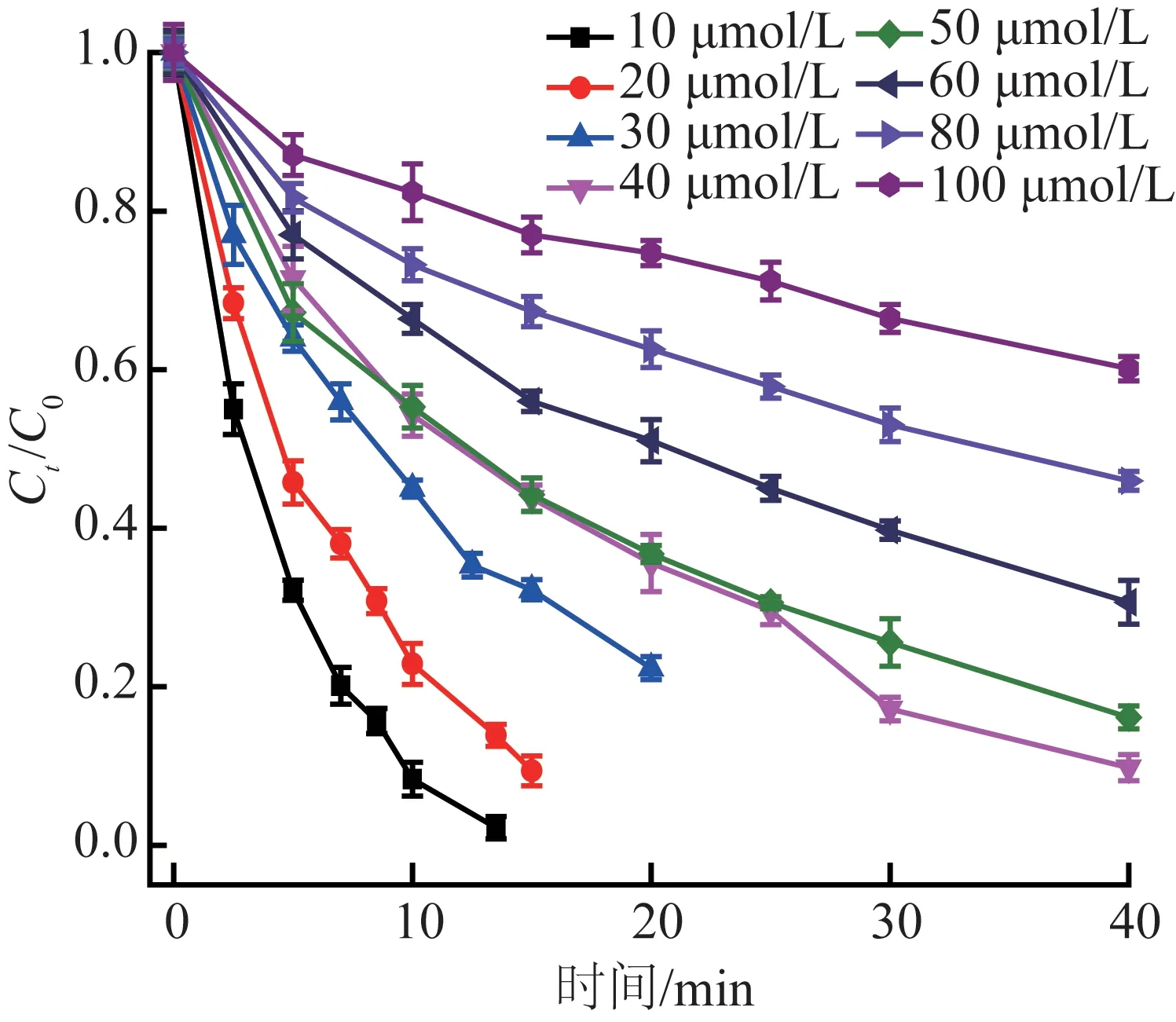
图2 甲基橙初始浓度对去除效果的影响Fig.2 Effect of initial concentration of methyl orange on its removal performance
由图2 可知,根据甲基橙残余比例Ct/C0趋势变化可知,随着甲基橙初始浓度从10 μmol/L 增大到100 μmol/L,反应速度越来越慢。利用准一级动力学方程(式1)描述不同甲基橙初始浓度的反应过程,所得的动力学参数见表1。

表1 不同甲基橙初始浓度的反应动力学参数Table 1 Kinetic parameters under different initial concentrations of methyl orange
由表1 可知,实验过程均符合准一级反应动力学,R2≥0.964。甲基橙反应速率从10 μmol/L 的0.271 min-1降低到100 μmol/L 的0.011 8 min-1,相应的半衰期则从2.6 min 增大到58.7 min,反应过程受到显著抑制。染料污染物在UV/PS体系下的降解主要通过两种途径〔9〕:(1)吸收紫外光能量直接破坏染料分子的化学键,根据单独汞灯辐照实验结果,甲基橙的直接光解并不显著;(2)紫外光辐照活化PS 产生SO4·-,SO4·-在溶液中通过一系列链式反应生成HO·〔20〕,见式(2)~(4),SO4·-、HO·等活性氧化物种破坏染料污染物分子的化学键,降解染料生成小分子,这是甲基橙去除的主要途径。当过硫酸钾投加量一定的情况下,在紫外光作用下,体系中产生的活性氧化物种是一定的,随着甲基橙初始浓度增加,溶液的透光率降低,反应所消耗的活性物种随之增加,因此速率越来越慢。此外以甲基橙初始浓度为40 μmol/L 为例,利用去除一个数量级(即90%)污染物消耗的能量EE/O(electric energy per order)进行能耗评价〔21〕,经计算UV/PS 技术的能耗包括紫外灯能量和过硫酸钾消耗,约为63.85 kW·h/m3,低于文献〔22〕报道的光-Fenton 工艺(100~167 kW·h/m3)、UV/H2O2(76.4~85.7 kW·h/m3)和UV/O3(85 kW·h/m3),体现了UV/PS体系去除甲基橙的优势和应用潜力。
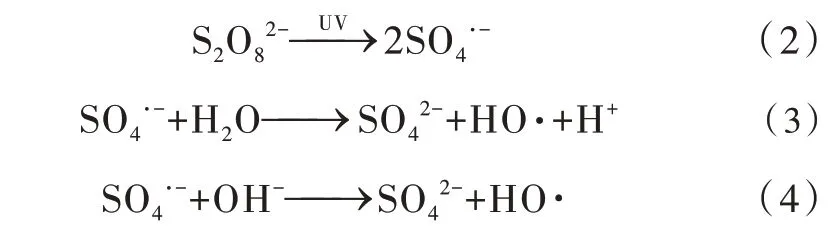
2.2 过硫酸钾投加量对甲基橙去除的影响
不同过硫酸钾投加量对UV/PS 体系去除甲基橙效果的影响见图3。
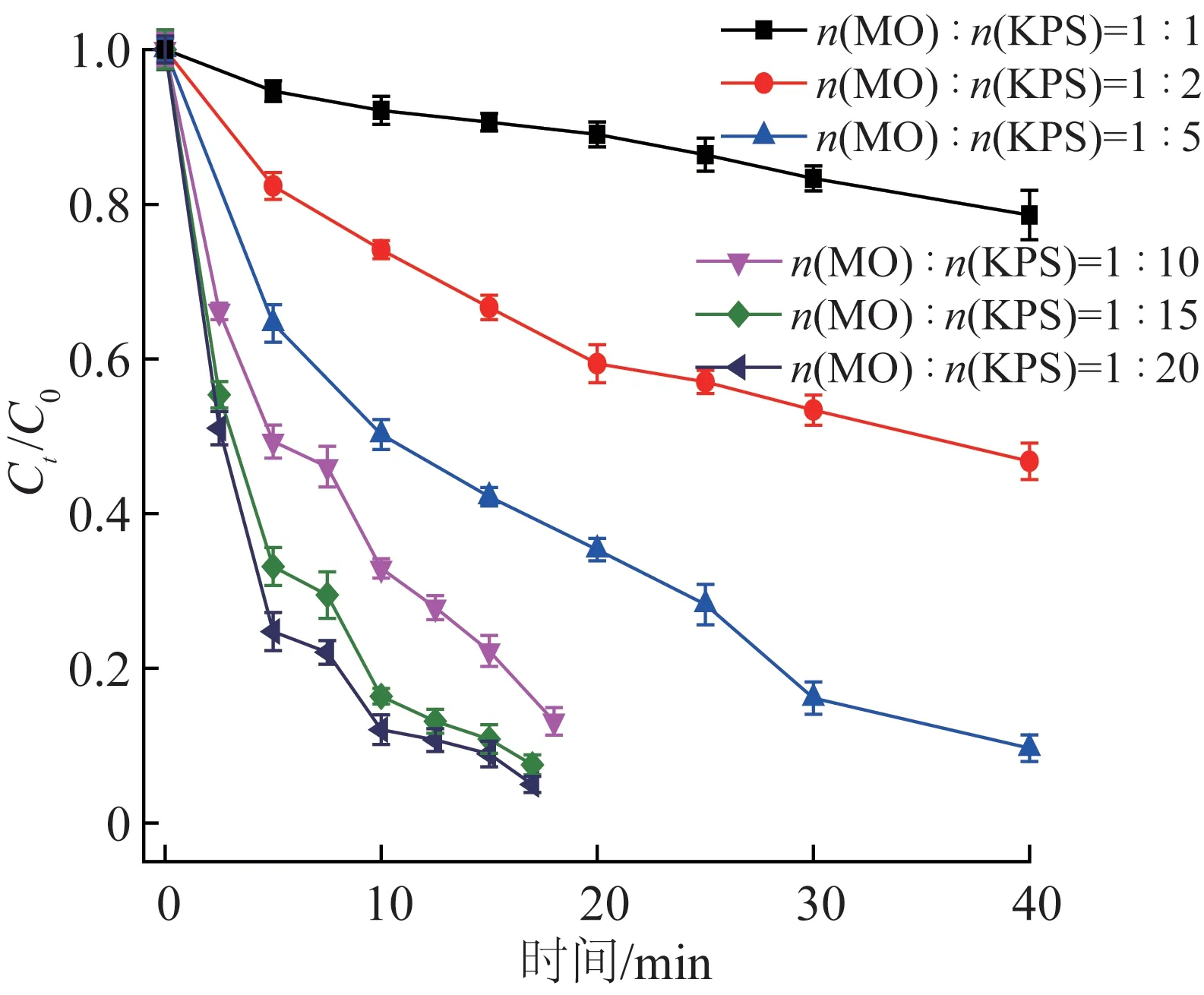
图3 PS 投加量对甲基橙去除的影响Fig.3 Effect of PS dosage on the removal of methyl orange
由图3 可知,随着PS 投加量的增加,n(甲基橙)∶n(PS)从1∶1 变化到1∶20,反应速度越来越快。利用准一级动力学方程(式1)描述不同PS 投加量下甲基橙的反应过程,所得动力学参数见表2。
由表2 可知,反应过程均符合准一级动力学,R2≥0.947。甲基橙浓度一定时,PS 投加量与反应速率呈现正相关关系,反应速率从过硫酸钾投加量40 μmol/L 的0.005 56 min-1逐渐增加到800 μmol/L 的0.159 min-1,相应的半衰期则从124.4 min 降低到仅为4.4 min。而且与不投加过硫酸钾的空白对照实验结果(图1)相比,投加过硫酸钾能显著提高甲基橙的去除效果。当紫外光光照强度一定时,随着PS 浓度增加,紫外光活化PS产生更多的活性氧化物种,而且PS 与受光激发的甲基橙碰撞增多,有利于甲基橙中光生电子向PS 传递,从而提高反应体系中活性氧化物种的数量,甲基橙去除速率加快。
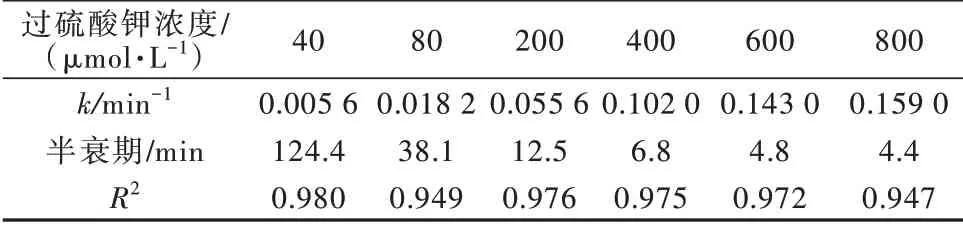
表2 不同PS 投加量的反应动力学参数Table 2 Kinetic parameters under different PS doses
2.3 无机阴离子对甲基橙去除的影响
无机阴离子如HCO3-、Cl-普遍存在于水中,可与高级氧化过程产生的活性氧化物种反应,影响活性物种的产生及染料降解转化效能。其中HCO3-作为清除剂,可与SO4·-、HO·发生反应,形成相应的二次自由基,见式(5)~(6);HCO3-还能与S2O82-反应形成过碳酸根离子和SO42〔-式(7)〕,因此HCO3-的存在会影响氧化剂过硫酸盐的稳定性。
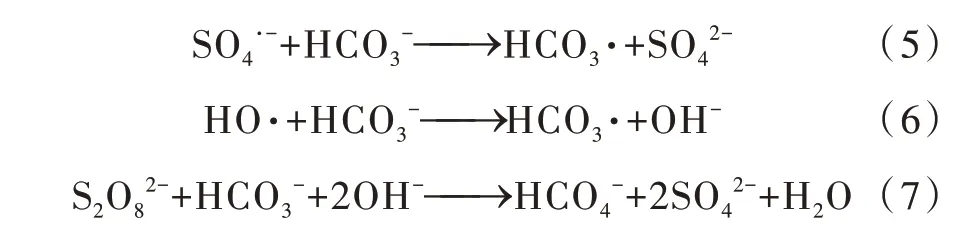
为探究HCO3-对UV/PS 去除甲基橙的影响,开展了不同HCO3-浓度的实验,实验条件为40 μmol/L甲基橙、200 μmol/L 过硫酸钾,甲基橙残余比例Ct/C0随时间的变化趋势见图4。
由图4 可知,HCO3-浓度的变化对甲基橙在UV/PS 体系的去除效果具有影响。利用式(1)拟合得到的动力学数据见表3。

图4 HCO3-浓度对甲基橙去除的影响Fig.4 Effect of bicarbonate concentration on the removal of methyl orange
由表3 可知,反应过程均符合准一级动力学方程,R2≥0.972。当HCO3-浓度从0 mmol/L 增加到0.5 mmol/L 时,k从0.055 9 min-1降低到0.044 1 min-1,相应的半衰期则从12.4 min 增加到15.7 min;当HCO3-浓度继续增加到5 mmol/L 时,反应速率反而呈现逐渐增加趋势,达到0.059 6 min-1,略高于不加HCO3-的0.055 9 min-1。HCO3-倾向于与紫外光活化PS 产生的SO4·-、HO·反应,消耗自由基,使得甲基橙去除速率降低;同时由于紫外光条件下可以激活HCO3-,因此HCO3-的存在可能导致碳酸氢根自由基的形成;而且HCO3-的加入,可以改变反应溶液的酸碱度,使溶液pH 升高,促进SO4·-、HO·的转化,HCO3-还能直接与过硫酸盐反应生成过碳酸盐,通过单电子氧化有机污染物〔23〕,这可能是HCO3-浓度进一步增加时,甲基橙去除速率轻微增加的原因。因此,在过硫酸盐高级氧化工艺中应考虑实际印染废水中HCO3-对氧化剂稳定性、染料去除效能的影响。
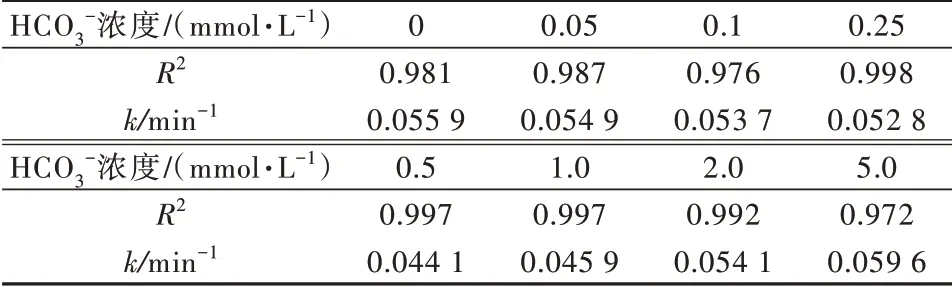
表3 HCO3-对UV/PS 体系去除甲基橙动力学的影响Table 3 Effect of HCO3- on the kinetic parameters of methyl orange by UV/PS process
Cl-作为水体中常见的无机阴离子,探究Cl-对UV/PS 体系氧化去除甲基橙效能的影响很有必要。考察了不同Cl-浓度对甲基橙去除的影响,反应条件为40 μmol/L 甲基橙、200 μmol/L 过硫酸钾,不同Cl-浓度下甲基橙残余比例Ct/C0的变化趋势见图5,拟合的动力学参数见表4。
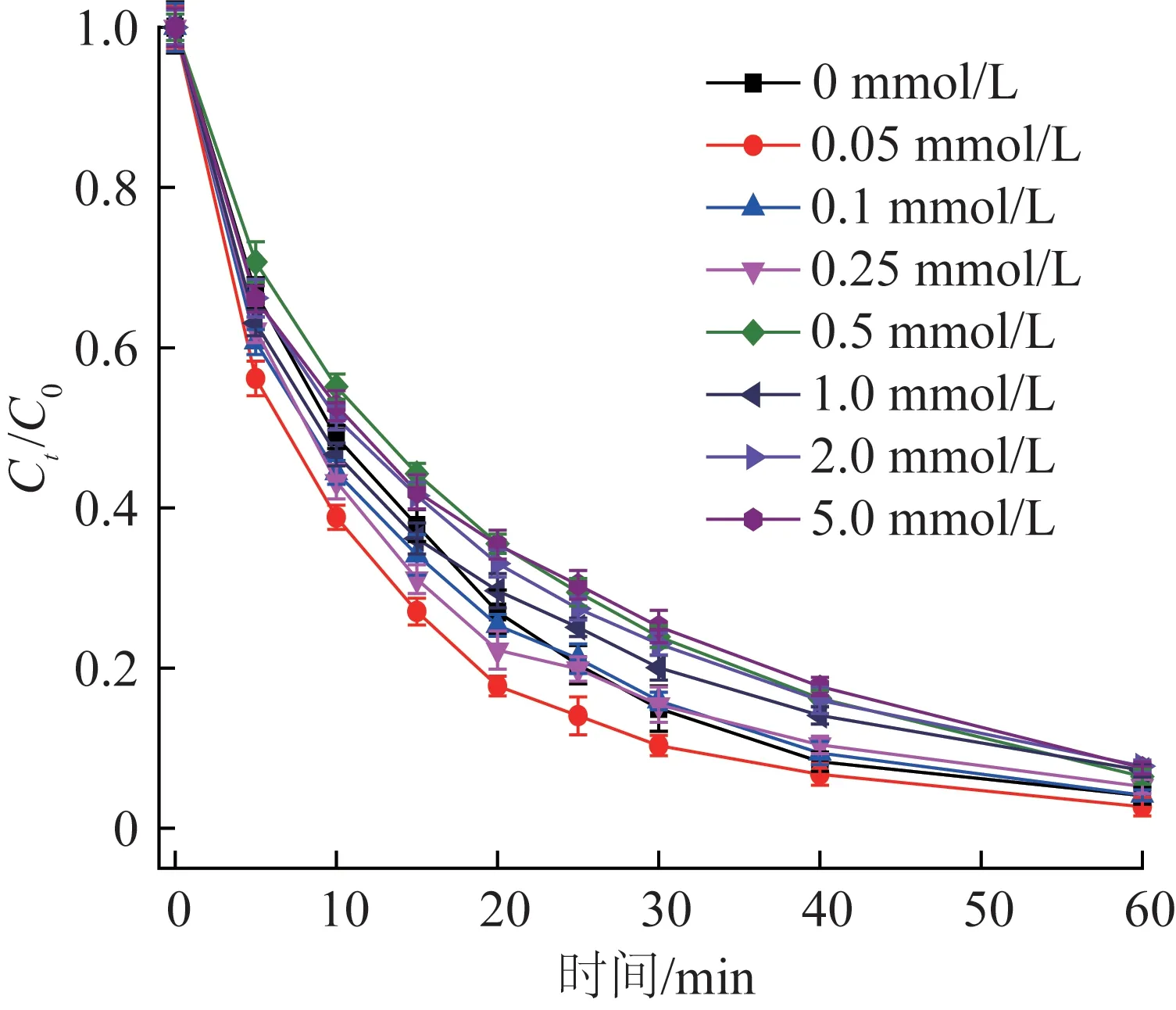
图5 Cl-浓度对甲基橙去除的影响Fig.5 Effect of chloridion concentration on the removal of methyl orange
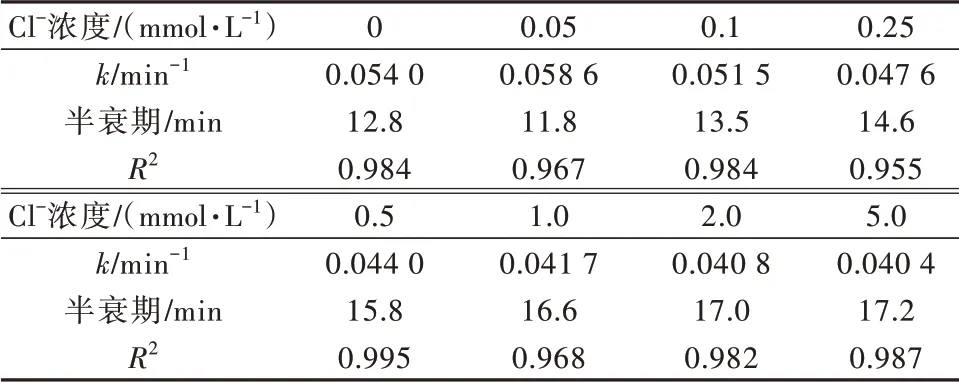
表4 Cl-对UV/PS 体系去除甲基橙动力学的影响Table 4 Effect of Cl- on the kinetic parameters of methyl orange by UV/PS process
由图5、表4 可知,低Cl-浓度(0.05 mmol/L)对甲基橙的去除起到轻微促进作用,k从0.054 0 min-1升高到0.058 6 min-1,继续增加Cl-浓度,反应过程受到抑制,速率越来越低,1 mmol/L Cl-时速率为0.0417 min-1,而当Cl-浓度进一步增大到5 mmol/L 时,反应速率降低幅度很小,抑制作用变得不明显。紫外光作为AOPs体系常用的均相活化方法,通过能量输入有效活化过硫酸盐产生SO4·-、HO·,Cl-的存在不影响能量输入,因此Cl-对紫外光的催化活性没有影响〔24〕,但Cl-会影响反应过程自由基的产生。UV/PS 体系去除甲基橙过程中,Cl-的影响呈现双重作用:低浓度Cl-对甲基橙去除有轻微促进作用,高浓度抑制去除,可能原因是低浓度下Cl-和SO4·-、HO·反应生成氯自由基Cl·,见式(8)~(10),作为AOPs 体系的衍生活性物质之一,Cl·具有更高的选择性,因此观察到轻微促进现象;而当Cl-浓度增加时,Cl·会与Cl-发生反应,见式(11),生成低活性的Cl2·-,降低反应过程的去除速率。此外,水体中存在Cl-时,Cl-浓度的增加可能会导致反应过程出现氯化中间产物,由于氯化中间产物的潜在风险,因此AOPs 实际应用修复纺织印染废水时,应密切关注水体中氯离子的影响。
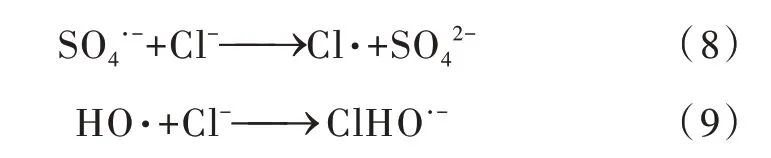
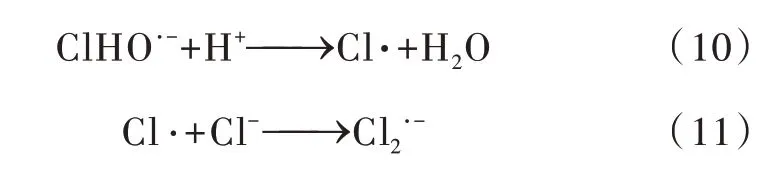
2.4 印染助剂对甲基橙去除的影响
在纺织印染废水中,除染料污染物外,印染助剂螯合剂(如柠檬酸钠)、表面活性剂(如十二烷基苯磺酸钠SDBS)等的存在同样不容忽视,对甲基橙去除效能的影响值得探究。研究考察了不同柠檬酸钠、SDBS 浓度下,UV/PS 体系氧化甲基橙的反应过程,反应条件为40 μmol/L 甲基橙、200 μmol/L过硫酸钾,反应趋势见图6,拟合的动力学参数见表5。
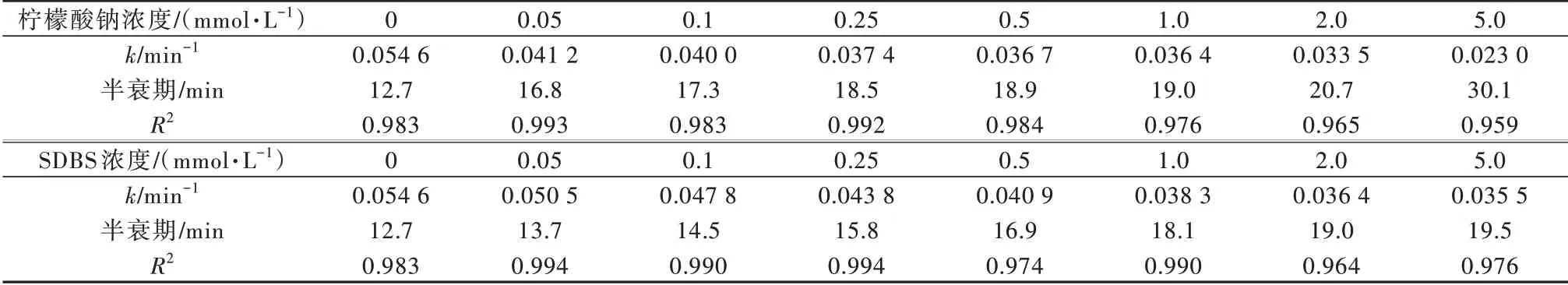
表5 印染助剂对UV/PS 体系去除甲基橙动力学的影响Table 5 Effect of dyeing auxiliaries on the kinetic parameters of methyl orange by UV/PS process

图6 柠檬酸钠(a)、十二烷基苯磺酸钠(b)浓度对甲基橙去除的影响Fig.6 Effect of sodium citrate(a)and sodium dodecyl benzene sulfonate(b)concentration on the removal of methyl orange
柠檬酸钠的存在会影响甲基橙去除速率,当柠檬 酸 钠 浓 度 从0 mmol/L 增 加 到5.0 mmol/L 时,k从0.054 6 min-1降低到0.023 0 min-1,相应的半衰期则从12.7 min 增加到30.1 min。随着柠檬酸钠浓度的增加,对甲基橙去除效果的抑制程度越高,这可能与柠檬酸钠作为一种缓冲试剂,可将反应溶液pH 稳定在一个范围有关。未添加柠檬酸钠时,过硫酸钾的活化分解作为一个释放H+的过程,通过检测反应过程的pH 变化发现,溶液的pH 降低,而当添加5.0 mmol/L 柠檬酸钠时,由于缓冲作用,反应过程pH 变化并不显著,从而干扰了活性氧化物种的产生路径,导致去除速率的降低。
十二烷基苯磺酸钠(SDBS)作为常用的阴离子表面活性剂,在纺织印染领域作为棉织物精炼剂、退浆助剂、染色匀染剂使用,在印染废水中会产生大量泡沫,阻碍气体溶解、水体与空气中氧气的交换,降低溶解氧含量,影响水体的自然净化和人工净化。由图6、表5 可知,SDBS 的存在同样会影响甲基橙去除速率,当SDBS 浓度从0 mmol/L 增加到5.0 mmol/L时,k从0.054 6 min-1降低到0.035 5 min-1,反应速率与SDBS 浓度呈负相关,SDBS 浓度越高,对甲基橙去除的抑制程度越高,这可能跟UV/PS 体系下SDBS 与甲基橙的竞争作用有关。紫外光辐照过硫酸钾活化产生的活性氧化物种如SO4·-、HO·,不仅可以去除甲基橙,还会促进SDBS 的去除,因此SDBS 的存在会消耗UV/PS 体系产生的自由基,降低用于氧化甲基橙的自由基含量,从而降低甲基橙去除速率,导致甲基橙去除速率随着SDBS 浓度的增加而逐渐降低。此外,与环境因子柠檬酸钠对UV/PS 体系去除甲基橙的影响相比,同样浓度的SDBS抑制程度较浅,例如5.0 mmol/L 柠檬酸钠时甲基橙的去除相比于未添加条件,反应速率k减少57.9%,而5.0 mmol/L SDBS 条件下k减少35.0%,推测可能与柠檬酸钠、SDBS 的影响方式不同有关。
2.5 UV/PS 体系自由基猝灭实验
为探究UV/PS 体系去除甲基橙过程起主导作用的活性氧化物种种类,研究向反应体系中投加一定量的自由基猝灭剂乙醇、叔丁醇(0、1.0、2.0、5.0、10.0 mmol/L),考察不同浓度对甲基橙去除的影响,结果见图7。
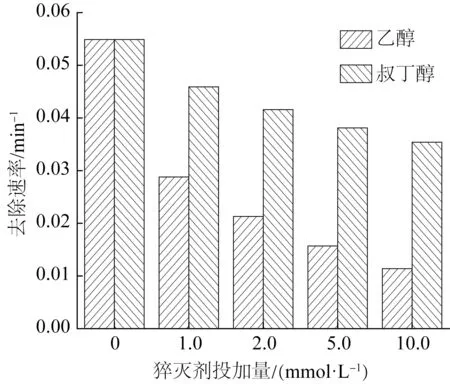
图7 猝灭剂投加量对甲基橙去除速率的影响Fig.7 Effect of scavenger concentration on the removal rate of methyl orange
由图7可知,加入1.0 mmol/L乙醇后,k从0.054 9 min-1显著降低到0.028 8 min-1,随着乙醇浓度增加到10.0 mmol/L时,k降低到0.011 4 min-1,甲基橙的去除在很大程度上受到抑制。当加入叔丁醇浓度从1.0 mmol/L增 加 到10.0 mmol/L 时,k从0.045 9 min-1下 降 到0.035 4 min-1,叔丁醇的抑制效果低于乙醇。乙醇、叔丁醇作为自由基反应常用的猝灭剂,研究表明基于猝灭剂与自由基之间的反应速率差异,可用于评估自由基的存在可能〔25〕。乙醇与HO·、SO4·-反应的二级速率常数分别为(1.2~2.8)×109L/(mol·s)、(1.6~7.7)×107L/(mol·s),均具有较高的反应活性,认为乙醇可同时猝灭HO·和SO4·-;而叔丁醇与HO·、SO4·-反应的二级速 率 常 数 分 别 为(3.8~7.6)×108L/(mol·s)和(4.0~9.1)×105L/(mol·s),认为叔丁醇是非常有效的HO·猝灭剂〔26〕。比较UV/PS 体系加入相同量的乙醇和叔丁醇,乙醇对甲基橙去除速率的抑制效果更显著,表明紫外光活化过硫酸钾时,SO4·-、HO·自由基是主要的活性氧化物种,共同对甲基橙的去除起作用;加入乙醇和叔丁醇的抑制作用差异可归因于SO4·-的相对贡献。基于添加10.0 mmol/L 乙醇、叔丁醇猝灭实验的反应速率,初步估算〔27〕SO4·-、HO·对甲基橙去除的贡献比例分别为43.7%、35.5%。
3 结论
(1)相比单独UV、单独PS,UV/PS 体系能显著去除甲基橙,甲基橙初始浓度为40 μmol/L、PS 投加量200 μmol/L时,甲基橙反应速率常数达到0.056 3 min-1;甲基橙去除效果随着初始浓度的增加或者PS 浓度的降低呈现减小的趋势。
(2)无机阴离子HCO3-、Cl-对甲基橙去除的影响趋势不同,随着HCO3-浓度升高,甲基橙反应速率呈现先降低后增加的趋势,而低浓度Cl-有利于甲基橙去除,高浓度抑制去除效果。
(3)甲基橙去除效果随着螯合剂柠檬酸钠、表面活性剂SDBS 的浓度升高而降低,柠檬酸钠的缓冲作用干扰活性氧化物种的产生路径,SDBS 与甲基橙存在竞争作用。
(4)通过自由基猝灭实验可知UV/PS 体系去除甲基橙过程中,SO4·-、HO·是对染料去除起重要作用的活性氧化物种。
