络合浸渍法制备Ag/Al2O3-TiO2催化剂及其催化燃烧丙烷性能
2022-06-01程丽军袁善良
程丽军, 刘 照, 袁善良, 蒋 毅*, 张 彪*
[1. 太原工业学院 环境与安全工程系,山西 太原 030008; 2. 中国科学院 成都有机化学研究所 挥发性有机物污染控制材料与技术国家工程实验室(成都),四川 成都 610041]
挥发性有机化合物(VOCs)是大气污染的主要组成部分,是颗粒物(PM 2.5)形成的主要前驱体,同时也是导致雾霾天气的重要元凶,将对人类健康产生有害影响。随着石油化工和化学工艺的发展,挥发性有机化合物的排放量也在不断增加[1-2]。因此,各种VOCs排放的治理技术成为了当前科研工作的热点之一。其中,催化燃烧技术具有起燃温度低、无二次污染及效率高等优点,被认为是最有效的治理挥发性有机化合物排放的途径之一。短链烷烃作为一种主要的VOCs排放源,由于其在催化剂表面的附着力相对较弱,且化学性质非常稳定[3]。因此,开发出低成本高活性的短链烷烃催化燃烧催化剂有重要意义。
目前用于短链烷烃催化燃烧的催化剂主要有贵金属(Pt[4]、 Pd[5]、 Ru[6])和过渡金属氧化物。负载型贵金属(Pt、 Pd、 Ru等)催化剂表现出较高的低温催化燃烧活性。然而,由于其成本高和容易中毒等缺点,其商业应用往往受到限制。过渡金属(Mn、 Co、 Ni等)氧化物具有来源广泛、价格低廉和抗毒性强等优点,但其催化燃烧VOCs的活性仍然较差[7-9]。而Ag的价格远低于Pt、 Pd、 Ru等,且Ag基催化剂作为许多氧化反应的有效催化剂而备受关注。目前,银基催化剂主要用于甲醇选择性制甲醛、乙烯环氧化等,近年来,在环境催化领域也有所研究,如银基催化剂在NOx消除[10]、甲醛[11]和甲苯[12]催化燃烧等方面表现出一定的催化活性。据文献报道,Tang等[13]发现在MnOx-CeO2混合氧化物上负载Ag后对HCHO具有良好的催化氧化活性,在100 ℃下甲醛的转化率为100%。 Zhang等[14]采用等体积浸渍法制备了Ag/TiO2、 Ag/Al2O3、 Ag/CeO2催化剂用于甲醛催化燃烧,其中Ag/TiO2催化剂活性最佳,只需在95 ℃甲醛中即可完全转化。Deng等[15]采用融熔盐法制备了低负载量的0.13wt% Ag/Mn2O3纳米线催化剂,甲苯仅在220 ℃下即可完全被氧化。
研究表明,银的种类和粒径大小对催化剂的活性有较高影响。例如,Qu等[16]报道了采用氧化-还原预处理Ag/SiO2催化剂对银的种类和粒径大小有影响,进而影响催化剂对CO氧化的活性。Zhang等[17]详细研究了银的粒径大小和活性中心对CO氧化的影响,由于8wt% Ag/SiO2催化剂相对较多的金属态银和合适的粒径大小(4.5~5.5 nm),而表现出最佳的催化性能。因此,通过调控银粒径大小和价态是设计高效催化燃烧银基催化剂的关键。
本课题组前期研究表明,适量TiO2的掺杂能明显提高Al2O3载体的抗烧结能力[18]。并且富含供电子基团的络合剂与金属离子的相互作用能改变前驱体的种类及分子大小。因此,本文以Al2O3-TiO2为载体,以丙烷催化燃烧为探针反应,采用不同络合剂浸渍法制备了一系列的8wt% Ag/Al2O3-TiO2催化剂,通过改变银前驱态来调控银的种类和粒径大小,从而提高催化剂的催化燃烧性能。
1 实验部分
1.1 仪器与试剂
Nove 2200e型全自动分析仪(-196 ℃下测定,测试前,样品均在300 ℃下真空脱气3 h); Rigaku D/max-2500/PC型X-射线衍射仪(Cu Kα射线,λ=0.15418 nm, Ni滤波,工作电压40 kV,工作电流20 mA,扫描速率为5°/min,扫描范围20°~80°,扫描步长0.02°); Tecnai G2 F20 S-Twin型透射电镜;Kratos XSAM800型X光电子能谱仪[Al Kα射线,以C 1s(284.8 eV)为内标进行荷电效应校正]。
硝酸银(AR),乙醇胺(ETA)、二乙醇胺(DTA)、三乙醇胺(TEA)、柠檬酸等(AR), Al2O3-TiO2(4wt%)载体。
1.2 催化剂的制备(以柠檬酸络合剂为例)
将0.637 g的AgNO3和0.720 g的柠檬酸(CA)溶解在6 mL去离子水中,再加入5.000 g Al2O3-TiO2载体(选用24~40目),等体积浸渍12 h。然后,在120 ℃下分别干燥10 h,空气气氛下升温至500 ℃焙烧3 h,制得Ag/Al-Ti(1CA)催化剂。其中1CA代表CA与Ag的物质的量比,固定银的负载量质量百分数约为8wt%,改变络合剂的种类和物质的量比,制得催化剂Ag/Al-Ti(xETA/DTA/TEA/CA),x代表CA与Ag的物质的量比。
1.3 催化性能测试方法
丙烷(C3H8)催化燃烧反应在固定床反应装置上进行,反应管为不锈钢管,内径8 mm。采用SC-8000 型气相色谱仪在线分析反应前后丙烷浓度变化。色谱柱为Agilent J&W GC柱,检测器为氢火焰检测器(FID)。原料气组成为0.3 vol.%丙烷+空气,气体总流速为100 mL/min,压力为常压,催化剂用量为0.2~1.0 g,空速6000~30000 mL·g-1·h-1,计算丙烷转化率。
2 结果与讨论
2.1 催化剂的催化性能
不同络合剂对Ag/Al-Ti催化剂催化燃烧丙烷活性的影响如图1所示。由图1可见,采用传统浸渍法制备的Ag/Al-Ti(IM)催化活性最差,其T90(丙烷转化率为90%的反应温度)仍然需要440 ℃高温。而络合浸渍法制备的Ag/Al-Ti催化剂催化活性明显提高,Ag/Al-Ti(1CA)、 Ag/Al-Ti(3ETA)、 Ag/Al-Ti(3DTA)和Ag/Al-Ti(3TEA)催化剂的T90分别为359 ℃、 392 ℃、 409 ℃和428 ℃,比Ag/Al-Ti(IM)催化剂的T90分别下降了81 ℃、 48 ℃、 31 ℃和12 ℃,说明络合浸渍法制备的催化剂的活性明显提高,并且其活性提高程度与络合剂的种类相关,其中,以CA络合剂制备的催化剂活性最佳。

Temperature/℃图1 不同络合剂对Ag/Al-Ti催化剂催化燃烧丙烷活性的影响Figure 1 Effect of different complexing agent on the catalytic combustion of propane over Ag/Al-Ti catalysts (The feed gas was 0.3% C3H8 in air and GHSV = 6000 mL·h-1·gcat-1)
进一步考察了银和柠檬酸物质的量比对Ag/Al-Ti(CA)催化剂催化燃烧丙烷活性的影响,实验结果如图2所示。由图可知,Ag/Al-Ti(CA)催化剂的催化活性与银和柠檬酸的物质的量比密切相关,在n(CA)/n(Ag)从0.5增加到3的过程中,催化剂催化活性呈现先增加后下降的趋势,以n(CA)/n(Ag)为1时活性最佳,这可能是由于n(CA)/n(Ag)较低时,柠檬酸不足以完全络合银离子,不利于银粒子在后续制备过程的高分散,而n(CA)/n(Ag)较高时,过量的柠檬酸会与柠檬酸银络合物发生竞争吸附,同样也不利于银粒子的高分散,从而一定程度上限制了Ag/Al-Ti(CA)催化剂活性的提升。
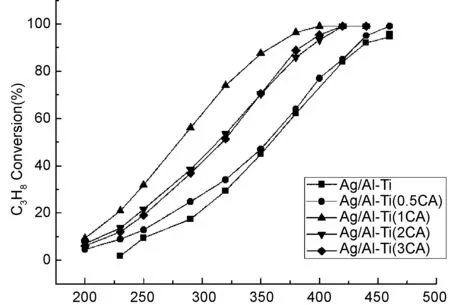
Temperature/℃图2 柠檬酸和银的物质的量比对Ag/Al-Ti(CA)催化剂催化燃烧丙烷活性的影响Figure 2 Effect of CA and Ag molar ratio on the catalytic combustion of propane over Ag/Al-Ti(CA) catalysts (The feed gas was 0.3% C3H8 in air and GHSV = 6000 mL·h-1·gcat-1)
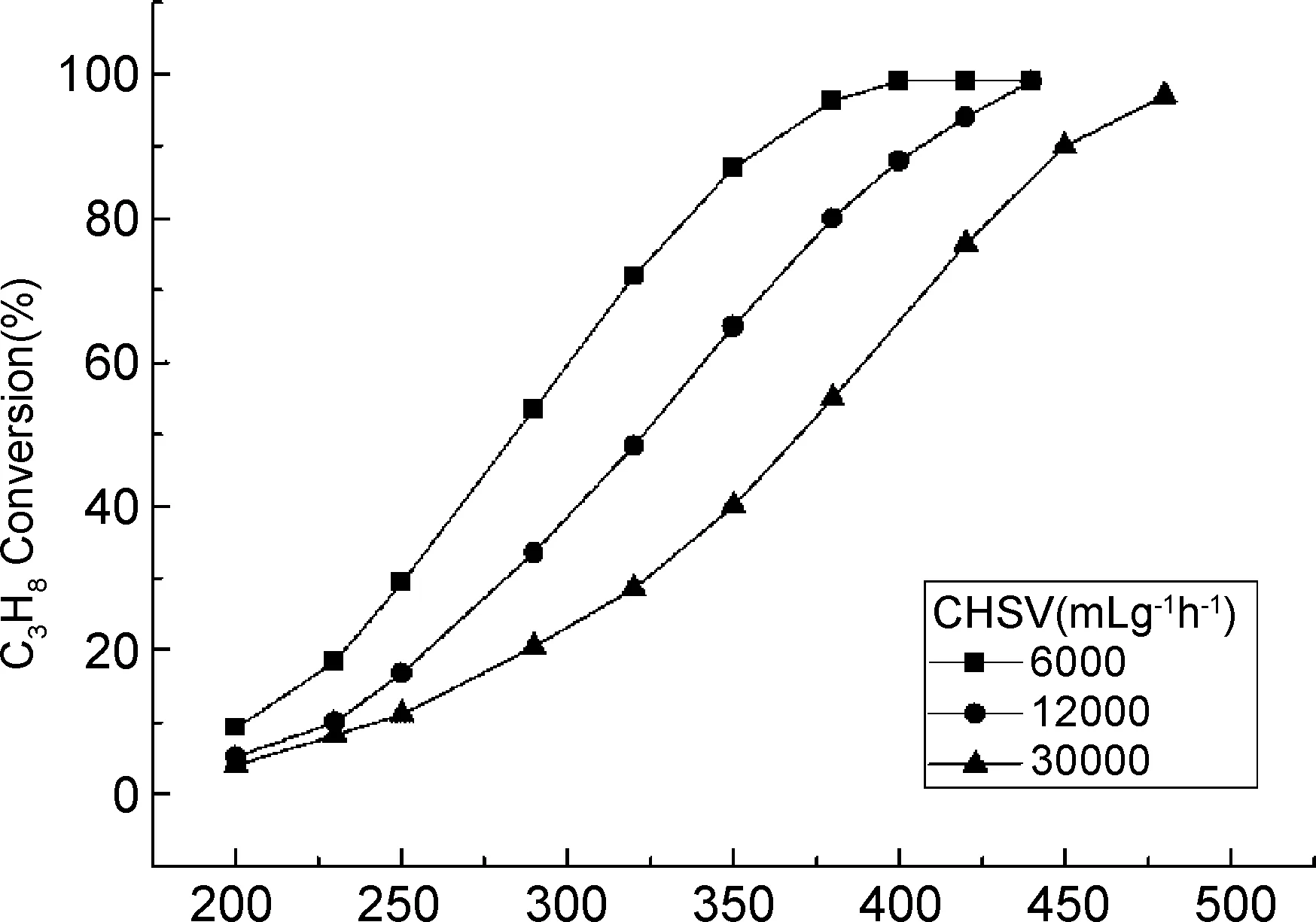
Temperature/℃图3 Ag/AlTi(1CA)催化剂在不同空速下的丙烷催化燃烧活性Figure 3 Propane conversion over the Ag/Al-Ti(1CA) catalyst under different GHSV conditions
在催化剂的实际应用中,空速是评价催化剂催化活性的一个重要参数。如图3所示,随着空速的增加,Ag/Al-Ti(1CA)催化剂的丙烷转化率会发生下降,这是由于空速提高引起的反应的停留时间缩短造成的。当空速提高到30000 mL/(g·h)时,该催化剂的T90需要高达450 ℃,说明随空速的提高该催化剂的催化活性有所降低。
催化剂的稳定性对工业应用至关重要,Ag/Al-Ti(1CA)催化剂的稳定性测试如图4所示,由图可知,在反应温度为359 ℃时,丙烷起始转化率为90%,随着反应时间的延长,丙烷转化率持续下降,当连续反应30 h后,转化率稳定在82%左右,表明Ag/Al-Ti(1CA)催化剂表现出较好的热稳定性。

Time/h图4 Ag/Al-Ti(1CA)催化剂的稳定性测试Figure 4 Reaction stability with time for propane oxidation over Ag/Al-Ti(1CA) catalyst (The feed gas was 0.3% C3H8 in air and GHSV = 6000 mL·h-1·gcat-1)
2.2 催化剂的表征
(1) BET表征
载体及各催化剂的织构性质如表1所示,由表可知,空白Al-Ti载体的比表面积和孔容分别为163 m2/g和0.41 cm3/g。与载体相比,负载活性组分银后,无论采用传统浸渍法还是络合浸渍法制备催化剂,其比表面积和孔容均有所下降,只是催化剂的表面积和孔容差异较小,因此,可认为催化剂的织构性质不是影响催化活性的主要因素。

表1 催化剂的织构性质Table 1 Textural properties of different catalysts
(2) XRD表征
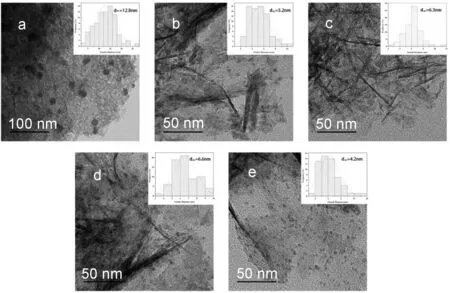
各催化剂的XRD表征如图5所示,由图可见,各催化剂均出现载体Al2O3-TiO2的明显衍射峰,其中衍射峰位于2θ=19.4°、 37.7°和66.8°归属于γ-Al2O3(JCPDS 79~1557),而衍射峰位于2θ=25.3°、 48.1°、 53.9°和55.1°归属于TiO2(JCPDS 83~2243)。此外,所有催化剂均能观察到Ag2O(JCPDS 42~0874, Cubic crystal, 2θ=34.2°)和Ag(JCPDS 87~0717, 2θ=38.1°、 44.3°、 64.4°和77.4°)衍射峰,说明银物种以Ag2O和Ag形式共存在催化剂表面,并且可以发现,采用络合浸渍法制备的催化剂,其活性组分银的衍射峰强度明显降低和宽化,说明络合浸渍法一定程度上能促进银粒子的分散,从而有利于活性中心的充分暴露,进一步有助于催化活性的提高。然而,对于Ag/Al-Ti(3ETA)、 Ag/Al-Ti(3DTA)和Ag/Al-Ti(3TEA)催化剂,在2θ=32.8°处还检测到Ag2O(JCPDS 75~1532, Hexagonal crystal)晶型,且Ag2O(JCPDS 75~1532, Hexagonal crystal, 2θ=32.8°)和Ag2O(JCPDS 42~0874, Cubic crystal, 2θ=34.2°)衍射峰强度随着络合剂分子结构(ETA 2θ/(°)图5 催化剂的XRD谱图Figure 5 XRD patterns of catalysts (3) TEM表征 采用透射电镜观测各催化剂表面活性组分银的分散情况,并统计了粒径分布,结果如图6所示。由图可见,活性组分银以球形颗粒分布在载体表面,制备方法和络合剂种类对银粒径分布有较大影响。根据银的粒径尺寸统计结果,传统浸渍法制备的Ag/Al-Ti(IM)催化剂中银粒子尺寸大约为12.8 nm,而采用络合浸渍法制备的Ag/Al-Ti(3ETA)、 Ag/Al-Ti(3DTA)、 Ag/Al-Ti(3TEA)和Ag/Al-Ti(1CA)催化剂银粒子尺寸分别为5.2 nm、 6.3 nm、 6.6 nm和4.2 nm,说明络合浸渍法能够明显降低银粒子的尺寸、提高其分散度,这与XRD测试结果相一致。进一步说明银粒子尺寸的减小是催化剂催化活性提高的原因之一。 图6 不同催化剂的TEM谱图和Ag粒径尺寸统计结果Figure 6 TEM images and size distribution of Ag particles of different samples: (a) Ag/Al-Ti(IM), (b) Ag/Al-Ti(3ETA), (c) Ag/Al-Ti(3DTA), (d) Ag/Al-Ti(3TEA), (e) Ag/Al-Ti(1CA) catalysts (4) XPS表征 X射线光电子能谱用于探究各催化剂表面的化学组成以及催化剂中各元素的微观化学状态。图7(a)和(b)为Ag 3d和O 1s的XPS分峰谱图。表2列出了Ag、 O、 Al的表面元素相对含量及Ag0和各氧物种的摩尔比。 表2 各催化剂的XPS数据分析Table 2 The XPS results of different catalysts 图7(a)为Ag 3d的XPS谱图,由图可见,Ag 3d3/2和Ag 3d5/2的特征峰分别位于375.0 eV和368.5 eV,其中Ag 3d5/2特征峰出现在(368.3~368.8 eV)和(367.4~367.9 eV)两个区间,分别归属于Ag0和Ag+物种[19-20],说明活性组分银元素主要以Ag0和Ag+形式共同存在。并且通过计算发现,络合浸渍法制备的催化剂表面Ag0/(Ag++Ag0)的摩尔比明显高于传统浸渍法,说明络合浸渍法能够有利于催化剂表面Ag0的生成,根据文献报道[21-22],在用于催化氧化的Ag基催化剂中,Ag0物种有利于氧分子的吸附和活化,从而促进催化剂活性的提高。 Binding energy/eV Temperature/℃图8 催化剂的H2-TPR谱图Figure 8 H2-TPR profiles of different catalysts 图7(b)给出了催化剂O 1s的XPS谱图。由图可知,所有催化剂的O 1s谱图均可分峰拟合为3个谱峰,结合能大小位于529.4~530.3 eV的谱峰归属于晶格氧,标记为OⅠ;位于530.9~531.7 eV的谱峰归属于表面吸附氧,标记为OⅡ;位于532.3~533.2 eV区间的谱峰归属于表面吸附的羟基氧和水分子中的氧,标记为OⅢ。其中,OⅡ具有最高的移动性,通常被认为是VOCs催化燃烧的活性氧物种[23]。因此,OⅡ氧物种越多,越有利于提高催化剂的丙烷催化氧化性能。 由表2可知,络合浸渍法制备的催化剂能够明显促进表面银含量的提高,说明络合浸渍法能够促进银的分散。各催化剂的氧物种的含量顺序由表2可知,与Ag/Al-Ti(IM)催化剂相比,采用络合浸渍法制备的催化剂的OⅡ氧物种含量明显提高,OⅠ氧物种有所下降,且OⅡ氧物种相对含量顺序依次为:Ag/Al-Ti(IM) (5) H2-TPR表征 图8是催化剂的H2-TPR谱图。由图可知,所有催化剂都在80 ℃附近出现明显的还原峰,而在130 ℃附近出现较弱的还原峰,其中,低温还原峰归属于晶粒尺寸较小或者表相Ag2O的还原峰,高温还原峰归属于晶粒尺寸较大或者体相Ag2O的还原峰[16,24]。可以看出,采用络合浸渍法制备的催化剂,无论是低温还原峰峰面积还是高温还原峰峰面积均小于传统浸渍法制备的Ag/Al-Ti(IM)催化剂,并且发现,还原峰峰面积顺序依次为:Ag/Al-Ti(IM)>Ag/Al-Ti(3TEA)≈Ag/Al-Ti(3DTA)>Ag/Al-Ti(3ETA)>Ag/Al-Ti(1CA),这与XPS测试催化剂表面Ag0/(Ag++Ag0)的含量结果相一致,说明络合浸渍法能够促进催化剂表面Ag0/(Ag++Ag0)含量的提高,但是并没有提升催化剂的低温还原性能。 结合催化剂的活性关系以及表征结果,推测传统浸渍法和柠檬酸络合浸渍法制备过程如图9所示,传统浸渍法主要是以硝酸银形式存在,其分子结构较小,在干燥、焙烧过程中容易发生结晶、团聚,因此,所制备的催化剂粒径相对较大,原子利用率较小,催化活性较低。而柠檬酸络合浸渍法中银的前驱体主要是以络合形式存在,在干燥、焙烧过程中银络合物会起到隔离作用,一方面柠檬酸络合剂包覆住银粒子有利于其高度分散,另一方面柠檬酸络合剂可能起还原剂作用,有利于金属态Ag0的生成。因此,所制备的催化剂活性较高。 图9 传统浸渍法和柠檬酸络合浸渍法制备催化剂的过程Figure 9 Preparation process of conventional impregnation and citric acid complex impregnation 与Ag/Al-Ti(IM)催化剂相比,络合浸渍法能够明显提高催化剂催化活性,其丙烷催化燃烧活性顺序依次为:Ag/Al-Ti(IM)



2.3 传统浸渍法和络合浸渍法的差异分析

